Crijevna mikrobiota utječe na način funkcioniranja mnogih tjelesnih procesa, kao što je imunološka funkcija, normalan metabolizam, i razvoj organizma. Također utječe na ponašanje domaćina, uključujući društvenu aktivnost i reakcije na stres, koji su povezani s mnogim različitim poremećajima mozga i/ili uma. Međutim, nema mnogo znanja o temeljnim mehanizmima pomoću kojih crijevne bakterije mogu promijeniti način funkcioniranja moždanih stanica, ili ponašanje većeg organizma.
Ranija istraživanja pružaju jasne naznake povezanosti zdravlja crijeva s nizom različitih bolesti poput ASD-a i posttraumatskog stresnog poremećaja. Mnoga su istraživanja pokazala da su autoimune bolesti povezane s abnormalnim crijevnim mikrobiomom, te na nekoliko psihijatrijskih i neuroloških stanja. Na primjer, upalne bolesti crijeva, multipla skleroza i psorijaza poremećaji su autoimunosti, te osobe imaju veći rizik od smanjenja broja različitih crijevnih bakterija, kao i veće šanse za tjeskobu, poremećaji raspoloženja i depresija. Čini se da su uobičajeni geni prisutni i u psihijatrijskim i u autoimunim stanjima.
U ovoj studiji, znanstvenici su pogledali mozak dviju vrsta miševa s abnormalnom crijevnom mikrobiotom:miševi koji su primili antibiotike za smanjenje rasta bakterija u crijevima, ili miševi koji su uzgojeni u potpuno sterilnom okruženju kako bi bili bez klica (GF). Prvo su izložili opasnosti ove populacije miševa, a zatim ga uklonio. Proučavajući odgovore učenja u ovim populacijama miševa, otkrili su da oboje pokazuju smanjeni kapacitet da nauče kako se više ne treba bojati opasnosti koja im prijeti (naziva se učenje izumiranja straha). Drugim riječima, normalni miševi razvijaju refleksni odgovor straha na prijeteću opasnost, ali s vremenom jer podražaj nije iznio nikakvu štetu nakon izlaganja, njihovi uvjetovani odgovori na strah opadaju. Ovo učenje nije bilo očito kod miševa liječenih GF-om ili antibioticima koji su s vremenom nastavili pokazivati uvjetovane reakcije straha.
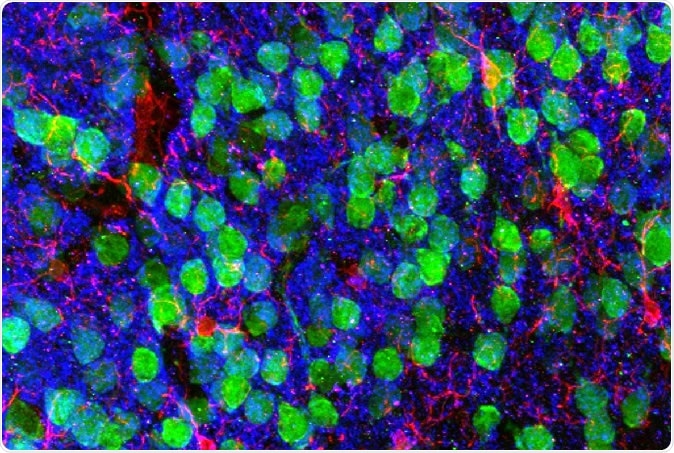 Snimanje mozga. Medijalni prefrontalni korteks koji pokazuje kortikalne neurone (zeleni), mikroglija (crvena), i post-sinaptički marker PSD95 (plavi). Slika ljubaznošću Dr. Christopher Parkhurst i David Artis (WCM).
Snimanje mozga. Medijalni prefrontalni korteks koji pokazuje kortikalne neurone (zeleni), mikroglija (crvena), i post-sinaptički marker PSD95 (plavi). Slika ljubaznošću Dr. Christopher Parkhurst i David Artis (WCM). Da biste saznali zašto, istraživači su sekvencirali RNK unutar mikroglije, imunološke stanice mozga. RNA je posredna molekula između genetskog plana u jezgri i konačnog proteina u citoplazmi, proizvedeno iz kodiranog gena. Tako RNK sekvenca pokazuje gen izražen u toj određenoj stanici.
Sekvenciranje RNA pokazalo je drugačiji obrazac ekspresije gena u stanicama mozga ovih populacija miševa, što je pak utjecalo na normalno preoblikovanje koje se događa kao dio učenja. Stanice mozga stvaraju veze ili sinapse kako bi međusobno prenosile informacije. Međutim, kako učenje napreduje, određene sinapse se uklanjaju, a druge dodaju, prema prometu impulsa duž tog puta. To se naziva obrezivanje sinapsi i važan je proces u učenju.
Ispitujući razlike u ekspresiji gena u medijalnoj prefrontalnoj kori mozga miša, znanstvenici su otkrili da za razliku od mikroglije kod zdravih miševa, te mikroglije nisu pokazale normalne promjene orezivanja, a to je zauzvrat smanjilo broj novih sinapsi koje su nastale tijekom iskustva učenja. Ova je promjena negativno utjecala na njihovu sposobnost učenja.
Postsinaptičke dendritičke bodlje također nisu normalno preuređene, i neuroni koji kodiraju znakove u ovom dijelu mozga nisu pokazali normalnu razinu aktivnosti. Uz mikrogliju, pobudni neuroni i drugi tipovi moždanih stanica pokazali su slične promjene.
U Dodatku, istraživači su otkrili da je došlo do promjena u razinama četiri kemikalije u mozgu GF miševa. Ove kemikalije obično su povezane s neuropsihijatrijskim bolestima poput shizofrenije i poremećaja iz spektra autizma. Promjene u tim kemikalijama stoga su usko povezane s promjenama u funkcioniranju mozga, što pak odlučuje kako osjećamo svoju okolinu i kako na njih reagiramo. Činjenica da je promijenjeni crijevni mikrobiom povezan s nečim tako temeljnim kao što je kemija mozga stoga je značajna u otkrivanju temeljnog obrasca. Kako kaže istraživač Frank Schroeder, "Kemija mozga bitno određuje kako se osjećamo i reagiramo na svoju okolinu, a postoje dokazi da kemikalije dobivene iz crijevnih mikroba igraju važnu ulogu. ”
Na trećoj fazi - istraživači su sada pokušali vratiti normalne sposobnosti učenja miševima vraćanjem crijevnih organizama kako bi zamijenili one koji su izgubljeni, u prvoj grupi, ili presađivanjem normalnih mikrobioma, u populaciji GF. Uspjeli su ako se crijevni mikrobiom vratio u normalu odmah nakon rođenja, s tretiranim miševima koji pokazuju normalne obrasce učenja. S druge strane, nedostatak poboljšanja kasnijim intervencijama ukazuje na bitnu potrebu za signalima iz zdravog crijevnog mikrobioma u mozak u razvoju čim se dijete rodi.
Istraživač Conor Liston komentira, "Ovo je bio zanimljiv nalaz, s obzirom na to da su mnoga psihijatrijska stanja povezana s autoimunim bolestima povezana s problemima tijekom ranog razvoja mozga. ”
Istraživač David Artis kaže, “Osovina crijeva i mozga utječe na svako ljudsko biće svaki dan u životu. Nitko još nije shvatio kako IBD i druga kronična gastrointestinalna stanja utječu na ponašanje i mentalno zdravlje. Naša studija pruža novi uvid u to kako mehanizmi funkcioniraju. ”
Razjašnjenje načina na koji crijevna disbioza utječe na funkcioniranje mozga na molekularnoj i staničnoj razini će, nadam se, ubrzati identifikaciju ciljnih molekula ili puteva za liječenje oboljelih ljudi u budućnosti.
 Rizik od raka jednjaka mogao bi se smanjiti esomeprazolom i niskim dozama aspirina
Rizik od raka jednjaka mogao bi se smanjiti esomeprazolom i niskim dozama aspirina
 Uobičajene gljivice na koži mogu uzrokovati upalnu bolest crijeva
Uobičajene gljivice na koži mogu uzrokovati upalnu bolest crijeva
 Ljudskim koronavirusima potrebni su organski materijali za učinkovit prijenos između površina
Ljudskim koronavirusima potrebni su organski materijali za učinkovit prijenos između površina
 Propuštena crijeva i mikrobna disbioza mogli bi pridonijeti oluji citokina u teško bolesnim slučajevima COVID-19
Propuštena crijeva i mikrobna disbioza mogli bi pridonijeti oluji citokina u teško bolesnim slučajevima COVID-19
 Imunološke stanice crijeva mogle bi biti odgovorne za promjene metabolizma, otkriva studija
Imunološke stanice crijeva mogle bi biti odgovorne za promjene metabolizma, otkriva studija
 Krvni test za mikrobnu DNK mogao bi upozoriti na rak
Krvni test za mikrobnu DNK mogao bi upozoriti na rak
 Izrada fizičke i genetske karte Cannabis sativa
The Cannabis sativa biljka se obično koristi za razne ljekovite, poljoprivredni, industrijske i rekreacijske svrhe u cijelom svijetu. Unatoč širokoj upotrebi, ostalo je malo genetskih podataka koji
Izrada fizičke i genetske karte Cannabis sativa
The Cannabis sativa biljka se obično koristi za razne ljekovite, poljoprivredni, industrijske i rekreacijske svrhe u cijelom svijetu. Unatoč širokoj upotrebi, ostalo je malo genetskih podataka koji
 Transplantacija izmeta od određenih donatora bolja je od drugih
Transplantacija fekalne mikrobiote ili transplantacija stolice od donatora korisna je za pacijente zaražene smrtonosnim recidivom Clostridium difficile što dovodi do teškog proljeva, bol i često ozb
Transplantacija izmeta od određenih donatora bolja je od drugih
Transplantacija fekalne mikrobiote ili transplantacija stolice od donatora korisna je za pacijente zaražene smrtonosnim recidivom Clostridium difficile što dovodi do teškog proljeva, bol i često ozb
 Bakterijski profil crijeva može predvidjeti oštećenje crijeva nakon radioterapije
Umjesto fizičkog otiska prsta, crijevni mikrobni uzorak može se koristiti za identificiranje određenih ranjivosti u pacijenata koji su na radioterapiji zbog prostate ili ginekološkog karcinoma, predvi
Bakterijski profil crijeva može predvidjeti oštećenje crijeva nakon radioterapije
Umjesto fizičkog otiska prsta, crijevni mikrobni uzorak može se koristiti za identificiranje određenih ranjivosti u pacijenata koji su na radioterapiji zbog prostate ili ginekološkog karcinoma, predvi