Studien deres med tittelen, "Tiopuriner aktiverer en antiviral utfoldet proteinrespons som blokkerer viral glykoproteinakkumulering i cellekulturinfeksjonsmodell, ”Ble publisert på nettet som et forhåndstrykk på nettstedet bioRxiv* .
Forskerne forklarte at virus som er innhyllet, som koronaviruset, har genetisk materiale som kan kode for membranproteiner som kan syntetiseres og modifiseres i det endoplasmatiske retikulum (ER) før de kan transporteres til forsamlingsområdene til delene av virionen.
Hvis ER -proteinfoldingskapasiteten er overveldet av for mange virionpartikler, det er en overbelastning av utfoldede proteiner i ER. Dette utløser en utfoldet proteinrespons (UPR). Dette aktiverer transkripsjonsfaktor-6 (ATF6), inositol som krever enzym-1 (IRE1) og PKR-lignende endoplasmatisk retikulumkinase (PERK). Disse kan føle at ER er under stress, og det er dermed en syntese av grunnleggende transkripsjonsfaktorer for leucinglidelås (bZIP).
Etter hvert som UPR blir aktivert, proteinfoldingskapasiteten til ER er økt. Dette utløser også ER-assosiert degradering (ERAD). Alle proteiner som ikke brettes riktig, bringes ut av ER og nedbrytes via 26S -proteasomet.
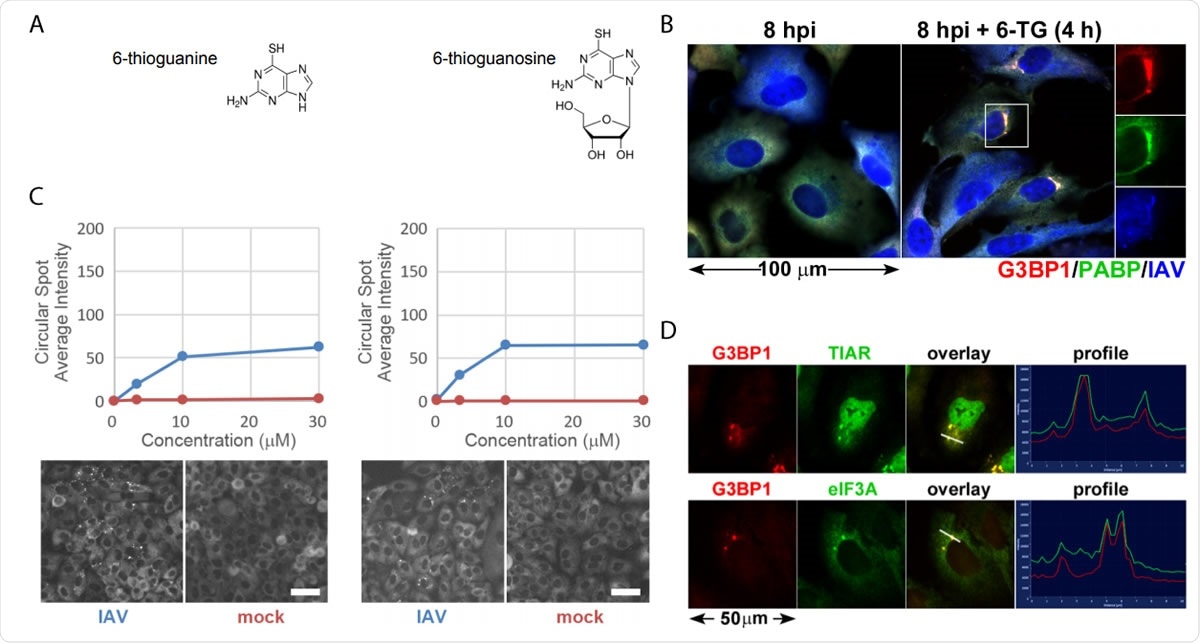 Tiopurinanaloger 6-TG og 6-TGo induserer selektivt stressgranulat i IAV-infiserte celler. (A) Strukturelle diagrammer over små molekyler identifisert på skjermen. (B) Kvantifisering av EGFP-G3BP foci dannelse i IAV-Udorn infiserte (blå) eller håne (røde) infiserte celler behandlet med økende doser av 6-TG og 6-TGo (øverst) og representative Cellomics bilder av EGFP kanal av celler behandlet med 30 uM 6-TG og 6-TGo (nederst). Ved 4 hpi, cellene ble behandlet med 0, 1, 10 og 30 uM doser av tiopurinanaloger 6-tioguanin (6- TG) eller 6-tioguanosin (6-TGo). Ved 8 hpi, cellene ble fikset og farget med Hoeschst 33342. Automatisert bildeopptak ble utført ved hjelp av en Cellomics Arrayscan VTI HCS -leser. 15 bilder ble tatt for hver brønn og gjennomsnittlig punktert EGFP-G3BP1 intensitet ble beregnet. (C) A549-celler ble infisert med IAV-CA/07 ved en MOI på 1. Ved 4 hpi, cellene ble behandlet med 6-TG eller mock-behandlet. Ved 8 hpi, cellene ble fikset og immunfarget med antistoffer rettet mot stressgranulatmarkørproteiner G3BP1 (rød), PABP (grønn) og et polyklonalt IAV -antistoff (blått) som oppdager antigener fra NP, M1, og HA, etterfulgt av farging med Alexa-konjugerte sekundære antistoffer. (D) A549-celler ble infisert med IAV-CA/07 ved en MOI på 1. Ved 4 hpi, cellene ble behandlet med 6-TG (10 uM). Ved 8 hpi, cellene ble fikset og immunfarget med antistoffer rettet mot stressgranulatmarkørproteiner G3BP1 (rød), TIAR (grønn) og eIF3A (grønn), etterfulgt av farging med Alexa-konjugerte sekundære antistoffer. Bilder tatt på et fluorescerende mikroskop av Zeiss Axioimager Z2. Representative bilder vist. Skalaer representerer 20 um.
Tiopurinanaloger 6-TG og 6-TGo induserer selektivt stressgranulat i IAV-infiserte celler. (A) Strukturelle diagrammer over små molekyler identifisert på skjermen. (B) Kvantifisering av EGFP-G3BP foci dannelse i IAV-Udorn infiserte (blå) eller håne (røde) infiserte celler behandlet med økende doser av 6-TG og 6-TGo (øverst) og representative Cellomics bilder av EGFP kanal av celler behandlet med 30 uM 6-TG og 6-TGo (nederst). Ved 4 hpi, cellene ble behandlet med 0, 1, 10 og 30 uM doser av tiopurinanaloger 6-tioguanin (6- TG) eller 6-tioguanosin (6-TGo). Ved 8 hpi, cellene ble fikset og farget med Hoeschst 33342. Automatisert bildeopptak ble utført ved hjelp av en Cellomics Arrayscan VTI HCS -leser. 15 bilder ble tatt for hver brønn og gjennomsnittlig punktert EGFP-G3BP1 intensitet ble beregnet. (C) A549-celler ble infisert med IAV-CA/07 ved en MOI på 1. Ved 4 hpi, cellene ble behandlet med 6-TG eller mock-behandlet. Ved 8 hpi, cellene ble fikset og immunfarget med antistoffer rettet mot stressgranulatmarkørproteiner G3BP1 (rød), PABP (grønn) og et polyklonalt IAV -antistoff (blått) som oppdager antigener fra NP, M1, og HA, etterfulgt av farging med Alexa-konjugerte sekundære antistoffer. (D) A549-celler ble infisert med IAV-CA/07 ved en MOI på 1. Ved 4 hpi, cellene ble behandlet med 6-TG (10 uM). Ved 8 hpi, cellene ble fikset og immunfarget med antistoffer rettet mot stressgranulatmarkørproteiner G3BP1 (rød), TIAR (grønn) og eIF3A (grønn), etterfulgt av farging med Alexa-konjugerte sekundære antistoffer. Bilder tatt på et fluorescerende mikroskop av Zeiss Axioimager Z2. Representative bilder vist. Skalaer representerer 20 um. Når viruspartikkelen invaderer en celle, den prøver å replikere raskt, og dette belaster legevakten. Viruset frigjør utbrudd av glykoproteiner som overvelder ER. Viruset, derimot, er i stand til å omgå UPR og fremmer effektiv replikering.
IAV kan kode for tre integrerte membranproteiner:hemagglutinin (HA), neuraminidase (NA), og matriseprotein 2 (M2). Mens IAV -replikasjonen forårsaker selektiv aktivering av UPR, spesifikke mekanismer kan aktivere UPR, men deretter omgå den for å fremme effektiv viral replikasjon. Teamet forklarer at effekten av NA- og M2 -proteiner på UPR ikke er klar, men HA kan fremme UPR.
Flere koronavirus (CoV) kan aktivere UPR. Dette inkluderer "smittsom bronkittvirus (IBV), musehepatittvirus (MHV), smittsomt gastroenterittvirus (TGEV), menneskelig koronavirus (HCoV) -OC43, og SARS-CoV-1. ” Hele den genetiske sekvensen, derimot, reagerer ikke på samme måte som CoV -replikasjonen.
Teamet identifiserte to FDA-godkjente tiopurinanaloger kalt "6- tioguanin (6-TG) og 6-tioguanosin (6-TGo)". Disse ble funnet å blokkere IAV- og HCoV-OC43-replikasjon når dosen ble økt gradert.
Pateamine A og Silvestrol hadde blitt testet tidligere. Disse to tiopurinene, derimot, ble funnet å forstyrre prosessen med akkumulering av virale glykoproteiner som kunne aktivere UPR. I cellene som hadde blitt behandlet med 6-TG, viral glykoproteinsyntese kan delvis gjenopprettes ved kjemisk inhibering av UPR.
CoV Spike (S) proteiner som uttrykkes på overflaten av viruset viste UPR -aktivering. S-proteinet fra det nye koronaviruset eller SARS-CoV-2 S forårsaket også UPR-aktivering. 6-TG hemmet akkumulering av S0 eller furin-spaltede S2 fusjonsproteiner i full lengde, bemerket de. Det påvirket ikke S1 ectodomain. 6-TG kan indusere UPR som akselererer ERAD-mediert omsetning av membranforankrede S0- og S2-glykoproteiner, laget fant.
Forskerne eksperimenterte og fant at en kjemisk lignende forbindelse tiopurin 6-merkaptopurin (6-MP) hadde liten effekt på UPR og ikke påvirket replikasjonen av IAV HCoV-OC43.
Grubler over mekanismen for UPR-induksjon av tiopurinforbindelsene 6-TG og 6-TGo, teamet skrev at disse effektene sannsynligvis ikke blir formidlet gjennom DNA eller RNA-inkorporering av 6-TG på grunn av flere årsaker. Den første grunnen er at stresset forbundet med virusreplikasjon ikke spesifikt induserer UPR. Den andre grunnen er at blant virale proteiner, akkumuleringen av glykoproteiner og behandlingen av dem ble selektivt avbrutt. Den tredje grunnen var at messenger -RNA -nivåene av HA og NA i IAV ikke ble signifikant påvirket. 6 MP, på den andre siden, kan omdannes til 6-tioguanosintrifosfat, men induserte ikke UPR og hadde ingen effekter på IAV-glykoproteiner eller OC43-replikasjon.
Teamet skrev at dataene deres avslører at "UPR-induserende molekyler kan være effektive vertsrettede antivirale midler mot virus som er avhengige av ER-prosesser for å støtte effektiv replikasjon." Induksjon av UPR med 6-TG og 6-TGo kan således være en ny metode som en antiviral mekanisme kan utløses av vertscellen selv. Dette har vært en tidligere ukjent unik virkningsmekanisme, laget skrev.
De skrev avslutningsvis "... disse dataene indikerer at 6-TG og 6-TGo er effektive vertsrettede antivirale midler som utløser UPR og forstyrrer akkumulering av virale glykoproteiner."
medRxiv publiserer foreløpige vitenskapelige rapporter som ikke er fagfellevurdert og, derfor, skal ikke betraktes som avgjørende, veilede klinisk praksis/helserelatert atferd, eller behandles som etablert informasjon.
 Plantefôr kan overføre antibiotikaresistente superbugs til mennesker
Plantefôr kan overføre antibiotikaresistente superbugs til mennesker
 Gode nyheter for IBS -lider da forskere identifiserer "tarmkløe"
Gode nyheter for IBS -lider da forskere identifiserer "tarmkløe"
 Irritabel tarmsykdom øker risikoen for demens
Irritabel tarmsykdom øker risikoen for demens
 Hvorfor trenger jeg en koloskopi?
Hvorfor trenger jeg en koloskopi?
 Rapporterer etiketter på kommersielle kefirprodukter mikrobielle nivåer riktig?
Rapporterer etiketter på kommersielle kefirprodukter mikrobielle nivåer riktig?
 Gå videre,
Gå videre,
 Fører hypertensjon alltid til alvorlig COVID-19?
Forårsaket av smittestoffet, alvorlig akutt respiratorisk syndrom coronavirus 2 (SARS-CoV-2), koronavirussyken 2019 (COVID-19) er ofte mer alvorlig hos personer med underliggende medisinske tilstander
Fører hypertensjon alltid til alvorlig COVID-19?
Forårsaket av smittestoffet, alvorlig akutt respiratorisk syndrom coronavirus 2 (SARS-CoV-2), koronavirussyken 2019 (COVID-19) er ofte mer alvorlig hos personer med underliggende medisinske tilstander
 Strategisering av beredskap for pediatrisk helse for den andre bølgen av COVID-19-pandemien
Selv om COVID-19-pandemien har hatt en relativt liten innvirkning på den pediatriske befolkningen så langt, det er fryktet at den andre bølgen, som allerede er i gang i mange deler av verden, kan ta s
Strategisering av beredskap for pediatrisk helse for den andre bølgen av COVID-19-pandemien
Selv om COVID-19-pandemien har hatt en relativt liten innvirkning på den pediatriske befolkningen så langt, det er fryktet at den andre bølgen, som allerede er i gang i mange deler av verden, kan ta s
 Hvorfor trenger jeg en koloskopi?
Folk har hørt nok skrekkhistorier om koloskopier til å fylle et Halloween -hjemsøkt hus. Selv om du ikke er gammel for å ha hatt en, du har sikkert hørt om dem. Så, hvis de er så slitsomme, hvorfor
Hvorfor trenger jeg en koloskopi?
Folk har hørt nok skrekkhistorier om koloskopier til å fylle et Halloween -hjemsøkt hus. Selv om du ikke er gammel for å ha hatt en, du har sikkert hørt om dem. Så, hvis de er så slitsomme, hvorfor