En ny studie genomfördes på en grupp med 32 extremt prematura spädbarn som fick stanna i antibiotikabehandling i 21 månader, en annan grupp med 9 spädbarn som fick antibiotika i en vecka eller mindre men också var extremt prematura, och en kontrollgrupp på 17 spädbarn födda vid termin eller sent född, som inte hade fått antibiotika (eller "antibiotika-naiva"). Forskarna använde en kombination av DNA -sekvensering, kulturer och datorbaserade algoritmer för att förstå tarmmikrobiomet och den typ av resistensgener som uttrycks hos dessa prematura barn som utsatts för antibiotika både under och efter sjukhusvistelsen. Detta jämfördes med tarmmikrobiomen hos friska barn som aldrig hade fått antibiotika.
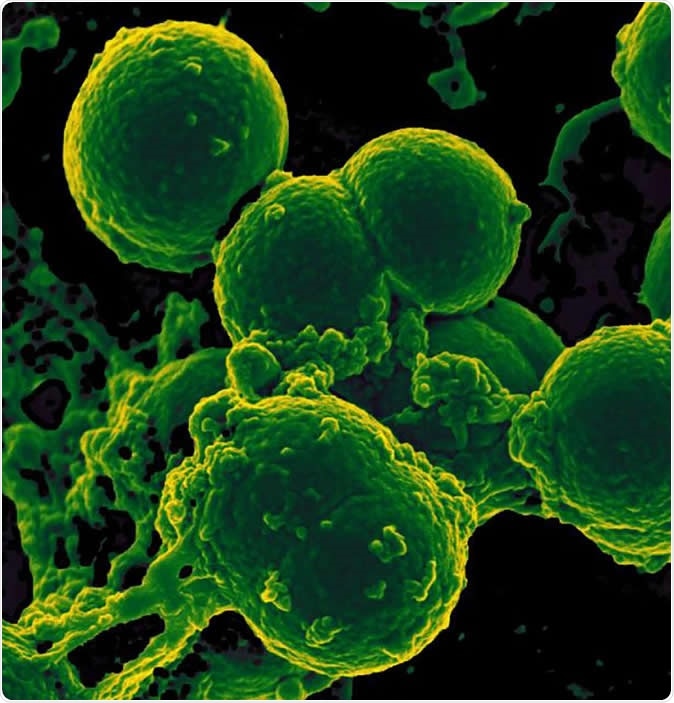 Elektronmikroskopi av neutrofiler som intar meticillinresistenta Staphylococcus aureus-bakterier. Bildkredit:NIAID
Elektronmikroskopi av neutrofiler som intar meticillinresistenta Staphylococcus aureus-bakterier. Bildkredit:NIAID Resultaten visade att antalet bakteriearter hos spädbarn som fått långvarig antibiotikabehandling reducerades avsevärt jämfört med den antibiotika-naiva gruppen. För det andra, antalet gener i tarmbakterierna som uttryckte antibiotikaresistens var mycket högre i denna grupp. Dessutom, några av dessa gener för resistens var riktade mot läkemedel som barnet aldrig hade utsatts för - eftersom dessa vanligtvis inte används hos nyfödda, som ciprofloxacin eller kloramfenikol. Forskarna föreslår att dessa gener kan ha kommit från multiresistenta bakterier. I detta fall, att utsättas för ett av de läkemedel som bakterien är resistent mot kan orsaka att andra arter raderas, medan den resistenta stammen lämnas för att föröka sig. Dessutom, barnet kommer också att visa resistens mot andra läkemedel på grund av det multipla motstånd som genen ger - oavsett om dessa läkemedel användes eller inte.
På nytt, tidigare studier visar ett samband mellan hudallergier, diabetes inflammatorisk tarmsjukdom, fetma och psoriasis, och antibiotikaanvändning i tidigt liv. Effekterna kan vara triviala men kan också främja patogena arter att växa i tarmen, samtidigt som tillväxten av "goda" bakterier hämmas.
Forskarna kallar dessa förändringar i genomet "mikrobiota ärr". Tidigare studier visade ett samband mellan allergiska hudsjukdomar som psoriasis eller hudallergi, diabetes, fetma och inflammatorisk tarmsjukdom, och behandling med antibiotika under det första levnadsåret.
Övergripande, spädbarn som fått antibiotika under en längre tid misslyckades med att utveckla ett rikt och varierat tarmmikrobiom som antibiotika-naiva barn. Antibiotika-exponerade barn fäller också Enterobacteriaeae, en opportunistisk patogen som var, I detta fall, läkemedelsresistent. Således, arten som etablerade sig i dessa barns tarmar drevs av deras antibiotikaresistens. Tarmmikrobiomet kan vara obalanserat till förmån för patogena arter, och resistenta infektioner kan uppstå med större lätthet hos dessa barn på grund av deras större resistom (total samling av antibiotikaresistenta gener).
Med forskarnas ord, ”Säkerhetsskadorna vid antibiotikabehandling tidigt i livet och sjukhusvistelse hos prematura barn är långvariga. Vi uppmanar utvecklingen av strategier för att minska dessa konsekvenser i mycket utsatta neonatala populationer. ”
Artikeln publicerades i tidningen Naturmikrobiologi den 9 september, 2019.
 Var inte rädd för koloskopi
Var inte rädd för koloskopi
 Bakterier i födelsekanalen kopplade till lägre risk för äggstockscancer
Bakterier i födelsekanalen kopplade till lägre risk för äggstockscancer
 Är det mer sannolikt att kvinnor utvecklar lång COVID?
Är det mer sannolikt att kvinnor utvecklar lång COVID?
 Forskare manipulerar bakteriearter i tarmen med hjälp av diet
Forskare manipulerar bakteriearter i tarmen med hjälp av diet
 Sömnkvalitet kan vara en indikator för senare studier av Alzheimers sjukdom
Sömnkvalitet kan vara en indikator för senare studier av Alzheimers sjukdom
 Är C-sektionen bra för barns hälsa?
Är C-sektionen bra för barns hälsa?
 Vad är problemet med hepatit C?
Hep C. Dessa dagar, du ser massor av tv -reklamfilmer om att testas och screenas för det. Det är lätt att anta att hepatit bara är ett tillstånd som berör dem som kan ha delade nålar under droganvändn
Vad är problemet med hepatit C?
Hep C. Dessa dagar, du ser massor av tv -reklamfilmer om att testas och screenas för det. Det är lätt att anta att hepatit bara är ett tillstånd som berör dem som kan ha delade nålar under droganvändn
 Viktminskning läkemedel Wegovy godkänt av FDA
U.S. Food and Drug Administration (FDA) har godkänt Wegovy (semaglutid) injektion (2,4 mg en gång i veckan) som en kronisk viktkontrollbehandling hos överviktiga eller överviktiga vuxna med ett viktre
Viktminskning läkemedel Wegovy godkänt av FDA
U.S. Food and Drug Administration (FDA) har godkänt Wegovy (semaglutid) injektion (2,4 mg en gång i veckan) som en kronisk viktkontrollbehandling hos överviktiga eller överviktiga vuxna med ett viktre
 Kost och näring påverkar mikrobiom i tarmslemhinnan
Kost är viktigt för att upprätthålla människors hälsa, men dess bakomliggande mekanism är ännu inte helt förstådd. Nu, ett team av forskare belyser sambandet mellan kost och hälsa, och det har något a
Kost och näring påverkar mikrobiom i tarmslemhinnan
Kost är viktigt för att upprätthålla människors hälsa, men dess bakomliggande mekanism är ännu inte helt förstådd. Nu, ett team av forskare belyser sambandet mellan kost och hälsa, och det har något a