Extracto
El tracto gastrointestinal de los animales está adaptada para su principal fuente de alimento para optimizar el uso de recursos y el consumo de energía. especies de murciélagos de clima templado se alimentan principalmente de artrópodos. Estos contienen la quitina carbohidratos rica en energía, lo que no es digerible por las enzimas endógenas del tracto digestivo de los mamíferos típico. Sin embargo, el tracto gastrointestinal de las especies de murciélagos debe adaptarse a su dieta y ser capaz de digerir la quitina. La hipótesis de que (i) las especies de murciélagos vespertilionid europeos tienen la quitinasa de enzimas digestivas y que (ii) la actividad quitinolıtica se encuentra en el intestino, como se ha encontrado para las especies de murciélagos en América del Norte. Los tractos gastrointestinales de siete especies de murciélagos ( Pipistrellus Pipistrellus Visto:. Strobel S, A, Roswag Becker NI, Trenczek TE, Encarnação JA (2013) murciélagos insectívoros Recopilación de quitina en el estómago utilizando La quitinasa ácida de mamíferos. PLoS ONE 8 (9): e72770. doi: 10.1371 /journal.pone.0072770 Editor: François Blachier, Instituto Nacional de Investigación Agronómica, Francia | Recibido: 26 Marzo, 2013; Aceptado: 12 de julio de 2013; Publicado: 3 Septiembre 2013 Derechos de Autor © 2013 Strobel et al. Este es un artículo de acceso abierto distribuido bajo los términos de la licencia Creative Commons Attribution License, que permite el uso ilimitado, distribución y reproducción en cualquier medio, siempre que el autor original y la fuente se acreditan Financiación:. Los autores no tienen el apoyo o la financiación para reportar Conflicto de intereses:.. los autores han declarado que no existen intereses en competencia Introducción los animales tienen que ingerir y digerir los alimentos para garantizar la funcionamiento continuo de su metabolismo interno, cubriendo, por ejemplo, su energía, proteínas y necesidades de vitaminas [1]. El proceso multi-etapa de la digestión incluye pasos enzimáticos mecánica, química y de nutrientes de conversión de [2]. Las especies de murciélagos tienen una demanda de energía-masa específica alta debido a su pequeño tamaño y la capacidad de volar de forma activa [3], [4]. En los animales que vuelan, los alimentos necesitan ser procesados rápidamente para reducir la demanda de energía causada por el aumento de masa de vuelo [2]. especies de murciélagos europeos tienen una dieta que consiste principalmente de artrópodos [5]. Tienen tiempos de retención cortos [6] pero una alta eficiencia digestiva [7]. Esto sugiere que el tracto gastrointestinal (GI) está muy adaptada a su dieta ya que digiere artrópodos rápida y completamente. Por lo tanto, se podría argumentar que las especies de murciélagos europeos dependen de las enzimas digestivas artrópodos específica. Desde los artrópodos se componen de hasta el 75% de quitina (contenido de energía de 21,2 kJ /g, [8]), es muy posible que las especies de murciélagos son capaces de digerir el material de quitina, como se ha demostrado en otros vertebrados tales como el lagarto verde europeo ( Lacerta viridis La quitina puede ser degradado por las quitinasas (EC 3.2.1.14) y algunos lisozimas (EC 3.2.1.17) [11], [12]. En los mamíferos, sólo dos quitinasas se han identificado: chitotriosidasa y quitinasa ácida de mamíferos (AMCase) [13], los cuales se clasifican como endochitinases [14]. Chitotriosidase es secretada principalmente por los fagocitos y actúa contra los patógenos que contiene quitina [15]. AMCase hasta ahora sólo ha sido identificado en ratones (Mus musculus), macacos (Macaca fascicularis) y seres humanos [16], [17]. Se expresa altamente en el estómago y de pulmón, lo que indica una doble función digestiva e inmunológica [16], [17]. quitinolıtica actividad también puede provenir de las enzimas endógenas, alimento ingerido presente en el tracto gastrointestinal, o enzimas producidas por microorganismos [18], [19]. quitinolıtica actividad en el tracto GI se ha encontrado en varias especies de murciélagos insectívoros [8], [9]. Sin embargo, no se tiene conocimiento acerca de la enzima correspondiente. Jeuniaux [9] verificó la actividad quitinolıtica en el tracto gastrointestinal de los Rhinolophus ferrumequinum Nuestra hipótesis es que (i) las especies de murciélagos insectívoros europeos de la familia Vespertilionidae poseen actividad quitinolıtica en el tracto gastrointestinal, como se ha demostrado para las especies de murciélagos insectívoros de América del Norte [8] y una especie de murciélago europeo de la familia Rhinolophidae [9] y (ii) la actividad quitinolıtica se encuentra en el intestino, como ha sido se muestra en las especies de América del Norte [8]. En este estudio, localizamos e identificamos la actividad quitinolıtica la enzima correspondiente, como AMCase usando un ensayo enzimático, inmunotransferencia e inmunohistoquímica. Ética declaración Todos los individuos utilizan en este estudio murió a los centros de rehabilitación voluntarias para los murciélagos. Fueron entregados por voluntarios sin ningún tipo de reembolso. De acuerdo con la Ley de Protección de los Animales de Alemania (TschG § 4. (3)) y de la Ley Federal de Protección de la Naturaleza (BNatSchG §45 (4)) no se requiere un permiso para trabajar en las canales. El estómago del ratón era un resto de un estudio realizado por el Instituto de Anatomía y Biología Celular de la Justus-Liebig Universidad de Giessen, que fue aprobado por el consejo regional (núm V54-19C20 /15C Giessen 20/23 400AZ). Ningún animal murió a los efectos de este estudio. Las canales se almacenaron inmediatamente después de la muerte a -20 ° C. Los murciélagos se entregaron el hielo congelado es decir, a la Universidad de Giessen. Las canales se almacenaron durante un máximo de seis meses a -80 ° C hasta la preparación del tejido. observaciones macro y microscópicas verifican la muy buena preservación de órganos y células que se hizo enzimáticas e histológicos exámenes de los tejidos posible. Preparación de tejidos Los cadáveres de siete especies de murciélagos insectívoros sin ningún signo de putrefacción ( Pipistrellus Pipistrellus gratis ( n Preparación de las fracciones de proteínas solubles segmentos del tracto gastrointestinal de las muestras no fijadas, frescos de P. pipistrellus gratis ( n Determinación de la actividad quitinolítica Para medir la actividad quitinolítica, placas de gel de agarosa se prepararon como se describe por Zou, Nonogaki &.; Welbaum [24] con algunas modificaciones. El ácido fosfórico quitina hinchado se preparó mezclando 10 g de quitina a partir de conchas de cangrejo (Roth, Alemania) con ácido fosfórico 100 ml 85% y se incubó durante 48 horas a 4 ° C. Entonces se añadió 2 L de agua del grifo fría y la torta resultante se lavó hasta que se alcanzó pH 6,5 [25], [26]. De agarosa (1,6%) se disolvió en tampón de incubación (pH 5,0) [24] en un horno de microondas y se enfrió a 50-60 ° C. Después, se añadió la quitina hinchado ácido fosfórico (0,5%) y 10 ml de esta suspensión se pipeteó en 85-mm placas de Petri. Después de la polimerización, pozos de 4 mm de diámetro se perforan en las piezas de gel de agarosa y se extrajeron usando una bomba de chorro de agua liofilizado en polvo de quitinasa estándar de Serratia marcescens gratis (5 U.; Sigma-Aldrich, Alemania) se disolvió en 1 ml de tampón de incubación como la solución patrón. Se añadió una concentración conocida de quitinasa estándar a cada placa como tampón de referencia y la incubación se utilizó como control negativo. En primer lugar, 6 muestras l de cada solución se pipetearon por pocillo, después de lo cual las placas se incubaron durante 20 min a temperatura ambiente para permitir que las muestras se difundan en el agar. Después, se añadió una muestra L adicional a cada pocillo y las placas se incubaron a temperatura ambiente durante 20 min seguido de incubación a 37 ° C durante 20 h. placas de agarosa fueron teñidas con 0,1% calcofluor (Calcofluor Abrillantador M2R; Sigma, MO, EE.UU.) durante 10 min y se lavaron con agua destilada durante 2 h. zonas líticas se visualizaron mediante transiluminación UV y fotografiados. Los diámetros de las zonas líticas se midieron utilizando GIMP (versión 2.6.11; www.gimp.org). Utilizando una serie de diluciones de la solución de referencia quitinasa de valores con actividades enzimáticas tampón de incubación se calcula diámetro de la zona frente al logaritmo de la concentración y la variación entre placas se ajustaron a las normas internas de quitinasa utilizados en cada placa de Petri. Para analizar la actividad enzimática a diferentes valores de pH, placas de gel se prepararon como antes, pero con diferentes valores de pH (pH 4,0, pH 5,0, pH 6,0, pH 7,0 y pH 8,0). Los sobrenadantes del estómago, el duodeno, yeyuno /íleon, íleon /colon y de colon /recto de un individuo de P. pipistrellus Expresión de quitinasa en el tracto GI Western blot. Western blot se realizó para identificar y localizar bioquímicamente quitinasa en el tracto gastrointestinal de las especies de murciélagos europeos y para excluir la actividad quitinolıtica causada por lisozimas. Los sobrenadantes de muestras de tejidos de seis especies de murciélagos (muestras sección tracto gastrointestinal (estómago, duodeno, yeyuno /íleon, íleon /colon y de colon /recto):. P pipistrellus gratis ( n = 2 Los sobrenadantes de cada tejido 750 g se mezclaron 01:01 en 2 × SDS tampón de carga de gel y se calentó a 95 ° C durante 3 min. De cada muestra, 15 l se sometió a un gel de resolución del 12% y 5% de gel de apilamiento. La electroforesis se realizó en condiciones reductoras a un voltaje de 100 V. Las proteínas separadas se sometieron a electrotransferencia durante 1 h a una corriente constante de 0,8 mA /cm 2 en membranas de PVDF. Las transferencias se bloquearon con leche en polvo 5% sin grasa en Tris solución salina tamponada (TBS, pH 7,5) que contiene 0,1% de Tween 20 (Roth) durante 1 h antes de la incubación con un anticuerpo policlonal de conejo dirigido contra el N-terminal de quitinasa ácida ( Biología AVIVA Systems, CA, EE.UU., diluido 1:1000 en TBS que contiene 1% de BSA) a 4 ° C durante la noche. Después de lavar con TBS que contiene 0,05% de Tween 20 y 0,1% de BSA, las membranas se incubaron durante 1 h con el anticuerpo conjugado con fosfatasa alcalina de cabra policlonal de IgG de conejo (H & L) (Roth, Anti conejo-AP 4751; diluyó 1:7500 en TBS que contiene 1% de BSA). Las transferencias se lavaron cuatro veces y la unión del anticuerpo se visualizó por incubación con fosfato bromochloroindoyl (Bethesda Research Laboratories, MD, EE.UU.) y el sustrato nitroazul de tetrazolio (Biotech Trade & Service GmbH, Alemania) de acuerdo con Harlow y Lane [30] la inmunohistoquímica. Para localizar AMCase en el nivel celular, se realizó un análisis inmunohistoquímico en los segmentos del tracto GI de P. pipistrellus gratis ( n actividad QUITINOLÍTICAS Hemos sido capaces de detectar quitinolıtica la actividad en las muestras de estómago de todos los individuos (por ejemplo Fig. 1) y en la muestra de colon /recto de uno, M. miotis, M. nattereri la expresión de quitinasa en el tracto GI Western blot de la M. musculus hipótesis que las especies de murciélagos insectívoros europeos de la familia Vespertilionidae tienen la quitinasa de enzimas digestivas. Esta hipótesis fue confirmada por la presencia de actividad quitinolítica en los estómagos de las especies estudiadas. Por otra parte, una verdadera quitinasa, más particularmente AMCase, se pudo identificar bioquímicamente en todas las muestras de estómago. quitinasas activas son comunes y conservada entre los mamíferos [14]. Sin embargo, la ubicación y la función de la AMCase difieren entre las especies y no se resuelven completamente [31]. Además, la hipótesis de que la actividad quitinolítica se encuentra en el intestino, especialmente en el intestino delgado, ya que es el sitio donde la principal digestión enzimática y tiene lugar la absorción [32]. Nuestros resultados no confirman esta hipótesis como actividad quitinolítica fue localizada principalmente en el estómago y por tres individuos a niveles bajos de actividad en el colon /recto. La alta variabilidad de la actividad quitinolıtica en los individuos estudiados podría ser causada por variación de la actividad digestiva de los individuos en el momento de la muerte. Esto es apoyado por diferentes cantidades de comida que se encuentran en los tractos gastrointestinales. La actividad quitinolıtica en muestras de estómago, pero no en muestras de colon /recto podría remontarse a la actividad de la AMCase y no a una lisozima por transferencia de Western. La actividad de la AMCase murciélago era óptima entre pH 5,0 y pH 6,0. Estos niveles de pH son comparables con el medio ácido en el estómago de las especies de murciélagos insectívoros como se mide en el presente estudio y reportado por Naumova y Zharova [33]. Esta es una primera indicación de la importancia biológica de AMCase durante la digestión en esta parte del tracto GI. Sin embargo, otros experimentos como ensayos eficiencia digestiva deben llevarse a cabo para poner a prueba si la actividad de AMCase plantea un significado biológico a la digestión de la quitina. AMCase tiene una doble función en la inmunidad y la digestión de los organismos que contienen quitina [34], [35]. Por ejemplo, AMCase humano no está adaptado para el ambiente ácido en el estómago, a diferencia de la AMCase encontró en ratones [31]. El estómago AMCase de M. musculus Los resultados inmunohistoquímicos de este estudio apoyan la localización de AMCase en el estómago de las especies de murciélagos, sobre todo en las glándulas gástricas de la mucosa . Además, se encontró que la enzima se encuentra en o alrededor de las células principales situados en la base de las glándulas gástricas, como se ha demostrado previamente para el estómago AMCase de M. musculus Agradecemos E. Mühlbach, R. Keil , N. y S. Dittrich Wiegand para las muestras de animales y Y. Kühnel, C. von Bredow, A. Diebel y el Grupo de Ecología de mamíferos por su ayuda.
, Plecotus Auritus
, Myotis bechsteinii
, Myotis nattereri
,
) se analizó la actividad quitinolıtica por ensayo de difusión. tractos gastrointestinales de P. pipistrellus
, P. Auritus
, M. nattereri
, M. miotis, España y N. leisleri
fueron examinados para quitinasa ácida de mamíferos por Western blot. Muestras de tejido del tracto gastrointestinal de P. pipistrellus
se analizaron por inmunohistoquímica para localizar la quitinasa ácida de mamíferos. Se detectó actividad quitinolıtica en los estómagos de todas las especies de murciélagos. Western blot confirmó la quitinasa ácida de mamíferos en las muestras de estómago. La inmunohistoquímica de la P. pipistrellus tracto gastrointestinal
indicó que la quitinasa de mamífero ácido se encuentra en las células principales del estómago en la base de las glándulas gástricas. En conclusión, especies europeas de murciélagos vespertilionid tienen quitinasa de mamífero ácido que se produce en las glándulas gástricas del estómago. Por lo tanto, el tracto gastrointestinal de las especies de murciélagos insectívoros desarrollaron una adaptación enzimática a su dieta
), el mirlo común ( Turdus merula
) y el zorro rojo ( vulpes vulpes
) [9], [10].
, una especie de murciélago europeo de la familia Rhinolophidae. Whitaker et al. [8] demostrado actividad quitinolıtica en el tracto gastrointestinal de América del Norte vespertilionid especies de murciélagos de los géneros Myotis
, Eptesicus
, Nycticeius
, Lasiurus
, Pipistrellus
y lasionycteris
. Se aislaron quitinasa productores de cepas de bacterias del intestino como fuente de la actividad quitinolítica. Por el contrario, [9] Jeuniaux encontró evidencia de actividad quitinolıtica en la mucosa gástrica del estómago de Rhinolophus ferrumequinum
mientras que el intestino no exhibió actividad quitinolıtica. Sin embargo, Buchholz, Wells & Conaway [20] no ha podido detectar cualquier quitinasa en las especies de murciélagos insectívoros Pipistrellus subflavus
y Myotis grisescens
. Además de las quitinasas, algunos lisozimas son capaces de disolver la quitina [11], [12]. Por ejemplo, Phillips, Weiss & Tandler [21] detecta la lisozima en las glándulas salivales de las especies de murciélagos insectívoros y especuló que podría actuar como una enzima quitinolítico en la saliva. Sin embargo, lisozimas son principalmente anti-bacteriana y son una parte importante del sistema inmune [22] o para la digestión de las bacterias en los rumiantes [12].
Materiales y Métodos
almacenamiento de tejidos
= 14), Plecotus auritus gratis ( n
= 3), Myotis bechsteinii gratis ( n
= 1), Myotis nattereri gratis ( n
= 3), Myotis daubentonii gratis ( n
= 2) , Myotis Myotis
( n
= 1) y noctula leisleri gratis ( n
= 1)) se utilizaron en este estudio (Tabla 1) . Después de abrir la pared abdominal, se separó el tracto GI, se lava con 0,9% de NaCl, y se seca en papel de filtro. El tracto gastrointestinal fue dividido en el esófago, el estómago, el duodeno, yeyuno /íleon, íleon /colon y de colon /recto después de Ishikawa et al. [23] y se pesó en una balanza digital (EW2200-2NM, exactitud: 0,01 g; Kern & Sohn GmbH, Balingen, Alemania). Además, el estómago de un Mus musculus
(cepa C57BL /6, Negro 6; n
= 1). Se utilizó como control positivo para la detección AMCase por Western Blot
= 11), P. Auritus gratis ( n
= 3), M. bechsteinii gratis ( n
= 1), M. nattereri gratis ( n
= 3), M. daubentonii gratis ( n
= 2), M. miotis
( n
= 1) y N. leisleri gratis ( n
= 1) y el estómago de M. musculus
se molieron individualmente en un mortero con arena de mar extra-puro (Merck, Alemania) y NaCl (cantidad estandarizada de tejidos: 1 ml por 100 mg de tejido) 0,9%. Los homogenados se incubaron durante la noche a 4 ° C [10] y luego se centrifugó (20 min, 3500 g, 4 ° C). Los sobrenadantes se guardaron a -20 ° C hasta su posterior análisis
se utilizaron. Las zonas líticas se visualizaron usando transiluminación UV y se analizaron como antes. Además, los valores de pH de las secciones del tracto GI de cinco individuos de P. pipistrellus
se midieron usando papel de pH multicolor codificados (pH 0,0 a 6,0: Acilit, exactitud 0,5; pH 6,5 a 10,0: indicador especial, la exactitud 0,3; Merck).
), P. auritus gratis ( n
= 2), M. nattereri gratis ( n
= 1), M. miotis gratis ( n
= 1) y N leisleri gratis ( n
= 1); muestras de estómago adicionales:.. P pipistrellus gratis ( n
= 9), M. nattereri gratis ( n
= 1), M. daubentonii gratis ( n =
2)) y el estómago de un M. musculus
utilizado como control positivo [27] se sometieron a electroforesis de poliacrilamida con dodecilsulfato de sodio (SDS-PAGE) (Laemmli [28] modificado después de Sambrook, Fritsch & Maniatis [29]).
= 3). Las partes del tracto GI se fijaron en 4% de paraformaldehído en solución salina tamponada con fosfato (pH 7,0) durante 24 h antes de que se lavaron 4 x 1 h con TBS. A continuación, los bloques de tejido se deshidrataron en una serie de etanol (30%, 50%, 70%, 90%, 100%) y, finalmente, se incluyeron en parafina. Los bloques de parafina se cortaron en secciones de 4-9 micras de espesor utilizando un microtomo trineo (Leitz, Alemania) y se secaron durante la noche. Para conseguir los sitios de unión al antígeno accesibles, secciones de tejidos fueron predigeridas con pepsina (Sigma) después de Goto et al. [27]. Las secciones se lavaron con 0,01% de Tween 20 en TBS. Los sitios no específicos se bloquearon con 5% de suero de cabra (Merck) en 3% de BSA (AppliChem, Alemania). Las secciones se expusieron al anticuerpo policlonal de conejo dirigido contra el N-terminal de quitinasa ácida (Biología de Sistemas AVIVA; diluido 1:200 en TBS que contiene 1% de BSA) en una cámara húmeda. Los anticuerpos no unidos se eliminaron por lavado con TBS, antes de que el anticuerpo secundario (ChromeoTM 546, Abcam, UK; diluyó 1:2500 en 0,5% de BSA en TBS) se aplicó. Para las secciones de la contratinción nuclear se incubaron con 0,05% 4 ', 6-diamidino-2-fenilindol (DAPI) (AppliChem). Después de un aclarado final con TBS, las secciones se montaron con 1,4-diazabiciclo [2.2.2] solución octano (DABCO) (Sigma). Para el control de la autofluorescencia y la especificidad de unión de los anticuerpos, las secciones se procesan con isotiocianato de fluoresceína (FITC) anticuerpo secundario marcado pero sin anticuerpo primario. Las secciones fueron evaluados utilizando un microscopio de fluorescencia (Olympus BX60 F-3; Olympus Optical Co LTP, Alemania).
Resultados
y N. leisleri
cada uno (Tabla 2). No hay actividad quitinolítica se podría medir en el duodeno, yeyuno /ileon o muestras de íleon /colon. La actividad quitinolítica en las muestras de estómago fue más alta entre pH 5,0 y pH 6,0 (Fig. 2). Apoyando a nuestros resultados anteriores, no se detectó actividad quitinolítica en las otras regiones del tracto GI, independientemente del valor pH. El valor de pH medio del tracto GI de P. pipistrellus gratis ( n
= 5) fue de 5,6 ± 0,2 en el estómago, 7,0 ± 0,3 en el duodeno, 7,1 ± 0,2 en el yeyuno /íleon, 7,0 ± 0,2 en el íleon /colon y 7,0 ± 0,5 en el colon /recto.
estómago mostró una banda característica a un peso molecular relativo de 46 k, que indica la presencia de AMCase. Además, en todas las muestras de estómago de P. pipistrellus, P. auritus, M. nattereri
, M. miotis
, y N. leisleri
se identificó una banda de proteína clara a los 46 k (para imágenes representativas de Western blot, véase la Fig. 3 para Pipistrellus
y la Fig. 4 para Plecotus, Myotis
y noctula
). Esta banda de proteína no se detectó en el esófago, duodeno, yeyuno /íleon, íleon /colon o muestras de colon /recto de las especies de murciélagos (Fig. 3). Todos los resultados de inmunohistoquímica fueron controlados por la autofluorescencia y la unión inespecífica del anticuerpo acoplado a FITC secundario. secciones de estómago fueron positivos para el etiquetado de anticuerpos anti-AMCase, mientras que en el esófago, duodeno, yeyuno /íleon, íleon /colon y de colon /recto secciones no se detectó la unión. En las secciones de estómago, etiquetado anti-AMCase se limita a la parte inferior de las glándulas gástricas a lo largo de la mucosa gástrica alrededor de los núcleos celulares con DAPI manchado (Fig. 5).
Discusión
contiene sustituciones de aminoácidos que son necesarios para la adaptación al medio ácido del estómago [31]. Además, Boot et al. [17] demostraron que el ARNm AMCase de M. musculus
sólo se encuentra en el estómago. Si estas sustituciones de aminoácidos están presentes en el AMCase de las especies de murciélagos queda por demostrar.
[27], [31], [34]. Las células principales segregan enzimas digestivas [36] que se encuentran en los numerosos gránulos citoplasmáticos [37]. Una enzima común producido por este tipo de células gástrico es pepsinógeno, un precursor de la pepsina enzima proteolítica [38]. Goto et al. [27] demostraron que el lugar de producción de estómago AMCase de M. musculus
es en estos gránulos de secreción. Por lo tanto, lo más probable es que AMCase también es secretada por célula principal en especies de murciélagos. Esto es contrario a los resultados de Whitaker et al. [8], quien afirmó que la quitinasa en las especies de murciélagos es producida por cepas de bacterias productoras de quitinasa (en su mayoría de la familia Enterobacteriaceae) en el intestino. Se sabe que las bacterias intestinales producen quitinasa para satisfacer sus propias necesidades nutricionales [39]. Sin embargo, las enterobacterias quitinasa productoras también se puede encontrar en el tracto GI de los mamíferos que no se alimentan de material de quitina [19]. Esto sugiere que no existe una estrecha conexión entre la digestión quitina y bacterias quitinolíticas. En este estudio, se midió la baja actividad quitinolítica en los intestinos de sólo unos pocos individuos, y no se pudo detectar AMCase al separar el intestino desde el estómago. Esta actividad quitinolítica ocasional puede ser explicado por el transporte de la AMCase producido en el estómago en el intestino con la comida, como se comenta por Suzuki et al. [34] y Boot et al. [17]. Además, la actividad quitinolítica bajo en el intestino puede ser causada por las enterobacterias quitinasa productoras de [8]. Sin embargo, sería necesaria la cuantificación de estas bacterias para verificar la participación en la digestión de la quitina por estos simbiontes. Por lo tanto, es plausible que la quitina en las especies de murciélagos insectívoros es digerida por una combinación de estómago endógeno AMCase y quitinasa secretada por las bacterias intestinales, como fue sugerido por M. musculus
[17]. Este estudio demuestra claramente que los murciélagos insectívoros europeos de la familia Vespertilionidae tienen la enzima digestiva AMCase. Hemos demostrado que esta enzima es activa y se encuentra en el estómago, especialmente en o alrededor de las células principales en la base de las glándulas gástricas.
Reconocimientos
 La revista San Antonio nombra a cuatro gastroenterólogos de SAGA como los mejores médicos de 2020
La revista San Antonio nombra a cuatro gastroenterólogos de SAGA como los mejores médicos de 2020
 Un nuevo ensayo muestra una mejor supervivencia para los pacientes con cáncer colorrectal avanzado con mutación BRAF
Un nuevo ensayo muestra una mejor supervivencia para los pacientes con cáncer colorrectal avanzado con mutación BRAF
 Bacterias en el canal del parto relacionadas con menor riesgo de cáncer de ovario
Bacterias en el canal del parto relacionadas con menor riesgo de cáncer de ovario
 Suplementos y tu microbioma intestinal
Suplementos y tu microbioma intestinal
 Los problemas gastroenterológicos pueden ser una desventaja para la cirugía para bajar de peso
Los problemas gastroenterológicos pueden ser una desventaja para la cirugía para bajar de peso
 La microbiota rural y urbana se diferencia de una edad temprana,
La microbiota rural y urbana se diferencia de una edad temprana,
 Prueba de ADN:¿Se puede comprobar si hay intolerancia al gluten?
Nuestra prueba de ADN comprueba la predisposición genética a la intolerancia al gluten. Esto es lo que necesita saber al respecto. Nuestro departamento de atención al cliente recibe una gran cantidad
Prueba de ADN:¿Se puede comprobar si hay intolerancia al gluten?
Nuestra prueba de ADN comprueba la predisposición genética a la intolerancia al gluten. Esto es lo que necesita saber al respecto. Nuestro departamento de atención al cliente recibe una gran cantidad
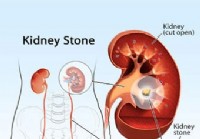 Los primeros signos de cálculos renales (nefrolitiasis)
Ilustración de riñones y cálculos renales. Datos sobre los cálculos renales Un cálculo renal es un material mineral cristalino duro que se forma dentro del riñón o del tracto urinario. Nefrolitiasis
Los primeros signos de cálculos renales (nefrolitiasis)
Ilustración de riñones y cálculos renales. Datos sobre los cálculos renales Un cálculo renal es un material mineral cristalino duro que se forma dentro del riñón o del tracto urinario. Nefrolitiasis
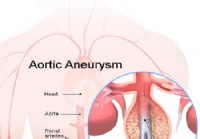 Aneurisma aórtico abdominal
Datos que debe saber sobre los aneurismas de aorta abdominal Imagen de stent injertado para reparar un aneurisma aórtico abdominal ¿Cuál es la definición médica de aórtica aneurisma? Un aneurism
Aneurisma aórtico abdominal
Datos que debe saber sobre los aneurismas de aorta abdominal Imagen de stent injertado para reparar un aneurisma aórtico abdominal ¿Cuál es la definición médica de aórtica aneurisma? Un aneurism