In qualità di pioniere nella tecnologia della piattaforma di dialisi enterica, La missione di Kibow® Biotech è sempre stata associata alla cura standard della terapia. Il prodotto integratore per la salute dei reni dell'azienda è stato sviluppato per supportare la normale funzione renale che può aiutare a rallentare la progressione della funzione renale in tutte le fasi della malattia renale cronica (CKD) e potenzialmente aiutare un risultato migliore per i pazienti in dialisi in tutto il mondo.
Kibow® Biotech Inc è orgogliosa di annunciare che durante i suoi 22 anni di attività, l'attenzione sul supporto e il mantenimento di una sana funzione renale con probiotici/prebiotici per ritardare potenzialmente la progressione verso la dialisi si basa sulla sua tecnologia della piattaforma di riduzione delle tossine enteriche denominata "Dialisi enterica®". Dal 2005, Kibow® è stato un pioniere e leader nel prodotto integratore per la salute dei reni attualmente commercializzato, Renadyl™*.
Kibow® ha partecipato ed esposto a vari incontri annuali di nefrologia e professionisti medici, come l'American Society of Nephrology (ASN), Fondazione nazionale per i reni (NKF), Associazione americana dei pazienti renali (AAKP), World Congress of Nephrology (WCN) e diverse altre conferenze mediche professionali dal 2005.
La partecipazione di Kibow®Biotech a questi eventi ha lo scopo di educare la nefrologia e tutti gli altri professionisti medici sull'importanza emergente e sul ruolo cruciale dei probiotici/prebiotici, connessione intestino-rene, disbiosi, e modulazione del Microbioma Intestinale con la sua innovativa piattaforma tecnologica "Enteric Dialysis®".
Kibow® si impegna a migliorare la salute dei reni nei pazienti con problemi renali, non solo per gli americani ma in tutti i paesi del mondo. Sebbene commercializzato e venduto come integratore alimentare, Renadyl™ è il primo e unico integratore per la salute dei reni sviluppato e formulato sulla base di risultati clinici che utilizzano la tecnologia brevettata e rivoluzionaria "Enteric Dialysis®" di Kibow® Biotech.
Anche prima dell'annuncio del presidente Trump, Kibow® Biotech ha preso provvedimenti per raggiungere e migliorare la vita di più pazienti diversificando Renadyl™ da integratore per la salute a un nuovo farmaco bioterapeutico vivo (microrganismi) e ottenendo l'approvazione come nuovo prodotto farmaceutico. Come farmaco umano approvato dalla FDA, Renadyl™ potrà essere commercializzato sulla base di specifiche indicazioni sui benefici per la salute che dovrebbero portare a una maggiore accettazione da parte degli operatori sanitari.
Inoltre aprirà la strada al suo rimborso medico e potrebbe comportare una riduzione dei costi di co-pagamento, sia da parte degli assicuratori privati che dalle autorità federali di Medicare/Medicaid. Oltre a mantenere la normale funzione renale e a rallentare la progressione della malattia renale, l'obiettivo sarebbe quello di ritardare la necessità di costosi, terapia dialitica fisicamente e mentalmente gravosa.
Come prodotto farmaceutico LBP, Renadyl™ può anche essere potenzialmente utile per ridurre la durata o la frequenza della dialisi con un miglioramento significativo della qualità della vita e aiutare a risparmiare diversi miliardi di dollari spesi non solo negli Stati Uniti ma in tutto il mondo.
Kibow® ha già avviato la domanda di pre-investigazione del nuovo farmaco (IND) e successivamente continuerà con il processo di domanda IND con il Center for Biological Evaluation Research (CBER) della FDA degli Stati Uniti per la sua formulazione migliorata di probiotici/prebiotici Renadyl™ come prodotto farmaceutico LBP.
Per ottenere l'approvazione del farmaco, A Kibow sarà richiesto di eseguire in modo ben controllato, test clinici randomizzati di efficacia e sicurezza. Kibow® ha pianificato il "Kibow® Hope Study", un multisito, Studio randomizzato controllato (RCT) su pazienti con CKD negli stadi III e IV.
Lo studio Kibow® Hope RCT proposto coinvolgerà circa 600 pazienti distribuiti in 20-25 ospedali/cliniche. L'azienda intende eseguire questo RCT multi-sito con la collaborazione di esperti ricercatori di studi clinici negli Stati Uniti presso le rispettive cliniche/istituzioni/ospedali. Studi clinici simili saranno proposti e intrapresi anche in molti altri paesi.
Per di più, è noto che il 40% dei pazienti con CKD soffre anche di gotta a causa di livelli più elevati di acido urico. Kibow® ha sviluppato un prodotto integratore alimentare che agisce per mantenere normali livelli di acido urico nel sangue, Gli studi sugli animali hanno dimostrato che il prodotto riduce le concentrazioni di acido urico e stabilizza anche la pressione sanguigna.
L'azienda sta effettuando studi clinici in aperto approvati dall'Institutional Review Board (IRB) per monitorare endpoint simili in soggetti umani. Successivamente, Kibow® prevede di esplorare il potenziale di un altro processo IND con la FDA/CBER statunitense e di richiedere l'approvazione della FDA per le applicazioni di gotta/iperuricemia. Tutti i prodotti Kibow® sono stati sviluppati sulla base della selezione di ceppi probiotici specifici per applicazioni rispettivamente di CKD e gotta.
Dottor Ranganathan, il fondatore e scienziato chiave di ricerca e sviluppo di Kibow® afferma,
L'uso di vari prodotti probiotici e prebiotici (fibre) come integratori alimentari sta guadagnando un maggiore interesse pubblico nei bambini e negli adulti per l'apparato digerente, immune, e la salute dell'intestino. Sono generalmente riconosciuti come sicuri (GRAS) dalla FDA statunitense. Renadyl™ come integratore per la salute dei reni è stato presentato ai consumatori statunitensi nel 2010 e successivamente esportato in vari paesi d'oltremare.
"Nessun evento avverso grave è stato notificato alla società o alla FDA statunitense dopo l'uso umano di Renadyl™ negli ultimi nove anni. Questa esperienza di mercato fornisce supporto per la sicurezza di Renadyl™ per applicazioni per la salute dei reni.
Kibow® è stata in prima linea nell'aver sviluppato e validato scientificamente il concetto di "DIALYSIS ENTERICA®" con il suo prodotto di punta Renadyl™. I professionisti medici e un'ampia base di clienti istruiti sono sempre alla ricerca e pronti ad adattarsi a un Trattamento naturale scientificamente fondato."
Il commento su invito del Dr. Ranganathan intitolato Reality of "Enteric Dialysis®" with Probiotics and Prebiotics to Delay the Need of Conventional Dialysis pubblicato nel Journal of Nephrology &Therapeutics nel 2018 è accessibile qui.
Ulteriori aggiornamenti saranno resi disponibili durante il prossimo meeting dell'American Society of Nephrology Kidney Week (5-10 novembre, 2019) a Washington DC dove Kibow® partecipa come espositore da 15 anni
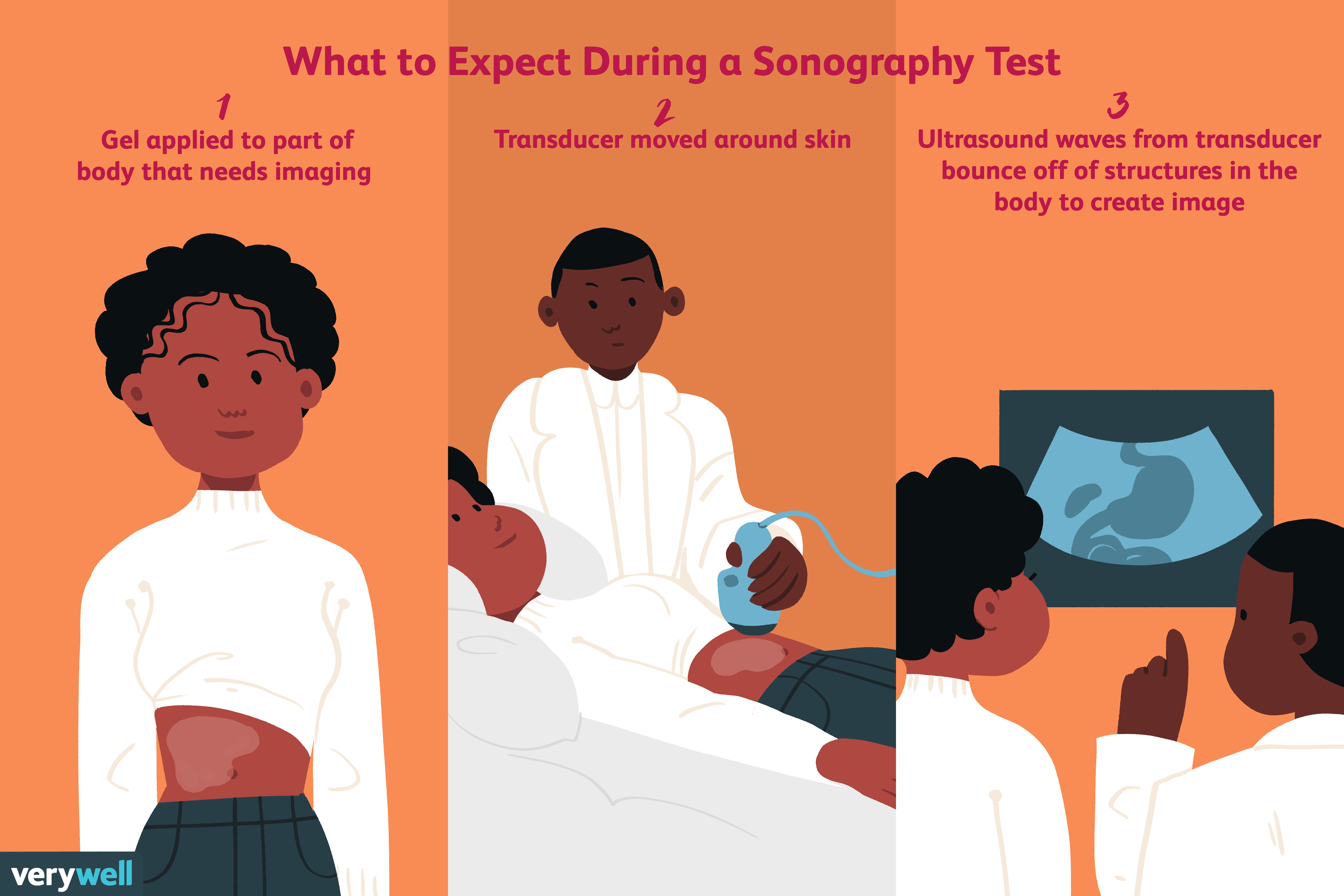 Che cos'è l'ecografia?
Che cos'è l'ecografia?
 Cosa c'è da sapere su SIBO – Parte 2
Cosa c'è da sapere su SIBO – Parte 2
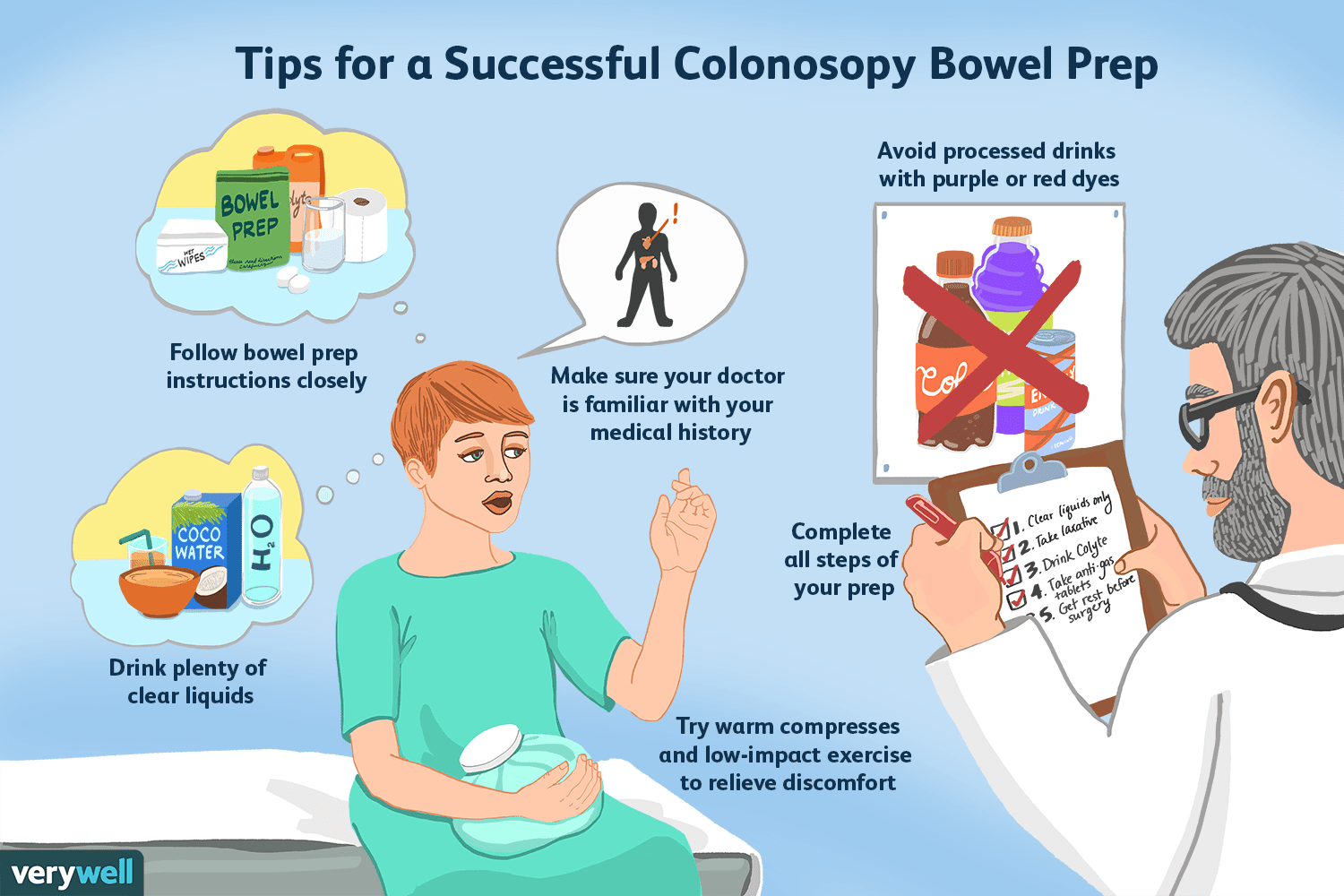 Come sapere quando la preparazione intestinale è completa
Come sapere quando la preparazione intestinale è completa
 Ridurre questi tipi di alimenti può aiutarti a ridurre notevolmente il verificarsi di reflusso acido
Ridurre questi tipi di alimenti può aiutarti a ridurre notevolmente il verificarsi di reflusso acido
 9 benefici per la salute del butirrato per il corpo e l'intestino
9 benefici per la salute del butirrato per il corpo e l'intestino
 Tutto su tutti gli sfinteri nel tuo corpo
Tutto su tutti gli sfinteri nel tuo corpo
 Scienziato dimostra il ruolo del microbioma nell'obesità
Nuova ricerca presentata dal Dr. Christoph Thaiss nel suo pluripremiato saggio per il “ Scienza e SciLifeLab Prize for Young Scientists” descrive diversi metaboliti batterici nellintestino umano che
Scienziato dimostra il ruolo del microbioma nell'obesità
Nuova ricerca presentata dal Dr. Christoph Thaiss nel suo pluripremiato saggio per il “ Scienza e SciLifeLab Prize for Young Scientists” descrive diversi metaboliti batterici nellintestino umano che
 Feocromocitoma
Fatti che dovresti sapere sul feocromocitoma Qualcuno con un feocromocitoma di solito ha tre sintomi classici:mal di testa, sudorazione e palpitazioni cardiache (un battito cardiaco accelerato) in as
Feocromocitoma
Fatti che dovresti sapere sul feocromocitoma Qualcuno con un feocromocitoma di solito ha tre sintomi classici:mal di testa, sudorazione e palpitazioni cardiache (un battito cardiaco accelerato) in as
 Come evitare il cancro al colon
La colonscopia è il gold standard per lo screening del cancro del colon-retto che consente al dottor Yamini di eseguire unispezione di cura allinterno del colon. Innumerevoli studi hanno dimostrato ch
Come evitare il cancro al colon
La colonscopia è il gold standard per lo screening del cancro del colon-retto che consente al dottor Yamini di eseguire unispezione di cura allinterno del colon. Innumerevoli studi hanno dimostrato ch