Abstrakt
Hintergrund
Assoziierte
Interleukin-32 (IL-32) ist ein kürzlich entdecktes proinflammatorische Zytokin bei entzündlichen beteiligt Krankheiten. Wir untersuchten die Expression von IL-32 und dessen Regulationsmechanismus in der Entzündungsreaktion von Patienten mit Helicobacter pylori IL-32-mRNA und Protein-Expression im Magengewebe wurde durch quantitative Echtzeit-PCR und Immunhistochemie nachgewiesen. Die Regulation der IL-32 in humanen AGS Magen-Epithelien Zelllinie wurde durch verschiedene Zytokinstimulation untersucht und verschiedene H. pylori Ergebnisse | Magen-IL-32-mRNA und Protein-Expression wurden bei Patienten erhöht mit H. pylori Schlussfolgerungen IL-32-Ebene bei Patienten erhöht ist, mit H . pylori Infektion Citation:. Peng L-s, Zhuang Y, Li W-h, Zhou Y-y, Wang T-t, Chen N, et al. (2014) Erhöhte Interleukin-32 Expression ist im Zusammenhang mit Helicobacter pylori Editor: Ivo G. Boneca, Institut Pasteur Paris, Frankreich Empfangen: 24. August 2013; Akzeptiert: 8. Januar 2014; Veröffentlicht: 14. März 2014 Copyright: © 2014 Peng et al. Dies ist eine Open-Access-Artikel unter den Bedingungen der Lizenz Creative Commons, die uneingeschränkte Nutzung erlaubt, die Verteilung und Vervielfältigung in jedem Medium, vorausgesetzt, der ursprüngliche Autor und Quelle genannt werden Finanzierung:. Diese Arbeit wurde durch Zuschüsse aus dem Medical Science Jugendausbildungsprojekt der chinesischen Volksbefreiungsarmee (13QNP108) und nationale Grundlagenforschung Programm von China (973 Programm, No. 2009CB522606) unterstützt. Die Geldgeber hatten keine Rolle in Studiendesign, Datenerfassung und Analyse, Entscheidung oder Vorbereitung des Manuskripts zur Veröffentlichung Konkurrierende Interessen:.. Die Autoren haben erklärt, dass keine Interessenkonflikte bestehen Einführung Helicobacter pylori H. pylori IL-32 ist ein neu proinflammatorische Cytokin identifiziert durch Immunzellen (NK-Zellen, T-Zellen, Monozyten) erzeugt und nicht-immune Zellen (Endothelzellen , Epithelzellen) [5] - [7]. Es wurde ursprünglich als ein durch IL-2 induzierte Gen kloniert und NK-4, genannt, aber seine Funktion war unbekannt, bis 2005 [5], [8]. Es gibt sechs Splice-Varianten einschließlich IL-32α, β, γ, δ, ε und ζ und diverse Rollen sind möglicherweise durch seine verschiedenen Isoformen gespielt. Jedoch wurde ein spezifischer Rezeptor für IL-32 nicht gefunden worden, obwohl neutrophil Proteinase 3 bindet an IL-32 mit hoher Affinität [9]. IL-32 spielt eine wichtige Rolle bei verschiedenen entzündlichen Erkrankungen und seine Expression wurde mit der Schwere der Krankheiten, bei rheumatoider Arthritis, Morbus Crohn und atopische Dermatitis [10] korreliert - [12]. Außerdem IL-32 hatte in einigen Infektionskrankheiten einschließlich H impliziert worden. pylori In der vorliegenden Studie haben wir festgestellt IL -32-Expression in Biopsien von Patienten mit H. pylori Materialien und Methoden Ethik Statement Human Magenschleimhaut Biopsien durch Routine Endoskopie am Xinqiao Krankenhaus des Dritten Military Medical University gesammelt wurden . Blut wurde aus dem gleichen Thema erhalten, die unterzog Endoskopie für H. pylori Themen Magen-Gewebe und Blut von 54 Patienten gesammelt wurden. (Männlich /weiblich = 27/27, Durchschnittsalter 47 ± 1,2 Jahre) mit H. pylori Biopsien und Histologie Bewertung Biopsie-Proben wurden von den Testpersonen bei jeder Endoskopie entnommen. Einer wurde sofort in flüssigem Stickstoff eingefroren und bei -80 ° C für die RNA-Extraktion gelagert. Der Rest von Biopsien wurden in Formalin und in Paraffin eingebettet. Hämatoxylin-Eosin (H & E) gefärbten Schnitte wurden von zwei erfahrenen histopathologist sucht. Die histologische Schwere der Gastritis wurde von normal bis schwerer abgestuft basierend auf der Dichte von einkernigen infiltrieren und polymorphkernigen Zellen nach den festgelegten Kriterien [17], [18]. Die Magen epithelialen Linie AGS (ATCC, American Type Culture Collection) wurde bei 37 ° C und 5% CO 2 in Ham-F12 (Hyclone, Logan, UT, USA) kultiviert, das 10% fötales Kälberserum (FCS) enthielt. AGS Die Zellen wurden bei einer Dichte von 1 in Sechs-Well-Platten ausgesät × 10 6 Zellen /Vertiefung und stimuliert mit 10 ng /ml TNF-α oder /und 10 ng /ml IL-1β (PeproTechs, Rocky Hill, NJ , USA); Zellen wurden zu den angegebenen Zeiten für die Analyse der IL-32-mRNA und Proteinexpression gesammelt. Für den Signalweg Inhibitionstest NF-kappaB-Inhibitor (BAY 11-7082), MEK1 /2-Inhibitor (U0126), p38 /MAPK-Inhibitor (SB203580), JNK-Inhibitor (SP600125), Inhibitor JAK I (alle bei 10 &mgr; M und alle von Calbiochem, San Diego, CA, USA) oder dem Fahrzeug DMSO (Sigma, St. Louis, MO, USA) wurden zu der Zellkultur 1 Stunde vor der Cytokin-Stimulation hinzugefügt. die Infektion von Zellen mit AGS H. pylori H. pylori RNA aus Biopsien oder Zellen durch TRIzol reagent® (Invitrogen, Carlsbad, CA, USA) und revers transkribiert in cDNA unter Verwendung von ReverTra Ace (Toyobo, Osaka extrahiert wurde, Japan). Quantitative real-time PCR wurde durch das iQ5 Detection System (Bio-Rad, USA) durchgeführt. Die PCR-Primer entworfen wurden, eine Exon-Intron-Grenze zu überschreiten und verwendet, um die mRNA-Expression von IL-32, TNF-α, IL-1β und β-Actin und ihre Sequenzen zu erkennen sind wie folgt: IL-32, nach vorne, 5 ' -ACGACTTCAAAGAGGGCTACC-3 '; umkehren, 5'-GCCTCGGCACCGTAATCCAT-3 '; TNF-α, vorwärts, 5'-TCTCTAATCAGCCCTCTGGC-3 '; umkehren, 5'-ATGAGGTACAGGCCCTCTGA-3 '; IL-1β, vorwärts, 5'-GTTCTTTGAAGCTGATGGCC-3 '; umkehren, 5'-GTGGTCGGAGATTCGTAGCT-3 '; β-Actin, vorwärts, 5'-TTCCTTCCTGGGCATGGAGTCC-3 '; umkehren, 5'-TGGCGTACAGGTCTTTGCGG-3 '. β-Actin wurde als interne Kontrolle verwendet. Die relative Genexpression wurde als fache Änderung der ΔΔCt-Methode berechnet. Vierzig in Paraffin eingebetteten Proben in 5-um-Schnitte geschnitten wurden. Nachdem sie in einem Mikrowellenofen und mit 3% Wasserstoffperoxid entparaffiniert und hydratisiert wurden die Schnitte in Citrat-Puffer (pH = 6,0) unterworfen induzierten Wärmerückgewinnung Antigen. Nach der Inkubation mit Kaninchen-anti-human IL-32 (Abcam, MA, USA) über Nacht bei 4 ° C, Objektträger wurden mit Meerrettich-Peroxidase konjugierten sekundären Anti-Kaninchen-Antikörper behandelt (Zhongshan Golden Bridge Biotech., Beijing, China), gefolgt von Substrat 3,3'-Diaminobenzidintetrahydrochlorid (DAB). Isotyp-Antikörper wurde als Negativkontrolle verwendet. Bilder wurden auf einem Mikroskop erworben ausgestattet mit einer digitalen Kamera Nikon Eclipse-80i (Tokyo, Japan). Für semi-quantitative Analyse der Immunhistochemie wurde jeder Abschnitt für die Bewertung IL-32-Immunfärbung im Magengewebe ausgewählt und bewertet wurde wie folgt: 0 punkten, keinen Ausdruck; Note 1, geringe Expression; Note 2, Zwischen Ausdruck; Note 3, hohe Expression. Western Blot Die Zellen wurden in eiskaltem PBS gewaschen und dann in Lysepuffer gestört (20 mM Tris, pH 7,5, 150 mM NaCl, 1 mM EDTA, 1 mM EGTA, 1% Triton X-100, 2,5 mM Natriumpyrophosphat, 1 mM Glycerophosphat, 1 mM Na3VO4, 1 &mgr; g /ml Leupeptin und Protease-Inhibitor). Die Proteinkonzentration wurde mit einem BCA-Protein-Assay-Kits (Boster, Wuhan, China) gemessen. Zelllysate wurden durch 12% SDS-PAGE getrennt und auf eine Polyvinylidendifluorid-Membran transferiert. Die Membranen wurden für 1 h mit 3% Rinderserumalbumin in Tris-gepufferter Kochsalzlösung-Tween bei Raumtemperatur blockiert und dann über Nacht bei 4 ° C mit Kaninchen-anti-human IL-32 (Abcam, MA, USA) oder Maus-anti- inkubiert menschlichen β-Aktin ((Tianjin Sungene Biotech Co., Ltd., China). Horseradish Peroxidase-konjugierten sekundären Antikörpers verwendet wurde gemäß den instructures des Herstellers. Die Proteine von Interesse wurden durch die Verwendung Supersignal® West-Dura Dauer Substratreagenz (Thermo, IL visualisiert USA,). statistische Analyse Alle Ergebnisse wurden als Mittelwert ± Standardfehler des Mittelwertes (SEM) zusammengefasst, und die statistische Analyse wurde durchgeführt, die GraphPad Prism 5.0-Software. die Unterschiede zwischen zwei . Gruppen, die durch den Mann-Whitney U-Test und mehrere Gruppen analysiert wurden durch eine Einwegvarianzanalyse (ANOVA) analysiert wurden, wenn Abweichungen festgestellt wurden, wurde Spearman-Korrelation verwendet, um den Grad der Assoziation zwischen Variablen auszuwerten P. < 0,05 galt statistisch signifikant. Ergebnisse | Erhöhte IL-32-mRNA-Spiegel in Patienten gefunden mit H. pylori-Infektion Um zu untersuchen, ob IL-32 in der Pathogenese von H beteiligt ist. pylori IL-32-Expression in Magen-Biopsie-Proben, die immunhistochemische Färbung von IL-32 wurde auf in Paraffin eingebetteten Gewebe durchgeführt, um zu visualisieren. Wie in gezeigt. 2B ein paar von IL-32-produzierenden Zellen wurden in H detektiert. pylori IL-32-mRNA und Protein-Ebene wurden nach oben reguliert durch TNF-α und IL-1β Weil wir eine positive Beziehung zwischen IL gefunden -32 mRNA-Spiegel und der Grad der Magenentzündung in Magengewebe und Korrelation zwischen IL-32 mRNA und IL-1β und TNF-α mRNAs wurde die Regulation von proinflammatorischen Zytokinen auf IL-32-mRNA-Expression in AGS-Zellen untersucht. Wie in gezeigt. 3A, nach 24 Stunden mit Zytokinen behandelten, IL-32 mRNA-Ebene war signifikant hochreguliert: 5,0 ± 0,5-fache durch TNF-α, 6,9 ± 0,5-fache durch IL-1β und 11,2 ± 1,4-fachen von IL-1β und TNF-α. Dieser Effekt war völlig abhängig von NF-kappaB Signalweg als Vorbehandlung mit NF-kappaB-Hemmer BAY 11-7082, aber nicht JNK, p38 /MAPK, MEK1 /2 oder JAK /STAT-Signal Inhibitoren gehemmt, die Induktion von IL-32-mRNA nach Stimulation durch TNF-α oder IL-1β (Fig. 3C). Darüber hinaus bestätigte Western blot, dass IL-32 Proteinebene auch von TNF-α und /oder IL-1β-Stimulation, die hing von NF &kgr; B-Signalwegs (Fig. 3B und D) induziert wurde. Wir untersuchten als nächstes, ob TNF-α oder IL-1β wurde in H beteiligt. pylori H. pylori Zur weiteren Untersuchung der unmittelbaren Wirkung von H. pylori auf die Expression von IL-32 in Magenepithelzellen Diskussion In der vorliegenden Studie haben wir festgestellt, dass Magen-IL-32 signifikant bei Patienten erhöht wurde mit H . pylori IL-32 vor kurzem als proinflammtory Faktor in vielen entzündlichen Erkrankungen wie chronische Rhinosinusitis beteiligt beschrieben wurde, ein Zustand, meist durch gram-positive Bakterien-Infektion [19], [20] verursacht. Erhöhte IL-32 wurde dann in HCV und HBV-infizierten Leber gemeldet und mit der Schwere der Leberentzündung und Leberfibrose zu korrelieren [15], [21]. In dieser Studie haben wir gezeigt, dass IL-32-mRNA-Spiegel bei Patienten mit H signifikant erhöht wurde. pylori Die klassische Magenentzündung mit H. pylori Unsere Ergebnisse zeigten auch, dass die IL-32 mRNA und Protein-Niveau in einer dosisabhängigen Weise erhöht wurden folgende H. pylori Abschließend unsere Daten zeigten, dass IL-32-Expression mit H bei Patienten erhöht wurde. pylori Grundinformationen
( H. Pylori
) Infektion.
Design und Methoden
Stamm-Infektion.
Infektion und positiv mit Gastritis korreliert. In H. pylori
infiziertem Patienten, die mRNA-Ebene von IL-32 wurde auch mit der proinflammatorischen Zytokine IL-1β und TNF-α korreliert. In-vitro-
IL-1β und TNF-α könnte IL-32-mRNA und Protein-Ebene in AGS-Zellen upregulate, die auf NF-kappaB Signalweg abhängig war. Die Regulation der IL-32-Expression in Reaktion auf H. pylori -Infektion
könnte durch Verwendung von neutralisierenden Antikörpern geschwächt werden IL-1β und TNF-α zu blockieren. Außerdem H. pylori
infiziertem AGS-Zellen auch IL-32-mRNA und Protein-Expression induziert, die auf CagA abhängig war.
und seine Expression wird durch proinflammatorische Stimuli reguliert, was nahe legt, dass IL-32 eine Rolle bei der Pathogenese von H spielen. pylori
-related Gastritis
-related Gastritis. PLoS ONE 9 (3): e88270. doi: 10.1371 /journal.pone.0088270
( H. pylori
) ist ein Gram-negative, microaerophilic Bakterium, das weltweit in den Magen von etwa 50% der Bevölkerung kolonisiert. Die persistierende Infektion von H. pylori
chronische und anhaltende Gastritis verursacht und erhöht das Risiko von Magengeschwüren und Magenkrebs.
infizierten Magenschleimhaut durch die Infiltration von Immunzellen und die Produktion von Entzündungsfaktoren charakterisiert. Th1 und Th2-Antwort wird berichtet, dass Immunantwort auf H vermitteln. pylori
und Th1-Antwort gedacht wird, vorherrschend zu sein [1]. Dann Induktion von Th17 Reaktion in H. pylori
infiziertem Magen bestätigt wird [2]. Neben Th1, Th2 und Th17-Zellen, regulatorische T-Zellen (Tregs) auch eine wichtige Rolle in H spielen. pylori
-bezogene Gastritis [3]. Inzwischen haben proinflammtory Zytokinen wie IL-1β, TNF-α und IL-6 auch in H erhöht werden, wurde gezeigt. pylori
-infizierten Magen [4], und diese Cytokine könnten T-Zell-Immunantwort bei entzündlichen Erkrankungen beeinflussen, was darauf hindeutet, dass Entzündungsfaktoren in entscheidender Bedeutung sein können H. pylori
-related Magenentzündung. Jedoch hat der genaue Mechanismus des Verfahrens nicht vollständig aufgeklärt worden.
Infektion [13] - [16]. Allerdings ist der Zusammenhang zwischen IL-32-Expression und H. pylori
-induzierte Gastritis und seine genaue Regelmechanismus einschließlich ob auto- /parakrine Effekte auf die Expression von IL-32 kann in den Prozess einbezogen werden, war noch unbekannt.
Infektion und analysiert die Beziehung zwischen Magen-IL-32-Ebene und der Schwere der Schleimhautentzündung. Anschließend erkundeten wir die Auswirkungen von proinflammatorischen Stimuli und H. pylori
Infektion auf die IL-32-Expression in humanen Linien Magen-Epithelien Zelle. Unsere Ergebnisse zeigten, dass IL-32 kann in der Pathogenese von H beteiligt sein. pylori
-related Gastritis.
Serologie-Test. Die Studie wurde von der Ethikkommission der Xinqiao Krankenhaus, Third Military Medical University genehmigt. Eine schriftliche Einverständniserklärung wurde von jeder Person erhalten
Infektion, die Endoskopie am Xinqiao Krankenhaus des Dritten Military Medical University unterzog. H. pylori
Infektion durch eine rasche-Urease-Test, Serologie-Test bestätigt, 13C-Harnstoff-Atemtest und Histologie. Die Patienten wurden als H eingestuft. pylori
positiv, wenn zwei der vier Tests positiv waren. Normale Magengewebe von 47 Probanden (männlich /weiblich = 23/24, Durchschnittsalter 47 ± 1,3 Jahre)., Die für alle vier Tests negative Ergebnisse hatten, wurden als Kontrollen eingeschrieben
Cell Culture
11637 Stamm und seine isogene CagA-negativen Mutantenstamm (CagA - Stamm) wurden auf Hirn-Herz-Infusions-Platten mit 10% Kaninchenblut bei 37 ° C unter mikroaerophilen Bedingungen (5% O 2 gewachsen CO, 10% 2, 85% N 2). H. pylori
wurde die Kulturplatten mit PBS gewaschen und zentrifugiert bei 2500 × g für 5 min, bevor sie resuspendiert in PBS für die optische Dichte Quantifizierung bei 600 nm (1 OD 600 = 1 × 10 9 abgewaschen H. pylori
/ml). Eine Multiplizität der Infektion (MOI) von 1, 10 und 100 wurde zur Infektion von AGS-Zellen verwendet. Für Neutralisationstests wurde in der Co-Kultur-System hinzugefügt Antikörper gegen TNF-α (nTNF-α, 1 &mgr; g /ml, BioLegend) oder IL-1β (NIL-1β, 1 &mgr; g /ml, eBioscience) Neutralisieren.
RNA-Isolierung und quantitative Real-time PCR
Immunhistochemie
Gastritis induziert wird, wir die IL-32-mRNA-Expression in Magen-Biopsien von Patienten mit und ohne H zuerst bestimmt. pylori
Infektion. Wie in gezeigt. 1A, IL-32-Expression war signifikant höher in H. pylori
-positiven Proben als in H. pylori
-negativen Proben (P < 0,001). Zu beurteilen, ob die Expression von IL-32 mit dem Grad der Entzündung im Zusammenhang wurde in H. pylori
infiziertem Magenproben, teilten wir die Proben in normalen und mild, mittelschwerer und schwerer Gastritis Gruppen auf der Grundlage Beurteilung Histologie, wie in Materialien und Methoden beschrieben. Die Ergebnisse zeigten, dass IL-32-mRNA-Spiegel in H. pylori
-positive Proben waren positiv mit dem Grad der Magenentzündung (Fig. 1B) korreliert. Darüber hinaus zeigte die Höhe der IL-32-mRNA auch eine positive Korrelation mit TNF-α und IL-1β-mRNA-Spiegel (Fig. 1C).
erhöhte IL-32-Proteinexpression in Patienten mit H. pylori-Infektion
-ausschließend Magengewebe, während in H. pylori -positiven
Magengewebe wurde beobachtet, dass IL-32-Protein-Expression wurde signifikant erhöht (Fig. 2C). Darüber hinaus bestätigte die semi-quantitative Bewertung der IL-32-Immunreaktivität dass die Expression von IL-32 in Magengewebe von H. pylori
infiziertem Patienten auf Proteinebene wurde ebenfalls deutlich erhöht im Vergleich zu denen in H. pylori
-ausschließend Magengewebe und in milden Gastritis.
-induzierte upregulation von IL-32-Expression. AGS-Zellen wurden mit H infiziert. pylori
und gleichzeitig mit neutralisierenden Antikörpern zu blockieren TNF-α oder IL-1β behandelt. Wie in gezeigt. 3E, H
. pylori
-induzierte IL-32-Protein-Expression wurde signifikant verringert durch Zytokine-blockierende Antikörper mit angegeben.
-induzierte IL-32 Expression
wurden AGS-Zellen mit H infiziert. pylori
bei einer MOI von 1, 10 und 100. Wie in Fig. 4A und B, IL-32 mRNA und Proteinmengen wurden nach H erhöht. pylori
Infektion in einer dosisabhängigen Weise. Wir analysierten als nächstes, ob H. pylori
Stamm Unterschiede würden auf unterschiedliche Expression von IL-32 bei. Die Zellen wurden mit H infiziert. pylori 11637
Stamm und CagA - Stamm. Obwohl CagA - Stamm-Infektion erhöhte sich leicht um die Expression von IL-32 in AGS-Zellen, die Induktion von IL-32-mRNA und Protein-Ebene von CagA - Stamm-Infektion war signifikant niedriger als die von H. pylori 11637
Stamm-Infektion (Abb. 4C und D).
bei Infektion sowohl mRNA und Protein-Ebene. Die erhöhte IL-32-mRNA-Ebene mit der Schwere der Magenentzündung korrelierten. Zusätzlich wurden IL-32-mRNA-Spiegel auch mit TNF-α und IL-1β-mRNA-Spiegel in H korreliert. pylori
positive Magen-Biopsie-Proben, und eine der beiden Zytokine konnte die IL-32-mRNA und Protein-Ebene upregulate. Darüber hinaus fanden wir, dass H. pylori
Infektion von Magen-epithelialen Zell-Linien auch IL-32-mRNA und Protein-Expression induziert. Diese Ergebnisse zeigen, dass IL-32 wahrscheinlich im Magen-Entzündung von Patienten mit H beteiligt ist. pylori
Infektion.
Infektion und eine hohe Korrelation zwischen IL-32-mRNA-und Magen-Entzündung wurde auch beobachtet, was darauf hindeutet, dass IL-32 in eine wichtige Rolle spielen können H. pylori
infizierten Magen. Darüber hinaus wurde die Immunhistochemie verwendet, um die Quelle von IL-32 und führt zu detektieren zeigten, dass IL-32 in Magen-Epithelzellen und seine hoch Ausdruck ausgedrückt wurde, wurde in H beobachtet. pylori
positivem Magengewebe. Weil IL-32 war die Produktion von IL-8 in Magenepithelzellen zu induzieren und hemmte die proangiogenic Faktor VEGF-Sekretion von bronchialen Epithelzellen [16], [22], und wir haben auch beobachtet, IL-32 mRNA-Ebene gefunden wurde positiv korreliert mit IL-8-Expression (Daten nicht gezeigt). Es ist vernünftig, dass IL-32 die Funktion von Magen-Epithelzellen in H beeinflussen. pylori
infizierten Magen.
Infektion durch Infiltrieren Immunzellen und inflammatorische Zytokine beeinflußt werden können, umfassen die später kann die kürzlich entdeckten IL-32 [19] - [22]. In unserer Studie fanden wir, dass in vitro TNF-α und /oder IL-1β AGS Zellen stimuliert IL-32 mRNA und Proteinexpression hochzuregulieren, die eine positive Beziehung zwischen IL-32 unterstützt und TNF-α und IL-1β in vivo . Jedoch Th17 Cytokin (IL-17A, IL-17F, IL-6), Th2 Zytokine IL-4, Treg Cytokins TGF-β1 und Th1 Zytokin IFN-y alle versagt IL-32 mRNA und Proteinexpression in unserem System zu induzieren, obwohl alle relevanten Immunzelltypen und Zytokine wurden berichtet zu infiltrieren H. pylori
infizierten Magen (siehe Abbildung S1). Diese Ergebnisse legten nahe, dass IL-32 wahrscheinlich vor der Infiltration dieser Zellen produziert wird, die durch den Bericht gestützt, dass IL-32 induziert Reifung dendritischer Zellen und fördert die Th1 und Th17 Polarisations [23]. Darüber hinaus wurde die Induktion von IL-32 mRNA und Protein durch TNF-α oder IL-1β blockiert durch NF- &kgr; B-Inhibitor BY 11-7082, das anzeigt, daß der molekulare Mechanismus dieser Prozess zugrunde liegt, ist wahrscheinlich, NF &kgr; B abhängig. Interessanterweise unter Verwendung von neutralisierenden Antikörpern zu blockieren TNF-α oder IL-1β parallel zu H. pylori
Infektion beobachteten wir, dass IL-32 Protein-Ebene wurde deutlich verringert. Daher gibt unsere Ergebnisse, dass epithelialen Zytokine (TNF-α und IL-1β) als Reaktion auf H. pylori
Infektion waren wichtig für die Regulation der IL-32-Expression.
Infektion, was darauf hindeutet, dass die Wirkung von H. pylori
Infektion auf IL32-Expression ist direkt physiologischen. Darüber hinaus CagA Mutationen in H. pylori
konnte die Expression von IL-32 in AGS-Zellen signifikant schwächen, was darauf hinweist, dass H. pylori
-induzierte IL-32 upregulation war abhängig von CagA. H. pylori
viele Proteine exprimieren ihrer Pathogenese zu erleichtern [24]. UreB ist auch eine wichtige Virulenz-Protein für die Besiedlung von H. pylori
und vermittelt H. pylori
-induzierte Dysfunktion von Magenbarriere [25], [26]. Wir fanden heraus, dass UreB Mutationen auch abgeschwächt H. pylori
-induzierte IL-32-mRNA-Expression (siehe Abbildung S2). Aus diesem Grund wurde die IL-32-Expression überwiegend durch Translokation von CagA in epithelialen Zellen reguliert und andere Virulenzproteine könnte auch die pathogene Reaktion von H beeinflussen. pylori
zu Magenepithelzellen.
Infektion und mit der Schwere der Magenentzündung korrelierten. Die Regulation der IL-32-Expression in Reaktion auf H. pylori
Infektion hängt von verschiedenen gegenseitig beeinflussende Faktoren. Diese Daten legen nahe zusammen, dass IL-32 eine wichtige Rolle in der Pathogenese von Gastritis spielt, verursacht durch H. pylori
Infektion.
Abbildung S1.
AGS-Zellen wurden in Sechs-Well-Platten bei einer Dichte von 1 × 10 ausgesät 6 Zellen /Vertiefung und mit 10 ng stimulierte /ml Th17 Cytokins (IL-17A, IL-17F, IL-6), Th2 Zytokin IL-4, Treg Cytokins TGF-β1 und Th1 Zytokin IFN-γ für 24 Stunden, und die Zellen wurden für die Analyse der IL-32-mRNA und Proteinexpression gesammelt. Daten sind Mittelwerte ± SEM von drei getrennten Experimenten und einem Vertreter Blot wurde gezeigt
doi:. 10.1371 /journal.pone.0088270.s001
(TIF)
Abbildung S2.
H. pylori
Stamm 26695 wurden auf Hirn-Herz-Infusions-Platten gezüchtet, das 10% Kaninchenblut bei 37 ° C unter mikroaerophilen Bedingungen (5% O 2, 10% CO 2, 85% N 2 ) und seine isogene Urease-Untereinheit B-negativen Mutantenstamm (UreB - Stamm) wurde wie zuvor beschrieben erhalten [27]. Eine Multiplizität der Infektion (MOI) von 100 wurde zur Infektion von AGS und GES-1-Zellen verwendet. Zellen wurden für die Analyse der IL-32-mRNA-Expression gesammelt. Daten sind Mittelwerte ± SEM von drei getrennten Experimenten. * P
< 0,05; ** P
< 0,01; *** P
< 0,001
doi:. 10.1371 /journal.pone.0088270.s002
(TIF)
 Ist es an der Zeit, sichere lebende Mikroorganismen als Bestandteile einer ausgewogenen Ernährung aufzunehmen?
Ist es an der Zeit, sichere lebende Mikroorganismen als Bestandteile einer ausgewogenen Ernährung aufzunehmen?
 Es gibt nicht nur eine Grundursache für Ihre Krankheit
Es gibt nicht nur eine Grundursache für Ihre Krankheit
 Süß &Herzhaft:Pikanter Brokkoli-Dip mit einfachen Crackern
Süß &Herzhaft:Pikanter Brokkoli-Dip mit einfachen Crackern
 Ursachen und Risikofaktoren von Bauchspeicheldrüsenkrebs
Ursachen und Risikofaktoren von Bauchspeicheldrüsenkrebs
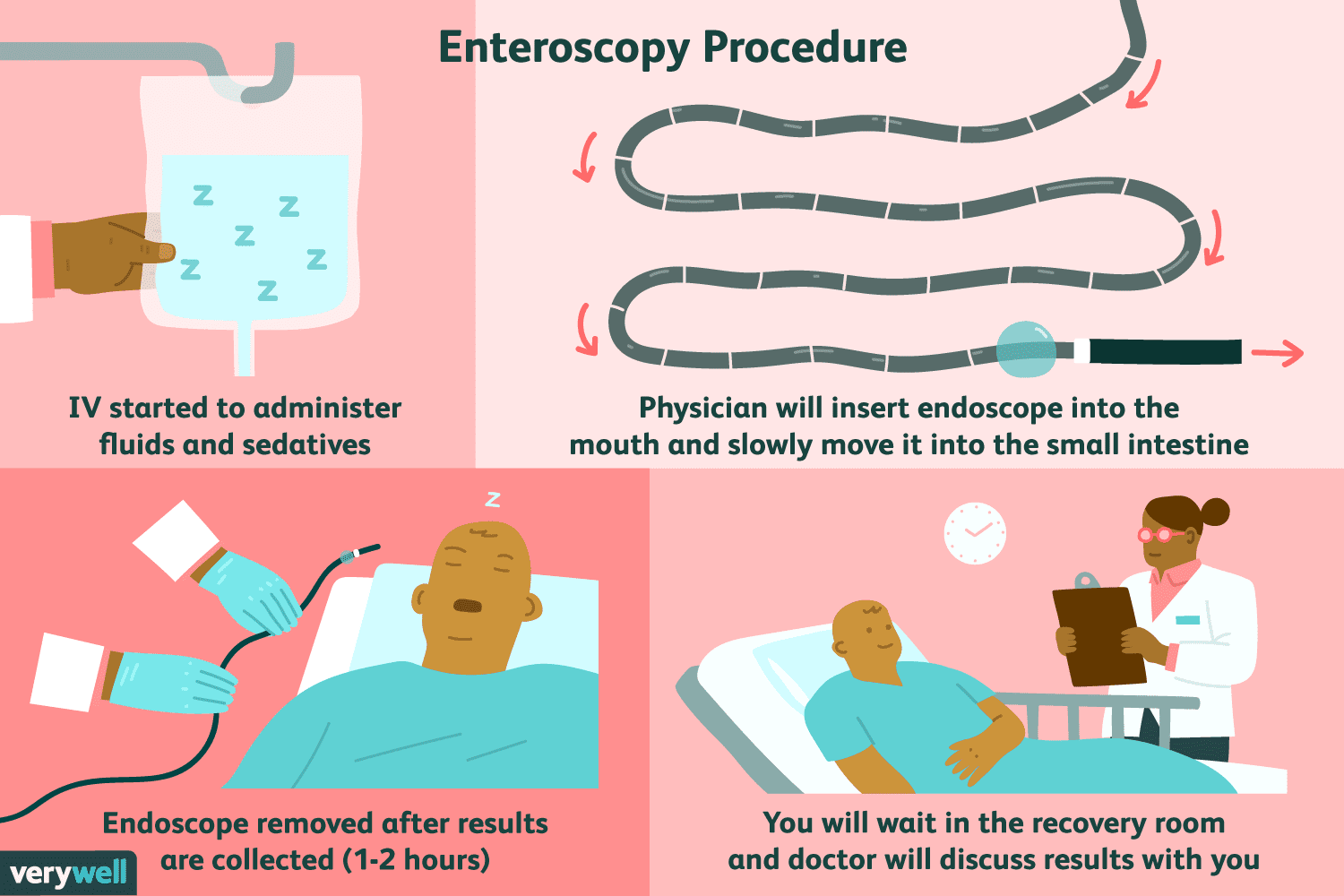 Was ist Dünndarm-Enteroskopie?
Was ist Dünndarm-Enteroskopie?
 Sommernahrung für Ihren Darm
Sommernahrung für Ihren Darm
 Steve’s SCD Diet Healing Journal:Week 24 – The Kale Chip Fail!
Der Mitbegründer von SCD Lifestyle Steve Wright ist endlich zusammengebrochen und hat seinen Weg zur Darmheilung begonnen. Nach vielen Jahren nicht diagnostizierter Verdauungskriege in seinem Körper w
Steve’s SCD Diet Healing Journal:Week 24 – The Kale Chip Fail!
Der Mitbegründer von SCD Lifestyle Steve Wright ist endlich zusammengebrochen und hat seinen Weg zur Darmheilung begonnen. Nach vielen Jahren nicht diagnostizierter Verdauungskriege in seinem Körper w
 Wissenschaftler lösen mysteriösen Fall von Auto-Brauerei-Syndrom
Forscher in China haben eine wichtige Entdeckung gemacht, die den verwirrenden Fall eines 27-jährigen Mannes erklärt, der in der Vergangenheit betrunken war, ohne tatsächlich Alkohol zu trinken. Sie
Wissenschaftler lösen mysteriösen Fall von Auto-Brauerei-Syndrom
Forscher in China haben eine wichtige Entdeckung gemacht, die den verwirrenden Fall eines 27-jährigen Mannes erklärt, der in der Vergangenheit betrunken war, ohne tatsächlich Alkohol zu trinken. Sie
 Was ist eine minimalinvasive Ösophagektomie?
Was ist eine minimal-invasive Ösophagektomie? Eine minimal-invasive Ösophagektomie ist eine Operation, bei der die gesamte Speiseröhre oder ein Teil davon entfernt wird. Die Speiseröhre ist ein
Was ist eine minimalinvasive Ösophagektomie?
Was ist eine minimal-invasive Ösophagektomie? Eine minimal-invasive Ösophagektomie ist eine Operation, bei der die gesamte Speiseröhre oder ein Teil davon entfernt wird. Die Speiseröhre ist ein