Ein solcher solider Tumor, der sich gut an Hypoxie anpasst, ist PDAC. eine aggressive Art von Bauchspeicheldrüsenkrebs. Es ist eine der häufigsten Ursachen für krebsbedingte Todesfälle, mit extrem schlechter Überlebensrate. Da spezifische Genexpressionsprofile unterschiedliche Eigenschaften verleihen, die das Tumorwachstum begünstigen, Das Verständnis intratumoraler Variationen wird Aufschluss über die komplexen molekularen Mechanismen geben, die der PDAC-Pathogenese zugrunde liegen. Während traditionelle Sequenzierungsstudien an Tumorgewebe Einblicke in die Genexpressionsmuster des Tumors geben, sie geben kein Aufschluss über räumliche Unterschiede zwischen verschiedenen Tumorregionen, auch als "intratumorale Heterogenität" bekannt. Außerdem, die Wirkung von Hypoxie auf eine solche Variation ist noch wenig verstanden.
Jetzt, Forscher des Tianjin Medical University Cancer Institute and Hospital (China) sind beim Verständnis der durch Hypoxie induzierten Genexpressionsvariationen bei PDAC noch einen Schritt weiter gegangen, mit "räumlicher Transkriptomik" (ST). Diese Technik ermöglicht die Sequenzierung einzelner Tumorregionen. Erklären Sie die Motivation hinter ihrer Arbeit, die in . veröffentlicht wurde Krebsbiologie &Medizin , Professor Jihui Hao und Baocun Sun, die entsprechenden Autoren, sagen, „Viele Patienten mit PDAC sterben schließlich an der Krankheit mangels wirksamer Behandlungsmethoden. Eine behandlungsinduzierte Hypoxie kann schädliche Veränderungen in Krebszellen auslösen; jedoch, die räumliche Verteilung dieser Veränderungen wurde bisher nicht untersucht."
Die Forscher begannen mit der Entwicklung eines "Xenograft"-Mausmodells, indem sie menschliches PDAC in die ischämischen Hinterbeine (die aus einer mangelnden Blutversorgung, die zu einem hypoxischen Zustand führt) der Tiere. Die Tumoren wurden geerntet und in verschiedene Abschnitte geschnitten, die verschiedenen Tumorregionen entsprechen. Diese Schnitte wurden dann verarbeitet und an "Einfangbereiche" angehängt, die Nukleotidsonden enthielten, die für verschiedene Gene und komplementäre Transkripte spezifisch waren. Diese Objektträger wurden zur Amplifikation und Herstellung einer Sequenzierungsbibliothek weiter in Reaktionskammern inkubiert. Nächste, eine Technik namens "RNA-Sequenzierung" wurde durchgeführt, um unterschiedliche Genexpressionsmuster in Tumoren zu identifizieren, die aus hypoxischen Bedingungen gegenüber Kontrollen isoliert wurden. Die erhaltenen Daten wurden in spezifische Cluster in der Hypoxie- und Kontrollgruppe aufgeteilt, basierend auf der Genfunktion aus der früheren Literatur.
Interessant, Gene, die am Zellzyklus beteiligt sind, Proliferation, Migration, und Metastasen wurden in den Kontrolluntergruppen hochreguliert, im Vergleich zu den hypoxischen Untergruppen. Eine dominante hypoxische Untergruppe, die von der invasiven Vorderseite des Tumors isoliert wurde, war mit diesen Merkmalen verbunden:zusätzlich zu Genen, die mit der Stressreaktion in Verbindung stehen, Stoffwechsel, und normale Pankreasfunktionen. Vor allem, die Expression von Hypoxie-bezogenen Genen war in den Untergruppen unterschiedlich, Hervorhebung ihrer Assoziation mit bestimmten krebsbezogenen Merkmalen. Dies deutet darauf hin, dass unter hypoxischen Bedingungen bestimmte Subpopulationen der Krebszellen überleben weiter und werden resistent gegen hypoxischen Stress.
Die Forscher bestätigten die klinische Relevanz ihrer Ergebnisse weiter, indem sie die Expressionsmuster mit der Patientenprognose korrelierten. Ein hypoxisches Genexpressionsmuster war in der Tat, mit schlechterer Prognose verbunden. Ihre Ergebnisse legten auch die Beteiligung des "PI3K"-Signalwegs in der aggressivsten hypoxischen Untergruppe nahe. Tumore mit Gensignaturen dieser Untergruppe können daher, sprechen auf eine Behandlung mit PI3K-Inhibitoren an.
Gesamt, Die Studie hebt hervor, dass Hypoxie eine bedeutende Rolle bei der intratumoralen Heterogenität bei PDAC spielt und klärt räumliche molekulare Variationen bei PDAC auf. Das Verständnis der molekularen Karte von PDACs kann die Entwicklung zielgerichteter Behandlungen in der Zukunft erleichtern.
Beschreibung der klinischen Implikationen ihrer Ergebnisse, Professor Jihui Hao und Baocun Sun schließen:" Unsere Ergebnisse kombinieren histologische und transkriptomische Variationen in PDAC, Aufzeigen einiger Mechanismen der Arzneimittelresistenz und potenzieller therapeutischer Angriffspunkte für die Behandlung von Bauchspeicheldrüsenkrebs T."
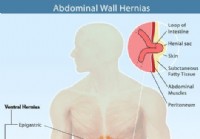 Hernie (Bauchbruch) 9 Arten, Symptome, Ursachen und Operation
Hernie (Bauchbruch) 9 Arten, Symptome, Ursachen und Operation
 OTC-Schmerzmittel und Fiebersenker
OTC-Schmerzmittel und Fiebersenker
 Fettleber
Fettleber
 Kennen Sie die verschiedenen Arten von Magen-Darm-Geschwüren
Kennen Sie die verschiedenen Arten von Magen-Darm-Geschwüren
 Die Ursachen von Blähungen und 10 Möglichkeiten, sie zu bekämpfen
Die Ursachen von Blähungen und 10 Möglichkeiten, sie zu bekämpfen
 Marihuana, echt oder gefälscht, kann zu ungewöhnlichen Magenproblemen führen
Marihuana, echt oder gefälscht, kann zu ungewöhnlichen Magenproblemen führen
 7 gesundheitliche Vorteile von Innereien (und Tipps, um sie erträglich zu machen)
Ernährungstrends kommen und gehen. In einem Jahr ist Acai das Must-Have-Superfood, und im nächsten Jahr sind Hanfherzen im Trend. Heutzutage werben verschiedene Experten für alle möglichen sogenannt
7 gesundheitliche Vorteile von Innereien (und Tipps, um sie erträglich zu machen)
Ernährungstrends kommen und gehen. In einem Jahr ist Acai das Must-Have-Superfood, und im nächsten Jahr sind Hanfherzen im Trend. Heutzutage werben verschiedene Experten für alle möglichen sogenannt
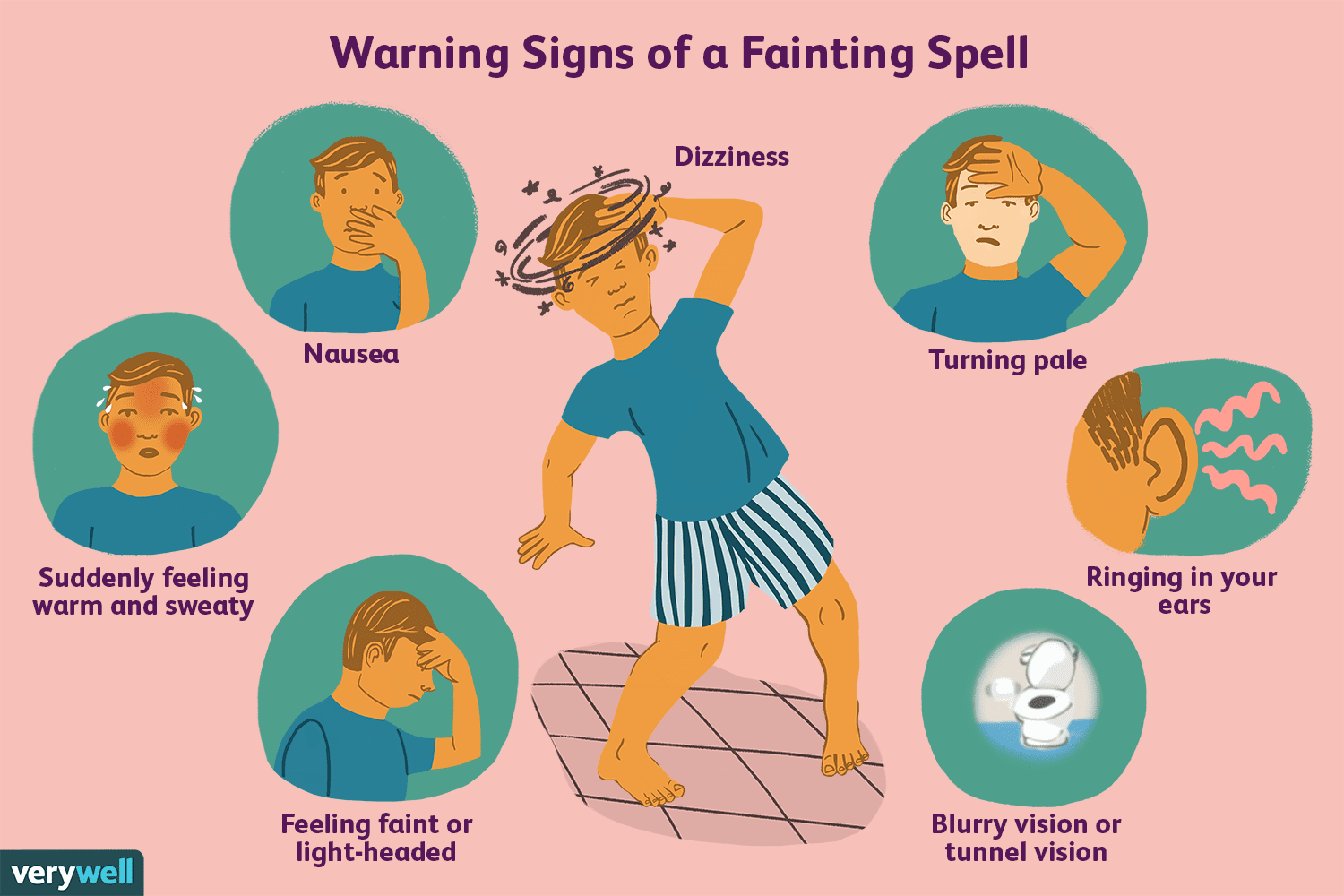 Überblick über den vasovagalen Reflex
Fangen Sie manchmal an zu schwitzen und haben das Gefühl, beim Stuhlgang ohnmächtig zu werden, oder fühlen Sie sich beim Anblick von Blut schwach? Es ist möglich, dass Ihr Vagusnerv dieses Gefühl veru
Überblick über den vasovagalen Reflex
Fangen Sie manchmal an zu schwitzen und haben das Gefühl, beim Stuhlgang ohnmächtig zu werden, oder fühlen Sie sich beim Anblick von Blut schwach? Es ist möglich, dass Ihr Vagusnerv dieses Gefühl veru
 Ernährung bei Divertikulitis:Was Sie wissen müssen
Der menschliche Darm ist ein komplexer Ort, an dem sich viele wichtige Strukturelemente befinden, darunter Schließmuskeln, Klappen, glatte Muskulatur und Schleimhaut (um nur einige zu nennen). Moral v
Ernährung bei Divertikulitis:Was Sie wissen müssen
Der menschliche Darm ist ein komplexer Ort, an dem sich viele wichtige Strukturelemente befinden, darunter Schließmuskeln, Klappen, glatte Muskulatur und Schleimhaut (um nur einige zu nennen). Moral v