Doppelbogen volumetrische modulierten Therapie verbessert Dosisverteilung im Vergleich zu statischen Portal IMRT und 3D-konforme Strahlentherapie für die adjuvante Therapie von Magenkrebs
Abstrakt
Hintergrund
das Ziel dieser Studie war es, die Dosisverteilungen von RapidArc (RA), statische Portalintensitätsmodulierte Strahlentherapie (IMRT) und dreidimensionale konforme Strahlentherapie (3dCRT) als adjuvante Strahlentherapie Modalitäten zu vergleichen für die Behandlung von Magenkrebs.
Methoden
Fünfzehn Patienten mit Magenkrebs, die eine begrenzte Lymphadenektomie von perigastrischen Lymphknoten unterzogen wurden in die Studie einbezogen. Dosimetrie-Werte für eine Gesamtdosis von 45 Gy (1,8 Gy /Tag) wurden für die RapidArc, IMRT berechnet und 3dCRT Modalitäten. Die folgenden Parameter wurden verglichen: D
99%, D 1%, V 95%, V 107%, und die Konformität und Homogenität Indexwerte (CI und HALLO, jeweils) für die geplante Zielvolumen (PTV). Dosisvolumen-Histogramm (DVH) und die Dosisverteilung der Risikoorgane (OAR), als die maximale Dosis an das Rückenmark, V 30 und V 40 des Dünndarms und V 20, V 30 von Leber und Niere wurden ebenfalls um jeweils bewertet.
Ergebnis einschränken RA, IMRT und 3dCRT alle erreicht wünschenswert PTV Abdeckung. Allerdings RA und IMRT signifikant verringert D 1% und V 107% und lieferte besser CI und HALLO-Werte im Vergleich zu 3dCRT (P
< 0,05). Außerdem RA erreicht auch eine deutlich geringere maximale Dosis für das Rückenmark, Leber V 30 und Niere V 20 im Vergleich zu IMRT und 3dCRT; während die mittlere Dosis für diese drei Orgeltypen nicht für die RA, IMRT unterschieden sich und 3dCRT Pläne.
Schlussfolgerungen
Sowohl RA und IMRT erreicht Abdeckung günstige PTV im Vergleich zu 3dCRT. Darüber hinaus erreicht RA besser Dosimetrie als IMRT und 3dCRT und lieferte einen besseren Schutz für das Rückenmark, Leber und Nieren.
Schlüsselwörter Doppelbogen volumetrisch modulierte Bogentherapie intensitätsmodulierte Strahlentherapie dreidimensionale konforme Strahlentherapie Magen Krebs Hintergrund
der INT0116 Studie ergab, die das Überleben Vorteile der postoperativen Strahlentherapie bei Patienten mit Magenkrebs [1, 2]. Außerdem können sowohl die 3-Jahres-und 11-Jahres-Follow-up-Ergebnisse bestätigt die Gesamtüberlebenszeit und krankheitsfreie Überleben Vorteile der Strahlentherapie [1, 2]. Trotz dieser Ergebnisse bleibt jedoch Magenkrebs Strahlentherapie umstritten. Insbesondere bleiben Bedenken Strahlung induzierte Toxizität in Bezug auf. Die Toxizitätswerte für die INT0116 Studie berichtet, enthalten Klasse 3 (40%), Klasse 4 (32%) und gastrointestinale Toxizität (33%), und drei Fälle betrafen behandlungsbedingten Todesfälle. Folglich behandlungsbedingter Toxizität bleibt ein limitierender Faktor für die Anwendung von Strahlentherapie Magenkrebs [1]. In den letzten Jahren
dreidimensionale konforme Strahlentherapie (3dCRT) und intensitätsmodulierter Strahlentherapie (IMRT) sind weit verbreitet für die Behandlung verwendet worden ist von Krebs. Diese Techniken adressieren die Nachteile der herkömmlichen anteroposterioren-posteroanterior Techniken wie Unterdosierung der Zielregionen und übermäßige Strahlung auf normale Strukturen umgibt. Ein Vorteil der IMRT-Technologie über 3dCRT zur Behandlung von Nasen-Rachen-Karzinom, Prostatakrebs und Lungenkrebs hat innerhalb des Zielbereichs, eine bessere Dosis Hotspot Steuerung und reduziert die Strahlenbelastung Risikoorgane (OAR) Dosisverteilung verbessert, einschließlich des Gehirns Stamm und Rückenmark [3-5]. Allerdings geht es weiter diskutiert werden, ob IMRT oder 3dCRT ist besser für Magenkrebs Strahlentherapie [6, 7]. In unserer früheren Studie wurde IMRT gefunden bessere Ziel Gleichförmigkeit und Konformität als Vier-Felder-3dCRT bereitzustellen. Jedoch IMRT hat die Dosis nicht reduzieren auf die OAR angewendet (beispielsweise die Leber und Nieren) [8]. Daher ist die Verfügbarkeit neuer Technologien von großem Interesse.
RapidArc (RA) ist eine Art von dynamischen IMRT, die Anwendung eines Rotationsstrahl zu Ottos Rotationstheorie intensitätsmodulierten Strahlentherapie gemäß beinhaltet. Kurz gesagt, durch dynamisch die Gantry-Rotationsgeschwindigkeit ändert, kann die Form der Multiblendenblätter, und die Dosisleistung, RA schnell und effizient überlegene Verteilung Strahlendosis erreichen [9]. Als solche hat RA-Technologie das Potential Behandlungszeit und verringert die Möglichkeit der Zielbewegung während der Behandlung zu verkürzen, wodurch die Behandlungsgenauigkeit erhöht. Derzeit konzentriert sich die Literatur bezüglich RA hauptsächlich auf die Behandlung von Brust-, Prostata- und Lungenkrebs [10-12]. Im Gegensatz dazu haben nur wenige Studien die klinische Anwendung von RA für Magenkrebs [13].
Bisher weder 3D-CRT noch IMRT haben einen klaren Vorteil bei Magenkrebs Strahlentherapie gezeigt. Dies ist vor allem auf die umfangreichen Bereich des OAR zugeschrieben, die beteiligt ist. Es bleibt auch, ob RA-Technologie bestimmt werden würde, das Ergebnis von Magenkrebs Strahlentherapie zu verbessern. Daher war das Ziel dieser Studie die Dosisverteilung von RA, statische Portal IMRT und 3dCRT für die Strahlentherapie Behandlung von Magenkrebs mit dosimetrischen Analyse zu vergleichen und zu bewerten, welche externe Strahlung Technologie am besten für die postoperative Behandlung von Magenkrebs ist.
Methoden
Patienten
Zwischen Oktober 2010 und Dezember 2011 15 Magenkrebs-Patienten, die D1 Operation in unserer Klinik unterzogen wurden in die Studie eingeschlossen. Nach der 2010 AJCC Staging-Handbuch für Magenkrebs [14], gab es 6 T3 Stadium Patienten und 9 T4 Stadium Patienten. Darüber hinaus wurden die Lymphknoten in 7/9 Patienten negativ. Die primären Tumoren wurden in der Cardia (n
= 4), die Pylorus (n
= 6) oder im Magenkörper (n
= 5) angeordnet ist. Für diese retrospektive Studie, alle Patienten abgeschlossen 3D-CRT-Behandlung vor Dezember 2011. Basierend auf den CT-Bildern, die gesammelt wurden, drei verschiedene Behandlungspläne (3dCRT, IMRT und RapidArc) erzeugt wurden, um die Dosisverteilungen von jedem zu vergleichen . Diese Studie wurde von der Ethikkommission des Krankenhauses genehmigt und informierte Zustimmung wurde von allen Patienten erhalten.
Patientenpositionierung
jeder Patient eine Rückenlage mit ihren Händen über ihre Brust erreicht. Diese Position wurde dann fixiert, um eine thermoplastische Maske. Die Patienten fasteten 4 h, bevor die Simulation Computertomographie (CT), und sie wurden Iohexol in 200 ml Wasser oral 10 min vor der Positionierung verabreicht. CT-Scans wurden mit einer Schichtdicke von 3 mm durchgeführt. CT-Bilder wurden dem Aria Network (Varian-System) übertragen und wurden mit der ECLIPSE Behandlungsplanungssystem rekonstruiert (Version 11, Varian Medical Systems, Palo Alto, CA, USA).
Ziel und OAR Abgrenzung
Laut Bericht 62 [15] von der Internationalen Kommission für Strahlungseinheiten und Messungen, die an CT und anderen bildgebenden Verfahren bezieht, die klinische Zielvolumen (CTV) wurde der Anastomose, Tumorbett und regionalen Lymphknoten. Das Planungszielvolumen (PTV) wurde als einheitliche 5 mm Ausdehnung des CTV definiert. Die Leber, linke Niere, rechte Niere, Rückenmark, Dünndarm, Herz und andere OAR wurden Schritt-für-Schritt abgegrenzt, wie zuvor beschrieben [16].
Behandlungsplanung
Drei Strahlentherapie Behandlungspläne wurden unter Verwendung erzeugte Varian Eclipse-Planungssystem (Version 11, Varian Medical Systems, Palo Alto, CA, USA) von einem erfahrenen Physiker. Für jeden der Pläne, 6 MV Photonenstrahlen von einer Trilogy Maschine (Varian Medical System) verwendet wurden und Dosisberechnungen wurden mit dem Acrous XB-Algorithmus durchgeführt. Für 4-Feld 3dCRT wurde das Zentrum des PTV das Zentrum des Bestrahlungsfeldes bezeichnet. Die Box-Technik in 3dCRT wurde die OAR zum besseren Schutz im Vergleich mit Halbstrahltechniken und die Verwendung von Keilen gefunden. Daher wird in dieser Studie wurde die Box-Technik ausgewählt, und die Einfallswinkel verwendet wurden 0 °, 90 °, 180 ° und 270 °. Die Dosis in der Mitte der Mittelebene angelegt wurde auch als Referenz eingestellt. Für Fest Feld Fenster IMRT Schiebe wurde der Faßlagerwinkel bei 0 °, 35 ° fixiert, 90 °, 180 ° und 315 °. Für RA umfasste die koplanaren Doppelbogen 358 ° -Drehung Therapie, mit 179 ° als Anfangswinkel und 330 ° als Ende Winkel. Eine maximale Dosisleistung von 600 Monitoreinheiten (MU) /min aufgetragen. Für alle drei Pläne war die vorgeschriebene Dosis für die PTV 45 Gy /25 F. Diese Dosis gestellt wurde, dass >sicherzustellen; 95% der PTV 45 Gy und 99% der PTV empfangen > 42,75 Gy. Für die OAR, weniger als 30% der gesamten Lebervolumen wurde erhalten >erlaubt; 30 Gy (V 30 ≤30%). Für die kontralaterale Niere, ausgesetzt das Volumen um mehr als 20 Gy auch auf <begrenzt war, 30% (V 20 < 30%). Die zulässige mittlere Dosis (D Mittelwert) für jede Niere < 18,0 Gy und die maximal zulässige Dosis für das Rückenmark war < 45 Gy. Strahlenbelastung in den Dünndarm wurde auch während der Erzeugung der Strahlentherapiebehandlungspläne minimiert. Die V 40 und V 25 für das Herz waren < 30% und < 50% bzw. [16, 17]
Auswertung und Vergleich der drei Behandlungspläne
Dosisverteilungen. die Zielorgane und die OAR für die fünfzehn Patienten wurden bewertet. Dosisvolumen Histogramme (DVH) wurden ebenfalls erzeugt und verglichen werden, mit den spezifischen Dosimetrie Parameter wie folgt bewertet:
Zielabdeckung zu bewerten, die Dosis um 99% und 1% des Volumens (beispielsweise D 99% erhalten und D 1%), wurden als Metriken für die minimale und maximale Dosen [18] definiert. Die Volumina Empfangen von mindestens 95% und 107% der verschriebenen Dosis (V 95% und V 107% betragen) sowie Ziel Homogenität und conformal Indexwerte (HALLO und CI, jeweils) waren ebenfalls verglichen. HALLO wurde wie folgt berechnet: HALLO = (D2-D98) /D50. Je größer der HALLO-Wert, desto schlechter ist die Gleichmßigkeit der Dosisverteilung [19]. CI wurde wie folgt berechnet: V T, ref /V T × V T, ref /V ref, wobei V T, ref das Volumen des Ziels durch die abgedeckt ist Referenz Isodosislinie, V T ist das Zielvolumen (= PTV) und V ref ist das Volumen der durch die Referenz Isodosislinie bedeckt Gewebe. Der Wert von CI variiert zwischen 0 und 1, und einen Wert näher an einem zeigt eine bessere Übereinstimmung der Dosis mit dem PTV [20, 21]. Die äquivalente einheitliche Dosis (EUD) für jeden PTV verglichen wurde.
Dosisverteilung lebenswichtiger Organe, einschließlich Niere, Leber, Dünndarm, und im Rückenmark, wurden ebenfalls bewertet. Die Parameter, die im Vergleich wurden mittlere Dosis enthalten (D Mittelwert) und V 20 für die Nieren (V 20 der prozentuale Volumen der Nieren ist, die mindestens 20 Gy), D bedeuten und V 30 für Leber, V 30 und V 40 für Dünndarm und die maximale Dosis (D max) und D 1% für das Rückenmark. Monitoreinheiten (MU) wurden auch im Vergleich zwischen drei Plänen.
Statistische Analyse
SPSS (Version 17.0, SPSS Inc., Chicago, IL, USA) wurde für die Datenanalyse verwendet. Nichtparametrische Wilcoxon Tests oder zweiseitigen t
-Tests wurden durchgeführt, Gruppen zu vergleichen. Ein p
-Wert von weniger als 0,05 wurde als statistisch signifikant angesehen.
Ergebnisse | PTV Vergleich
Alle drei Pläne erfüllt die Dosis Anforderung, und es gab keine signifikanten Unterschiede in der D 99% Mindest Dosis und die V 95% Zielvolumen zwischen ihnen. Allerdings hat die RA-Plan deutlich die maximale Zieldosis zu reduzieren und die hohe Dosisvolumen (zB D 1% und V 107%, respectively) im Vergleich zu den 3dCRT und IMRT-Pläne, und die Differenz zwischen dem 3dCRT und IMRT Pläne war nicht signifikant. Sowohl IMRT und RA signifikant die EUD des PTV gesenkt im Vergleich zu 3dCRT (P
< 0,05). Im Hinblick auf Ziel Einheitlichkeit sowohl IMRT und RA verbessert auch die PTV Gleichmäßigkeit im Vergleich zu 3dCRT (P
< 0,05). Darüber hinaus waren die CI-Werte 0,91 ± 0,02 für RA, 0,89 ± 0,04 für IMRT und 0,71 ± 0,01 für 3dCRT. Der erstere war deutlich näher an einem Wert von 1 im Vergleich mit der IMRT und 3dCRT Pläne (P
< 0,05) (Tabellen 1 und 2; Fig. 1 und 2) .Tabelle 1 Zusammenfassung der DVH-Parameter untersucht
Parameter Bei
3dCRT Mittelwert ± SD
IMRT Mittelwert ± SD
RA Mittelwert ± SD
PTV
D1% (Gy)
49,9 ± 0,29
48,2 ± 0,17
48,4 ± 0,24
D99% (Gy)
40,5 ± 0,43
40,3 ± 0,41
40,1 ± 0,37
V95% (%)
96,6 ± 0,61
98,9 ± 0,33
98,5 ± 0,62
V107% (%)
13,6 ± 3,7
1,02 ± 0,01
1,02 ± 0,01
EUD (Gy)
47,3 ± 0,09
46,8 ± 1,45
46,4 ± 0,06
HALLO
0,1 ± 0,01
0,05 ± 0,01
0,07 ± 0,01
CI
0,71 ± 0,02
0,89 ± 0,04
0,90 ± 0,02
normale Leber
Dmean (Gy)
17,6 ± 0,82
14,2 ± 0,73
15,3 ± 1,1
V30 (%)
12,3 ± 1,6
12,7 ± 1,3
6,90 ± 1,4
linke Niere
Dmean (Gy)
13,2 ± 1,21
15,3 ± 0,63
14,1 ± 0,61
V20 (%)
29,9 ± 2,5
27,7 ± 1,8
22,4 ± 3,6
Rechte Niere
Dmean (Gy)
11,9 ± 1,4
13,5 ± 0,65
12.2 ± 0,90
V20 (%)
19,2 ± 1,1
16,2 ± 1,1
12,7 ± 1,3
Dünndarm
Dmean (Gy)
13,1 ± 0,83
12,4 ± 0,39
13,1 ± 0,76
V30 (%)
17,2 ± 0,61
16,5 ± 0,67
15,6 ± 0,83
V40 (%)
11,0 ± 0,38
9,78 ± 0,93
9,15 ± 0,44
Rückenmark
D1% (Gy)
33,0 ± 0,74
31,0 ± 0,29
27,8 ± 0,75
MU
250 ± 3,4
694 ± 3,9
399 ± 6,8
Abkürzungen: 3dCRT: 3D-konforme Strahlentherapie; IMRT: intensitätsmodulierte Strahlentherapie; RA: RapidArc; PTV: geplant Tumorvolumen; Dn%: Dosis um n% des Volumens erhalten; Gy: Gray (Einheit); Vx%: Das Volumen ≥ x% der verschriebenen Dosis zu empfangen; EUD: äquivalente einheitliche Dosis; HALLO: Homogenitätsindex; CI: Konformitätsindex; Dmean: die mittlere Dosis für die Orgel; Vn: Das Volumen Empfangen n Strahlendosis (Gy); MU: Monitoreinheiten; EUD: entspricht einheitliche Dosis
Tabelle 2 Unterschiede zwischen den drei Methoden im Hinblick auf die DVH Parameter
Parameter
P
-Werten
Insgesamt
3dCRT vs. IMRT
3dCRT vs. RA
IMRT vs. RA
PTV
D1% (Gy)
0,003
3dCRT > IMRT **
3dCRT > RA **
- D99% (Gy)
0.803
- -
- V95% (%)
0.533
- -
- V107% (%)
0,005
3dCRT > IMRT *
3dCRT > RA *
- EUD (Gy)
0,012
3dCRT > IMRT *
3dCRT > RA *
_
HALLO
0,03
3dCRT > IMRT *
3dCRT > RA *
- CI
0,001
3dCRT < IMRT *
3dCRT < RA *
- Normale Leber
Dmean (Gy)
0.058
3dCRT > IMRT **
-
- V30 (%)
0,006
- 3dCRT > RA **
IMRT > RA **
linke Niere
Dmean (Gy)
0.335
- -
- V20 (%)
0.137
- 3dCRT > RA *
- Rechte Niere
Dmean (Gy)
0,912
- -
- V20 (%)
0,005
-
3dCRT > RA **
- Dünndarm
Dmean (Gy)
0.657
- -
- V30 (%)
0,075
-
-
- V40 (%)
0.453
- -
- Rückenmark
D1% (Gy)
0,011
-
3dCRT > RA *
IMRT > RA *
MU
0.001
IMRT > 3dCRT **
IMRT > RA **
Abkürzungen: 3dCRT: 3D-konforme Strahlentherapie; IMRT: intensitätsmodulierte Strahlentherapie; RA: RapidArc; PTV: geplant Tumorvolumen; Dn%: Dosis um n% des Volumens erhalten; Gy: Gray (Einheit); Vx%: Das Volumen ≥ x% der verschriebenen Dosis zu empfangen; EUD: äquivalente einheitliche Dosis; HALLO: Homogenitätsindex; CI: Konformitätsindex; Dmean: die mittlere Dosis für die Orgel; Vn: Das Volumen Empfangen n Strahlendosis (Gy); MU: Monitoreinheiten
* P
< 0,05; ** P
< 0,01
Abb. 1: Vergleich der PTV isodose Verteilungen mit 3dCRT erreicht, IMRT und RapidArc adjuvante Strahlentherapie Modalitäten
Abb. 2 mittlere Dosis Volumen-Histogramme für PTV, CTV, OAR und gesundes Gewebe für die globale Analyse nach Behandlungsplan. 3dCRT: 3D-konforme Strahlentherapie (blau); IMRT: intensitätsmodulierte Strahlentherapie (rot); RapidArc: Doppelbogen RapidArc (grün)
Bewertung von OAR
Frühere Untersuchungen haben gezeigt, dass die D bedeuten und V 30 für die Leber sind wichtige Prädiktoren der strahleninduzierten Leberschädigung [8] . In der vorliegenden Studie, V 30 für die Leber war (12,32 ± 1,61)% für 3dCRT (12,73 ± 1,33)% für IMRT und (6,90 ± 1,41)% für RA. Letztere war signifikant niedriger als die beiden anderen Methoden (P
< 0,05). Darüber hinaus bedeutet die D für die Leber 17,61 ± 0,82 Gy für 3dCRT, 14,22 ± 0,23 Gy für IMRT und 15,31 ± 1,11 Gy für RA war. Sowohl IMRT und RA reduziert die durchschnittliche Strahlungsdosis für die Leber, aber der Unterschied war nicht signifikant (Tabelle 1 und 2, Fig. 2). In einer früheren Studie von Matzinger und Dawson [16, 17], die empfohlenen Toleranzdosen für die Nieren waren V 20 < 30% und D bedeuten, < 18 Gy. In der vorliegenden Studie wurden die V 20 für die linke oder rechte Niere mit dem RA-Plan war niedriger als die für die IMRT und 3dCRT Pläne. Insbesondere verringert RA-Behandlung die V 20 der linken Niere von 25,17%, und die rechte Niere von 33,94%. Zusätzlich war die durchschnittliche Dosis für beide Nieren höher sowohl für die IMRT und RA Pläne gegenüber 3dCRT, obwohl der Unterschied nicht signifikant war (P
> 0,05) (Tabelle 1 und 2, Fig. 2).
die V 30 und V 40 sowie die D bedeuten, für den Dünndarm wurden ebenfalls bewertet. Im Vergleich mit 3dCRT, IMRT und RA nur mäßig reduziert V 30 und V 40, und die Unterschiede waren nicht signifikant. Im Gegensatz dazu erhöhte sich leicht RA die D bedeuten, des Dünndarms, obwohl dieser Unterschied auch nicht signifikant war (P
> 0,05) (Tabellen 1 und 2, Fig. 2).
Für die Wirbelsäulen Schnur, alle drei Pläne, die Dosis Anforderungen erfüllt. Die maximale Strahlungsdosen für D 1% waren 32,98 ± 0,74 Gy für 3dCRT, 31,01 ± 0,29 Gy für IMRT und 27,80 ± 0,75 Gy für RA. Im Vergleich mit 3dCRT, RA deutlich gesenkt das Rückenmark D max-Wert von 15,71% (Tabellen 1 und 2, Fig. 2).
Von MU und Abgabeparameter
Die MU für IMRT und RA waren 694,25 ± 3,91 und 399,00 ± 6,81, respectively. Somit reduziert RA signifikant die Strahlendosis um 42,5% im Vergleich mit IMRT erhalten. Jedoch erforderlich, RA eine größere Anzahl von MU als 3dCRT. Zusätzlich wurde ein physikalischer Keil nicht für die 3dCRT Behandlungen verwendet, da dies die Anzahl von MU erhöhen könnte, und es könnte auch das Potential für Leckstrahlung (Tabellen 1 und 2) erhöhen. Die Dosisleistung für jede Technik betrug 400 MU /min für 3dCRT, 600 MU /min für IMRT, und fast 600 MU /min für ARC. So waren die relativen Behandlungszeiten für jede Technik. 3,2 ± 0,3 min für RA, 6,6 ± 1,2 min für Instant Messaging und 4,2 ± 0,5 min für CRT
Diskussion
Derzeit ist die postoperative Radiochemotherapie eine der wichtigsten Behandlungen für Fälle von Magenkrebs mit einer schlechten Prognose. Jedoch aufgrund der Nähe dieser Region zu viele lebenswichtige Organe, bleibt es eine Herausforderung wirksam das Zielgebiet zu bedecken und den benachbarten lebenswichtigen Organe zu schützen. Für die adjuvante Strahlentherapie Modalitäten, war es schwierig, eine optimale Dosisverteilung mit traditionellen 3dCRT zu erreichen, während IMRT ist in der Lage, gleichzeitig Zieldosis optimieren und die Exposition von OAR verringern. IMRT hat auch effektiv die lokale Tumorkontrolle zu verbessern, gezeigt worden, um das Ausmaß der Strahlenschäden an normalen Geweben zu reduzieren und Lebensqualität der Patienten zu verbessern [22]. Jedoch in unserer früheren Studie von 3dCRT und IMRT für die Behandlung von Magenkrebs, Strahlungsdosimetrie Daten zeigten, dass IMRT keinen signifikanten Vorteil gegenüber 3dCRT mit 3dCRT wobei überlegen IMRT für V 20 der linken und rechten Nieren zeigten [8]. Daher werden neue Strahlentherapie-Techniken für die Behandlung von Magenkrebs noch benötigt.
RA-Technologie hat das Potenzial, die Behandlungszeit zu verkürzen und die Möglichkeit der Zielbewegung während der Behandlung zu verringern, die Behandlungsgenauigkeit würde dazu dienen, zu erhöhen [18]. RA ist zuvor zur Behandlung von vielen Arten von Tumoren angewendet worden [23, 24]. Beispielsweise in der Arbeit von Verbakel et al. [25], zwölf Patienten mit fortgeschrittenem Kopf- und Halskrebs erhalten IMRT gegenüber RA Strahlentherapie. Die Behandlung mit RA wurde gefunden Zieldosis Einheitlichkeit zu verbessern und die Exposition von benachbarten OAR zu reduzieren. Darüber hinaus stellte Doppelbogen RA weitere dosimetrische Vorteile im Vergleich zu einzelnen Bogen RA und IMRT. Diese Vorteile wurden bei der Behandlung von Lungenkrebs und Prostatakrebs mit Doppelbogen RA bestätigt [11, 12]. Jedoch für Magenkrebs Strahlentherapie, die Form des Bestrahlungsziels ist unregelmäßig und die umgebenden Organe, einschließlich Leber und Niere, haben eine geringe Toleranz für die Strahlung. Somit bleibt es, ob eine Drehvolumen IMRT-Technik bestimmt werden, wird für Magenkrebs Strahlentherapie von Vorteil sein.
Die studierte Kohorte 15 postoperativen Magenkrebs-Patienten eingeschlossen. Basierend auf den Standort der Läsionen und der CT-Bildgebung, 3dCRT (4-Feld), IMRT (5-Feld) oder RA Behandlungspläne angewendet wurden. Das Rezept Dosis enthalten 45 Gy /25 F auf den PTV angewendet, mit > 95% der PTV Empfang 45 Gy und 99% der PTV Empfang 42.75 Gy. Alle drei Pläne erfüllten die Dosisbedarf und es gab keine signifikanten Unterschiede zwischen ihnen. Darüber hinaus IMRT und RA reduziert die maximale Zieldosis und der hohen Dosisbereich (D 1%, V 107%) im Vergleich zu 3dCRT. IMRT und RA waren auch überlegen 3dCRT für Zielvolumen Einheitlichkeit. Der CI-Wert für RA deutlich näher an einer als die CI-Werte für IMRT und 3dCRT, was darauf hindeutet, eine verbesserte Konformalität erzielt wurde. Für Ziele mit größeren und komplexeren Formen, wurde RA gefunden sind mit früheren Studien konsistent bessere Dosisverteilung, besser PTV Ziel Konformalität und eine bessere Zieldosisverteilung, und diese Ergebnisse zur Verfügung zu stellen [13]. Somit RA das Potenzial hat, behandlungsbedingte Nebenwirkungen zu reduzieren.
In den frühen Studien der Organ Toleranz gegenüber ionisierender Strahlung, Strahlenempfindlichkeit der Leber unterschätzt worden sein. Toleranz Dosen wurden nach dem Risiko der RT-induzierte Lebererkrankung begrenzt, und die mittlere Dosis und V30 für die Leber wurden wichtige dosimetrische Parameter mit erhöhter Toxizität Risiko angesehen [26]. Inzwischen haben neuere Studien gezeigt, dass normale Leberzellen gegenüber Strahlung empfindlich sind, insbesondere dann, wenn die Leber mit dem Hepatitis-B-Virus infiziert ist [26]. Dementsprechend Dawson et al. [27] haben vorgeschlagen, dass die Toleranzdosis für die Leber weniger als 30% für V 30 sein sollte, und die D Mittelwert sollte weniger als 30 Gy sein. Für die Fälle, Hepatitis-B-Infektion beteiligt, die D Mittelwert sollte weniger als 23 Gy sein. Weiterhin wird gemäß der quantitativen Analyse von normalem Gewebe Effekte in der Klinik (QUANTEC) Aufwand, sollte die mittlere Leberdosis weniger als 28 Gy in 2-Gy-Fraktionen für primären Leberkrebs, und sollte weniger als 32 Gy in 2-Gy Fraktionen für Lebermetastasen [26]. In der vorliegenden Studie, Leber V 30 war (12,32 ± 1,61)% für 3dCRT (12,73 ± 1,33)% für IMRT und (6,90 ± 1,41)% für RA, wobei letztere deutlich niedriger als die beiden ersteren Werte (P
< 0,05). Leber-D Mittelwert war 17,61 ± 0,82 Gy für 3dCRT, 14,22 ± 0,23 Gy für IMRT und 15,31 ± 1,11 Gy für RA, und diese unterscheiden sich nicht signifikant. Im Vergleich mit 3dCRT und IMRT, RA signifikant Leber V reduziert 30, noch nicht die durchschnittlichen Leberdosis beeinflussen. Darüber hinaus trotz der deutlichen Reduzierung der Leber V 30, eine Analyse des Volumens aus der DVH zeigte, dass V 10 erhöht. Diese Ergebnisse stehen im Einklang mit denen für eine Leberkrebs Bestrahlung Studie von Kuo et al berichtet. [28].
Die Niere ist ein weiteres wichtiges Organ, das von Magenkrebs Strahlentherapie bedroht ist. Nierengewebe ist strahlenempfindlich, und die empfohlenen Strahlungstoleranz Dosen über 23 Gy für die gesamte Niere, 30 Gy für 2/3 der Niere und 50 Gy für 1/3 der Niere. Eine Studie von Jansen et al. weiter vorgeschlagen, dass die durchschnittliche Nieren Dosis war weniger wichtig als V 20. Daher ist es, dass <empfohlen; 70% der Nierenvolumen erhalten sollte 20 Gy (V 20 < 70%), während die V 20 für die kontralaterale Niere sollte < 30% [29] . Insgesamt ausgesetzt Nierengewebe zu mehr als 20 Gy nicht mehr als 50% der gesamten Nieren übersteigen sollte, da sonst, strahlungsinduzierte Schädigung der Niere auftreten können, wie beispielsweise eine Abnahme der glomerulären Filtrationsrate und /oder Nierenversagen. Somit ist eine ständige Ziel, die Strahlendosis auf die Nieren während der postoperativen Strahlentherapie bei Magenkrebs zu reduzieren. Minn et al. [30] untersuchten die Dosimetrie, Wirksamkeit und Toxizität von Strahlentherapieplanung mit 3dCRT und IMRT für 57 Fälle von Magenkrebs und wurde IMRT gefunden Niere V zu reduzieren 20. In unserer früheren Studie keinen offensichtlichen Unterschied in der V 20 von Nieren zwischen IMRT und 3D-CRT wurde beobachtet, obwohl IMRT das Rückenmark und Leber günstige Tumorabdeckung und die Überlegenheit zeigten in schützen. Allerdings wurde diese Überlegenheit nicht in der Niere gegenüber 3D-CRT beobachtet. Somit muss IMRT anscheinend nicht eine bessere Behandlung für Magenkrebs dar [8]. In ähnlicher Weise wurde in unserem nachfolgenden einzigen Bogen RA-Studie, Nierenstrahlendosis nicht signifikant verringert, noch Doppelbogen RA signifikant verringert Niere V 20 im Vergleich zu IMRT und 3dCRT für beide Nieren. Inzwischen gab es keinen offensichtlichen Unterschied in der D bedeuten für beide Nieren unter den 3D-CRT, IMRT und RA-Behandlungen. Zusammengenommen legen diese Ergebnisse nahe, daß RA eine Schutzwirkung für Nieren liefern im Vergleich zu IMRT.
Gastrointestinal-Toxizität ist die wichtigste limitierende Faktor für die Anwendung von Strahlentherapie Magenkrebs. Entsprechend aufgrund der Strahlentherapie der Schlüssel Toxizität zu reduzieren, ist die Belichtung des Gastrointestinaltraktes mit Strahlung zu steuern. In vielen Studien IMRT und RA wurden, um die Strahlungsdosis an den Gastrointestinaltrakt während abdominal Strahlentherapie gezeigt zu verringern. Zum Beispiel Minn et al. [30] zeigten, dass IMRT Darm-V 45 im Vergleich zu 3dCRT reduziert. In einer weiteren Untersuchung von 14 Fällen von Bauchmetastasen mit Strahlentherapie behandelt, Mario et al. [30] berichteten, dass RA und IMRT die durchschnittliche Dosis und maximale Dosis an den Magen und Dünndarm verringert im Vergleich zu 3dCRT. Jedoch war der Unterschied nicht signifikant. In der vorliegenden Studie, die durchschnittliche Dosis (D Mittelwert) für den Dünndarm, sowie V 30 und V 40, wurden untersucht. D bedeuten für den Dünndarm nicht signifikant zwischen den drei Planungsmethoden unterschieden sich, noch ein DVH-Chart-Analyse zeigte, dass IMRT und RA V erhöht 10 und reduziert V 30 und V 40 im Vergleich zu 3dCRT. Somit erhöhte sich das Volumen der Niedrigdosisbereich gleichzeitig mit einer Abnahme des Volumens der Hochdosisbereich. Diese Ergebnisse stehen im Einklang mit der Beobachtung, dass die durchschnittliche Dosis keinen signifikanten Unterschied zeigte.
Das Rückenmark ist eine lange, dünne, rohrförmige Bündel von Nervengewebe, und es ist anfällig für Verletzungen von lokalen hohen Strahlendosen. Kirkpatrick et al. [31] berichteten, dass die Inzidenzrate für Strahlung Myelitis 0,2, 6, und 50% der Gesamtdosis für 50 Gy, 60 Gy, and_69 Gy jeweils, wenn sie bei der herkömmlichen Anteil von 2-Gy pro Tag verabreicht. Darüber hinaus wird gemäß der Strahlenonkologie-Gruppe der Europäischen Organisation für Forschung und Behandlung von Krebs, die maximale Strahlendosis, die auf das Rückenmark angewendet werden sollte, ist 45 Gy, und es sollte auch nicht mehr als 40 Gy nicht überschreiten, wenn Oxaliplatin-Chemotherapie verabreicht wird [16]. Daher wird die maximale Dosis für das Rückenmark im allgemeinen bei nicht mehr als 45 Gy eingestellt. In der vorliegenden Studie, die an das Rückenmark angewendet Dosen mit jeder der drei Techniken waren alle innerhalb der tolerierten Dosis. Darüber hinaus, im Vergleich zu 3dCRT, die D max für das Rückenmark mit RA wurde um bis zu 15,71% deutlich reduziert.
RA ist eine adjuvante Strahlentherapie Modalität, die vor kurzem entwickelt worden und verwendet worden hohen Dosen zu liefern Strahlung zu einer Vielzahl von Tumoren. Allerdings bleibt ihre Rolle bei der Behandlung von Magenkrebs umstritten wegen der unregelmäßigen Zielvolumina beteiligt und die geringe Strahlentoleranz kritischer Organe umgibt. In unserer früheren Studie zur Verfügung gestellt RA überlegen Dosishomogenität im Vergleich zu 3dCRT und IMRT, aber nicht einen besseren Schutz der OAR. Darüber hinaus, während die einzelnen Lichtbogentechnik nicht erfolgreich war, die doppelte Lichtbogentechnik konnte die gleiche Dosisverteilung als IMRT zu erreichen, während signifikant die OAR und proximalen gesundes Gewebe zu schonen. Dieser verbesserte Schutz der Leber und Nierengewebe im Vergleich mit IMRT schlägt eine höhere Dosis an ein Zielvolumen mit doppelseitigem arc RA angewendet werden könnte. Jedoch ist es wichtig, die Grenzen unserer Studie als auch zu berücksichtigen. Zuerst wurde eine Atmungs Gating-Technik nicht verwendet werden, und deren Einfluss auf die Dosisverteilung wurde nicht untersucht. Darüber hinaus hatte die vorliegende Studie eine geringe Größe Probe und keine Beurteilung der klinischen Wirksamkeit und Toxizität. Daher sind weitere Untersuchungen notwendig, um die technische Machbarkeit der Festlegung eines Doppelbogens RA auf die Behandlung von Magenkrebs zu bestätigen, und diese sollten eine größere Probengröße und der Beurteilung der klinischen Wirksamkeit und Toxizität umfassen.
Schlussfolgerungen
Zusammengefasst Doppel
 Was sind Oxalate? (Lebensmittel, die man aus gesundheitlichen Gründen essen oder nicht essen sollte)
Antinährstoffe sind hinterhältige Verbindungen, die Ihrem Körper aktiv Nährstoffe stehlen, wenn Sie sie essen. Zu den Antinährstoffen gehören Dinge wie Lektine, Phytate und Oxalate (worüber wir heute
Was sind Oxalate? (Lebensmittel, die man aus gesundheitlichen Gründen essen oder nicht essen sollte)
Antinährstoffe sind hinterhältige Verbindungen, die Ihrem Körper aktiv Nährstoffe stehlen, wenn Sie sie essen. Zu den Antinährstoffen gehören Dinge wie Lektine, Phytate und Oxalate (worüber wir heute
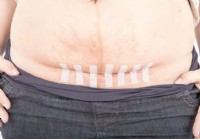 Welche Arten von Bauchschnitten gibt es?
Ein Bauchschnitt ist ein Schnitt durch Ihre Haut am Bauch, um die Bauchorgane freizulegen oder eine Operation zu erleichtern oder ein Verfahren. Einschnitte oder Schnitte am Bauch werden meistens w
Welche Arten von Bauchschnitten gibt es?
Ein Bauchschnitt ist ein Schnitt durch Ihre Haut am Bauch, um die Bauchorgane freizulegen oder eine Operation zu erleichtern oder ein Verfahren. Einschnitte oder Schnitte am Bauch werden meistens w
 Wo Sie die besten Urlaubsrezepte für die SCD-Diät finden
Die Feiertage sind eine schöne Zeit des Jahres – Nächte voller lockerer Gespräche, liebevoller Erinnerungen und üppiger Mahlzeiten. Leider sind große Familientreffen für mich und viele andere SCD-Anhä
Wo Sie die besten Urlaubsrezepte für die SCD-Diät finden
Die Feiertage sind eine schöne Zeit des Jahres – Nächte voller lockerer Gespräche, liebevoller Erinnerungen und üppiger Mahlzeiten. Leider sind große Familientreffen für mich und viele andere SCD-Anhä