Egyidejű kompozit mellékvese phaeochromocytoma több gyomor stroma tumorok és pseudohermaphrodism egy beteg von Recklinghausen kór katalógusa Abstract katalógusa Bár phaeochromocytoma előfordul 1% -ánál von Recklinghausen-kór, kompozit daganatok ezt a szindrómát sokkal ritkábbak, elszigetelt eset jelentések a szakirodalomban. A legtöbb gasztrointesztinális stroma tumorok (GIST) magányos és szórványos. Többszörös GIST azonban, amelyek kapcsolatban vannak a klinikai szindrómák, különösen von Recklinghausen-kór. Úgy véljük, ez az első jelentés a kompozit mellékvese phaeochromocytoma és több Lényeg, amelyek egy 82 éves nő neurofibromatózis 1-es típusú (NF1) megnyilvánuló csikló és a bőr alatti neurofibromák, epilepszia és Lisch csomók. Az extrém clitoromegalia aggályokat vet fel a pseudohermaphrodism a bemutató. Katalógusa Bevezetés katalógusa neurofibromatózis 1-es típusú (NF1) egy heterogén, dominánsan öröklődő betegség társul számos különböző jó- és rosszindulatú. Pheochromocytoma előfordul 1% -ánál NF1, mivel összetett daganatok A mellékvese-velő sokkal ritkábbak. Definíció szerint egy összetett tumor áll phaeochromocytoma neuroblastomás, ganglioneuroblastoma vagy ganglioneuroma. Mindkét sejtvonal, a kromaffin sejtek és a symapathetic ganglion sejtek neurális taréj eredetű. Gasztrointesztinális stroma tumorok (GIST-ek) a leggyakoribb mesenchymalis neoplazmák a gyomor-bél traktus és a már szintén leírták társulva NF1. GIST-ek immunohisztokémiailag pozitív KIT tirozin-kináz receptor, és ez a jellemző is megtalálható az intersticiális sejtek Cajal, a pacemaker sejtek szabályozó vegetatív motoros aktivitás. Feltételezik, hogy a GIST-ek származnak multipotens prekurzor sejtek, amelyek megkülönböztetik az interszticiális sejt Cajal fenotípus. Neurofibromák a csikló ritkán közöltek. Ez jelenti a differenciál diagnózis, amelyet meg kell vizsgálni pseudohermaphrodism.
NF1 járt, bár ritkán, kompozit ganglioneuroma-ganglioneuroma A mellékvese-velő, multifokális gyomor GIST és neurofibroma a csikló, de úgy véljük, ez az első esetismertetés, amely szerint minden ilyen rendellenességek fordulnak elő ugyanabban a betegben NF1. katalógusa Esetismertetés
egy 82 éves özvegy és három gyermek édesanyja a neurofibromatózis kórházba került, a következő roham miatt nem tartása a görcsoldó gyógyszert Her epilepszia volt előzőleg jól kontrollált fenitoin napi 300 mg. Cranial komputertomográfia (CT) kiderült, hogy a régi baloldali frontális agyi infarktus. A beteg további kórtörténetben szereplő enyhe érszűkület, törött bal nyakán combcsont és vashiányos vérszegénység. Gasztroszkópia és kolonoszkópia végeztünk 3 évvel korábban, amikor megvizsgáltuk melena és nincs nyilvánvaló oka talált. A glibenklamid 5 mg tds már megkezdett a lány általános orvos tüneti glycosuria. Ő volt semmi más gyógyszert.
Ebben felvételi, a betegnél a gyomor-pszeudo-elzáródás, amelyet konzervatívan menedzselt. Ez volt a vizsgálat során az ő székrekedés és progresszív haspuffadás hogy clitoromegalia megjegyezték vizsgálatán és egy 2,5 cm bal mellékvese tömegét található hasi CT.
A beteg adott történetét csikló bővítés a születés, és emlékeztet a klitorisz csökkentése műtét kínált és csökkent a 4-éves. Ő kifejlesztett számos subcutan csomók 16-éves és bőr neurofibroma megerősítette biopszia a bőrcsomók akkoriban. Volt egy család történetét neurofibromatózis, sújtó mind anyai nagyanyja és dédanyja, és a beteg saját legfiatalabb lánya.
Mivel az egyesület a neurofibromatózis és phaeochromocytoma, a beteg megkérdőjelezték kapcsolatos rohamokban jelentkező tüneteket szívdobogás, fejfájás, izzadás , kipirulás vagy látászavar, de ezek nem voltak jelen. A vizsgálat volt normális vérnyomású egy testtartási csepp 135/60 Hgmm 110/60 Hgmm. A pulzusszám 80 és rendszeres, és nem volt hallható, lágy, aorta szűkült zörej. Elterjedt bőr neurofibromák és café-au-lait foltok nem észleltek. Clitoromegalia jelen volt a csikló mérő 10 × 4 × 4 cm. A vizuális mezőket és fundi normális volt, bár Lisch csomók voltak jelen a bal írisz. A betegnek kétoldali sensineural hallásvesztés, de nincs más neurológiai deficit detektáltunk.
Biokémiai vizsgálatok megerősítették, emelkedett 24 órás vizelet katecholamin kiválasztás után 6 nappal felvételi: adrenalin 232 nmol /nap (referencia intervallum < 120 nmol /nap), a noradrenalin 465 nmol /nap (ref. < 600); és 24 óra vizelet kreatinin 4,6 mmol /nap (ref. 5,0-16,0). Egy ismételt 24 óra vizelet katekolamin három nappal később is megerősítette tartós emelkedése vizelet adrenalin 149 nmol /nap vizelet kreatinin 4,4 mmol /nap. A vizelettel történő kiválasztódás kortizol volt 530 nmol /nap (ref. ≪ 590). A beteg biokémiai euthyreoid a szabad tiroxin 13 pmol /l (ref. 9-19) és a TSH 3,15 mU /L (ref. 0,30-4,00). A prolaktin 380 mU /L (ref. ≪ 420), és ő volt normocalcemic, teljes plazma kalcium korrigálva albumin, 40 g /l 2,47 mmol /l (ref. 2,25-2,60) és az ionizált kalcium 1,18 mmol /l (ref . 1,12-1,32) pH-ját 7,4. A szérum nemi hormon profilt kiderült tesztoszteron 3,1 nmol /L (ref. ≪ 3,5), ösztradiol 110 pmol /l (ref. 40-130), szabad androgén index 2,3 (ref. 1-5), DHEA-szulfát < 0,2 nmol /L (ref. 0,4-2,4), és androsztenedion 4,4 nmol /L (ref. 1,6-9,3). Her szérum 17-hidroxi-progeszteron enyhén megemelkedett 2,3 nmol /L (ref. 0,3-1,8), de ezt érezték, hogy nincs klinikai jelentősége. Citogenetikai vizsgálat perifériás vérből kiderült normális női kariotípus.
Mivel a tartósan emelkedett vizelet adrenalin kiválasztást, a CT megállapítása egy 2,5 cm bal mellékvese daganat valószínűleg funkcionális és ezt megerősítette a
123I-MetaIodoBenzyl guanidin ( MIBG) szcintigráfia. A beteg számára készült műtét fenoxi-30 mg bd egy héttel a műtét előtt propranolollal 40 mg hozzáadott BD napon a műtét előtt. A laparoszkópos bal mellékvese került sor, de ez lett átalakítva nyitott mellékvese technikai nehézségek miatt. Ezen eljárás során, körülbelül tíz csomók mérésére 3 és 5 mm észleltek a serosa felszínen a gyomor, amelyek közül az egyiket biopsziát. Ellenőrzés a többi hasűri zsigerek volt jelentéktelen. Core biopszia a kibővített csikló vettünk. A műtét utáni eseménytelen volt, a beteget kitűnően hasznosítás. Ismétlés vizelet katekolamin kiválasztás előtt mentesítés normális volt.
Két hónapos nyomon követés után neki mellékvese, a clitorectomy végeztünk, amikor egy fájdalmas fekély alakult ki a csikló. Katalógusa kóros elváltozásokat
Gyomor savós góc
Makroszkóposan, a biopszia állt szabálytalan darab cég rózsaszínes tan szövet mérő 6 × 5 × 4 mm. Mikroszkópos volt egy lobulated tumor álló hosszúkás egységes spindled sejteket elválasztottuk kollagén stromában. A sejtmagok voltak elrendezve Palisades, és nem volt citológiai atípia, és nincs mitoses voltak jelen. Kis daganatgócot terjeszteni a szomszédos simaizom. Immunhisztokémia mutatott erős és diffúz festődést a c-kit (CD117) és CD34. Volt még fokális festéssel desmin és simaizom aktin. Nem volt festődés a S100. Az eredmények összhangban voltak egy kis gasztrointesztinális sztróma tumor (GIST).
Clitoral biopszia és clitorectomy
biopszia állt egy mag puha, fehéres szürke szövet mérésére 9-X-7x-1,5 mm, és a teljes tumor állt a bőr alá tartozó polypoid tömege hozzávetőlegesen 90 × 40 mm. Volt egy nagy vese alakú fekélyes terület jól definiált fehéres árrés mérő 43 × 30 mm. Mikroszkóposan voltak kis körülírt fészkeit idegi típusú szerkezetek emlékeztető szenzoros Meissnerian részecskéken elválasztva kissé nyálkás stroma, amely nagyszámú hízósejtek. Fokálisan volt egy diffúz építészeti minta rosszul definiált füzetek a citológiailag egységes orsó sejtek bőséges fibrillaris mátrix. Immunhisztokémia kimutatta S100 pozitivitást. A szövettani diagnózis a csikló neurofibroma.
Bal mellékvese tumor katalógusa A bal mellékvese mért 48 × 25 × 50 mm és megmérjük 11 gramm. Domború felülete felett volt góc mérő 20 × 20 × 13 mm volt, ami tarka szürke-sárga-narancssárga a vágási felületen. A 6 mm-es szürkés góc találták belül a szomszédos zsírszövet. Mikroszkópos, a többség a tumor (70%) mutatott tipikus jellemzői a pheochromocytoma, diszkrét fészkek tumorsejtek elválasztott finom fibro-érrendszeri szeptummal. Ezek a sejtek nagy szembetűnő szemcsés citoplazma és megmutatta pleomorphism, sok sejtnek különböző nucleolusok. A mitotikus alakok nem látott, és nem volt elhalás. A sejteket kiterjesztette a kapszulát fokális a peri-mellékvese zsír. Nem érinvázió volt látható. Néhány területen a tumorsejteket szélesebb körben elválasztva vastag sávok kollagén. A második komponens a tumor (30%) mutatott jellemzői ganglioneuroma, nagy érett ganglion típusú sejtek nagy magok, a központi eozinofil nucleolusok és bőséges citoplazma ágyazva egy fibrilláris neurális kötőelemek tartalmazó citológiailag egységes orsó alakú sejtek. Nem primitív neuroblastic elemek látták. A két tumor komponens jól körülhatárolt egyes területeken, de fokálisan megjelent összekeverjük. Katalógusa immunhisztokémiai festéssel nem mutatott a tumor elemek proliferációs marker Ki-67, vagy a p53 fehérjét. Pozitív festéssel az S100 proteint azonosítottak a sustentacular sejtek normális mellékvese velő és a phechromocytoma, valamint a ganglion sejtek a ganglioneuroma. A mellékvese tumor tehát vegyes phaeochromocytoma /ganglioneuroma vagy összetett phaeochromocytoma.
A góc megjegyezte mellett a fő mellékvese duzzanata állt kibővített ganglion habosított és torz idegrostok. A látszat azt fokális bevonásának neurofibroma. Katalógusa Vita katalógusa neurofibromatózis 1-es típusú (NF1) az egyik leggyakoribb dominánsan öröklődő betegségek, a születési előfordulása 1 3000 [1]. A klasszikus értelmezése szerint a patológus von Recklinghausen több mint egy évszázaddal ezelőtt jól megfelel a leggyakoribb klinikai kép [2]. A National Institutes of Health konszenzus nyilatkozat [3] felvázolt hét diagnosztikus kritériumai NF1 és két vagy több kritériumokat kell jelen lennie ahhoz, hogy a diagnózist. Ezek a kritériumok a következők: 6 vagy több café-au-lait foltok (méret > 5 mm pre-pubertás betegek és méret > 15 mm utáni pubertás betegeknél); 2 vagy több neurofibrómák vagy 1 vagy több Plexiform neurofibrómák; hónalji vagy lágyéki freckling; 2 vagy több Lisch csomók; optikai gliomák; specifikus csontos diszpláziás léziók; vagy az első fokú rokon NF1 diagnosztizálták a fenti kritériumoknak.
kifejezése NF1 nagyon változó. Betegekben a betegség fokozott előfordulása jó- és rosszindulatú daganatok. Ezt mutatja a vizsgálat során 70 felnőtt NF1 betegeknél Svédországban [1]. Rosszindulatú daganatok számoltak négyszer gyakrabban az NF1 csoportban, mint az általános népesség körében. Az NF1 csoport, 24% alakult a rosszindulatú daganatok (16% karcinóma, szarkóma 7%, 1% melanoma), és 17% alakult jóindulatú daganatok (7% GIST, 6% phaeochromocytoma, 3% adenoma és 1% meningeoma). Feokromocitoma (Pheo) jól ismerik a beállítás NF1, és azt mondta, hogy 10-szer gyakoribb, mint a lakosság. [4] NF1 megtalálható 5-25% -ánál Pheo [4], mivel a teljes incidenciája Pheo az NF1 1% [5].
Kompozit mellékvese medulláris tumorok, a másik viszont, nagyon ritkák. Egy elemzés a Nemzeti Rákkutató Intézet 120 mellékvese és extra mellékvese Pheos, csak négy volt kompozit fenotípus, így a teljes előfordulási 3% [7]. A felülvizsgálat Moore és Biggs [8] már csak 13 esetben összetett phaeochromocytoma-ganglioneuroma (Pheo-GN) az irodalomban. Ezek közül csak három jelentést talált kompozit Pheo-GN előforduló beállítását NF1 [6, 9, 11]. Esetünkben a jelentés a negyedik ilyen jelentett előfordulása. Ezen túlmenően, a mellékvese ganglioneuroma és egy ellenoldali Pheo olyan betegben, NF1 számoltak [10].
Bolande [12] volt az első, hogy tegyen javaslatot a koncepció neurocristopathies vagy tumorok származó idegtaréj-eredetű sejtek. Ezek a daganatok idegtaréjban eredetű állnak különböző kombinációi mellékvesevelő vagy extra-mellékvese kromaffin sejtek, neuroblaszt vagy szimpatikus ganglion sejtek különböző differenciálódási stádiumai, akár jóindulatú vagy rosszindulatú. Pheo, paraganglioma, GN, neuroblasztóma és neurofibroma képviselnek ilyen neurocristopathies.
Sympathogonia származó egyes idegtaréjban sejtek differenciálódnak neuroblaszt és pheochromoblasts. Ezek idegtaréjban származó sejtek vándorolnak ventralisan és különbséget okozhat a sejtes elemei a szimpatikus ganglionok és a mellékvese velő. Bármilyen migrációs zavar vagy maldevelopment a idegtaréjban vezethet a fejlesztési kompozit daganatok. Mivel ezek a sejt populációk hasonló levezetés várhatnánk összetett mellékvese velő tumorok gyakrabban, mint ami a szakirodalom ismerteti, és ez jelenthet hogy a bejelentett vagy a ismerése ezt a feltételt.
NF1 befolyásolja a gyomor-bél traktusban 10 -25% -ában [15], és ez így négy alapelv formában: stromalis tumorok, neuronális hiperplázia, ganglioneuromatosis és endokrin tumorok, a duodenumban és periampullaris régiókban. Akut vagy visszatérő gasztrointesztinális vérzés előfordulhat akár 40% -át ezek a betegek [16]. Gasztrointesztinális stroma tumorok (GIST-ek) között mesenchymalis tumorok a gyomor-bél traktusban, amelyek nem rendelkeznek semmilyen az azonosító jellemzőit jelző eredetű specifikus kötőszöveti sejt. Ezek különböznek simaizom daganat mindkét immunfenotípus és molekuláris. Nemrégiben ultrastrukturális hasonlóságokat találtak között GIST sejtek és az intersticiális sejtes Cajal (gasztrointesztinális pacemaker sejt) [13], és ezenkívül vannak immunhisztokémiai hasonlóságokat egyaránt expresszáló KIT tirozin-kináz-receptor. Azt javasolták, hogy a GIST-ek származhatnak őssejtek, amelyek megkülönböztetik felé pacemaker sejt és a simaizom sejt. Lényeg fejezheti számos különböző fenotípusok, ami azt eredményezte, hogy számos betűszavak őket leíró [14]. Myoid sejttípus hívták simaizom GIST (smGIST) idegsejt típusok úgynevezett gyomor-autonom idegrendszer daganatai (GANT), Cajal sejttípusok úgynevezett gyomor-pacemaker sejt tumorok (GIPACT) és kevert típusú sejtek (vegyes GIST). A biológiai viselkedése GIST volt nehéz megjósolni. Többváltozós túlélési adatokat 1004 Lényeg kimutatta a tumor mérete és elhelyezkedése, mitotikus mértéke és az életkor is fontos prognosztikai faktorok [17]. Azonban nem módszer vagy módszerek kombinációja bizonyult megbízhatónak malignitás meghatározásához minden esetben.
Genitourinary neurofibrómák ritkák és clitoris bevonása NF1 ritkán beszámoltak. Azonban, amikor ez bekövetkezik, clitoromegalia gyakran a bemutató jel. Sok esetben ez veleszületett. Egy vizsgálatban 236 családok NF1, négy betegnél csikló bevonása és három bevonása volt, csak a csikló [18]. A felülvizsgálatot a szakirodalom által Sulphen [18] talált 26 beteg NF1 és a klitorisz bevonásával.
Ez esetben a jelentés bemutatja a heterogenitás NF1 egyidejű bemutatásával három ritka megnyilvánulása ez a lenyűgöző rendellenesség, azaz összetett Pheo-GN a mellékvese velő több gyomor GIST és neurofibroma a csikló. Tudomásunk szerint ez az első eset, hogy ilyen esetben számoltak be a szakirodalomban. 1. ábra A: Neurofibroma a csikló. B: clitoromegalia.
2. ábra A gyomor gasztrointesztinális sztróma tumor (GIST), mely füzetek egységes orsó sejtek (A, H &E eredeti nagyítás × 250), és a c-kit-festéssel a tumorsejtek képest hiányzik festődés szomszédos simaizom bal felső (B, c-kit eredeti nagyítás × 100).
3. ábra Neurofibroma a csikló mutató növekedési mintázata Meissner szervek (H &E, az eredeti nagyítás × 250).
4. ábra Kompozit mellékvese tumor phaeochromocytoma (bal alsó) összevonása ganglioneuroma (jobb felső) (H &E, az eredeti nagyítás × 250). katalógusa nyilatkozatok katalógusa Szerzők eredeti beküldötteknek képeket
alábbiakban a linkeket a szerzők eredeti benyújtott fájlok képeket. 12956_2006_42_MOESM1_ESM.pdf A szerzők eredeti fájlt az 1. ábra szerinti 12956_2006_42_MOESM2_ESM.tiff A szerzők eredeti fájl 2. ábrán 12956_2006_42_MOESM3_ESM.tiff A szerzők eredeti fájl 3. ábra 12956_2006_42_MOESM4_ESM.tiff A szerzők eredeti fájl a 4. ábra
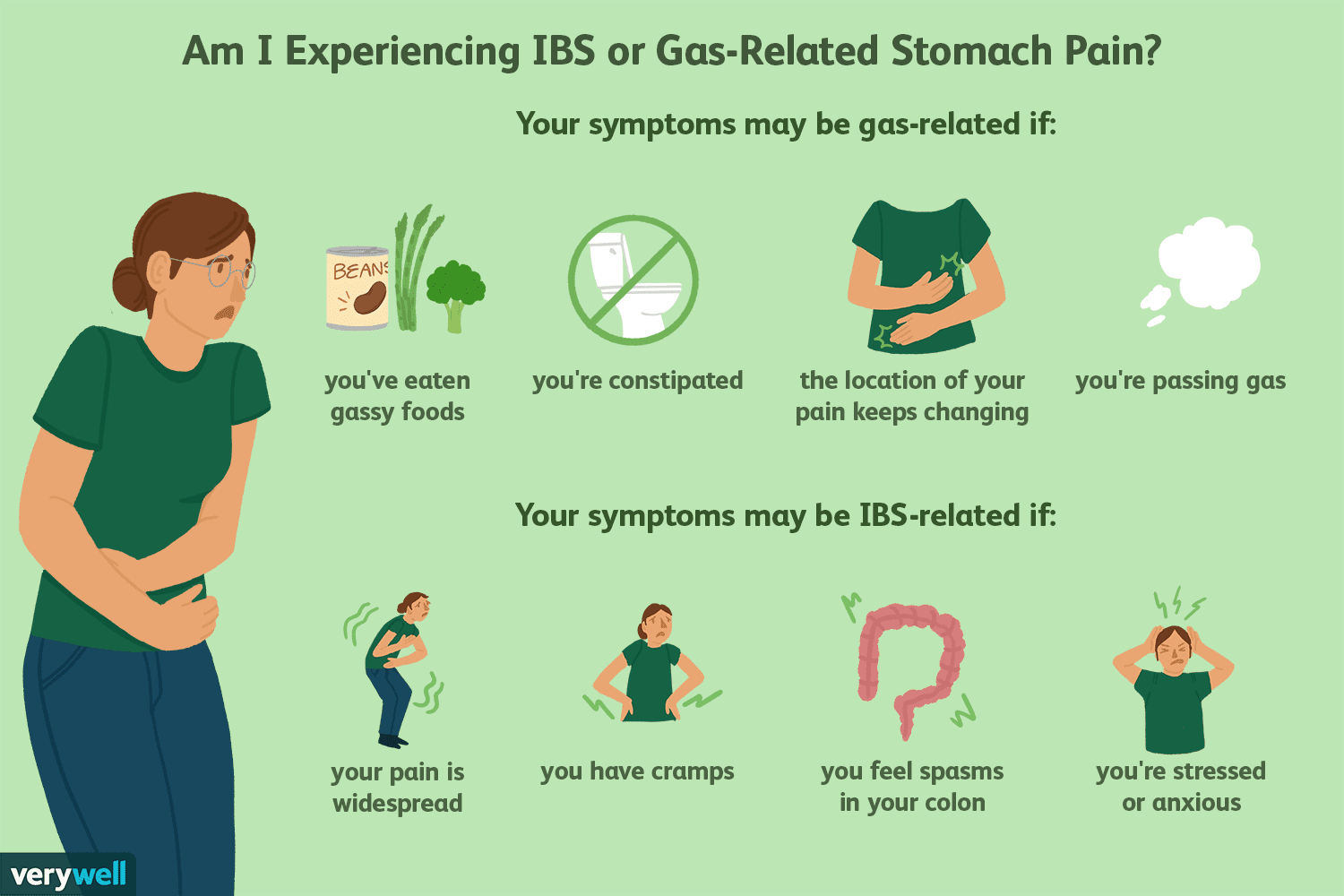 Beszorult gázfájdalom és egyéb IBS hasi fájdalomforrások
Ha irritábilis bélszindrómában (IBS) szenved, azt gondolhatja, hogy a hasi fájdalmát a bennrekedt bélgáz okozza. De egy része más forrásból származhat. A bélgázok a bélbaktériumok ételre gyakorolt
Beszorult gázfájdalom és egyéb IBS hasi fájdalomforrások
Ha irritábilis bélszindrómában (IBS) szenved, azt gondolhatja, hogy a hasi fájdalmát a bennrekedt bélgáz okozza. De egy része más forrásból származhat. A bélgázok a bélbaktériumok ételre gyakorolt
 A kutyájának is szednie kell probiotikumot?
Ez a kép a két kutyámról, Breáról és Gracie-ről. Mindketten 9 év körüliek ezen a képen. Amikor felvették, lehetett látni, hogy éreztek életkorukat. Brea rossz ízületi gyulladással bicegett a csípőjéb
A kutyájának is szednie kell probiotikumot?
Ez a kép a két kutyámról, Breáról és Gracie-ről. Mindketten 9 év körüliek ezen a képen. Amikor felvették, lehetett látni, hogy éreztek életkorukat. Brea rossz ízületi gyulladással bicegett a csípőjéb
 A probiotikumok terápiás előnyöket kínálhatnak a biopoláris betegek számára
A baltimore -i Sheppard Pratt Health rendszer tanulmánya kimutatta, hogy a probiotikumok potenciális terápiás megközelítésként szolgálhatnak a bipoláris zavar és más pszichiátriai állapotok kezelésére
A probiotikumok terápiás előnyöket kínálhatnak a biopoláris betegek számára
A baltimore -i Sheppard Pratt Health rendszer tanulmánya kimutatta, hogy a probiotikumok potenciális terápiás megközelítésként szolgálhatnak a bipoláris zavar és más pszichiátriai állapotok kezelésére