Polymorfismer i ERCC1, GST, TS og MTHFR forutsi klinisk utfall av magekreft pasienter behandlet med platina /5-Fu-basert kjemoterapi: en systematisk
Abstract
Bakgrunn
tross genetisk polymorfisme i respons til platina /5 -Fu kjemoterapi i magekreft (GC) har blitt studert, data rapportert så langt er motstridende og kritisk vurdering er nødvendig før oversettelse til behandling av GC.
Metoder
Vi utførte en meta-analyse ved hjelp av 20 utvalgte studier å undersøke polymorfismer av ERCC1, GST, TS og MTHFR i forutsi kliniske utfall (responsrate, total overlevelse og toksisitet) av GC pasienter behandlet med platina /5-Fu-basert kjemoterapi. Foreningen ble målt ved hjelp av tilfeldige /fast effekt odds ratio (ORS) eller hazard ratio (HRS) kombinert med sine 95% konfidensintervall (CIS) i henhold til de studiene heterogenitet. Statistisk analyse ble utført med programvaren STATA 9.0 pakke
. Resultater
Ingen signifikant sammenheng ble funnet mellom responsrate og genetisk polymorfisme i TS, MTHFR, ERCC1, GSTM1 og GSTP1. Men svarprosenten var høyere i GSTT1 (+) genotype sammenlignet med GSTT1 (-) genotype (T- /T +: OR = 0,67, 95% KI: 0,47 til 0,97). Med hensyn til langsiktig utfall, kunne vi observere en betydelig lengre total overlevelse i TS 3R /3R [(2R2R + 2R3R) /3R3R: HR = 1,29, 95% KI: 1,02 til 1,64] og GSTP1 GG /GA [(GG + AG) /AA: HR = 0,51, 95% KI: (0,39, 0,67)] genotyper. I tillegg ble signifikant sammenheng påvist mellom giftighet og genetisk polymorfisme i TS, MTHFR og GSTP1 i inkluderte studiene.
Konklusjon
Polymorfisme av ERCC1, GST, TS og MTHFR var nært knyttet til kliniske utfall av GC pasienter behandlet med platina /5-Fu-basert kjemoterapi. Studier med stor utvalgsstørrelsen ved hjelp av metoden for multi-variant analyser kan hjelpe oss til å gi mer overbevisende data på den antatte foreningen i fremtiden.
Nøkkelord
Magekreft Genetisk polymorfisme Kjemoterapi Meta-analyse Bakgrunn
I hele verden, magekreft (GC) er fortsatt en av de viktigste årsakene til kreft-relaterte dødsfall på verdensbasis [1]. Kirurgi er den primære modalitet for å håndtere tidlig stadium og lokalt avansert sykdom. Men selv etter gastrektomi, mange pasienter tilbakefall med lokalt tilbakefall eller fjernmetastaser [2]. I tillegg, omtrent 20-30% av pasientene har inoperabel sykdom ved diagnose. Derfor, de fleste av pasientene trenger en systemisk behandling på et tidspunkt i sykdommen sin.
Palliativ kjemoterapi for avansert GC har blitt allment akseptert som en standard behandling i flere tiår. Og nyere studier har vist at peri-operative adjuvant kjemoterapi (pre- eller postoperativ) kan forbedre overlevelse og livskvalitet hos pasienter med GC [3]; imidlertid forventet overlevelse for avansert sykdom er generelt dårlig (mindre enn ett år). Inntil nå, 5-fluorouracil (5-FU) og platina er de vanligste legemidlene som brukes for GC både i adjuvant og avanserte innstillinger, men det finnes ingen standard kombinasjonsregimer [4]. I tillegg har effekt utfall for en rekke nye forbindelser (som paclitaxel, oksaliplatin og kapecitabin) ikke vist definitive klinisk nytte eller overlegenhet til eldre legemidler hos pasienter med avansert GC [5-7]; og hos noen pasienter terapi resulterer i alvorlige, uforutsigbar toksisitet uten tumorrespons. Følgelig, for å tillate det å kunne skjelne pasienter der en spesiell terapi vil utøve en reell fordel, er det avgjørende å identifisere faktorer som er relevante for å respons på fluorouracil /platina, så vel som faktorer som er predisponert for utvikling av alvorlig toksisitet. I denne forbindelse, Farmakogenetikk, et forskningsfelt som identifiserer arvelig genetisk variasjon som kan påvirke behandlingsresultatene, kan tillate en skreddersydd administrasjon regime som maksimerer klinisk respons mens begrense de negative effektene av behandling [8, 9]., En økende mengde bevis tyder på at inter-individuell variasjon i narkotika enzymer og nucleotide excision reparasjon (NER) system kan påvirke kreft narkotika effekt ved å påvirke DNA-reparasjon eller relaterte enzymaktivitet [10]. Nylig, finner mange studier som gener involvert i DNA avgiftning (glutation S-transferaser, GST) og reparasjon (excision reparasjon kryss fallende 1, ERCC1) kontrollere effekten av platina [11, 12], mens metylentetrahydrofolat reduktase (MTHFR) og tymidylatkinase syntase (TS) er forbundet med 5-Fu metabolisme [11, 13]. Til tross for genetisk polymorfisme i respons til platina /5-Fu kjemoterapi i GC er blitt rapportert [14], rapporterte data så langt er motstridende og kritisk behandling er nødvendig før oversettelse for behandling av GC. Derfor er en systematisk gjennomgang utelukkende for å gi en omfattende og up-to-date oversikt vedrørende mulige roller for genetisk polymorfisme i GC-behandling.
I denne studien, vurderte vi litteratur eksisterende og gjennomførte en meta-analyse for å undersøke polymorfismer av ERCC1, GST, TS og MTHFR forutsi kliniske utfall av GC pasienter behandlet med platina /5-Fu-basert kjemoterapi.
Metoder
søke~~POS=TRUNC strategi~~POS=HEADCOMP
En dataassistert søk på Pubmed /Medline og Embase var utført for å identifisere relevante og tilgjengelige publiserte artikler ved hjelp av disse søkeordene: magekreft /carcinoma /svulst /tumor /svulst, kreft i magesekken /carcinoma /svulst /tumor /svulst, polymorfisme /polymorfisme og kjemoterapi. Den øvre grensen for søketidspunktet var ikke begrenset, og den nedre grensen var januar 2012. Både fritekst og MeSH søk etter søkeord som ble brukt. Språket at papirene ble skrevet i var ikke begrenset. . For å identifisere flere potensielt relevante studier, referanselister fra utvalgte studier gjennom elektronisk søking ble hånd søkte
inklusjons- og eksklusjonskriterier
Den inklusjonskriterier i denne meta-analysen var som følger: 1) patologisk bekreftet GC med en målbar lesjon; 2) ikke samtidig ukontrollert medisinsk sykdom; 3) pasienter som fikk ingen annen adjuvant behandling, for eksempel strålebehandling eller immunterapi; 4) kliniske utfall [responsrate (RR), total overlevelse (OS) eller toksisitet) om genetisk polymorfisme [ERCC1-118, GST (GSTM1, GSTP1-105 eller GSTT1), TS 5'-uoversatt region eller MTHFR-667] i GC pasienter behandlet med platina /5-Fu-basert kjemoterapi ble rapportert
eksklusjons~~POS=TRUNC kriteriene~~POS=HEADCOMP var:. 1) inkluderte pasienter med karsinom annet enn magen; 2) in vitro-studier; 3) studiene var ikke original forskning, for eksempel artikkel; 4) platina /5-Fu ble ikke inkludert i kjemoterapikurer. Vi inkluderte litteraturen med største utvalgsstørrelsen ved gjentatte publikasjoner
data utvinning
To forfattere (Zhen Wang og Jun-Qiang Chen) hentet ut data uavhengig av alle kvalifiserte studier med forhåndsdefinerte tabeller, som inkluderte elementer som følger:. Førsteforfatter, publikasjon tid, land og etnisitet av pasientene, molekylære markører, sample size, evalueringskriterier, kjemoterapikurer og kliniske utfall (RR, OS og toksisitet). Om nødvendig, ble forfatterne av den opprinnelige litteratur kontaktet etter tilgjengelige data. Uenighet ble løst ved konsensus.
Statistisk analyse
Hazard ratio (HRS) og deres 95% konfidensintervall (CIS) for OS ble oppnådd fra hver primærstudie. I tilfelle dataene ikke var direkte registrert i grunnskolen rapporter beregnet vi HR og deres 95% CI fra overlevelseskurver ved hjelp publisert metode [15, 16]. Kaplan-Meier-kurver av inkluderte studiene ble lest av Engauge Digitaliserer versjon 2.11 (fri programvare lastet ned fra http:. //Sourceforge net). HR beregning regneark ble fritt lastes ned fra http:.. //Www trialsjournal com /content /supplerende /1745-6215-8-16-s1 xls.. Den odds ratio (OR) for RR og timer for OS ble beregnet på grunnlag av en fast effekt modellen først ved hjelp av Stata 9.0 pakken. Heterogenitet mellom inkluderte studiene ble testet ved hjelp av χ
2 test (betraktet som signifikant dersom P
< 0,10). Hvis hetrogeniteter var til stede, var en av de følgende tiltak benyttes for å forsøke å forklare dem: (1) subgruppe analyse; (2) sensitivitetsanalyse; eller (3) tilfeldig-effekt modell for meta-analyse. Alle P
verdiene var tosidig og alle konfigurasjonsenheter hadde en tosidig sannsynlighet dekning på 95%.
Resultater
Study utvalg og beskrivelse
Ifølge søkestrategi referert, totalt 224 litteratur ble gitt: 130 i PubMed og 94 i EMBASE. Ved å bla gjennom titler og abstracts, fant vi at mange av artiklene var irrelevant og noen ble identifisert duplicately, dermed 69 artikler forble for potensielle inkludering og ble innhentet i fulltekst. Etter gjennomgang av hele teksten, ble 49 litteratur ekskludert. De viktigste årsakene til eksklusive studiene var som følger: studie type (oversiktsartikler og in vitro studier), deltakere (inklusjon av pasienter med karsinom annet enn magen), intervensjoner (utelukkelse av platina /5-Fu i kjemoterapikurer) og repeterende utgivelse. Endelig 20 studier (2189 pasienter) ble ansett som kvalifisert for inkludering [11, 14, 17-34]. Fremgangsmåten i studien utvalg ble oppført i figur 1. Figur 1 QUORUM flytskjema for studier.
Blant de 20 inkluderte studiene, antallet TS, MTHFR, ERCC1 og GST-polymorfisme studien var 10 (952 pasienter), 9 (988 pasienter), 10 (1080 pasienter) og 10 (1187 pasienter), respektivt. Utvalgsstørrelsen varierte 25-200 og publikasjonen gang var fra 2002 til 2011. Deltakerne var asiatisk og europeisk. De viktigste kjennetegn ved 20 inkluderte studiene ble oppført i tabell 1.Table 1 Kjennetegn på studier inkludert i den systematiske gjennomgang
Study (referanse)
Pasienter
Molekylær markør
Etnisitet (land)
Vurderingskriterier
Utvalgsstørrelse størrelse~~POS=HEADCOMP
kjemoterapikurer
Outcomes
Goekkurt 2006, [11]
Pasienter med avansert GC
TS, GST, MTHFR, ERCC1-118
Europeisk (Tyskland)
RECIST
52
5-Fu + cisplatin + folinsyre
RR og OS
RUZZO 2006 [14]
Pasienter med avansert GC
TS, GST, MTHFR, ERCC1-118
Europeisk (Italia)
Andre
175
fluorouracil /cisplatin
RR og OS
Shim 2010 [17]
Pasienter med residiverende eller metastatisk GC
GST
asiatiske (Korea)
RECIST
200
Paclitaxel /docetaxel + cisplatin
RR og OS
Park 2011 [18] Hotell Pasienter med metastatisk GC
ERCC1-118
asiatiske (Korea)
RECIST
108
S-1 + cisplatin
RR og OS
Han 2010 [19]
Pasienter med residiverende eller metastatisk GC
TS, ERCC1-118
asiatiske (Korea)
RECIST
38
5-Fu + folinsyre + oksaliplatin
RR og OS
Stocker 2009 [20]
Neoadjuvant kjemoterapi for lokalavansert GC uten fjernmetastaser
ERCC1-118
Europeisk (Tyskland)
Andre
178
5-Fu + folinsyre + cisplatin
RR og OS
Seo 2009 [21]
Pasienter med residiverende eller metastaserende GC
TS, GST, ERCC1-118
asiatiske (Korea)
RECIST
94
5-Fu + oksaliplatin /irinotecan
RR, OS og giftighet
Liu 2011 [22]
Pasienter med avansert GC
GST, ERCC1-118
Asia (Kina)
NR
126
5-FU + leukovorin + oksaliplatin
OS
Ott 2008 [23]
Neoadjuvant kjemoterapi for lokalavansert GC uten fjernmetastaser
GST
europeiske (Tyskland)
Andre
139
5-Fu + folinsyre + cisplatin
RR og OS
Li 2010 [24]
Pasienter med avansert GC
GST
asiatiske (Kina)
Andre
92
5-Fu + oksaliplatin
RR, OS og giftighet
Lu 2004 [25] Hotell Pasienter med fremskreden GC
MTHFR
asiatiske (Kina)
WHO
75
5-Fu + folinsyre
RR og giftighet
Huang 2009 [26] Hotell Pasienter med GC etter kurativ kirurgi
GST, ERCC1-118
asiatiske (Kina)
NR
102
5-Fu + folinsyre + oksaliplatin
OS
Shitara 2010 [27]
Pasienter med inoperabel GC
TS, MTHFR
asiatiske (Japan)
NR
132
5-Fu et al.
OS og giftighet
Huang 2009 [28]
Pasienter med GC etter kurativ kirurgi
TS, MTHFR
asiatiske (Kina)
NR
116
5-Fu + folinsyre et al.
OS
Ishida 2002 [29]
Pasienter med GC etter operasjonen
TS
asiatiske (Japan)
NR
51
5-Fu et al.
OS
Keam 2008 [30] Hotell Pasienter med residiverende eller metastatisk GC
GST, ERCC1-118
asiatiske (Korea)
WHO
73
5-Fu + folinsyre + oksaliplatin
RR og OS
Goekkurt 2009, [31 ]
Pasienter med avanserte GC
TS, GST, MTHFR, ERCC1-118
Europeisk (Tyskland)
Andre
134
5-Fu + folinsyre + oksaliplatin /cisplatin
RR, OS og giftighet
Ott 2006 [32]
Neoadjuvant kjemoterapi for pasienter med lokalavansert GC
TS, MTHFR
Europeisk (Tyskland)
Andre
135
5- Fu + cisplatin
RR og OS
Ott 2011 [33]
Neoadjuvant kjemoterapi for pasienter med lokalavansert GC
MTHFR
Europeisk (Tyskland)
Andre
144
5-Fu + folinsyre + cisplatin
OS
Lee 2005 [34]
Pasienter med avansert GC
TS, MTHFR
asiatiske (Korea)
NR
25
5-Fu et al
OS
GC. magekreft; Andre: evalueringskriterier som ble beskrevet i originale papirer; NR: ikke rapportering; RR: svarprosent; OS:. Total overlevelse
Association mellom TS, MTHFR polymorfisme og 5-Fu basert kjemoterapi
Svarprosent (RR)
Fem studier (534 pasienter) rapporterte sammenhengen mellom TS polymorfisme og RR [11, 14, 19, 31, 32]. P
verdi av heterogenitet testen var 0,471 og et fast-effekt-modellen ble anvendt. Den samlede analysen viste at det var ingen signifikant forskjell mellom RR av pasienter med 3R /3R genotype, og at pasienter med 2R /3R og 2R /2R genotyper [(2R2R + 2R3R) /3R3R: OR = 0,92, 95% KI : 0,62 til 1,37]. Tatt i betraktning at RR kan bli påvirket av etnisitet, evalueringskriterier og formålet med kjemoterapi, utførte vi subgruppeanalyse. Og ingen sammenheng ble observert mellom TS polymorfisme og RR ved hjelp av metoden for subgruppe analyse (tabell 2). Tabell 2 Sammenhengen mellom TS polymorfisme og kliniske resultater
Study (referanse)
RR (n /N)
OS (HR, 95% KI)
Toxicity
Goekkurt 2006 [11]
3R3R: 3/12; 2R2R + 2R3R: 9/32
NR
NR
RUZZO 2006 [14]
3R3R: 22/61; 2R2R + 2R3R: 48/114
NR
NR
Han 2010 [19]
3R3R: 16/28; 2R2R + 2R3R: 5/10
NR
NR
Seo 2009 [21]
NR
NR
NSS
Shitara 2010 [27]
NR
(2R2R + 2R3R) /3R3R: 1,28 (0,85, 1,96)
NSS
Huang 2009 [28]
NR product: (2R2R + 2R3R) /3R3R: 1,54 (0,879, 2,698)
NR
Ishida 2002 [29]
NR product: (2R2R + 2R3R) /3R3R: 1,26 (0,81, 1,95)
NR
Goekkurt 2009 [31]
3R3R: 17/33; 2R2R + 2R3R: 35/101
NR
grad 3/4 leukopeni: P
= 0,047
Ott 2006 [32]
3R3R: 10/41; 2R2R + 2R3R: 23/94
2R2R /3R3R: 0,33 (0,22, 0,51); 2R3R /3R3R: 0,52 (0,37, 0,74)
NR
Lee 2005 [34]
NR product: (2R2R + 2R3R) /3R3R: 1,16 (0,68, 1,99)
NR
kombinert analyse (OR /HR, 95CI%)
OR: (2R2R + 2R3R) /3R3R plakater (2R2R + 2R3R) /3R3R
___
Totalt: 0,92 (0,62, 1,37);
Totalt: 1,29 (1,02, 1,64)
RECIST undergruppe: 0,93 (0,33, 2,63);
Alle studiene rapporterte data var asiatisk
Andre undergruppe: 0,92 (0,60, 1,41);
Palliativ undergruppe : 1,16 (0,68, 1,98)
asiatisk undergruppe: 0,75 (0,18, 3,19);
Adjuvans undergruppe: 1,33 (1,02, 1,73)
europeiske undergruppe: 0,94 (0,62, 1,41)
Palliativ undergruppe: 0,90 (0,58, 1,40)
Neoadjuvant undergruppe: 1,00 (0,43, 2,36)
RR: svarprosent; OS: total overlevelse; OR: odds ratio; HR: hazard ratio; NR: ikke rapportering; NSS. Ingen statistisk signifikans
data for 5 inkludert studier (571 pasienter) anvendelig for å analysere sammenhengen mellom MTHFR polymorfisme og RR [11, 14, 25, 31, 32]. P
verdi av heterogenitet testen var mindre enn 0,1 og en tilfeldig-effekt-modellen ble anvendt. Kombinert analyse viste at det var ingen signifikant forskjell mellom RR av pasienter med C /C genotype og at pasienter med C /T og T /T genotype [(CT + TT) /CC: OR = 1,12, 95% KI: 0,49 -2,55]. For å utforske kilder til heterogenitet, utførte vi subgruppeanalyse. Resultatene av subgruppeanalyse viste at ingen signifikant sammenheng unntatt asiatisk og WHO undergrupper, hvor bare ett inkluderte studier rapportert [25] en signifikant høyere RR i C /T eller T /T genotyper sammenlignet med C /C genotype (OR = 7,1, 95% KI: 1,5 til 33,53; Tabell 3). Tabell 3 Sammenhengen mellom MTHFR polymorfisme og kliniske resultater
Study (referanse)
RR (n /N)
OS (HR, 95% KI)
Toxicity
Goekkurt 2006 [11]
CC: 10/28; CT + TT: 3/22
NR
NR
RUZZO 2006 [14]
CC: 13/34; CT + TT: 57/141
NR
NR
Lu 2004 [25]
CC: 2/24; CT + TT: 20/51
NR
Kvalme /oppkast: P
= 0,002
Shitara 2010 [27]
NR
TT /(CT + CC): 0,57 (0,33 , 0,97)
NSS
Huang 2009 [28]
NR
TT /(CT + CC): 0,595 (0,349, 1,012)
NR
Goekkurt 2009 [31]
CC: 18/59; CT + TT: 34/75
NR
NSS
Ott 2006 [32]
CC: 16/50; CT + TT: 17/85
CT /CC: 1,8 (1,13, 2,88); TT /CC: 0,93 (0,54, 1,62)
NR
Ott 2011 [33]
NR
CT /CC: 0,8 (0,50, 1,36); TT /CC: 0,5 (0,18, 1,49)
NR
Lee 2005 [34]
NR
CT /CC: 0,91 (0,58, 1,43); TT /CC: 1,16 (0,65, 2,08)
NR
Kombinert analyse (OR /HR, 95CI%)
OR: (CT + TT) /CC
CT /CC (totalt): 1,10 (0,67, 1,79);
___
Totalt: 1,12 (0,49, 2,55); RECIST undergruppe: 0,28 (0,07, 1,20);
CT /CC (Asian undergruppe): 0,91 (0,58, 1,43);
WHO undergruppe: 7,1 (1,5, 33,53);
CT /CC (European undergruppe ): 1,21 (0,54, 2,67);
Andre undergruppe: 1,05 (0,51, 2,16);
CT /CC (Palliativ undergruppe): 0,91 (0,58, 1,43);
asiatisk undergruppe: 7,1 (1,5, 33.53);
CT /CC (Neoadjuvant undergruppe): 1,21 (0,54, 2,67) TT /CC (totalt): 0,94 (0,65, 1,37);
Europeisk undergruppe: 0,85 (0,41, 1,77)
TT /CC (Asian undergruppe): 1,16 (0,65, 2,08);
Palliativ undergruppe: 1,40 (0,55, 3,60);
TT /CC (European undergruppe): 0,81 (0,50, 1,33);
Neoadjuvant undergruppe : 1,12 (0,49, 2,55)
TT /CC (Palliativ undergruppe): 1,16 (0,65, 2,08);
TT /CC (Neoadjuvant undergruppe): 0,81 (0,50, 1,33)
RR: svarprosent; OS: total overlevelse; OR: odds ratio; HR: hazard ratio; NR: ikke rapportering; NSS. Ingen statistisk signifikans
Total overlevelse (OS)
Fem studier (459 pasienter) rapporterte sammenhengen mellom TS polymorfisme og OS [27-29, 32, 34], men dataene rapportert av Ott et al. kan ikke brukes til kombinert analyse [32], som viste at 2R /2R eller 2R /3R genotyper var signifikant assosiert med en gunstig OS (2R2R /3R3R: HR = 0,33, 95% KI: 0,22 til 0,51; 2R3R /3R3R: HR = 0,52, 95% KI: 0,37 til 0,74). Derfor ble data fra 4 Asiatiske studier (324 pasienter) kombinert [27-29, 34]. P
verdi av heterogenitet testen var 0,909 og et fast-effekt-modellen ble anvendt. Meta-analyse viste at en betydelig lengre OS ble observert i 3R /3R genotype sammenlignet med 2R /2R eller 2R /3R genotyper [(2R2R + 2R3R) /3R3R: HR = 1,29, 95% CI: 1,02 til 1,64; Tabell 2. (tilleggsfiler 1: Figur S1). Når du vurderer formålet med kjemoterapi, fant vi signifikant sammenheng i adjuvant undergruppe men ingen betydning i palliativ undergruppe (tabell 2).
Data fem inkluderte studier (552 pasienter) var aktuelt for å analysere sammenhengen mellom MTHFR polymorfisme og OS [27 , 28, 32-34], men de data som rapporteres av Shitara et al. og Huang et al. kunne ikke brukes for kombinert analyse [27, 28]. Disse to studiene rapporterte pasienter med TT genotype hadde en lengre OS sammenlignet med C /T eller C /C genotyper; selv om forskjellen ikke var statistisk signifikant i studien av Huang et al. (Tabell 3). Derfor ble data fra 3 inkluderte studiene (323 pasienter) samlet [32-34]. Meta-analysen viste ingen signifikant sammenheng ble sett mellom MTHFR polymorfisme og OS (CT /CC: HR = 1,10, 95% KI: 0,67 til 1,79; TT /CC: HR = 0,94, 95% KI: 0,65 til 1,37). I tillegg var det undergruppeanalyse ikke viser signifikant forskjell (tabell 3). (Tilleggsfiler 2: Figur S2)
Toxicity
Fordi ulike evalueringskriterier ble brukt og svært få studier rapporterte resultatene, vi gjorde ikke kombinere data. Tre studier (360 pasienter) rapporterte sammenhengen mellom TS polymorfisme og toksisitet [21, 27, 31]. To studier fant ingen signifikant genetisk type ble observert i forbindelse med TS polymorfisme [21, 27]; men Goekkurt et al. rapporterte at bærere av minst én 3R haplotype var på lavere risiko for å utvikle grad 3/4 leukopeni med en OR på 0,12 (95% KI: 0,02 til 0,88). [31]
Data tre inkluderte studier (341 pasienter) var aktuelt for å analysere sammenhengen mellom MTHFR polymorfisme og toksisitet [25, 27, 31]. To studier fant ingen signifikant sammenheng mellom MTHFR polymorfisme og toksisitet [27, 31]; imidlertid, Lu et al. rapporterte at MTHFR TT var assosiert med høyere frekvens av nonhematologic toksisitet (kvalme /oppkast) [25].
Association mellom ERCC1, GST polymorfisme og platinumbasert kjemoterapi
Svarprosent (RR)
Syv studier (674patients) evaluert sammenhengen mellom ERCC1 polymorfisme og RR [11, 14, 18, 19, 21, 30, 31]. Alle pasientene gjennomgikk palliativ kjemoterapi. P
verdi av heterogenitet testen var 0,696 og et fast-effekt-modellen ble anvendt. Den sammenslåtte OR for RR var 0,77 (95% KI: 0,54 til 1,11 Tabell 4), som antydet at det var ingen signifikant sammenheng mellom ERCC1 polymorfisme og RR. Subgruppe analyse ble utført i henhold til etnisitet og evalueringskriterier. Den sammenslåtte OR 0,56 (95% KI: 0,32 til 0,97) for europeiske undergruppe og 0,56 (95% KI: 0,32 til 1,00) for "annet" undergruppe, som foreslo at RR var betydelig høyere i C /C genotype sammenlignet med C /T eller T /T genotyper. Men forskjellen var ikke statistisk signifikant i asiatisk, RECIST eller WHO undergruppen (tabell 4). Tabell 4 Sammenhengen mellom ERCC1 polymorfisme og kliniske resultater
Study (referanse)
RR (n /N)
OS (HR, 95% KI)
Toxicity
Goekkurt 2006 [11]
CC: 2/5; CT + TT: 11/44
NR
NR
RUZZO 2006 [14]
CC: 21/38; CT + TT: 49/137
NR
NR
Park 2011 [18]
CC: 35/64; CT + TT: 23/44
TC /CC: 0,94 (0,556, 1,587); TT /CC: 1,918 (0,748, 4,919)
NR
Han 2010 [19]
CC: 12/23; CT + TT: 9/15
NR
NR
Stocker 2009 [20]
NR
CT /CC: 0,72 (0,40, 1,31); TT /CC: 1,07 (0,59, 1,95)
NR
Seo 2009 [21]
CC: 11/42; CT + TT: 7/33
NR
NSS
Liu 2011 [22]
NR product: (CT + TT) /CC: 2,388 (1,448, 3,937)
NR
Huang 2009 [26]
NR product: (CT + TT) /CC: 1,072 (0,620, 1,855)
NR
Keam 2008 [30]
CC: 17/40; CT + TT: 15/33 plakater (CT + TT) /CC: 1,251 (0,68, 2,302)
NR
Goekkurt 2009 [31]
CC: 9/21; CT + TT: 43/113
NR
NSS
Kombinert analyse (OR /HR, 95CI%)
OR: (CT + TT) /CC
HR: (CT + TT) /CC
___
Total (Palliativ kjemoterapi): 0,77 (0,54, 1,11);
Totalt: 1,5 (0,90, 2,49)
Palliativ undergruppe: 1,77 (0,94, 3,33);
RECIST undergruppe: 0,89 (0,52, 1,53);
Adjuvans undergruppe: 1,07 (0,62, 1,85);
WHO undergruppen: 1,13 (0,45, 2,85);
Alle studiene rapporterte data var
Andre undergruppe: 0,56 (0,32, 1,00);
asiatisk
asiatisk undergruppe. 0,98 (0,61, 1,59);
Europeisk undergruppe: 0,56 (0,32, 0,97)
RR: svarprosent; OS: total overlevelse; OR: odds ratio; HR: hazard ratio; NR: ikke rapportering; NSS. Ingen statistisk signifikans
Seks studier (794 pasienter) evaluert assosiasjonen mellom GSTM1 polymorfisme og RR [11, 14, 17, 21, 23, 31]. P
verdi av heterogenitet testen var 0,734 og et fast-effekt-modellen ble anvendt. Den sammenslåtte OR for RR var 1,16 (95% KI: 0,85 til 1,58; tabell 5), som antydet at det var ingen signifikant sammenheng mellom RR av pasienter med M- genotype og at pasienter med M + genotype. Subgruppeanalyse i henhold til etnisitet, evalueringskriterier og kjemoterapi formål også ikke viste signifikant sammenheng (tabell 5). Tabell 5 Sammenhengen mellom GST polymorfismer og kliniske utfall
Study (referanse)
RR (n /N)
OS (HR, 95% KI)
Toxicity
Goekkurt 2006 [11]
GSTM1: M-: 9/32; M +: 4/18
NR
NR
GSTP1: AA: 7/30; GA + GG: 6/18
GG /(GA + AA): 0,65 (0,43, 1,00)
NR
GSTT1: T-: 8/38; T +: 5/12
NR
NR
RUZZO 2006 [14]
GSTM1: M-: 36/78; M +: 34/97
NR
NR
GSTP1: AA: 20/87; GA + GG: 50/88
GG /AA: 0,58 (0,43, 0,80)
NR
GSTT1: T-: 6/21; T +: 64/154
GA /AA: 0,54 (0,40, 0,74)
NR
NR
Shim 2010 [17]
GSTM1: M-: 48/124; M +: 29/76
M- /M +: 1,10 (0,80, 1,51)
NR
GSTP1: AA: 46/133
AG /AA: 1,12 (0,79, 1,58)
NR
GA + GG: 31/67
GG /AA: 0,76 (0,33, 1,77)
NR
GSTT1: T-: 40/106; T +: 37/94
T- /T +: 0,77 (0,57, 1,06)
Seo 2009 [21]
GSTM1: M-: 12/49; M +: 6/26
NR
NR
GSTP1: AA: 10/47; GA + GG: 8/28
NR
NR
GSTT1: T-: 8/39; T +: 10/36
NR
NR
Liu 2011 [22]
GSTP1: NR plakater (GG + AG) /AA: 0,53 (0,36, 0,80)
NR
Ott 2008 [23]
GSTM1: M-: 15/52; M +: 13/60
M- /M +: 1,38 (0,92, 2,08)
NR
GSTP1: AA: 12/55; GA + GG: 21/77
AG /AA: 0,80 (0,55, 1,15)
NR
GSTT1: T-: 5/23; T +: 24/87
GG /AA: 0,95 (0,53, 1,71)
NR
T- /T +: 1,09 (0,69, 1,72)
Li 2010 [24]
GSTP1: AA : 17/44; GA + GG: 29/41 plakater (GG + AG) /AA: 0,44 (0,25, 0,78)
SS
Huang 2009 [26]
GSTM1: NR
M- /M +: 1,425 (0,822, 2,469)
NR
GSTP1: NR plakater (GG + AG) /AA: 0,471 (0,252, 0,878)
NR
Keam 2008 [30]
GSTP1: AA: 22/44; GA + GG: 10/29 plakater (GG + AG) /AA: 0,621 (0,452, 1,606)
NR
Goekkurt 2009 [31]
GSTM1: M-: 26/72; M +: 26/62
NR
NR
GSTP1: AA: 26/64; GA + GG: 26/69
NR
SS
GSTT1: T-: 5/23; T +: 47/111
T- /T +: 1,94 (1,14, 3,32)
NR
Kombinert analyse (OR /HR, 95CI%)
GSTM1 (OR), M- /M + Totalt: 1,16 (0,85, 1,58)
GSTM1 (HR), M- /M + Totalt: 1,23 (0,98, 1,55)
___
RECIST undergruppe: 1,07 (0,66, 1,74)
asiatisk undergruppe: 1.17 ( 0,89, 1,55)
Andre undergruppe: 1,23 (0,82, 1,84)
europeiske undergruppe: 1,38 (0,92, 2,07)
asiatisk undergruppe: 1,04 (0,62, 1,74)
Palliativ undergruppe: 1,10 (0,80, 1.51)
europeiske undergruppe: 1,24 (0,84, 1,82)
Adjuvans undergruppe: 1,42 (0,82, 1,47)
Palliativ undergruppe: 1,04 (0,73, 1,49)
Neoadjuvant undergruppe: 1,38 (0,92, 2,07)
Neoadjuvant undergruppe: 1,59 (0,86, 2,92)
GSTP1 (HR), (GG + AG) /AA, Total: 0,51 (0,39, 0,67)
GSTP1 (OR), (GG + AG) /AA
Palliativ undergruppe: 0,52 (0,39, 0,70)
Adjuvans undergruppe: 0,47 (0,25, 0,88)
Totalt: 1,63 (0,98, 2,70)
Alle studiene rapporterte data var asiatisk
. RECIST undergruppe: 1,60 (0,98, 2,60)
GSTP1 (HR), GG /AA, Total: 0,66 (0,51, 0,85)
WHO undergruppen: 0,53 (0,20, 1,38)
Andre undergruppe: 2,1 (0,93 , 4,74)
asiatisk undergruppe: 0,76 (0,33, 1,76)
asiatisk undergruppe: 1,51 (0,72, 3,16)
europeiske undergruppe: 0,65 (0,49, 0,85)
europeiske undergruppe: 1,74 (0,77, 3,91 )
Palliativ undergruppe: 0,60 (0,45, 0,80)
Palliativ undergruppe: 1,67 (0,93, 2,99)
Neoadjuvant undergruppe: 0,95 (0,53, 1,71)
Neoadjuvant undergruppe: 1,34 (0,60, 3,03)
GSTP1 (HR), AG /AA, Total: 0,78 (0,51, 1,20)
GSTT1 (OR), T- /T + Total: 0,67 (0,47, 0,97)
RECIST undergruppe: 0,79 (0,49, 1,27 )
asiatisk undergruppe: 1,12 (0,79, 1,58)
Andre undergruppe: 0,53 (0,29, 0,97)
Europeisk undergruppe: 0,65 (0,44, 0,95)
asiatisk undergruppe: 0,87 (0,52, 1,43)
Palliativ undergruppe: 0,77 (0,38, 1,58)
europeiske undergruppe: 0,51 (0,29, 0,88)
Neoadjuvant undergruppe: 0,80 (0,55, 1,16)
Palliativ undergruppe: 0,67 (0,45, 0,99)
GSTT1 (HR), T- /T + Total: 1,14 (0,68, 1,90)
Neoadjuvant undergruppe: 0,73 (0,24, 2,18)
asiatisk undergruppe: 0,77 (0,56, 1,05)
europeiske undergruppe: 1,43 (0,81 , 2,51)
Palliativ undergruppe: 1,19 (0,48, 2,94)
Neoadjuvant undergruppe: 1,09 (0,69, 1,72)
RR: svarprosent; OS: total overlevelse; OR: odds ratio; HR: hazard ratio; NR: ikke rapportering; SS.: Statistisk signifikans
data fra 8 studier (959 pasienter) kan brukes for å evaluere forbindelsen mellom GSTP1 polymorfisme og RR [11, 14, 17, 21, 23, 24, 30, 31]. P
verdi av heterogenitet testen var mindre enn 0,1 og en tilfeldig-effekt-modellen ble anvendt. Det sammenslåtte OR for RR var 1,63 (95% CI: 0,98 til 2,70; tabell 5), noe som antydet at pasienter med G /G eller A /G genotype hadde en høyere RR sammenlignet med A /A genotype, selv om forskjellen ikke var statistisk signifikant. Resultatet ble ikke endret ved hjelp av fremgangsmåten ifølge undergruppeanalyse ifølge etnisk, evalueringskriterier og kjemoterapi formål (tabell 5).
Data 6 studier (794 pasienter) var tilgjengelig for GSTT1 [11, 14, 17, 21, 23, 31]. P
verdi av heterogenitet testen var 0,664 og et fast-effekt-modellen ble anvendt. Kombinert analyse antydet at RR var høyere i T + genotype sammenlignet med T- genotype (T- /T +: OR = 0,67, 95% KI: 0,47 til 0,97; tabell 5). Når den brukes metoden for subgruppeanalyse, ble resultatet endret i asiatisk, RECIST og neo-adjuvant undergrupper, men ikke endret i europeisk eller "annet" undergrupper (tabell 5).
Total overlevelse
Fem studier (587 pasienter ) evaluerte forbindelsen mellom ERCC1 polymorfisme og OS [18, 20, 22, 26, 30], men de studier av Park et al. og Stocker et al. kan ikke brukes til meta-analyse, som rapporterte ble ikke observert noen signifikant sammenheng mellom ERCC1 polymorfisme og OS [18, 20].
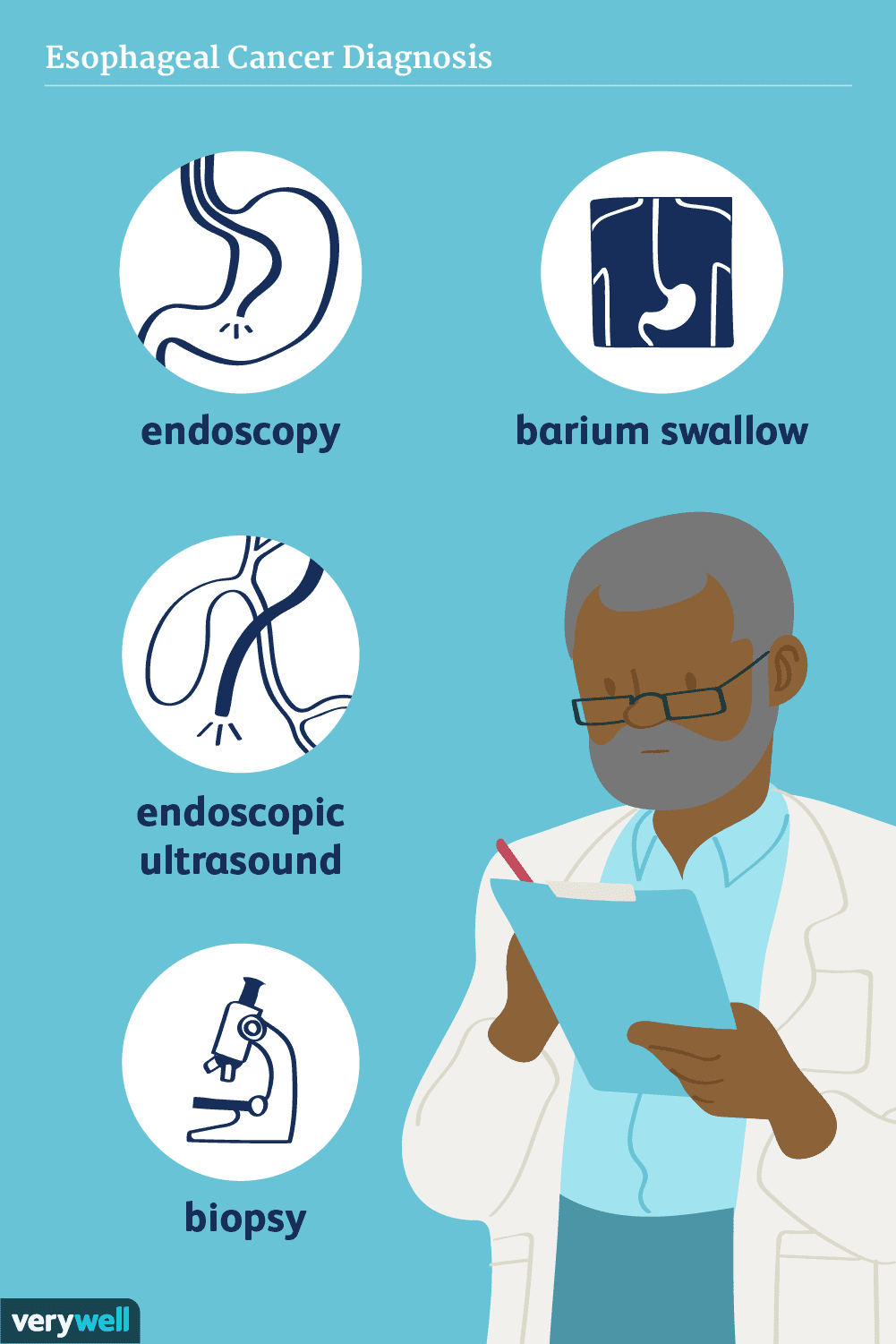 Hvordan esophageal cancer diagnostiseres
Diagnosen av kreft i spiserøret kan omfatte tester som en bariumsvelge, endoskopi og endoskopisk ultralyd. Du kan trenge en evaluering for mulig kreft i spiserøret hvis du har problemer med å svelge,
Hvordan esophageal cancer diagnostiseres
Diagnosen av kreft i spiserøret kan omfatte tester som en bariumsvelge, endoskopi og endoskopisk ultralyd. Du kan trenge en evaluering for mulig kreft i spiserøret hvis du har problemer med å svelge,
 Rollen til betennelse i irritabel tarmsyndrom
Konvensjonell visdom har alltid hevdet at betennelse ikke sees hos pasienter med irritabel tarmsyndrom (IBS). Vel, tidene kan de endre seg. Nyaktig forskning har begynt å finne bevis på lavgradig bete
Rollen til betennelse i irritabel tarmsyndrom
Konvensjonell visdom har alltid hevdet at betennelse ikke sees hos pasienter med irritabel tarmsyndrom (IBS). Vel, tidene kan de endre seg. Nyaktig forskning har begynt å finne bevis på lavgradig bete
 Prevotella-bakterier i tarm, munn og vaginal mikrobiomhelse
Prevotella er bakterier som bor i mange deler av kroppen. Selv om de er vanlige i tarmmikrobiomet, kan de være et tegn på problemer eller infeksjon hvis de finnes andre steder. Kroppen er full av f
Prevotella-bakterier i tarm, munn og vaginal mikrobiomhelse
Prevotella er bakterier som bor i mange deler av kroppen. Selv om de er vanlige i tarmmikrobiomet, kan de være et tegn på problemer eller infeksjon hvis de finnes andre steder. Kroppen er full av f