oksytocin forlenger magetømmingstid hos pasienter med diabetes mellitus og gastroparese, men påvirker ikke metthetsfølelse eller volum inntak hos pasienter med funksjonell dyspepsi
Abstract
Bakgrunn
Oxytocin er utgitt i respons til en fet måltid. Blokkering av oxytocin reseptoren ført til tregere ventrikkeltømming mens stimulering resulterte i mindre metthetsfølelse hos friske frivillige. Pasienter med diabetes mellitus og gastroparese mangler oxytocin høyde, og dyspepsi er delvis forårsaket av redusert fundus overnatting forårsaker tidlig metthet og relaterte symptomer. Målet med denne studien var derfor å undersøke effekten av oksytocin på gastrisk tømming, metthetsfølelse og voluminntak hos pasienter med gastrointestinal patologi.
Resultater
Gastric tømming scintigrafi ble utført to ganger i 12 pasienter med diabetisk gastroparese, en gang med oksytocin og en gang med saltløsning som intravenøse infusjoner. Pasientene scoret sitt følelse av metthet hjelp av en visuell analog skala (VAS). Den magetømmingen hos pasienter med gastroparese ble forlenget i løpet oksytocininfusjon (p
= 0,034) uten å påvirke metthetsfølelse. En langsom satiety drikking test ble utført på 14 pasienter med funksjonell dyspepsi. Pasientene mottok sin metthetsfølelse hvert femte minutt inntil maksimal metthetsfølelse var nådd, og det totale volum ble bestemt. VAS ble også gjennomført 30 minutter etterpå. Testen ble utført to ganger, en gang med oksytocin og en gang med saltløsning som intravenøse infusjoner. Det var ingen forskjell i satiety score eller volum av næringsinntak mellom saltvann og oxytocin infusjoner, enten før, under eller etter måltidet.
Konklusjoner
Oxytocin forlenger ventrikkeltømming hos pasienter med diabetes mellitus og gastroparese, men har ingen effekt på volumet av næringsinntak eller metthetsfølelse og andre relaterte symptomer hos pasienter med funksjonell dyspepsi.
nøkkelord
Diabetes mellitus funksjonell dyspepsi gastroparesis Gastric tømming scintigrafi Slow metthet drikking test Bakgrunn
Oxytocin og dens reseptor uttrykkes gjennom hele mage ( GI) [1, 2]. Oxytocin er utgitt i respons til en fet måltid hos friske individer [3], men pasienter med diabetes mellitus og gastroparese har blitt funnet å mangle dette svaret [4]. Videre administrasjon av oksytocin reseptoren antagonist Atosiban forsinket ventrikkeltømming hos friske [5].
Effekten av oksytocin på human magetømmingen er ikke helt etablert, med noen studier som viser en akselerert effekt etter en halvfast måltid [6 , 7] og andre som viser ingen effekt etter en halvfast eller solid måltid [5, 8]. I dyreforsøk, har studier vist at oksytocin øker gastrisk tømming tid og induserer metthetsfølelse på grunn av både sentrale og perifere effekter [9-12]. På den annen side har en dyrestudie funnet at oksytocin øker gastrisk trykk og trekker seg sammen gastriske muskelfibre [13]. Denne doble effekten kan forklares ved oxytocin utøve sin virkning både via cholecystokinin (CCK) frigivelse og CCK-reseptorer med påfølgende inhibering av gastrisk tømming [11, 12], og via oxytocin-reseptorer som stimulerer gastrisk kontraksjon [13].
Patofysiologi av dyspepsi er ennå ikke fullstendig kjent, men en teori er redusert ventrikkel overnatting i fundus fører til ulike symptomer, for eksempel tidlig metthetsfølelse. En langsom drikking satiety testen kan brukes til å vurdere boligen og eventuelle farmakologiske effekter på overnatting og symptomer [14, 15]. I en tidligere studie med friske forsøkspersoner, fant vi at oxytocin redusert følelse av metthet uten å påvirke volumet av matinntaket eller ventrikkeltømming [8]. Å se at funksjonell dyspepsi og gastroparese er de viktigste kliniske syndromer assosiert med mage motorisk dysfunksjon [15], begge disse lidelsene krever videre studier i forhold til oxytocin og dens virkninger.
Målet med denne studien var å undersøke effekten av oksytocin 1) på gastrisk tømming hos pasienter med diabetes mellitus og gastroparese, og 2) på metthetsfølelse og voluminntaket hos pasienter med funksjonell dyspepsi.
Resultater
gastric tømming test
ventrikkeltømming test viste at oksytocin forlenget gastrisk tømming i betydelig grad sammenlignet med saltvannsoppløsning (figur 1). Kun en pasient hadde lenger gastrisk tømming tid i løpet av saltvann enn i løpet av oxytocin infusjoner. Selv om alle pasientene inkludert hadde bekreftet gastroparese i løpet av året før inkludering, syv hadde en normal magetømmingen ved saltvann rettssaken, og tre i oxytocin rettssaken. Tre av pasientene hadde normal magetømmingen i begge studiene. Figur 1 Oxytocin infusjoner forlenget magetømmingstid sammenlignet med saltvann hos pasienter med diabetes mellitus og gastroparese (p = 0,034). Verdiene er gitt som boksplott som representerer median (interkvartilt område). Wilcoxon test.
Den fastende blodsukkerverdier viste ingen forskjeller mellom saltvann og oxytocin studier (tab 1). Også, visuell analog skala (VAS) score i forhold til å starte verdi, 30 og 70 minutter etter inntak av mat, ikke skiller mellom de to forsøkene (figur 2) .table 1 Laboratorie karakteristikker av pasienter med diabetes mellitus og gastroparese
Parameter
Verdi
Diabetes varighet (år)
32,0 (15,5 til 39,3)
BMI (kg /m2)
25,8 (22,4 til 30,0 )
HbA1C (mmol /mol)
64,0 (59,0 til 68,8)
fastende blodsukker, saltvann studie (mmol L-1)
9.3 (07.01 til 12.02)
fastende blodsukker, oxytocin prøve (mmol L-1)
9.6 (06.09 til 10.05)
BMI = body mass index, HbA1c = glykosylert hemoglobin. Verdiene er gitt som median (interkvartilt område).
Figur 2 Det var ingen forskjeller mellom saltvann og oxytocin i VAS score på 30 og 70 minutter etter inntak av mat i løpet av magetømmingen scintigrafi hos pasienter med diabetes mellitus og gastroparese (p = 0,594 respektive p = 0,799). Verdiene er gitt som boksplott som representerer median (interkvartilt område). . Wilcoxon test
Det var en statistisk signifikant negativ sammenheng mellom alder og HbA1c (r = -0,68, p
= 0,016), men ingen sammenheng mellom alder og T1 /2 for saltvann eller oxytocin infusjoner (p
= 0,639 og p = 0,687
, henholdsvis). Heller ikke var det noen tendens til sammenheng mellom HbA1c og T1 /2 for saltvann eller oxytocin infusjoner (p
= 0,989 og p
= 0,610, henholdsvis).
Satiety test
metthet test viste ingen forskjell i det totale volumet av næringsinntaket mellom saltvann og ende oksytocin-infusjon (p
= 0,149). Satiety score før, ved maksimal metthetsfølelse og 30 minutter etter avsluttet måltidet ikke skiller mellom saltvann og oxytocin studier (p
= 0,483, p
= 0,449 og p
= 0,450, henholdsvis). Fem pasienter stoppes testen etter 40 min. Arealet under kurven (AUC) for metthetsfølelse score opp til denne tid ble beregnet, og ingen signifikant forskjell ble observert (figur 3; p
= 0,953). Figur 3 Arealet under kurven (AUC) for satiety score mellom saltvann (a) og oxytocin (b) infusjoner hos pasienter med funksjonell dyspepsi ikke forskjell (p = 0,953). Verdiene er gitt som boksplott som representerer median (interkvartilt område). Plassen inne i boksplott representerer gjennomsnittsverdien. Wilcoxon test.
Grad av magesmerter, kvalme, fordøyelsesbesvær og oppblåsthet, registrert i VAS symptomer danne 30 minutter etter avsluttet måltidet ikke skiller mellom saltvann og oxytocin infusjoner (p
= 0,735, p
= 0,374, p
= 0,674 og p
= 0,735, henholdsvis).
Når dele gruppen av pasienter med funksjonell dyspepsi til de med og de uten overveiende tidlig metthetsfølelse, ingen forskjeller i volumet av næringsstoff inntak, metthetsfølelse score før, under og 30 minutter etter, og heller ikke i de registrerte symptomene etter at testen ble funnet (data ikke vist).
diskusjon
Denne studien viste at oksytocin forlenget ventrikkeltømming tid hos pasienter med diabetes mellitus og gastroparese, men ikke påvirke volumet av næringsinntaket hos pasienter med funksjonell dyspepsi. Oksytocininfusjon ikke resulterte i lavere metthetsfølelse sammenlignet med saltvannsinfusjon.
Gastroparesis er en lidelse hvor gastrisk tømming forsinket uten mekanisk hindring [16]. Patofysiologien er multifaktoriell, med følgende sykdommer kjent for å date: vågal parasympatiske dysfunksjon, hyperglykemi, tap av enteriske nerveceller, tap av nerve nitrogenoksid uttrykk, glatt muskulatur misdannelser og avbrudd av interstitiell celler av Cajal nettverk [17-19]
Tidligere studier har vist at oxytocin receptor antagonist atosiban forlenget gastrisk tømming hos friske individer [5] og diabetespasienter med gastroparese manglet en riss av oxytocin plasmakonsentrasjon postprandially sammenlignet med pasienter uten gastroparese [3, 4]. Disse funn førte til den hypotese at oxytocin kan ha en viktig rolle i GI motilitet, spesielt gastrisk tømming. Men vi kunne ikke se noen effekt av oxytocin på magetømmingen [5, 8]. Dette kan forklares ved den doble effekten oxytocin fremkaller på vanlig GI fysiologi. Først en direkte effekt av oxytocin på sine reseptorer fører til stimulering av mave muskelkontraksjon [13]. For det andre, som oxytocin stimulerer til CCK frigjøring, er en indirekte virkning via CCK-reseptorene aktivert, noe som fører til inhibering av gastrisk tømming [11, 12]. Som Atosiban bare blokkerer oxytocin receptor, forsinket ventrikkeltømming ble sett under administrasjon av dette spesifikke stoffet [5].
I denne studien, oxytocin langvarig magetømmingen i diabetisk gastroparese. Den tidligere observert lavere oxytocin-konsentrasjon i plasma hos pasienter med gastroparese må derfor være en sekundær, og ikke en primær etiologi av forsinket gastrisk tømming [4]. Det er sannsynlig at oksytocinreseptoren reaksjonsveien blir ødelagt før den CCK-reseptoren vei, som fører til et tap av contractory stimulering av oxytocin, men med en bevart hemming av CCK-reseptorer [11-13]. Spenning av den gastriske vegg gir opphav til afferente signaler til hjernen [20]. Som oxytocin ytterligere forsinkelser gastrisk tømming i en dysfunksjonell magen, dette kan føre til en redusert oxytocin sekresjon fra hypofysen av en feedback mekanisme som involverer hypothalamus [21]. Oxytocin utøver både perifere og sentrale virkninger på mage-tarmkanalen når den passerer blod-hjernebarrieren [22]. Imidlertid er den sistnevnte vei er ikke først og fremst ved hvilken oxytocin påvirker gastrisk motilitet, som er blitt funnet når oxytocin og oksytocin-antagonister har fått en sentral [23]. Det ville være interessant å undersøke effekten av atosiban i gastroparese, men dette stoffet hever blodsukkernivået og kan ikke benyttes på pasienter med diabetes mellitus av etiske grunner.
Virkningen av CCK reseptor antagonist loxiglumide, som blokkerer hemmende virkning på gastrisk tømming [24], vil også være en interessant medikament for å studere i denne sammenheng. Hos friske personer, en intravenøs infusjon av loxiglumide stimulert antrum sammentrekning og redusert ventrikkeltømming halv tid [25]. R-isomeren av loxiglumide, dexloxiglumide, har vært testet på pasienter med funksjonell dyspepsi [26] og funksjonell konstipasjon [27], men ikke i pasienter med gastroparese. I funksjonell dyspepsi, CCK-reseptor antagonist motvirket økningen i magevolum og dyspeptiske symptomer under duodenal lipidinfusjonen, samtidig redusere mage etterlevelse [26]. Imidlertid har effekten på funksjonell konstipasjon vært mangelfulle [27].
Oksytocin har i en tidligere studie har vist seg å være effektiv i behandling av funksjonell abdominal smerte og nedsatt humør [28]. Dette, sammen med den beskrevne smertestillende effekten av oxytocin i rotter [29], gjør oytocin analoger for å være lovende medikamenter i fremtiden behandling av irritabelt tarmsyndrom (IBS) og depresjon. De foreliggende resultatene av forlengelse av gastrisk tømming av oksytocin understreker viktigheten av å behandle IBS pasienter med oxytocin eller de nyutviklede analoger, først når GI dysmotility er utelukket.
Pasienter som har symptomer fra den øvre GI-systemet i fravær av en hvilken som helst organisk sykdom er diagnostisert som lider av funksjonell dyspepsi [30]. Dyspepsi er en av de mest vanlige lidelser i mage-tarmkanalen. Resultatene av cellulær patologi i dyspepsi er meget tynt, hvorav noen få studier har antydet en øket mengde av mage-mastceller, eosinofile celler degranulering og afferente dysfunksjon [31, 32]. Andre studier har vist overfølsomhet i mage-tarmkanalen til mekanisk mage oppblåsthet, noe som tyder på økt oppfatning av fysiologiske signaler [33-35].
Redusert ventrikkel innkvartering etter måltidet inntak har blitt beskrevet i 40% av pasienter med dyspepsi [36]. Ifølge Tack et al. [37] redusert Boligen er forbundet med tidlig metthetsfølelse, noe som gjør det til et viktig symptom i denne undergruppen av pasienter. Den langsomme drikking metthet testen er utviklet for å måle ventrikkel overnatting til et måltid, og er derfor spesielt egnet for å studere denne undergruppen [14, 15]., En tidligere utført studie av vår gruppe viste at oksytocin reduserer følelsen av metthet uten å påvirke volumet av næringsinntaket eller magetømmingen hos friske personer [8]. Dermed kan det muligens påvirke tidlig metthet og andre symptomer hos pasienter som lider av funksjonell dyspepsi, hvorfor vi utførte satiety test på disse pasientene. Interessant, vi kunne ikke finne en forskjell i metthetsfølelse, voluminntak, magesmerter, kvalme, fordøyelsesbesvær og oppblåsthet i disse pasientene med oxytocin versus saltvann. Metthetsfølelse var heller ikke berørt i løpet av magetømmingen test. Vi har tidligere beskrevet at oksytocin reduserer abdominal smerte og depresjon i pasienter med funksjonsforstyrrelser, men har ingen effekt på forstoppelse [28]. Dermed synes oxytocin for å ha noen effekt på sensoriske funksjoner, men er ikke effektiv ved behandling av GI dysmotility og symptomer relatert til den dysmotility. Effekten på magesmerter hos IBS kan forklares ved at smerteopplevelsen i IBS, og smertelindring av oksytocin, er hovedsakelig sentrale effekter [29, 38], mens effekter gjengivelses tidlig metthet kan hovedsakelig være av perifere tegn [23, 37] .
en av begrensningene i denne studien er at selv om alle pasienter ble nylig diagnostisert som lider av gastroparese, noen av dem hadde normal tømming i denne studien. Dette kan delvis forklares ved variasjonen i GI motilitet fra en dag til en annen [39]. Videre forlenger hyperglykemi ventrikkeltømming [40], og pasientene kan ha vært i bedre metabolsk kontroll på den tiden da de kom inn i denne studien, enn på tidspunktet for deres siste ventrikkeltømming scintigrafi. Ikke desto mindre, kan pasientene ikke anses for å ha normal gastrisk funksjon som de har hatt kliniske symptomer på dysfunksjon som fører til opptak for gastrisk scintigrafi, og ha en gang blitt klassifisert som gastroparetic ved den samme metode. En annen begrensning er den lille prøvestørrelsen, som avhenger av vanskeligheter med å recruite pasienter i en god metabolsk kontroll. Den kvinnelige overvekt i studien er avhengig av at disse lidelser er mer vanlig hos kvinner enn hos menn [17, 41].
Konklusjon
Oxytocin forlenger ventrikkeltømming hos pasienter med diabetes mellitus og gastroparese, men har ingen effekt på volum av næringsinntak eller metthetsfølelse og andre relaterte symptomer hos pasienter med funksjonell dyspepsi.
Metoder
studien er utført i henhold til Helsinkideklarasjonen, og ble godkjent av etikkomiteen ved Lunds universitet og Swedish Medical Agency ( DNR 2009/502). Skriftlig, ble informert samtykke innhentes fra alle deltakerne. Alle fagene gjennomført testene og ingen bivirkninger ble rapportert bortsett fra noen få pasienter som lider av hodepine. Trial påmelding: NCT01152047, NCT00776360
Fag
Pasienter med diabetes mellitus og gastroparese, verifisert av en tidligere tømming scintigrafi i løpet av året, ble invitert til å gjennomgå ventrikkeltømming scintigrafi ved to anledninger, en med saltvann og en med. oksytocininfusjon, med minst 2 dager i mellom. Pasientene ble rekruttert fra Institutt for endokrinologi, Institutt for klinisk fag, Seksjon for gastroenterologi og en primærhelsetjenesten senter i Malmö
Eksklusjonskriterier var alder <.; 18 år > 65 år og alvorlige komplikasjoner eller hjertesymptomer, som kan ha medført mulig risiko for bivirkninger. Tolv pasienter (10 kvinner), median alder på 56,5 (52.0-64.8) år, i god metabolsk kontroll akseptert å delta i studien. Glykosylert hemoglobin (HbA1c) ble analysert ved Institutt for kjemi, Skåne universitetssykehus, Malmö, ifølge kliniske rutiner. HbA 1c verdier ble samlet inn som Mono-S og deretter konvertert til den nasjonale glycohemoglobin Standardization Program (NGSP) standard ved bruk av følgende algoritme: 0,923 × HbA 1c (Mono-S) × 1,345 = HbA 1c (NGSP) [42]. Prosentvis HbA 1c verdiene ble konvertert til International Federation of Clinical Chemistry (IFCC) standard i mmol /mol i henhold til følgende ligning: IFCC (mmol /mol) = ([NGSP (%)] - 2152) /0.09148 [ ,,,0],42].
ti av 12 pasienter hadde andre diabetiske komplikasjoner bortsett fra gastroparese, med retinopati som er den mest vanlige (tabell 2). For ytterligere pasientkarakteristika se tabell 1 og 2.Table 2 Kliniske karakteristika for pasienter med diabetes mellitus og gastroparese (n = 12)
Nei (%)
Diabetes mellitus type 1
9 (75)
Diabetes mellitus type 2
3 (25)
kvinner
10 (83)
menn
2 (17)
Andre komplikasjoner av diabetes mellitus
10 (83)
- retinopati
8 (67) Anmeldelser - Perifer nevropati
7 (58)
- Nefropati
2 (17)
- Andre
7 (58)
Farmakologisk behandling for gastrointestinal dysmotility
4 (33)
Insulin behandling
10 (83)
perorale hypoglykemiske legemidler
3 ( 25)
Hypotyreose
3 (25)
Pasienter med funksjonell dyspepsi ble invitert til å utføre en langsom drikking satiety test ved to anledninger, en med saltvann og en med oksytocininfusjon. Alle pasienter med dyspepsi oppfylte Roma III kriteriene for funksjonell dyspepsi [41]. De ble rekruttert av reklame eller fra en primærhelsetjenesten senter i Malmö. De mest dominerende symptomer ble registrert (Tabell 3). Eksklusjonskriterier var alder < 18 år > 65 år, en annen organisk GI lidelse eller andre alvorlige sykdommer. Fjorten pasienter (12 kvinner), median alder på 37,5 (24.0-44.5) år, akseptert å delta. Ingen av pasientene brukte noen medikamenter som påvirker GI motility.Table 3 Kliniske karakteristika for pasienter med funksjonell dyspepsi (n = 14)
|
Nei (%)
kvinner
12 (86)
menn
2 (14)
Oppblåsthet som dominerende symptom /symptomer
5 (36)
Tidlig metthet som dominerende symptom /symptomer
6 (43)
Epigastric smerte som dominerende symptom /symptomer
2 (14)
Epigastric brenning som dominerende symptom /symptomer
2 (14)
visuell analog skala (VAS)
pasientene ble bedt om å fylle ut et spørreskjema gradering sin sult og /eller følelse av metthet, ved hjelp av VAS satiety score gradert fra 0, for de mest ekstreme sult, til 20, for de mest ekstreme satiety [5, 8]. VAS skala var merket med ulike beskrivelser av sult og metthet, fra smertefull sult til metthetsfølelse kombinert med kvalme, noe som gjør det mer illustrerende. Pasientenes stillingen i utgangspunktet var satt til null, og verdiene målt etterpå ble satt i forhold til dette punktet. Skalaen ble brukt i både mage emptying- og treg drikking satiety test.
Drugs
fagene ble undersøkt på to forskjellige anledninger og fikk enten en infusjon av fysiologisk saltvann eller av oxytocin i tilfeldig rekkefølge under forsøkene . Syntocinon © (Novartis, Täby, Sverige), en syntetisk analog av oksytocin, ved en konsentrasjon på 8,3 ug ml -1 ble oppløst i 1000 ml saltvann og gitt som intravenøs infusjon for varigheten av forsøket. Den oksytocininfusjon ble gitt ved konsentrasjoner på 80 og 40 mU min -1, respektivt. Disse dosene ble valgt, da de var de mest effektive i dose-respons studier utført tidligere i friske frivillige, og gjengis farmakologiske plasmakonsentrasjon av oxytocin [8]. Både pasienter og ansatte å utføre magetømming og metthetsfølelse testene var ikke klar over hvor infusjonen ble gitt.
Gastric tømming test
Pasientene ble undersøkt i morgen etter en natts faste. Pasienter på faste medisiner påvirker GI motilitet ble bedt om å stoppe denne behandlingen to dager før scintigrafi testen. Blodglukose ble målt før starten av forsøket. Hvis b-glukose var > 18 mml L -1 forsøket ble stoppet og pasienten ble sendt hjem. Når b-glukose var > 12 mmol L -1, fikk pasientene halvparten av sin vanlige insulindose på laboratoriet før starten av forsøket., En testmåltid ble fremstilt ved tilsetning av tinn kolloid som er merket med 30-50 MBq 99 MTC til en egg, som ble pisket i et glassbeger i et varmt vannbad inntil koagulert. Egg og en skive ristet loff ble kuttet i biter mindre enn 1 x 1 cm og servert med 100 ml 37 ° C vann. Måltidet ble spist i løpet av fem minutter. Umiddelbart etterpå et stort felt tohodet gammakamera (Philips Skylight, Philips Medical Systems, Best, Nederland) ble plassert anteriort og posteriort parallelt med den øvre bukveggen. Radioaktiviteten ble målt kontinuerlig (1-min rammer) i 70 minutter starter umiddelbart etter måltid inntak. En Region of Interest (ROI) som representerer magen ble opprettet og aktiviteten til det første bildet ble tatt som 100%. Den gradvise minkende radioaktivitet, målt som antall radioaktiviteten avtar per minutt (slag /min), ble plottet mot tid. Tiden som gikk for å nå en 50% reduksjon av aktivitet i ROI (T1 /2) ble identifisert som det punkt ved hvilket dette plottet krysset 50% verdi. Verdiene av den målte radioaktiviteten ble korrigert for den halveringstid på 99 m Tc, og for dempning ved hjelp av de geometriske middelverdier for de nedbrytingskurvene som oppnås fra de to gammakamera hoder som brukes. T1 /2 > 2 standardavvik (SD) for friske kontrollpersoner (70 min) ble ansett som unormal [43].
En tilførsel av enten saltvann eller 80 mU oxytocin min -1 ble startet samtidig som måltidet inntaket begynte , og ble gitt gjennom forsøkene. Fagene også scoret sitt metthetsfølelse ved hjelp av en VAS score, ved tid 0 når måltidet inntaket begynte, og 30 og 70 minutter etter måltidet inntak. Den ventrikkeltømming tid og VAS score ble brukt for statistiske beregninger.
Satiety test
metthet Testen ble utført i henhold til en tidligere utviklet protokollen ved Tack et al. [14] under anvendelse av en noe modifisert VAS skala som er blitt anvendt i andre studier utført av vår gruppe [5, 8]. Pasientene ble undersøkt i morgen etter en natts faste. En peristaltisk pumpe fylt en av to begerglass med en hastighet på 15 ml min -1 med et flytende måltid bestående av 13% protein, 48% karbohydrat og 39% lipider (Nutridrink ©; Nutricia, Bornem, Belgia) , noe som gir 1,5 kcal ml 1. Pasientene ble bedt om å opprettholde deres inntak på fyllehastigheten, vekslende begrene som de ble fylt og tømt. Deltakerne ble bedt om å avslutte sitt måltid når maksimal satiety ble nådd, og de kunne ikke fortsette å drikke noe mer. Ved starten av forsøket og med fem minutters mellomrom, de spilte inn sin metthet bruker VAS før de avsluttet sitt måltid. En ytterligere VAS score for metthetsfølelse og et eget VAS å score andre GI symptomer, nemlig, magesmerter, kvalme, fordøyelsesbesvær og oppblåsthet, ble ferdigstilt 30 minutter etter slutten av måltidet. En infusjon av saltvann eller 40 mU oxytocin min -1 ble startet samtidig som måltidet inntaket begynte og ble avsluttet når måltidet ble avsluttet. Volumet av næringsinntak og registrerte VAS score ble brukt i de statistiske beregningene.
Statistiske analyser
Verdiene er gitt som median (interkvartilt område, IQR). VAS score i forhold til baseline og AUC for VAS score ble beregnet. Statistikk forskjeller i magetømming tid og relaterte VAS score i magetømmingen test og forskjeller i satiety score, AUC for VAS, volumet av næringsinntak og VAS skår for GI symptomer i satiety testen ble bestemt ved hjelp av Wilcoxon test. Korrelasjoner ble bestemt med Spearmans test. P < 0,05 ble ansett som statistisk signifikant
Forkortelser
AUC. Areal under kurven
CCK:
Cholecystokinin
GI:
Gastrointestinal
HbA1c:
glykosylert hemoglobin
IBS:
irritabel tarm syndrom
IFCC:
International Federation of klinisk kjemi
NGSP:
National glycohemoglobin standardiseringsprogram
ROI:
aktuelle området
SD:
Standardavvik avvik~~POS=HEADCOMP
T1 /2:
Tid medgått til å nå en 50% reduksjon av aktiviteten i ROI
bilder VAS:.
visuell analog skala
bilder Erklæringer
Takk
Denne studien ble støttet med tilskudd fra Stiftelsen utvikling av regionen Skåne, den Crafoord Foundation og Bengt Ihre Foundation.
Vi ønsker å takke de ansatte ved Institutt for Nuclear Medicine, Diagnostic Centre of Imaging and Functional Medicine, og på Internal Medicine Research Group, Skåne universitetssykehus, Malmö for å utføre forsøkene. Vi takker også Mikael Truedsson, M.D., for å bidra til å rekruttere pasienter med funksjonell dyspepsi til studiet.
Forfatternes opprinnelige innsendte filer for Images Nedenfor er linkene til forfatternes opprinnelige innsendte filer for bilder. 13104_2011_1441_MOESM1_ESM.jpeg Forfatteroriginalfilen for figur 1 13104_2011_1441_MOESM2_ESM.jpeg Forfatteroriginalfilen for figur 2 13104_2011_1441_MOESM3_ESM.jpeg Forfatteroriginalfilen for figur 3 konkurrerende interesser
Forfatterne hevder at de ikke har noen konkurrerende interesser.
|  Type 1 diabetes knyttet til tarmmikrobiom og genetiske faktorer
Type 1 diabetes knyttet til tarmmikrobiom og genetiske faktorer
 Tidlige tegn og symptomer på Hantavirus lungesyndrom (HPS)
Tidlige tegn og symptomer på Hantavirus lungesyndrom (HPS)
 Kvinner født med keisersnitt har større risiko for fedme og diabetes
Kvinner født med keisersnitt har større risiko for fedme og diabetes
 Endoskopi vs. koloskopi
Endoskopi vs. koloskopi
 Hvordan behandles Zenkers divertikulum?
Hvordan behandles Zenkers divertikulum?
 Hva er den beste maten å spise hvis du har GERD?
Hva er den beste maten å spise hvis du har GERD?
 Rollen til betennelse i irritabel tarmsyndrom
Konvensjonell visdom har alltid hevdet at betennelse ikke sees hos pasienter med irritabel tarmsyndrom (IBS). Vel, tidene kan de endre seg. Nyaktig forskning har begynt å finne bevis på lavgradig bete
Rollen til betennelse i irritabel tarmsyndrom
Konvensjonell visdom har alltid hevdet at betennelse ikke sees hos pasienter med irritabel tarmsyndrom (IBS). Vel, tidene kan de endre seg. Nyaktig forskning har begynt å finne bevis på lavgradig bete
 Hva forårsaker inkontinens?
Har du problemer med å komme deg på badet i tide? Legger du merke til problemer som lekkasje, spesielt når du passerer gass? I så fall er dette tegn på fekal eller tarminkontinens. Selv om dette er et
Hva forårsaker inkontinens?
Har du problemer med å komme deg på badet i tide? Legger du merke til problemer som lekkasje, spesielt når du passerer gass? I så fall er dette tegn på fekal eller tarminkontinens. Selv om dette er et
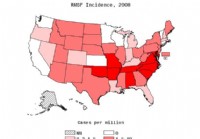 Rocky Mountain Spotted Fever
Fakta du bør vite om Rocky Mountain flekkfeber Rapportert forekomst av RMSF per million mennesker i 2008; NN=ikke rapportert. KILDE:CDC. RMSF er en potensielt alvorlig flåttbåren sykdom, og den er de
Rocky Mountain Spotted Fever
Fakta du bør vite om Rocky Mountain flekkfeber Rapportert forekomst av RMSF per million mennesker i 2008; NN=ikke rapportert. KILDE:CDC. RMSF er en potensielt alvorlig flåttbåren sykdom, og den er de