Гигантские желудочно-кишечного тракта стромальных опухолей (GIST) желудка причиной высокой кишечной непроходимости: хирургическое лечение
Аннотация
Справочная информация
Желудочно-кишечные стромальные опухоли (гов) составляют 85% всех мезенхимальных новообразований, которые влияют на желудочно-кишечный тракт (ЖКТ) , Эти гов варьируются в размерах от небольших повреждений до больших масс. Часто они являются клинически молчание, пока они не достигают значительных размеров, поэтому их открытие, как правило, случайно.
Клинический случай
67-летний мужчина был принят в нашем общем отделение хирургии с постоянной болью в животе в левом подреберье , связанная с тошнотой и рвотой. Клиническое обследование выявило ощутимое массу в эпигастрии и в левом подреберье, которая была примерно 40 см в длину. Ультразвук и компьютерная томография брюшной полости показала большую массу 40 × 25 см, которая простиралась от задней стенки желудка к селезенке, включая тело и хвост поджелудочной железы. Пациенту была смежная блока резекцию массы, рукав резекцию желудка и дистального панкреатэктомии-спленэктомии. Гистопатология резецированных образца согласуется с желудочно-кишечной стромы опухоли желудка (положительный для CD 117) с высоким риском развития злокачественной опухоли (митотическую подсчета > 5/50 высокой мощности fieldand Ki67 /Mib1 > 10%). Послеоперационный курс был беспрецедентен и лечение с иматиниба мезилата начались сразу. Пациент, как представляется, без признаков заболевания после четырех лет.
Выводы
Гигантские гов желудка встречаются редко. Хирургическая резекция с лечебной целью является возможным. Сочетание хирургической резекции и иматиниб может обеспечить долгосрочную termdisease выживаемость без. R0 резекция является наилучшим достижимым лечение, поэтому пациент должен быть оценен в течение долгого времени для потенциального резектабельности.
Ключевые слова
Giant GIST Хирургическое лечение желудочно-кишечного тракта Фон
стромальных опухолей (гов) составляют 85% всех мезенхимальных новообразований, что влияют на желудочно-кишечный тракта (ЖКТ) [1].
В прошлом эти опухоли были классифицированы как лейомиома, leiomyosarcomas или leiomyoblastomas. Только в последнее время, с помощью иммуногистохимии, имеют гов стали рассматриваться как отдельное юридическое лицо. Эти опухоли, как полагают, возникают из-KIT (CD117) положительная междоузельник Кахала, кардиостимулятора клетки желудочно-кишечного тракта [2, 3].
Примерно 85% гов гавани активирующий KIT
мутации, что приводит к конститутивной активации KIT
и его функции тирозин-киназы. Примерно 3% до 5% вместо гов несут мутации в гене PDGFRA
, и около 10% до 15% опухолей содержат формы дикого типа комплекта
и PDGFRA
Протоонкогены [ ,,,0],4-6].
Эти опухоли расположены в основном в желудке (от 60% до 70%), а также их открытие часто случайно [7]. Гов в диапазоне размеров от небольших повреждений до больших масс. Они клинически молчат, пока они не достигают значительных размеров; Именно поэтому их открытие, как правило, случайно [1]. Во многих случаях гов проявляется болями в животе, желудочно-кишечного кровотечения или ощутимая масса. В других случаях они могут быть выявлены из-за осложнения: непроходимость кишечника, спонтанный разрыв в брюшную полость, ведущей к перитонит, или разрыва опухоли в желудке [8-10]. Мы сообщаем о необычном случае гигантского GIST, который вызвал проксимальный непроходимость кишечника.
Клинический случай
A 67-летний мужчина поступил в отделение общей хирургии Университета Катании с постоянной болью в животе в левое подреберье, связанные с тошнота, рвота, и потеря веса (5 кг в течение двух месяцев). Клиническое обследование выявило ощутимое массу в эпигастрии и в левом подреберье, которая была примерно 40 см в длину. Масса в животе, как представляется, фиксируется на соседние структуры, с ее пределами плохо определены.
Все обычные результаты анализа крови и уровни опухолевых маркеров (CEA, CA 19-9, α-фетопротеин) были в пределах нормы. Ультразвук и компьютерная томография брюшной полости показала большую массу 40 × 25 см, которая простиралась от задней стенки желудка к селезенке, обволакивающий тело и хвост поджелудочной железы (рисунки 1 и 2). Кроме того, масса находилась в непосредственной близости от левой толстокишечной изгибом. Рисунок 1 Саггитальная вычислен томограмму, показывающие степень опухоли и сжатие левой ободочной изгибом.
Рисунок 2 корональных компьютерной томограммы, показывая большую массу 40 × 25 см, которая простиралась от задней стенки желудка к селезенке, обволакивающий тело и хвост поджелудочной железы.
После соответствующей инфузионной терапии и позиционирования назогастральный зонд, пациент был срочно доставлен в операционную для разведки. был выбран двусторонний подреберье подход. Гигантская масса занимала центральную часть живота и перемещенными желудка кпереди. Опухоль примыкала окружающих структур тесно, особенно слева колики прогиб, который был сжат. Там не было никаких доказательств печени или перитонеального метастазирования. После разделения желудочно-колики связки, стало ясно, что гигантская масса происходит от задней стенки желудка, и заключенная тело и хвост поджелудочной железы без проникновения чревного ствола или сосудов брыжейки. Интраоперационная биопсия массы показали неопределенную 'веретена опухолевых клеток ".
После того, как техническая возможность вмешательства было установлено, селезеночной сосуды были лигированы в верхнему краю поджелудочной железы, и пациент был подвергнут EN- блокировать резекцию массы на дистальном spleno-панкреатэктомии и гильза резекцией вдоль большой кривой желудка. Масса была твердой, измеренная 37 × 24 × 13 см, весил 8,5 кг, и имел киста и геморрагические области; она не пропитывать селезенки и поджелудочной железы (рисунок 3). Рисунок 3 удалена опухоль.
Окончательный гистопатология резецированных образца показал рак веретенообразные клетки с митотического подсчета 5/50 поля высокой мощности и высоким индексом пролиферации Ki67 /Mib1 &GТ; 10%. Иммуногистохимия показала, что опухоль была положительной для CD 117 /C-комплект и для CD 34, и отрицательный для десмина, виментину, актин гладких мышц, мышц-специфический актин, S-100 протеина, и нейрон-специфической енолазы. Таким образом, окончательный диагноз был гигантский GIST желудка с высоким риском развития злокачественных новообразований.
Послеоперационный курс был беспрецедентен и лечение с иматиниба мезилат 400 мг один раз в день начала немедленно. Пациент, как представляется, без признаков заболевания после четырех лет.
Обсуждение
Желудочно-кишечные стромальные опухоли (гов) являются редкими мезенхимальные опухоли с неопределенным биологическим поведением, которые возникают в стенке желудочно-кишечного тракта. Несмотря на недавний прогресс, достигнутый в диагностике этих опухолей, их нозологическая классификация остается сложной из-за их высокой фенотипической полиморфизма, а также их способности приобретать широкий спектр клинических фенотипов, от праздного-доброкачественная злокачественных с высокой метастатической способности. Эта особенность отражает неспособность предсказать исход пациентов с этими опухолями и сильно ограничивает прогностическую оценку.
Гов может представить в ряде различных способов и часто диагностируется случайно. Симптомы, вызванные гов связаны с их расположением, что приводит к массовым обоих эффектов и внутриполостного кровотечения. Большие гов может вызвать расплывчатое дискомфорт в животе, боли, вздутие живота, раннее насыщение, и, в редких случаях, окклюзии, сжатие окружающих структур, и перитонит из-за спонтанного разрыва в брюшину [8, 9]. В некоторых случаях ядро опухоли больших размеров приводит к внутриочаговой дегенерации, некроза или развития абсцесса [10]. Мы сообщаем о случае очень большого GIST желудка с необычной презентации, непроходимость кишечника из-за левого сжатия колики прогиб.
Гов, вместе с другими опухолями мягких тканей, следует рассматривать в дифференциальной диагностике пациентов с неопределенным брюшная масса, даже если патологический диагноз GIST не уверен, до или во время операции. Для неопределенной брюшной массы, предоперационная биопсия обычно выполняется, но для гов рассмотрение для биопсии должна основываться на степени заболевания. Для локализованными или потенциально резектабельными гов, для которых предоперационная иматиниб не рассматривается, предоперационное гистологическое подтверждение не должно быть необходимым [1]. Биопсия рекомендуется для окончательно неоперабельной или метастатической болезни и в тех случаях, когда предоперационная терапия иматинибом которая указана из-за незначительной резектабельного заболевания или потенциально резектабельного заболевания у пациентов с высоким риском [1]. Эндосонографические наведением тонкоигольной биопсии аспирация предпочтительнее чрескожной биопсии, вследствие ограниченного кровоизлияния, риск разрыва опухоли и распространения информации. Тем не менее, многие патологи не может произвести диагностику с помощью тонкой иглы аспирацию и биопсию ядро-игла может быть безрезультатным, если некротический или геморрагический часть опухоли оцифровывается [1].
В нашем случае, несмотря на большой размер, мы провели только интраоперационного биопсию массы, поскольку нам нужно было продолжить хирургическое иссечение, вследствие сопутствующего непроходимости кишечника. Интраоперационное патология была неопределенной, поскольку он лишь показал "веретена рак клеток.
После удаления любого подозрительного GIST, послеоперационная оценка патологии имеет важное значение для подтверждения диагноза и определения правильного размера и митотический индекс, которые очень важны для стратификация риска [11].
хирургия остается терапия выбора для пациентов с первичным GIST без признаков метастазирования, и должны быть начальная терапия, если опухоль технически резектабельными и связанная с приемлемым риском заболеваемости [1] , Целью операции является полное брутто резекцию с отрицательным микроскопическом краем (R0 резекция) без кровотечения и разрыв псевдокапсулы [12]
На обнаружение микроскопически положительных краев в случае больших гов. (> 10 см) имеет сомнительную ценность, так как во время хирургических маневров существует возможное отслоение неопластических клеток непосредственно в брюшину [13]. Кроме того, нет четкой связи между микроскопически положительными краями и худшим результатам выживания. Иссечение следует рассматривать на индивидуальной основе к случаю, и часто зависит от конечности первой операции, судя по мультидисциплинарной команды.
Решение использовать предоперационную иматиниб оправдано для локально передовых гов и неоперабельным рецидивирующим или метастатического заболевания [1]. Предоперационное иматиниб также вариант для облегчения функции, сохраняющие операции по поводу опухолей в желудочно-пищеводного перехода и прямой кишки [14, 15]. Роль предоперационной иматиниба для лечения первичного локализованного GIST вызывает сомнения, поскольку нет никаких четких доказательств о роли предоперационной иматиниба для получения R0 резекция. Считается, что воздействие предоперационной иматиниба может привести к понижающей регуляции экспрессии с-набора с следовательно селекции иматиниба резистентных клонов раковых клеток, которые могут препятствовать преимущество хирургической резекции и адъювантной терапии [16]. Роль новых препаратов (сунитиниба) еще не завершена оценка у больных с прогрессирующим заболеванием [17]. Тем не менее, оптимальная продолжительность предоперационной терапии и оптимальные сроки резекции остаются неизвестными. Другой опасный побочный эффект может быть интралезиональный кровоизлияние внутри гигантской массы, с гемоперитонеум или перфорации [18].
Выводы
хирургического лечения гигантского GIST является сложным вопросом. Мы рекомендуем, чтобы пациенты постоянно оценивали хирургической бригады для возможного резектабельности, потому что мы считаем, что лучшей стратегией является «хирургическое вмешательство, когда это возможно», направленная на получение резекция R0, когда это возможно. Даже в этом случае гигантских GIST из желудка, резекция R0 может быть безопасно достигнуто.
Согласие
Письменное информированное согласие было получено от пациента к публикации этого доклада дела и сопровождающие изображения. Копия письменного согласия доступна для рассмотрения главного редактора главного журнала
Сокращения
CA 19-9:.
Углеводный антиген 19-9
CD 34:
кластера дифференциации 34
CD 117 /C-кит:
Кластер дифференциации 117 /прото-онкогенов с-комплекта
CEA:
Карциноэмбриональный антиген
GI:
желудочно-кишечного тракта
гов:
Желудочно-кишечные стромальных опухолей
KIT:
тирозин-протеинкиназы набор
PDGFRA:
тромбоцитарный фактор роста рецептора.
декларациях
Авторы 'оригинальные представлены файлы для изображений изображения Ниже приведены ссылки на авторов оригинала, представленных файлов для изображений. 'Исходный файл для Рисунок 1 12957_2013_1374_MOESM2_ESM.tif Авторского 12957_2013_1374_MOESM1_ESM.tif авторов исходного файла для Рисунок 2 12957_2013_1374_MOESM3_ESM.tif Авторского исходного файла для фигурного 3 конкурирующими интересами
Авторы заявляют, что у них нет конкурирующих интересов.
Авторы " вклад
AC и GP подготовил проект статьи; FC, AC, ELM, VC контролировал написание статьи. Все авторы читали и одобрили окончательный вариант рукописи.
 Средства от синдрома раздраженного кишечника (СРК)
Средства от синдрома раздраженного кишечника (СРК)
 Болезнь Крона:что это такое и как с ней бороться
Болезнь Крона:что это такое и как с ней бороться
 Неалкогольная жировая болезнь печени:что вам следует знать
Неалкогольная жировая болезнь печени:что вам следует знать
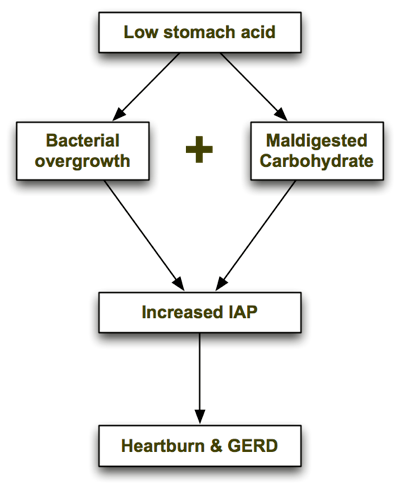 Специфическая углеводная диета лечит ГЭРБ?
Специфическая углеводная диета лечит ГЭРБ?
 Примите участие в акции "Здоровый кишечник"
Примите участие в акции "Здоровый кишечник"
 Как начальная колоноскопия может защитить мое здоровье?
Как начальная колоноскопия может защитить мое здоровье?
 Роль дисбиоза может играть роль в вашем здоровье
Дисбактериоз — это состояние, при котором наблюдается дисбаланс микроорганизмов в нашем организме или внутри него. В балансе эти колонии микроорганизмов, как правило, оказывают благоприятное воздейств
Роль дисбиоза может играть роль в вашем здоровье
Дисбактериоз — это состояние, при котором наблюдается дисбаланс микроорганизмов в нашем организме или внутри него. В балансе эти колонии микроорганизмов, как правило, оказывают благоприятное воздейств
 Могут ли камни в желчном пузыре уйти сами по себе?
Что такое желчный пузырь? Некоторые камни в желчном пузыре могут раствориться и исчезнуть после вмешательства, в то время как другие требуют более обширного лечения. желчный пузырь представляет со
Могут ли камни в желчном пузыре уйти сами по себе?
Что такое желчный пузырь? Некоторые камни в желчном пузыре могут раствориться и исчезнуть после вмешательства, в то время как другие требуют более обширного лечения. желчный пузырь представляет со
 Какашки 101:4 признака того, что ваши какашки здоровы
Вы не поверите, что некоторые люди присылают нам фотографии какашек. Я избавлю вас от подробностей, но я видел больше селфи какашек от людей на всю жизнь. Наша команда начала размещать в этих письмах
Какашки 101:4 признака того, что ваши какашки здоровы
Вы не поверите, что некоторые люди присылают нам фотографии какашек. Я избавлю вас от подробностей, но я видел больше селфи какашек от людей на всю жизнь. Наша команда начала размещать в этих письмах