Teknikken kan fremskynde identifikationen af resistensdeterminanter for multiresistente (MDR) patogener og udviklingen af nye anti-resistens strategier.
Forskningen åbnede en ny vej til genomisk at redigere disse vilde bakteriearter og isolater, såsom dem med klinisk og miljømæssig betydning og dem, der danner humant mikrobiom. Det gav også en ramme til at udnytte andre CRISPR-Cas-systemer, der er udbredt i prokaryote genomer og udvide de CRISPR-baserede værktøjskasser. Forskningen er blevet offentliggjort i det førende videnskabstidsskrift Nucleic Acids Research .
CRISPR-Cas system omfatter det adaptive immunsystem i prokaryoter, der afvæbner invaderende vira ved at spalte deres DNA. På grund af dens unikke evne til at målrette og ændre DNA -sekvenser, CRISPR-Cas er blevet udnyttet som den næste generations genomredigeringsmetode.
Metoden er baseret på klasse 2 type II CRISPR/Cas9 system, som har revolutioneret genetik og biomedicinsk forskning i et væld af organismer og blev tildelt Nobelprisen i kemi i 2020. Imidlertid, klasse 2 CRISPR-Cas systemer repræsenterer kun ∼10% af CRISPR-Cas systemer kodet naturligt i prokaryoter. Deres applikationer til at redigere bakterielle genomer er ret begrænsede.
Bemærkelsesværdigt, CRISPR-Cas-systemer, der tilhører forskellige klasser og typer, identificeres løbende, og de fungerer som et dybt reservoir til udvidelse af de CRISPR-baserede værktøjskasser. De mest forskelligartede og bredt distribuerede CRISPR-Cas-systemer er type I-systemet, der tegner sig for 50% af alle identificerede CRISPR-Cas-systemer og har potentiale til at udvide de CRISPR-baserede værktøjssæt med særprægede fordele, der ikke er tilgængelige med klasse 2-systemerne, såsom høj specificitet, minimal off-targeting, og kan slette store fragmenter.
Imidlertid, type I CRISPR-Cas system afhænger af et multi-komponent effektorkompleks betegnet som Cascade for at interferere DNA, som ikke let kan overføres til heterologe værter, hindrer den udbredte anvendelse af disse naturligt rigelige CRISPR til genomredigering og terapi.
Tidligere har teamet har identificeret et meget aktivt type I-F CRISPR-Cas-system i et klinisk multiresistent stof P. aeruginosa stamme PA154197, som blev isoleret fra en infektionstilfælde i blodbanen på Queen Mary Hospital. De karakteriserede dette CRISPR-Cas-system og udviklede med succes en genomredigeringsmetode, der kan anvendes i MDR-isolatet baseret på dette native I-F CRISPR-Cas-system. Metoden muliggjorde hurtig identifikation af resistensdeterminanterne for det kliniske MDR-isolat og udviklingen af en ny anti-resistensstrategi ( Cellerapporter , 2019, 29, 1707-1717).
For at overvinde barrieren for at overføre den komplekse type I Cascade til heterologe værter, i dette studie, holdet klonede hele typen I-F cas operon i en integrationskyndig vektor mini-CTX og leverede kassetten til heterologe værter ved konjugering, en almindelig DNA -overførselsmetode. Mini-CTX-vektoren muliggjorde integration af hele Cascade på den bevarede attB genetisk locus i de heterologe værts genom gør det muligt for dem at have et "native" type I-F CRISPR-Cas-system, der kan udtrykkes stabilt og fungere.
Teamet viste, at den overførte type I-F Cascade viser en signifikant større DNA-interferenskapacitet og højere belastningsstabilitet end det overførbare Cas9-system og kan bruges til genomredigering med effektivitet (> 80%) og enkelhed, dvs. ved en et-trins transformation af et enkelt redigeringsplasmid.
Desuden, de udviklede et avanceret overførbart system, der omfatter både en meget aktiv type I-F Cascade og en rekombinase for at fremme anvendelsen af systemet i stammer med en dårlig homolog rekombinationskapacitet, vild P. aeruginosa isolerer uden genomsekvensinformation, og i andre Pseudomonas arter.
Endelig, de indførte type I-F Cascade-gener kan let fjernes fra værtsgenomerne gennem I-F Cascade-medieret deletion af store DNA-fragmenter, hvilket resulterer i skarp genomredigering i værtscellerne. Anvendelsen af det overførbare system til genrepression blev også demonstreret, fremhæver de robuste og mangfoldige anvendelser af det udviklede overførbare type I-F CRISPR-system.
Dr Aixin Yan forudsagde, at denne nye metode vil blive udvidet til at redigere ikke kun patogener, men også mikrobiom for at fremme menneskers sundhed.
Vi tror på, at CRISPR-baseret teknologi og terapier vil bringe nye forhåbninger til at beregne superbugs i fremtiden . "
Dr Aixin YAN, Lektor, Forskningsafdeling for molekylær og cellebiologi, Det Naturvidenskabelige Fakultet, University of Hong Kong
 Det, du spiser, kan ændre den måde, antibiotika påvirker din tarm på
Det, du spiser, kan ændre den måde, antibiotika påvirker din tarm på
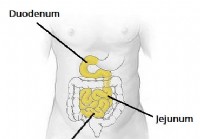 Tyndtarmen
Tyndtarmen
 Syre-pH forbedrer SARS-CoV-2-infektionen ved at opregulere ACE2-receptoren
Syre-pH forbedrer SARS-CoV-2-infektionen ved at opregulere ACE2-receptoren
 Lungemikrober kan hjælpe med at forudsige resultater hos alvorligt syge
Lungemikrober kan hjælpe med at forudsige resultater hos alvorligt syge
 Sommerfare:BBQ-grillbørsteledninger forårsager store helbredsproblemer
Sommerfare:BBQ-grillbørsteledninger forårsager store helbredsproblemer
 Otte almindelige fødevareallergier:Symptomer og behandling
Otte almindelige fødevareallergier:Symptomer og behandling
 Tarm og orale mikrobiomer forudsiger sværhedsgraden af COVID-19
Et spørgsmål, der fortsat er ubesvaret under den igangværende coronavirus-sygdom 2019 (COVID-19) pandemi, har været, hvorfor er der et karakteristisk hit-and-miss-mønster, når det kommer til alvorlig
Tarm og orale mikrobiomer forudsiger sværhedsgraden af COVID-19
Et spørgsmål, der fortsat er ubesvaret under den igangværende coronavirus-sygdom 2019 (COVID-19) pandemi, har været, hvorfor er der et karakteristisk hit-and-miss-mønster, når det kommer til alvorlig
 Hvad forårsager mavesmerter?
En kvinde på sin seng og oplever mavesmerter. Definition af mavesmerter og fakta Mavesmerter er smerter eller ubehag, der mærkes i den del af stammen under ribbenene og over bækkenet. Det kommer fra
Hvad forårsager mavesmerter?
En kvinde på sin seng og oplever mavesmerter. Definition af mavesmerter og fakta Mavesmerter er smerter eller ubehag, der mærkes i den del af stammen under ribbenene og over bækkenet. Det kommer fra
 IBS vs. IBD:Hvad er forskellene mellem symptomer?
IBS vs. IBD:Er de den samme tarmsygdom? Almindelige symptomer på IBS og IBD er smerter og træthedsfølelse. IBS (irritabel tyktarm) og IBD (inflammatorisk tarmsygdom) er ikke de samme problemer m
IBS vs. IBD:Hvad er forskellene mellem symptomer?
IBS vs. IBD:Er de den samme tarmsygdom? Almindelige symptomer på IBS og IBD er smerter og træthedsfølelse. IBS (irritabel tyktarm) og IBD (inflammatorisk tarmsygdom) er ikke de samme problemer m