Et højt niveau af TMB (TMB-H), som afspejler forhøjet totalt antal ikke-synonyme somatiske mutationer pr. kodende område af et tumorgenom og normalt stammer fra genpaneltest, anerkendes som en lovende biomarkør for ICI -behandlinger af forskellige solide kræftformer. Imidlertid, i klinisk praksis, det er ikke muligt at udføre genpaneltest for alle kræftpatienter.
Dr. Yoshifumi Shimada og kolleger fra Division of Digestive and General Surgery, Graduate School of Medical and Dental Sciences, Niigata Universitet, betragtede TMB-H fra en specifik CRC-patientundergruppe, som en mere robust markør til forudsigelse af effektiviteten af ICI'er, og udviklede et konvolutionsnervalt (CNN) baseret algoritme til at forudsige TMB -H CRC direkte ud fra de histopatologiske egenskaber, i særdeleshed, TIL, opnået fra hæmatoxylin og eosin (H&E) farvede objektglas. Et repræsentativt mikroskopisk billede af H &E-farvet tumor mutationsbyrde-høj kolorektal kræfttumor er vist i den ledsagende figur, demonstrere tilstedeværelsen af tumorinfiltrerende lymfocytter i signifikant forhøjet niveau sammenlignet med normalt omgivende væv.
Digital information fra sådan denne neoplastiske og også ikke-neoplastiske billeder hentet fra JP-CRC-kohorte transformeres og normaliseres til opbygning af en forudsigende konvolutet neuralt netværksmodel, der anvender Inception V3-læringsmodel, af Dr. Shimada -gruppen. Den CNN-baserede model, der er udviklet af Dr. Shimada og kolleger, har potentiale til ikke kun at reducere byrden ved korrekt diagnose på patologer, men også give den nødvendige information om patienternes lydhørhed over for ICI-baserede terapier, uden brug af dyre, tidskrævende og ikke let tilgængelig genpaneltest. Denne undersøgelse af Dr. Shimada og kolleger er offentliggjort i en nylig udgave af Journal of Gastroenterology (2021; bind 56:s. 547-559; https:/
Ud over, undersøgelserne af Dr. Shimada-gruppen gav også midler til kun at forudsige TMB-H CRC ved at bruge TIL-informationen fra H&E dias fra patienternes tumorvæv. Imidlertid, i betragtning af at patienterne i den undersøgte kohorte ikke blev behandlet med ICI'er, der kunne ikke drages nogen konklusioner vedrørende deres ICI-respons efter TMB-H-diagnosen, og det blev foreslået, at fremtidige kliniske forsøg skal udføres for at tage fat på, om TIL alene kan være nyttig som en forudsigelig biomarkør for effektiviteten af ICI'er.
Dr. Shimada siger om den nuværende undersøgelse:" Vi har udviklet kunstig intelligens til at forudsige genetiske ændringer i tyktarmskræft ved dyb læring ved hjælp af hæmatoxylin og eosin dias. Denne kunstige intelligens er vigtig for at løse omkostningsproblemerne forbundet med genetisk analyse og lette personlig medicin mod tyktarmskræft . "
Samlet set, undersøgelser foretaget af Dr. Shimada og associerede medarbejdere giver en omkostnings- og tidseffektiv og pålidelig metode til at informere klinikerne, hvis den CRC-patient, de administrerer, kan drage fordel af Immune Checkpoint Inhibitor (herunder hæmmere af PD-1-proteinet og dets ligand, PD-L1) terapi, uden at implicere brugen af genpanel.
 Sådan spiser du glutenfri og aldrig bliver glutenfri igen
Sådan spiser du glutenfri og aldrig bliver glutenfri igen
 Hvilke hjemlige retsmidler dræber halsbrand? 15 retsmidler
Hvilke hjemlige retsmidler dræber halsbrand? 15 retsmidler
 Hvad er anden specificeret fodrings- og spiseforstyrrelse (OSFED)?
Hvad er anden specificeret fodrings- og spiseforstyrrelse (OSFED)?
 Steve's SCD Diet Healing Journal:Uge 24 – The Kale Chip Fail!
Steve's SCD Diet Healing Journal:Uge 24 – The Kale Chip Fail!
 Ernæring og ikke-cøliaki hvedefølsomhed
Ernæring og ikke-cøliaki hvedefølsomhed
 Uge 2 gennemgang af 8-ugers blodsukkerdiæt
Uge 2 gennemgang af 8-ugers blodsukkerdiæt
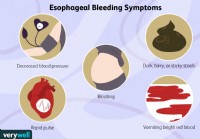 Årsager til blødning fra esophageal-varicer
Esofagus-varicer er åreknuder i spiserøret. Disse årer, som alle åreknuder, kan briste og bløde meget let. Esophageal variceal blødning er en potentielt livstruende tilstand, som skal genkendes og beh
Årsager til blødning fra esophageal-varicer
Esofagus-varicer er åreknuder i spiserøret. Disse årer, som alle åreknuder, kan briste og bløde meget let. Esophageal variceal blødning er en potentielt livstruende tilstand, som skal genkendes og beh
 Hjælper det at skubbe en hæmoride tilbage?
Hvad er en hæmoride? Hæmorider er meget almindelige og opstår, når venerne under slimhinden i endetarmen og anus bliver hævede og buler. Ja, du kan skubbe en hæmoride ind igen. Hæmorider er meget
Hjælper det at skubbe en hæmoride tilbage?
Hvad er en hæmoride? Hæmorider er meget almindelige og opstår, når venerne under slimhinden i endetarmen og anus bliver hævede og buler. Ja, du kan skubbe en hæmoride ind igen. Hæmorider er meget
 Bakteriofager kan behandle E. coli uden at skade tarmen,
siger ny undersøgelse Forskere i USA har udviklet en ny terapi, der bruger en unik bakteriofag til behandling af E. coli -infektioner. Bakteriofagen viste sig at være ens i sin effektivitet mod infekt
Bakteriofager kan behandle E. coli uden at skade tarmen,
siger ny undersøgelse Forskere i USA har udviklet en ny terapi, der bruger en unik bakteriofag til behandling af E. coli -infektioner. Bakteriofagen viste sig at være ens i sin effektivitet mod infekt