Udstyr review: Gastric intramucosal pH-måling
Introduktion
Gastric tonometri har vist sig som en attraktiv, relativt ikke-invasiv teknologi til vurdering af mave-perfusion og iltning ved at afsløre acidose i tarmvæggen. Adskillige kliniske undersøgelser har vist, at gastrisk intramucosal acidose opdaget af denne procedure forudsiger øget dødelighed af critcally syge voksne i medicinsk og kirurgisk intensiv afdeling (ICU) indstillinger [1,2,3], og at det er en bedre indikator for dødelighed fra kritisk sygdom end andre mesures af global ilttilførsel og systemiske hæmodynamik [4]. Det er også blevet foreslået, at korrigere intramucosal acidose kan øge overlevelsen i udvalgte kritisk syge patienter [5].
Formålet med denne gennemgang er at diskutere faktorer, der påvirker in vivo pålidelighed og variabilitet af gastrisk tonometri, og at analysere årsagerne til den . lejlighedsvis fejlfortolkning af resultaterne
den gastriske tonometri teknik - årsager til fejlfortolkning af resultaterne
målingen af maveslimhinden acidose ved gastrisk tonometri er baseret på princippet om, at væsken i en hul Indgange kan bruges til at estimere gas spændinger i det omgivende væv. Den vigtigste forudsætning er, at efter en given ligevægt tid, luminale og slimhinde CO
2 partialtryk (PCO 2) vil være ens. Følgelig den øgede produktion væv af CO 2 under hypoxi (fra reaktionen mellem hydrogen anioner og bicarbonat) kan detekteres ved at analysere væsken inden den gastriske lumen.
Konventionel gastrisk tonometri indebærer placeringen af en modificeret nasogastrisk ( NG) rør, udstyret med en gas-permeabel, saltvand fyldt silikone ballon ved sin spids, ind i maven [6,7] (fig 1). At tillade tilstrækkelig tid til ækvilibrering af CO 2 mellem fluidet i ballonen og mavens lumen (30-90 min), saltvand derefter aspireret, og dens PCO 2 bestemmes ved anvendelse af en blodgasanalysator. Således kan gastrisk tonometri bestemme intraluminale PCO 2 (Pico 2), som antages at være i equilbrium med maveslimhinden PCO 2. Intramucosal pH (PHIM) kan beregnes ved Henderson-Hasselbach-ligningen ved hjælp af Pico 2 værdi bestemt ved gastrisk tonometri og koncentration den arterielle bicarbonat, forudsat at væv bicarbonatkoncentration den er i ligevægt med det i kapillærerne, som . er yderligere antages at være den samme som bestemt for arterielt blod
derfor kan årsager til vildledende fortolkninger af gastrisk tonometri opdeles som følger:
en. dem, der "stammer fra patientens, og faktisk forvirre den logiske fortolkning baseret på kliniske bestemmelser (hovedsageligt, forstyrrelser i systemisk syre base balance),
to. lokale faktorer i mavens lumen, som kan ændre forholdet mellem Pico 2 og slimhinde PCO 2, og
3. faktorer, der ligger i den teknik, som kan forårsage fejlagtige bestemmelser af Pico 2. Figur 1 Gastric tonometri bestemmer intraluminal pCO2 som antages at være i ligevægt med PCO2 i maveslimhinden. Intramucosal pH (Phim) kan beregnes af Henderson-Hasselbach ligningen ved hjælp af PCO2 værdi bestemt af gastrisk tonometri og koncentration af bikarbonat i arterieblod
Patient faktorer -. Fra Phim at DPCO2
Ifølge en rapport [8] , gastrisk tonometri ikke præcist estimere størrelsen af faldet i pH i vævet betingelser med lav perfusion (hel eller delvis okklusion af øvre mesenteriske arterie); direkte måling af pH med mikroelektroder viste sig at være mere præcis. En sandsynlig forklaring på den unøjagtighed af gastrisk tonometri i disse lave perfusion betingelser er, at vævet bikarbonat niveauer overvurderet når bestemmes via arterielle koncentration. Dette skyldes, væv bicarbonat forbruges af pufring protoner, der genereres af iskæmisk væv, derfor reducere tilførslen af frisk bicarbonat. Som et klinisk eksempel på dette fænomen, Benjamin et al
[9] rapporterede, at beregnet PHIM blev normal med natriumhydrogencarbonat administration i behandlingen af en patient med alvorlig systemisk acidose trods laparotomi gennemprøvede massiv mesenterisk iskæmi, hvilket resulterer i en korrektion af den beregnede Phim.
Men en undersøgelse af bidraget fra maveslimhinden til sin egen syre-base-status skal indeholde en vurdering af arterielt blod perfusion dette område. Hvis arteriel bicarbonat er lav på grund acidose opstår end mave-tarmkanalen eller andet sted, kan derefter beregnet PHIM være lav på trods normal Pico 2.
Faktisk studier i kritisk syge patienter har vist en slående sammenhæng mellem PHIM og målinger af metabolisk acidose [4,10]. Derfor måler Pico 2 alene er enklere og eliminerer arteriel bikarbonat som en fejlkilde
Tissue PCO 2 -. Parameteren vi sigter mod at bestemme ved gastrisk tonometri - equilbrates næsten præcis med kapillar PCO 2 og ifølge den Fick princip, er relateret til væv CO 2-produktion og arteriel CO 2 indhold, og er omvendt relateret til regional blodgennemstrømning. Derfor ændringer i arteriel PCO 2 (Paco 2) bør påvirke væv PCO 2. Det er blevet vist, at respiratorisk acidose fører til væv hyperkapni i dyr [11]. Denne observation er i overensstemmelse med de kliniske undersøgelser, der viser, at patienter med hyperkapni har en betydeligt højere Pico 2 end dem uden, og at deres Phim er også signigficantly lavere [12]. Forholdet mellem Paco 2 og Pico 2 er også blevet observeret i enkelte patienter, hvis Paco 2 blev ændret af ændringer i dødt rum [13]. Således Phim vurderer ikke kun splanknisk iltning, men også arteriel syre-base-status.
Gradient mellem Pico 2 og Paco 2 (DPCO 2), som udelukkende bestemt af forholdet mellem blodgennemstrømning og CO 2 produktion i vævet, bør være et bedre mål for slimhinde perfusion. Et nyt spørgsmål udspringer denne påstand - hvor meget koster DPCO 2 nødt til at stige for at angive ikke bare lave gastrisk blodgennemstrømning, men også anaerob generation af CO 2 [14]? Schlichtig og Bowles [15] for nylig rapporteret, at den begyndende intestinal anaerobiose i normale hunde forekom, når Pico 2 var steget til 65 mmHg og DPCO 2 var steget til 25-35 mmHg.
Anvendelse af gradient mellem intramucosal og arteriel pH [16] synes at være mere besværlige og mindre præcise end DPCO 2 [17].
Endelig bør vi spørge, om maveslimhinden acidose altid indikerer væv hypoperfusion. Som de fleste undersøgelser validering gastrisk tonometri, den førnævnte artikel af Schlichtig og Bowles [15] anvendte en model for gradvis nedsættelse flow. Men der er tegn fra dyr sepsis modeller af intestinal slimhinde acidose, der er relateret til vævshypoksi [18,19]. Derfor kan væv acidose i sepsis skyldes andre end cellulære dysoxia årsager. Det er blevet foreslået, at en præferentiel stigning i anaerob glukoseudnyttelse på bekostning af oxidativ glucosemetabolisme, selv i nærvær af passende eller endda supranormale iltindhold, kan føre til væv acidose [20,21]. Dette koncept har vigtige kliniske implikationer - vi skal tage særlig omhu, når de deltager til septiske patienter med gastrisk mucosa acidose fordi det kan faktisk ikke være uomtvistelige beviser på væv hypoperfusion [21]
Lokale faktorer, der kan påvirke mavens tonometri
. forholdet mellem høj Pico 2 og slimhinde iskæmi i maven er ugyldig i tilfælde, hvor CO 2 er produceret i lumen. Buffering af mavesyre ved bicarbonat, enten fra en eksogen kilde, eller fra gastriske eller duodenale sekreter, er en væsentlig årsag til øget intraluminal CO 2.
Studier i humane frivillige forsøgspersoner har vist, at administration af ranitidin, en H 2 receptor blokerende middel, reducerer fejl i Pico 2 måling [22,23,24]. Derfor er hæmning af syresekretion nu anses for at være obligatorisk for korrekt vurdering af intraluminale PCO 2. Imidlertid har denne anbefaling ikke valideret i kritisk syge patienter; undersøgelser tyder på, at brugen af H 2-blokkere i den kritisk syge har ingen effekt på vurderingen af intraluminale PCO 2 [25,26]. Uoverensstemmelser mellem resultater i raske frivillige og kritisk syge patienter kan være relateret til en reduceret mavesyre sekretion i sidstnævnte som følge af kompromitteret visceral perfusion [27,28,29]. Imidlertid blev disse studier af kritisk syge patienter udført med små patientprøver og over en kort periode, uden ændringer i deres hæmodynamiske status. Resultaterne kan derfor ikke finde anvendelse på hæmodynamisk ustabile patienter.
Effekten af andre behandlinger almindeligvis gives via et NG rør på målingen Phi ved gastrisk tonometri fortsat uklart. Andetsteds [30] undersøgte vi effekten af sucralfat, som er meget brugt til stress ulcus blødning profylakse fordi det ikke væsentligt reducere gastrisk pH og mindskes yderligere risiko for gastrisk bakteriel overvækst. Vores resultater antydede, at enteral administration af sucralfat ikke ændrer bestemmelsen af Phim ved gastrisk tonometri i kritisk syge patienter.
Enteral ernæring kan også påvirke præcis vurdering af PICO 2. Når maden kommer ind i maven stimulerer sekretion af mavesaft og bicarbonationer. Denne kombination sammen med fordøjelsen af næringsstoffer, kan generere CO 2 inde i gastriske lumen. Hos dyr er det blevet vist, at gastrisk instraluminal PCO 2 stiger efter fodring [31]. Denne virkning er også blevet observeret hos asymptomatiske forsøgspersoner [32] og i kritisk syge patienter [33]. Derfor er det i øjeblikket anbefales at enterale fodringer afbrydes for omkring 1-2 timer før måling Phim. Denne periode kan være nødvendigt at være længere i patienter med forsinket gastrisk tømning.
I normale conditioins, blodtilførslen til hver del af mavetarmkanalen er proportional med niveauet af lokal aktivitet. Blood flow stiger efter fodring med 100-150% for 3-6 h. Betyder, at hvis strømmen ikke kan øge hensigtsmæssigt, kan enteral ernæring resultere i gastrointestinal hypoxi med mucosal acidose. Faktisk har tilstedeværelsen af slimhinde acidose efter fodring blevet anvendt til at påvise kronisk gastrisk iskæmi [32]
Faktorer relateret til teknik -. Fra saltvand til luft
Gastric tonometri præsenterer de vigtigste kilder til problem - den nødvendige tid fra ligevægt, målingen af saltvand PCO 2, og det potentielle tab af CO 2 under transport af prøven.
den første af disse, den nødvendige tid til ligevægt, er en vigtig faktor. Ligevægtsindstilling følger ficks love. Fuldstændig ækvilibrering af tonometer opløsning med mucosal PCO kræver 2 mindst 60-90 minutter, med kortere tider resulterer i målingen bliver meget variabel.
Måling af saltvand PCO er 2 også en vigtig kilde til fejl og, som vist ved Takala et al
, afhænger af både den anvendte analysator og den faktiske PCO 2 plan [34]. De fleste analysatorer undervurderet saltvand PCO 2 ved 5-19%. Især udførelsen af alle analysatorer markant forbedret, når en bufferopløsning blev brugt. Hvorfor så ikke bruge en buffer løsning i stedet for saltvand? Problemet er, at på grund af den højere CO 2-bindingskapacitet af bufferen, der kræves mere tid til ækvilibrering af væv og prøve CO 2, hvilket reducerer evnen af intragastrisk tonometer at reagere på ændrede væv PCO 2.
andet alternativ til anvendelse af saltvand er luft. Brugen af 'balloonless' luft tonometri er blevet rapporteret hos dyr, og Salzman et al har påvist en god sammenhæng mellem tonometrisk PCO 2 målinger opnået samtidig fra prøver af luft og saltopløsning [11]. Selv om der i ovennævnte undersøgelse luften blev analyseret ved en blodgas analysator, har brugen åbnet af muligheden for at bestemme intramucosal PCO 2 ved kapnografi.
Kapnografi er grundlaget for nogle nye systemer for næsten kontinuerlig overvågning af intramucosal PCO 2. En nylig valideret system tillader kontinuerlig recirkulation af gas gennem ballonen af tonometer [35]. Det nye system blev sammenlignet med et konventionelt tonometer i en in vivo eksperiment på hunde med hypoksi. Luften systemet viste en højere følsomhed i detektion af vævshypoksi. Den sandsynlige forklaring på den større følsomhed af det kontinuerlige målesystem var, at den recirkulerende gas var allerede i ligevægt med Pico 2 umiddelbart før induktion af hypoxi.
Et automatiseret tonometrisk system, der også bruger kapnografi med en konventionel tonometer er nu kommercielt tilgængelige [36]. Dette system giver mulighed for samtidig bestemmelse af end-tidal CO 2 med Pico 2 at estimere DPCO 2. Dette system fungerer ved at indføre en vis mængde luft ind i ballonen, som er periodisk aspireret for at bestemme PCO 2. Det samme luft sendes tilbage til ballonen efter bestemmelse tonometrisk PCO 2. Derfor, som med det ovenfor beskrevne system, der bruger recirkulerende gas, det øger følsomheden over for ændringer i intramucosal PCO 2, så prøvetagning gange kortere end 30 min.
Udover højere følsomhed, de forventede fordele ved disse systemer er :
en. kortere prøvetagningstidspunkter,
to. det valgte tidspunkt for ligevægt er altid konstant, og
3. det faktum, at der ikke er behov for saltvand aspiration og transport til en blodgasanalysator, undgå risikoen for CO 2 tab under transport og dermed reducere det faktiske antal fejlkilder i teknikken.
Konklusion
sammenfattende gastrisk tonometri er forholdsvis simpel teknik, men at opnå pålidelige resultater og fortolke dem nøjagtigt kræver en omfattende viden om teknik og omhyggelig opmærksomhed til mindste detalje. Målefrekvens er begrænset af den nødvendige tid og personale indgriben involveret. Brugen af luft i stedet for saltvand, og PCO 2 bestemmelse ved kapnografi synes at være lovende metoder til at undgå nogle af de problemer, at teknikken gaver.
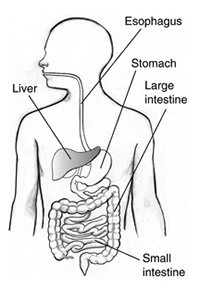 Hepatitis
Hepatitis betyder en betændelse i leveren. Betændelse forårsager smertefuld, rød hævelse og opstår, når væv bliver såret eller inficeret. Betændelsen kan forårsage, at organer ikke fungerer korrekt.
Hepatitis
Hepatitis betyder en betændelse i leveren. Betændelse forårsager smertefuld, rød hævelse og opstår, når væv bliver såret eller inficeret. Betændelsen kan forårsage, at organer ikke fungerer korrekt.
 Nanoteknologi og COVID-19 diagnose og behandling
Udviklingen af nano-biosensorer og nanopartikelbaserede vacciner og medicin har åbnet en ny vej mod bedre håndtering af coronavirus-sygdommen 2019 (COVID-19) pandemi. I en nyligt offentliggjort arti
Nanoteknologi og COVID-19 diagnose og behandling
Udviklingen af nano-biosensorer og nanopartikelbaserede vacciner og medicin har åbnet en ny vej mod bedre håndtering af coronavirus-sygdommen 2019 (COVID-19) pandemi. I en nyligt offentliggjort arti
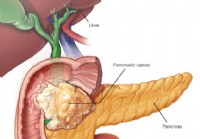 Bugspytkirtelkræft (adenokarcinom)
Bugspytkirteltumorer kan klassificeres i fire kategorier:Vi vil fokusere på adenocarcinom her, da det er den type kræft, der findes i 95 % af diagnosticeret bugspytkirtelkræft. Epitel:Duktalt epitel
Bugspytkirtelkræft (adenokarcinom)
Bugspytkirteltumorer kan klassificeres i fire kategorier:Vi vil fokusere på adenocarcinom her, da det er den type kræft, der findes i 95 % af diagnosticeret bugspytkirtelkræft. Epitel:Duktalt epitel