Epstein-Barr virus inficeret gastrisk adenocarcinom udtrykker latente og lytiske virale transkripter og har en distinkt human genekspressionsprofil
Abstract
Baggrund
EBV DNA er fundet inden de maligne celler fra 10% af gastriske cancere. Moderne molekylær teknologi letter identifikation af virusrelaterede biokemiske effekter, der kunne hjælpe i tidlig diagnose og sygdom management.
Metoder
I denne undersøgelse, RNA udtryk profilering blev udført på 326 macrodissected paraffinindlejrede væv, herunder 204 kræft og, når rådighed, der støder ikke-malign slimhinde. Nanostring NCounter sonder målrettet 96 RNA (20 virale, 73 menneske, og tre spiked RNA).
Resultater
I 182 væv med passende Husholderske RNA blev tydelige profiler findes i inficeret versus
inficerede kræftformer, og i maligne versus
tilstødende benign slimhinde. EBV-inficerede gastriske cancere udtrykt næsten alle de 18 latent og lytisk EBV RNA'er i testpanelet. Niveauer af EBER1
og EBER2
RNA var højeste og var proportional med mængden af EBV genomer som målt ved Q-PCR. Blandt protein-kodende EBV RNA, EBNA1
fra Q-promotoren og BRLF1
var stærkt udtrykt mens EBNA2
niveauer var lav positiv på kun 6/14 inficerede kræftformer. Samtidig opregulering af cellulære faktorer indebærer, at virus er ikke en uskyldig tilskuer, men snarere er knyttet til NFKB signalering (FCER2, TRAF1
) og immunrespons (TNFSF9, CXCL11, IFITM1, FCRL3, MS4A1 og PLUNC)
, med PPARG
ekspression implicerer ændret cellulær metabolisme. Sammenlignet med tilstødende ikke-maligne slimhinde, gastrisk kræft konsekvent udtrykt INHBA, SPP1, Thy1, SERPINH1, CXCL1, FSCN1, PTGS2 (COX2), BBC3, ICAM1, TNFSF9, SULF1, SLC2A1, Tyms
, tre kollagener, cellens proliferation markører MYC
og PCNA
, og EBV BLLF1
mens de manglede CDH1 (E-cadherin), CLDN18
, PTEN, SDC1
(CD138), GAST
(gastrin) og sin nedstrøms effektor CHGA
(chromogranin). Sammenlignet med lymphoepithelioma-lignende karcinom i livmoderhalsen, gastrisk kræft udtrykte CLDN18, EPCAM, REG4, BBC3, OLFM4, PPARG
, og CDH17
mens de havde formindsket niveauer af IFITM1
og HIF1A
. Den druggable mål ERBB2 (HER2), MET, og HIF vej, samt flere andre potentielle farmakogenetiske indikatorer (herunder EBV infektion selv, samt SPARC, Tyms, FCGR2B
REG4
) blev identificeret i nogle tumor prøver.
Konklusion
Denne undersøgelse viser, hvordan moderne molekylær teknologi, der anvendes til arkivering faste væv udbytter nye indsigter i viral onkogenese, der kunne være nyttige i forvaltningen berørte patienter.
Nøgleord
gastrisk adenocarcinom Epstein-Barr virus RNA udtryk profil Stromaceller Farmakogenetisk test Baggrund
mavekræft er den anden hyppigste årsag til global dødelighed kræft med næsten en million nye tilfælde om året [1, 2]. Omkring ti procent af gastriske adenokarcinomer er Epstein-Barr virus (EBV) smittet, og EBV betragtes som en klasse 1 onkogen patogen af Verdenssundhedsorganisationen [3-6]. Forekomsten er stigende for de kræftformer i den proksimale del af maven (Cardia, corpus) hvor EBV er oftere involveret [7-14]. Nyt data fra National Cancer Institute kræft overvågningsprogram viser en bekymrende stigning i gastrisk kræft forekomst blandt unge voksne i USA [7, 8, 15]. Emerging målrettet terapi gør det endnu mere vigtigt at identificere inficerede kræftformer og til at karakterisere biokemiske defekter såsom ERBB2 overekspression, der øger sandsynligheden for respons på trastuzumab i metastatisk gastrisk kræftpatienter [16-18]. EBV-inficerede i forhold til ikke-inficerede mavekræft har en gunstig prognose [19], og kliniske forsøg er begyndt at udforske virus målrettet behandling såsom 1) infused EBV-specifikke cytotoksiske T-celler eller NK-celler [20-23], 2) at vende EBV-relaterede methylator fænotype [24], 3) udløser lytisk viral replikation, der kunne så opildne kroppens medfødte og adaptive immunrespons til at dræbe inficerede tumorceller [25-33], og 4) lytisk induktion terapi administreres samtidigt med antiviral nukleosid analoge såsom gancyclovir, der er phosphoryleret og dermed aktiveres af virale kinaser fremmer cytotoksicitet [34-41].
Kliniske studier, der undersøger effekten af målrettet terapi ville drage fordel af laboratorieanalyser, der hjælper med at identificere kandidater, der kan reagere, og kunne drage fordel af laboratoriet analyser der tilkendegiver effekten af intervention de tilsigtede biokemiske veje. Moderne molekylær teknologi tillader nu klinisk kvalitet analyse af flere relevante analytter via RNA ekspressionsprofil [42]. fabrikanter Device har produceret følsomme, specifikke og tilpasses probe arrays til samtidigt at måle flere RNA'er, herunder ikke-kodende RNA som EBV-kodet RNA 1 eller 2, som er rigeligt til udtryk i inficerede tumorer. Nylige fremskridt i kvalitetssikring strategier har modnet til det punkt, at RNA udtryk profiler bliver gennemført i indstillinger kliniske laboratorium [42].
At være praktisk i kliniske omgivelser, skal en analyse gælde for rutinemæssigt indsamlede prøver såsom arkivering, paraffin -embedded væv [42]. I den aktuelle undersøgelse, målt vi viral og humane gen-ekspression i arkivering gastriske cancere og i tilstødende mucosa og kontroller til at udvikle en testsystemer, der kan anvendes til pålideligt karakterisere signaturer til forudsigelse af respons på målrettet terapi. En 96-RNA-array testsystem, som vi dubbe den Gastrogenus v1 ™ panel blev tilpasset til at måle relevante latente og lytiske virale RNA sideløbende klinisk relevante menneskelige mRNA, der tidligere blev rapporteret til at være en) gastrisk kræft specifikke, 2) indikerer inflammation og /eller 3) til forudsigelse af respons på specifikke medikamenter. Disse assays samt spidse og endogen kontrol RNA'er, blev målt i macrodissected paraffinsnit ved hjælp af Nanostring NCounter testsystemet [43-45]. Korrelative histologiske og molekylære undersøgelser blev gjort for at vise, at testsystemet udført som forventet. Vores resultater viser, at EBV-relaterede kræftformer udtrykker mere latente og lytiske udskrifter end blev tidligere indregnet, og at inficerede kræftformer har unikke biologiske egenskaber i sammenligning med ikke-inficerede kræftformer. To større undertyper af kræft blev fundet, hvilket indebærer, at gastrisk kræftstrategier tidlig påvisning eller overvågning tests kunne skræddersys til at registrere de relevante underskrifter kendetegner store molekylære undertyper. Endelig pilot data afslører ekspression af udvalgte virale og cancerrelaterede gener i tilstødende ikke-malign slimhinde, hvilket tyder på en felt-effekt, der kunne være vigtige i udviklingen eller vedligeholdelse cancer.
Resultater Salg genekspressionsprofilering blev udført på en total af 326 væv, herunder 187 gastrisk kræft, 17 lymphoepithelioma-lignende livmoderhalskræft, og 118 matchede ikke-maligne slimhinde fra samme kirurgiske indgreb (hvis de findes). Efter data normalisering, en varme kort over de 182 væv der har den bedste kvalitet RNA, som bedømt ved højeste gennemsnitlige niveau af fire husholdning RNA'er, viste mønstre af genekspression, der afveg i gastrisk versus Salg cervikale kontrol væv. Endvidere i både gastriske og cervikale klynger, maligne og ikke-maligne væv tendens til at klynge sammen, understøtter evne NCounter testsystem til måling af klinisk vigtige biologiske funktioner. (Se Figur 1). Figur 1 Expression profiler af 182 væv til 20 virale gener og 73 humane gener. Et zonekort viser ukontrollerede hierarkisk klyngedannelse af hvert væv i en separat kolonne, og hver RNA i en separat række. Dataene er median-centreret med rød indikerer relativ overekspression og grøn indikerer forhold under-udtryk for hvert gen. Korrelative data over kortet angiver histopatologisk klassifikation med yderligere underopdeles af mavekræft kohorte i 14 EBV inficerede og 104 EBV negative kræft baseret på EBV-DNA-niveauer. Under kortet er hver gastrisk cancer kategoriseret efter andelen af maligne celler, og geografisk oprindelse af hvert væv er vist. Salg One gruppe af gastriske carcinomer overudtrykkes stort set alle de EBV RNA'er. For at afgøre, hvilke gastrisk kræft bør udpeges som EBV-inficerede, blev 71 vævene med de højeste kombinerede niveau af EBER1
og EBER2
RNA ved Nanostring NCounter vifte yderligere undersøgt for EBV genom niveauer inden for samme væv ved Q PCR. Der var en lineær sammenhæng mellem mængden af EBER1
og EBER2
RNA og mængden af EBV-genomet. (Se Figur 2). Vores tidligere konstaterede cutoff [46] for niveauet af EBV-genomet svarende til lokalisering af virus til maligne celler resulterede i 14 cancere de placeres i EBV-inficerede kategori. De resterende gastrisk kræft blev kaldt EBV-negative, og blandt dem den højeste registrerede RNA-niveauer var 174.016 for EBER1
27.972 for EBER2
. I modsætning hertil blandt de EBV-inficerede gastrisk kræft den laveste EBER1
niveau var 263.589, og den laveste EBER2
niveau var 140.081. Foreslåede cutoffs for at identificere en væv som EBV-inficerede, er vist i Figur 2. Figur 2 EBV-kodet RNA-niveauer er høje i inficeret gastrisk cancer og er proportionalt med EBV-genomet niveau. A. Box plots af EBER1
og EBER2
i godartede og ondartede væv afslører, at EBV-inficerede mavekræft har væsentligt højere niveauer af EBER1
og EBER2
ikke-kodende RNA end gør inficerede kræft og kontrol væv. Foreslåede tærskler for EBER1
eller EBER2
vises ud over hvilken en mavekræft kunne pålideligt udpeges som EBV-inficerede. Hver prik repræsenterer en individuel analytisk resultat på en log 2 normaliseret enhed (NU) skala. B. Parvis sammenligning af EBER1
og EBER2
RNA niveauer ved Nanostring NCounter array og EBV DNA viral load ved Q-PCR afslører en lineær sammenhæng mellem niveauerne af hver af disse analytter. Pearson korrelationskoefficienter (P > 0,86) er vist. Den tidligere valideret niveau af EBV-DNA virusbelastningen er vist over hvilket EBER
var altid lokaliseret til maligne celler ved EBER in situ
hybridisering (tærskel på 10,558 EBV genomer pr 100.000 celler, hvilket svarer til 13,37 på denne log2 skala ) [46]. Foreslåede cutoffs for RNA-niveauer er angivet for både EBER1
(200.000 NU, eller 17,61 på denne log 2 skala) og EBER2
(100.000 NU, eller 16,61 på denne log2 skala). Den ene outlier er en ikke-malign gastrisk mucosa, som var placeret ved siden af en EBV-inficerede gastrisk cancer, og denne mucosa havde en EBV DNA belastning svarende til den for inficerede cancere, men det ville have været korrekt udelukket fra EBV-inficerede kræft gruppe, hvis enten EBER1
eller EBER2
RNA-niveauer blev brugt, eller hvis histologi blev brugt, til at screene for EBV-relaterede malignitet.
Gener overudtrykt i EBV-inficerede versus EBV-negative mavekræft
Tyve otte gener blev signifikant udtrykkes forskelligt i EBV-inficerede cancere sammenlignet med EBV negative gastriske cancere (p < 0,05). Interessant alle 28 blev opreguleret i stedet nedreguleret i de inficerede cancere, og denne skævhed er forklaret i det mindste delvist af vores udvalg af positive snarere end negative markører for infektion valg af de RNA'er, der skal profileres til denne undersøgelse. Manglende identificere eventuelle nedreguleret gener var stadig overraskende i betragtning rapporter om, at EBV er associeret med en CpG ø methylator fænotype og derudover virus kan destabilisere cellulære mRNA'er globalt [47].
Blandt generne signifikant opreguleret i inficerede cancere var alle 18 EBV RNA'er undersøgt såvel som cytomegalovirus-pp65 (UL83). Cytomegalovirus pp65 (UL83) resultat vil sandsynligvis være falsk positiv (formodet at være probe krydshybridisering), som vist ved fravær af en anden lytisk RNA, cytomegalovirus pol (UL54), i EBV-inficerede cancere. Endvidere blev UL83 men ikke UL54 udtrykt i EBV-inficerede, men ikke i EBV-negative kontroller cellelinje (data ikke vist). En anden mulig forklaring på falsk positiv viral RNA-ekspression er probe krydsreaktivitet med viralt DNA. Ni menneskelige RNA'er blev signifikant opreguleret i EBV-inficerede forhold til EBV negative gastrisk kræft: FCER2, MS4A1 (CD20), PLUNC, TNFSF9, TRAF1, CXCL11, IFITM1, PPARG
, og FCRL3
. (Se Figur 3). Figur 3 Multiple humane RNA'er overudtrykt i EBV-inficerede gastrisk cancer sammenlignet med EBV-negative cancer. Box plots demonstrere de menneskelige RNA'er niveauer i inficerede forhold til ikke-inficerede gastrisk kræft og kontroller, der omfatter lymphoepithelioma-lignende livmoderhalskræft, livmoderhalskræft slimhinde, og godartet gastrointestinale slimhinde. Hver prik repræsenterer en individuel analytisk resultat på en log2 normaliseret enhed skala. Salg Gener udtrykkes forskelligt i gastrisk cancer sammenlignet med ikke-malign gastrointestinal mucosa
Twenty seks gener blev signifikant dysreguleret i gastrisk cancer sammenlignet med ikke-malign gastrisk mucosa ( p < 0,05). De menneskelige RNA opreguleret i mavekræft var INHBA, SPP1, Thy1, SERPINH1, CXCL1, FSCN1, COL1A1, SPARC, COL1A2, PTGS2 (COX2), BBC3, ICAM1, TNFSF9, MYC, SULF1, SLC2A1, COL3A1, PCNA, og Tyms
, mens de nedreguleret RNA var CDH1 (E-cadherin), CLDN18
, CHGA
(chromogranin), PTEN, SDC1
(CD138) og GAST
(gastrin). Den eneste virale faktor, differentielt blev udtrykt var BLLF1
der var signifikant højere i kræft end i ikke-malign gastrisk mucosa (p = 0,004). BLLF1
koder for sene virale kappeprotein gp350 /220, hvilket antyder, at virioner er betydeligt mere udbredt i cancer end i ikke-malign gastrisk væv. BLLF1
var ikke specifik for gastrisk cancer, dog, som det også blev udtrykt i nogle godartede og ondartede cervikale væv, samt. Salg gener associeret med gastrisk cancer sammenlignet med lymphoepithelioma-lignende livmoderhalskræft
Ni gener var signifikant dysreguleret i gastrisk cancer sammenlignet med lymphoepithelioma-lignende livmoderhalskræft (p < 0,05). De syv RNA opreguleret i mavekræft var CLDN18, EPCAM, REG4, BBC3, OLFM4, PPARG
, og CDH17
, mens de to nedreguleret gener var IFITM1
og HIF1A
.
Mønstre i latent og lytisk viral genekspression i EBV-inficerede gastriske cancere
de 14 EBV-inficerede gastriske cancere i denne undersøgelse konsekvent co-udtrykt næsten alle de EBV latente og lytiske gener, som er noget overraskende i betragtning, at forudgående litteratur beskriver en noget begrænset latenstid mønster [48-51]. Det er muligt, at Nanostring NCounter analytisk teknologi er mere følsomme end traditionelle metoder til påvisning.
Mest stærkt udtrykt viral RNA blev EBER1 på
et gennemsnit på over 1 million normaliserede enheder pr EBV-inficerede kræftvæv, efterfulgt af EBER2
, BRLF1
og EBNA1
fra af Q-promotoren. EBNA2
var den mindste udtrykte viralt RNA med en gennemsnitlig ekspression af kun 10 normaliserede enheder pr inficeret væv og EBNA2
var helt fraværende i 8 af de 14 inficerede gastriske cancere. Mønstre af viral genekspression er afbildet i Figure4. Figur 4 Latent og lytiske EBV gener co-udtrykkes i mavekræft. En portion af den varme, kort fra Figur 1 vises i høj kontrast at dechifrere relative ekspressionsniveauer af EBV-gener i de 14 EBV-inficerede gastriske cancere og omgivende prøver. Alle væv er gastriske cancere undtagen en enkelt ikke-malign gastrisk mucosa, er vist i gråt, dissekeret fra den samme paraffinblokken som en EBV-inficeret mavekræft. Mean ekspressionsniveauet af hvert RNA i EBV-inficerede mavekræft kohorte er vist til højre for hvert gen symbol.
Geografisk oprindelse og tumorcelle andel ikke fortrinsvis forbundet med EBV status mavekræft
Under zonekort i Figur 1 er fordelingen af gastriske kræfttilfælde efter geografisk oprindelse fra Honduras (n = 86), Japan (n = 5), eller USA (n = 17). Der var ingen signifikant sammenhæng mellem geografisk oprindelse og EBV-positive versus
negative gruppering af gastrisk kræft (Fishers eksakte test p = 0,9), hvilket tyder på, at den geografiske oprindelse er ikke den største drivkraft for hierarkisk klyngedannelse.
Bunden af Figur 1 viser også fordelingen af EBV-inficerede versus Salg EBV-negative gastriske cancere klassificeret af andelen af maligne celler input til ekspressionsprofil assay. Der var ingen signifikant sammenhæng mellem andelen af maligne celler og EBV-inficerede versus Salg EBV-negative grupper af mavekræft. Overraskende har kræft væv med lav maligne celleindhold ikke fortrinsvis klynge med de ikke-maligne gastriske væv. Kræft med lav maligne celle indhold (1 til 25% maligne celler), blev fordelt på forskellige segmenter af zonekort sammen med kræft med medium (26 til 50%) eller høj (> 50%) maligne celle indhold (Fishers eksakte test p = 0,5), hvilket tyder på, at de samlede transkriptom funktioner opvejer tumorceller forhold som føreren af hierarkisk klyngedannelse.
Holde i tankerne, at lymphoepithelioma-lignende livmoderhalskræft i denne undersøgelse var rig på lymfoide stroma, som er mange EBV-inficerede gastrisk kræft det er bemærkelsesværdigt, at disse to klasser af kræft grupperet separat fra hinanden og også opnået rimeligt godt adskillelse fra tilstødende ikke-malign slimhinde. For de fleste gener i panelet, der er betydeligt overlap i niveauer på tværs af sygdomsområder typer. Mens profiler er mere informativ og mere overbevisende end er individuelle udskrift resultater, der er en vis overlapning i profiler så godt, som betyder, at profilering analyseresultater skal være korreleret med histologiske træk for nøjagtigt at klassificere et væv som godartet eller ondartet.
Farmakogenetisk prædiktorer og druggable mål
EBV infektion selv betragtes som en handlingsrettet mål, i det mindste for 14/108 (13%) smittet gastriske cancere vi identificeret. Denne undersøgelse viser en hidtil ukendt måde at identificere virusinficerede cancere ved RNA profilering af paraffinsnit så der kan betragtes prognostisk og prædiktiv information i patientens ledelsesbeslutninger. Cellular faktorer farmakogenetisk potentiale omfatter HIF vej, SPARC, Tyms, FCGR2B, MET,
og ERBB2 (HER2)
. (Se Figure5). Sammenlignet med gastrisk kræft, livmoderhalskræft tendens til at have højere niveauer af HIF1A
indikerer hypoxi reaktion, selv om lige så høje niveauer i ikke-maligne cervikal slimhinde hæve muligheden for ex vivo
stimulering af denne ilt-sensing faktor. Yderligere undersøgelse er nødvendig for at skelne tekniske faktorer fra in vivo
opregulering, der ville berettige overvejelse af angiogenese-hæmmere. Figur 5 Nogle gastrisk kræft har betydelig dysregulering af faktorer, der viser lovende som farmakogenetiske prædiktorer. Kassediagrammer demonstrerer ekspression af udvalgte farmakogenetiske mål i inficerede versus ikke-inficerede gastriske cancere såvel som ikke-malign gastrisk mucosa og cervikale histopathologies. Hver prik repræsenterer en individuel analytisk resultat på en log2 normaliseret enhed skala.
Vi bekræftede, at SPARC
er opreguleret i mavekræft sammenlignet med godartet maveslimhinden. Reaktion på docetaxel, er en taxan stof, der hæmmer mitosespindelen forsamling, efter sigende påvirket af mængden af SPARC proteinekspression i gastrisk kræft [52]. Gastric og livmoderhalskræft begge havde højere thymydylate syntase (Tyms)
end gjorde deres respektive godartede slimhinder modstykker. Høje Tyms
niveauer bidrager sigende til erhvervet resistens over for 5FU kombinationsbehandling [53].
Enkelte gastrisk kræft havde ekstremt høje niveauer af Fc-receptoren, FCGR2B
, som kunne påvirke narkotika internalisering og farmakodynamik terapeutiske antistoffer såsom cetuximab in vivo.
Fire gastrisk kræft udtrykt stærkt MET,
og yderligere otte tilfælde stærkt overeksprimeres udtrykte ERBB2 (HER2)
, øge muligheden at denne analyse kunne forudsige respons på tyrosinkinasehæmmer terapi.
diskussion
Denne undersøgelse anvendte moderne molekylære metoder til at undersøge et stort panel menneske og virale RNA i mavekræft. Så vidt vi ved, er dette den største panel af virale genprodukter, der skal undersøges i samråd med humane RNA'er i arkivering, paraffinindlejrede væv. EBV-inficerede undertype af mavekræft er dramatisk tydeligt i den tilsvarende zonekort skabt af uovervåget klyngedannelse, og EBV infektion blev bekræftet af høje EBV DNA virale belastninger i disse væv. Ekspression af udvalgte virale og menneskelige gener i de kræftformer bekræftet adskillige kendte virus- og kræftrelaterede påvirkninger samt afslørede nye fund, som kaster lys over patogenese og mulige management sygdom strategier.
Overraskende de inficerede gastrisk kræft overudtrykt alle 18 latente og lytiske EBV-gener, som blev testet. Vi opdagede høje niveauer af BRLF1
RNA (der koder for umiddelbare tidlige virusprotein udløse lytisk replikation i samråd med BZLF1) og moderat høje niveauer af BXLF1
(den virale thymidinkinase, der konverterer penicyclovir til en toksisk form antyder en mekanisme til terapi) [54]. BLLF1
(der koder for det sene virale kappeprotein gp350 /220) blev udtrykt på et moderat niveau, der ikke desto mindre var betydelig højere end i ikke-maligne slimhinde, hvilket antyder, at EBV lytisk infektion er ikke mislykkede men snarere er i stand til at producere den sene virale kappe protein gp350 /220. Blandt de latente gener, EBNA1
fra Q-promotoren, EBNA-LP, og EBNA3C
transkripter var mest udbredt. EBNA2
blev fokalt detekteret ved lavt niveau, men var stadig betydeligt højere i inficeret end hos ikke-inficerede gastriske cancere. Forud histokemisk arbejde har generelt ikke afsløret protein-ekspression af EBNAs eller lytiske virale genprodukter, så yderligere arbejde er påkrævet for at lære, hvis disse viralt koder RNA er lokaliseret til maligne celler, lymfocytter, eller måske endda til exosomer eller virioner i den ekstracellulære milieu.
Sammenlignet med ikke-inficerede kræftformer, de inficerede kræftformer havde en betydelig opregulering af ni cellulære faktorer (FCER2, MS4A1 (CD20), PLUNC, TNFSF9, TRAF1, CXCL11, IFITM1, PPARG
, og FCRL3
), hvilket indebærer, at EBV er ikke en uskyldig tilskuer med hensyn til biokemisk virkning. De virus-associerede ændringer, vi fandt var i veje kendt for virale onkologer, nemlig NFKB og HAK signalering (FCER2, TRAF1, PPARG
) og slimhinder immunrespons (PLUNC, TNFSF9, CXCL11, IFITM1, FCRL3
). MS4A1 (CD20) er B-celle specifikke, minder os om, at nogle af de faktorer opreguleret i EBV-inficerede forhold til ikke-inficerede gastrisk kræft kunne stamme fra stromale elementer snarere end fra maligne epitelceller. PLUNC
er tidligere beskrevet som en tumormarkør for gastriske og nasopharyngeale carcinomer, og det koder for et secerneret protein involveret i medfødte immunreaktion [55-57]. TNFSF9, et cytokin af tumornekrosefaktorfamilien, stimulerer T-celleaktivering og udløser IFNg produktion, som igen inducerer det proinflammatoriske kemokin CXCL11 og det medfødte antivirale faktor IFITM1. PPARG er som en nuklear receptor kontrollerende glukosemetabolismen og mikrotubuli netværk, og det er et lovende mål for hæmmende lægemidler [58]. Den FCRL3
immunrespons gen er muteret i autoimmune sygdomme som leddegigt, lupus, og Graves sygdom.
Vores resultater støtte arbejdet i Lee et al
der fundet tydelige menneskelige ekspressionsmønstre i inficeret versus
uinficerede gastriske cancere [10]. Selv om deres undersøgelse målrettet protein og vores målrettede RNA, vores resultater er aftalt med deres for 4 af de 5 faktorer i fælles mellem de to undersøgelser (BCL2, PTEN, CDH1, PTGS2
). Der var en potentiel Afvigelsen for ERBB2
der var signifikant mindre hyppigt udtrykkes i inficerede sammenlignet med ikke-inficerede gastriske cancere, når de testes på proteinniveauet [10], mens den nuværende undersøgelse viste ingen signifikant forskel på RNA-transkript niveau. Forstyrrende faktorer indbefatter 1) andelen af tumorceller til stede i prøverne evalueret, 2) forskellige kriterier for kategorisering ekspressionsstatus og 3) RNA versus protein-targets.
Generelt array teknologi, der blev anvendt i denne undersøgelse fungeret enestående godt i at generere RNA-profiler, der var troværdigt i kraft af distinktionen mellem en kendt godartet versus
maligne og gastrisk versus
cervikale histopathologies. Endvidere co-ekspression af analytter i samme sti eller det samme smitstof giver mening fra et patobiologien og virologi perspektiv. Interessant, blev alle de cervikale væv grupperet sammen, og benigne og maligne cervikale læsioner stort set adskilt selvom Gastrogenus v1 ™ testpanel ikke var blevet specielt designet til at opnå disse endpoints. Mangel på flere co-udtrykte EBV mRNA i cervikale væv forstærkede hvad vi vidste om deres EBV-negativitet fra guldstandarden EBER in situ
hybridiseringsanalyse.
Blandt de syv gener, der var betydeligt mere til udtryk i gastrisk kræft (uanset for infektion status) sammenlignet med lymphoepithelioma-lignende livmoderhalskræft, blev fire tidligere rapporteret som mavekræft markører (CLDN18, REG4, OLFM4, CDH17
) [55, 59-63]. To andre (EPCAM epitelcellespecifik transmembrane glycoprotein, og PPARG chemokin), samt REG4, udforskes til målrettet cancerterapi [64-66]. Den sidste af de syv, BBC3 (også kaldet p53 opreguleret modulator af apoptose, eller PUMA) er efter sigende opreguleres af EBV LMP2A og regerede i af EBV miR-BART5 i cellelinje modeller [67, 68], hvilket tyder på, at denne BCL2 familie medlem er stramt reguleret af virus.
En af de to RNA, der var væsentligt højere i livmoderhalskræft sammenlignet med mavekræft var IFITM1
, som du kan huske viste sig også at være overudtrykt i inficeret forhold til ikke-inficerede gastrisk kræft. Yderligere arbejde er nødvendigt for at udforske, om livmoderhalskræft (formentlig human papillomavirus-inficeret) og EBV-inficerede gastrisk kræft deler en fælles virus-relaterede mekanisme til overekspression af denne medfødte immunrespons faktor. Den anden gen signifikant overudtrykt i livmoderhalskræft sammenlignet med mavekræft var HIF1A
hvis udtryk var forbundet med den af fire downstream angiogenese mæglere i vores panel (VEGFA, SLC2A1, SLC2A3
og EPAS1
) som det fremgår af positiv Pearsons korrelationskoefficienter (data ikke vist). Hvis bekræftet at være operativ i vivo
, HIF pathway stimulation indebærer, at angiogenese inhibitorer er værd at undersøge.
Benign versus
maligne gastrisk væv tendens til at klynge særskilt på zonekort, med visse undtagelser. Felt effekt [69] eller exosomal overførsel af faktorer til tilstødende områder af det lokale miljø [70, 71] kunne forklare, hvorfor nogle kræftformer og tilstødende reaktive væv havde lignende profiler. Mens macrodissection blev anvendt til forsigtigt at adskille godartet fra maligne læsioner, kan vi ikke udelukke okkult malignitet som bidragyder til afvigende klyngedannelse.
Blandt de 19 gener signifikant opreguleret i gastrisk cancer sammenlignet med tilstødende ikke-malign gastrisk mucosa, de fleste blev tidligere rapporteret som gastrisk kræft specifikke markører [72-76], og vi nu bekræfte, at deres opregulering kan påvises i arkivers paraffinindstøbt væv. Lavere niveauer af GAST
(gastrin) RNA i cancer væv kan hjælpe med at forklare den samtidige tab af gastrin signalering faktor CHGA
(chromogranin). Den mest konsekvent nedreguleret faktor i gastrisk cancer versus
tilstødende benign slimhinde var tumorsuppressorgenet CDH1 (E-cadherin)
tyder enten 1) CDH1
promotor hypermethylering [77], 2) sjældne kimlinie mutation af CDH1
forbundet med arvelig prædisposition for gastrisk cancer [78], eller 3) nedregulering af CDH1
efter EBV LMP1 som beskrevet i cellelinje modeller [79].
LMP1 er tidligere rapporteret at være fraværende i inficeret gastrisk cancer undtagen i sjældne tilfælde [50, 51, 80, 81]. Det var derfor overraskende, at Nanostring NCounter matrix profilering viste konsistent omend lav ekspression af LMP1
RNA sammen med stort set alle de andre EBV RNA'er, som blev afprøvet i de inficerede gastriske cancere niveau. Koordineret co-ekspression af flere virale gener hævder, at udtrykket er sandt positive. Vores microarray resultater rejser den mulighed, at de virale RNA'er Vi har registreret ikke koder proteiner eller at proteinerne er 1) kun forbigående udtrykt, 2) hurtigt nedbrydes, 3) lokaliseret til sjældne celler, der straks anerkendt og ødelagt af immunsystemet, eller 4) til stede ved en sådan lavt niveau, at de traditionelle analyser er for ufølsomme til at opdage dem [82]. Det NCounter testsystem producent hævder analytisk følsomhed svarer til rtPCR [43].
Mens de fleste virale gener blev udtrykt næsten udelukkende i den inficerede gastrisk kræft kohorte, EBER1
og EBER2
var almindeligt udtryk i hver enkelt de benigne og maligne gastriske og cervikale kohorter, omend ved meget lavere værdier end sås i hver af EBV-inficerede gastriske cancere. Faktisk vores undersøgelse afslørede en ny måde at identificere EBV-inficerede mavekræft ved at måle EBER1
og /eller EBER2
RNA i arkivering væv, og vi har foreslået grænseværdier, der med held skelne smittet fra inficerede mavekræft.
støtte til aktiv viral infektion hos inficerede mavecancerpatienter kommer fra serologisk tegn på højere titere mod viral capsid antigen sammenlignet med EBV-negative patienter gastrisk cancer og godartede kontroller [83]. Lavt niveau lytisk infektion er tidligere beskrevet i mucosale lymfoide celler [31, 82, 84] og i inficerede gastriske epiteliale cellelinjer [85]. BARF1 vides at blive udtrykt i gastrisk cancer, hvor det foreslås at fungere som en latent snarere end en lytisk faktor [50, 51]. Brug af følsomme rtPCR teknologi, blev flere EBV lytiske transkripter detekteret ved Luo et al i gastrisk cancer væv [50].
 Crohns sygdom og colitis ulcerosa Lignende tegn og symptomer
Crohns sygdom og colitis ulcerosa Lignende tegn og symptomer
 Sådan passer du på din fordøjelsessundhed:regelmæssigt indtag af fermenteret mælk kan forbedre milde fordøjelsessymptomer
Sådan passer du på din fordøjelsessundhed:regelmæssigt indtag af fermenteret mælk kan forbedre milde fordøjelsessymptomer
 Kan antispasmodika behandle IBS?
Kan antispasmodika behandle IBS?
 Cologuard-test vs. koloskopi
Cologuard-test vs. koloskopi
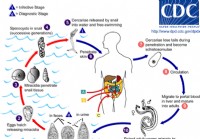 Schistosomiasis
Schistosomiasis
 Sådan afhjælper du forstoppelse med naturlig bevægelse
Sådan afhjælper du forstoppelse med naturlig bevægelse
 Beskyttelse af lungerne under abdominal kirurgi kan mindske komplikationer
Seneste fordøjelsesnyt Når nyretransplantation mislykkes, er det bedst at prøve igen Lad ikke halsbrand ødelægge din feriefest Efterspørgslen efter levertransplantation stiger kraftigt Lavdosis CT-sc
Beskyttelse af lungerne under abdominal kirurgi kan mindske komplikationer
Seneste fordøjelsesnyt Når nyretransplantation mislykkes, er det bedst at prøve igen Lad ikke halsbrand ødelægge din feriefest Efterspørgslen efter levertransplantation stiger kraftigt Lavdosis CT-sc
 Hvorfor stopper Prednison diarré?
Har du nogensinde undret dig over, hvorfor de fleste mennesker med en diarré, der blusser op, får en recept på Prednison? Det er ikke fordi diarré er forårsaget af lavt niveau af Prednison i kroppen.
Hvorfor stopper Prednison diarré?
Har du nogensinde undret dig over, hvorfor de fleste mennesker med en diarré, der blusser op, får en recept på Prednison? Det er ikke fordi diarré er forårsaget af lavt niveau af Prednison i kroppen.
 Sådan behandles prostatakræft
Behandlingsmulighederne for prostatacancer kan variere baseret på mange faktorer, herunder tumorens aggressivitet, sygdomsstadiet, personlige præferencer og mere. Kurative muligheder kan omfatte kirur
Sådan behandles prostatakræft
Behandlingsmulighederne for prostatacancer kan variere baseret på mange faktorer, herunder tumorens aggressivitet, sygdomsstadiet, personlige præferencer og mere. Kurative muligheder kan omfatte kirur