Serum trefoil faktor 3 er en lovende non-invasiv biomarkør for gastrisk kræftscreening: En monocentriske kohortestudie i Kina
Abstrakt
Baggrund
søgen efter bedre ikke-invasive biomarkører for mavekræft forbliver i gang. Vi undersøgte forudsigelseskraft af serum trefoil-faktor (TFF) niveauer som biomarkører for mavekræft i sammenligning med pepsinogen (PG) test. Salg Metoder
patienter med gastrisk cancer, kronisk atrofisk gastritis (CAG) eller kronisk ikke- atrofisk gastritis (CNAG), og sunde mennesker blev rekrutteret. Serumkoncentrationer af TFFs, PG I og PG II, samt tilstedeværelsen af antistoffer mod Helicobacter pylori
, blev målt ved enzym-bundet immunosorbent assays (ELISA). Receiver opererer egenskaber (ROC) blev brugt til at sammenligne de prædiktive beføjelser udvalgte faktorer.
Resultater Salg The serumkoncentrationer af TFF1, TFF2, og TFF3 i kontrolgrupperne var betydeligt lavere end i mavekræft gruppen med undtagelse af TFF2 som blev forhøjet i KAG. Arealet under ROC-kurven for TFF3 var større end for PG I /II-forholdet (0,81 vs 0,78). TFF3 havde også en signifikant højere forudsigelseskraft til at skelne mavekræft end PG test (odds ratio: 10.33 vs 2,57). Desuden kombinerer TFF3 og PG test serum til mavekræft havde bedre forudsigelseskraft end enten alene.
Konklusioner
Serum TFF3 kan være en bedre indikator for mavekræft end PG testen, mens den kombinerede test af serum PG og TFF3 kunne forbedre effekten af gastrisk kræftscreening.
Nøgleord
mavekræft Diagnose Serum kløverblad faktorer Pepsinogen Baggrund
mavekræft er den næsthyppigste årsag til kræft død. Omkring en million nye tilfælde af mavekræft er diagnosticeret årligt på verdensplan [1]. I de fleste lande, herunder Kina, er mavekræft normalt påvises på et fremskredent stadium, når prognosen er dårlig. I Japan har et omfattende screeningsprogram hjælp photofluorography og endoskopi lykkedes at diagnosticere de fleste af gastrisk kræft på tidligere stadier, hvilket har ført til et fald i associeret dødelighed [2-4] 40-60%. Men udbredt endoskopi screening er ikke på lager i Kina. Derfor er den første udvælgelse af højrisiko-individer med en enkel og effektiv non-invasiv biomarkør, før endoskopisk undersøgelse, er blevet foreslået som en fornuftig strategi for mavekræft masse screening.
Serum pepsinogen (PG) afprøvning, en nuværende fremgangsmåde til gastrisk cancer screening, har den fordel at være enkel og billig. Det har været anvendt som en del af store screening i Japan. Men på grund af utilstrækkelige beviser, PG testen endnu ikke anbefales, for populationsbaseret screening [5, 6]. Desuden, mens en kombination af serum PG og Helicobacter pylori
(HP) antistof test er rapporteret at være overlegen med PG testning alene til forudsigelse gastrisk cancer risiko, denne metode har også endnu ikke nået et niveau, hvor det kan anvendes direkte til at screene for mavekræft [7].
trefoil faktor (TFF) familie består af tre varmestabile og protease-resistente proteiner, TFF1, TFF2, og TFF3 [8]. Disse proteiner menes at spille en central rolle i mucosal beskyttelse mod beskadigelse [9]. Deres onkogent potentiale er også blevet rapporteret at være forbundet med celleproliferation, apoptose, migration og invasion og angiogenese [10-16]. Ekspressionen af disse peptider i mavetarmkanalen forekommer i en vævs- og cellespecifik måde. TFF1 og TFF2 overvejende udtrykt i maveslimhinden [17], mens TFF3 udtrykkes i slimceller i tarmen og også ved lavere niveauer i andre organer, såsom i brystet, spytkirtel, luftveje, og hypothalamus [18-22]. For nylig, serumniveauer af TFFs i kræftpatienter, herunder dem med mavekræft, er blevet rapporteret til at blive øget, og derfor kunne være nyttige biomarkører til screening [23-27].
I vores undersøgelse, vi undersøgte serumniveauer af TFFs i patienter med gastrisk cancer. Effekten af serumniveauer af TFFs som biomarkører for mavekræft blev yderligere analyseret i forhold til PG test.
Metoder
Emner
Seventy-to patienter med mavekræft, som gennemgik behandling fra januar 2012 til oktober 2012 på den Institut for Gastrointestinal Kirurgi på Ningbo Medical center of Lihuili Hospital blev rekrutteret til denne undersøgelse. Serumprøver blev opnået før behandling. Klinisk-patologiske data, herunder TNM fase af tumorer og den histologiske type, og ifølge Lauren klassificering, blev også opsamlet. Sixty-én patienter med kronisk atrofisk gastritis (KAG) og 27 patienter med kronisk non-atrofisk gastritis (CNAG) blev også rekrutteret fra Institut for Gastrointestinal Endoskopi siden marts 2012 til juli 2012. CAG og CNAG blev diagnosticeret ved endoskopisk pathohistology, hvor CAG blev defineret som et tab af gastriske kirtelceller eller de erstattes af intestinal og fibrøst væv i antrum eller corpus af fundus ved biopsi. De serumprøver fra 37 raske mennesker, der rapporterede ingen historie af øvre gastrointestinale lidelser, blev indhentet fra sundhedstjekket Center of Lihuili Hospital fra Juli 2012 til oktober 2012. Forsøgspersonerne blev udelukket, hvis de præsenteres med svære co-morbiditet, herunder lever-, nyre-, hjerte-, og hæmatologisk sygdom, eller havde tidligere gennemgået øvre gastrointestinal kirurgi eller vagotomi. Skriftligt informeret samtykke blev opnået fra alle deltagere i overensstemmelse med Helsinki-deklarationen. Godkendelse fra videnskabsetisk komité af Lihuili Hospital blev også opnået.
Immunoassays for TFFs, pepsinogen I, Pepsinogen II, og Anti-HP IgG
Serum indsamlet fra fastende patienter med mavekræft, CAG og CNAG, eller den sunde kontroller blev opbevaret ved -80 ° C indtil analyse. Serum TFFs, pepsinogen I, pepsinogen II, og anti-HP immunglobulin (Ig) G niveauer blev målt ved enzym-bundet antistof (ELISA).
Konkret serumniveauer af TFF1, TFF2, og TFF3 blev målt ved hjælp af kommercielle ELISA kits fremskaffet fra USCN Life Science (Wuhan, Kina) og udført ifølge producentens anvisninger. Kort fortalt blev oprensede polyklonale antistoffer coatet på en 96-brønds mikrotiterplader. Dernæst 100 pi assaybuffer, som en negativ kontrol, serumprøver, eller fortyndinger af den passende humant TFF standard, blev tilsat til deres respektive brønde, og pladerne blev inkuberet i 2 timer ved 37 ° C. Pladerne blev derefter vasket og den passende fortyndet biotin-mærket TFF polyklonalt antistof blev tilsat til hver brønd. Efter inkubation i 1 time ved 37 ° C blev pladerne vasket og fortyndet streptavidin konjugeret til peberrodsperoxidase blev tilsat til hver brønd. Efter inkubation i yderligere 30 minutter ved 37 ° C blev pladerne vasket og tetramethylbenzidin (TMB) opløsning blev tilsat i 20 minutter ved 37 ° C. Endelig stopopløsning tilsat til hver brønd, og absorbansen ved 450 nm blev målt. Koncentrationerne af humane TFFs i prøverne blev derefter beregnet fra arbejdsfluidet standardkurven. De assay følsomheder for TFF1, TFF2, og TFF3 var 44, 13,5 og 52 pg /ml.
Den serumkoncentrationer af PG I og PG II blev målt ved kemiluminescerende enzym immunoassay kits fra Biohit Plc (Helsinki, Finland). Serum PG status blev betragtet som positive (PG +) til forudsigelse mavekræft når PG I niveau serum var ≤ 70 ng /ml, og PG I /II-forholdet var ≤ 3.
HP infektion blev diagnosticeret ved påvisning af serum HP IgG-antistof under anvendelse af et kommercielt enzymimmunassay kit (Biohit Plc).
statistisk analyse
Alle statistiske analyser blev udført ved anvendelse af Graphpad Prism 5,01 (La Jolla, CA, USA). Kontinuerlig data for patienter og kontroller blev først kontrolleres for at bekræfte, om de var tæt på en normalfordeling, og derefter statistisk analyseret af t-test for normalfordelinger eller af Mann-Whitney test for ikke-normale fordelinger. En to-sidet P-værdi på < 0,05 blev betragtet som statistisk signifikant. Modtageren opererer karakteristiske (ROC) kurver og arealet under disse kurver (AUC) blev beregnet til at sammenligne de prædiktive beføjelser udvalgte faktorer.
Resultater
Baseline karakteristika for patienter og kontroller
Den baseline karakteristika af undersøgelsen fag er vist i tabel 1. Den gennemsnitlige alder af de 72 patienter med mavekræft var 61,7 ± 1,4 år (mand /kvinde ratio = 1,23), og at de 61 CAG-patienter var 56,7 ± 1,4 år (mand /kvinde ratio = 0,91), således at der var en 5-års alderen forskel mellem de to grupper. Gennemsnitsalderen for CNAG patienter var 48,1 ± 2,8 år, og at der af raske forsøgspersoner var 56,7 ± 2,8 år, og dermed CNAG gruppen var 8,6 år yngre end den sunde group.Table 1 baseline karakteristika og HP-infektion status, serum PG test af mavekræft og kontroller
mavekræft (n = 72)
CAG (n = 61)
CNAG (n = 27)
Sund kontrol ( n = 37)
Alder (år, betyder ± SD)
61,7 ± 1.4ζ
56,7 ± 1,4
48,1 ± 2,8
56,7 ± 2,8
Mand /kvinde-forholdet
1,23
0,91
0,5
1,31
Histologisk type,
Intestinal typen
25 (34,7%)
Diffuse typen
47 (65,3%)
TNM stadie
Tidlig mavekræft
16 (22,2%)
Avanceret mavekræft
56 (77,8%)
HP-infektion status
HP positiv
48 (66,7%)
30 (49,2%)
14 (51,8%)
18 (48%) pg test pg I (ng /ml)
76,91 ± 4,78 *
72,02 ± 5.48
79,64 ± 5,74
84.52 ± 4,44 pg II (ng /ml)
25,10 ± 2,35 **
19,44 ± 1,27
18,27 ± 1,93
14,39 ± 1,12
PG I /II-forholdet
3,91 ± 0.29ξ
3,99 ± 0,24
5.84 ± 0,72
7.18 ± 0,69
ζ: Ingen forskel mellem mavekræft og sund gruppe (P
= 0,08); mavekræft vs CAG P = 0,0179; mavekræft vs CNAG, P < 0.001
*: Ingen forskel mellem kræft gruppe og KAG, CNAG og sund gruppe
**:.. Gastrisk kræft vs KAG, P
= 0,0459; mavekræft vs. CNAG, P
= 0,0927; Gastrisk kræft vs sund, P
= 0,002
ξ:. Mavekræft vs. KAG, P
= 0,8485; mavekræft vs. CNAG, P
= 0,0038; mavekræft vs. sund, P
< 0,0001.
I mavekræft gruppen, 16 (22,2%) patienter havde tidligt mavekræft (fase 0, IA og IB), mens 56 (77,8%) patienter havde fremskreden mavekræft. Ifølge Lauren klassificering, 47 (65,3%) patienter præsenteret med diffus typen gastrisk cancer, mens den anden 25 (34,7%) viste intestinal type. HP smittestatus var meget tæt med en HP + vifte af 48-66,7% på tværs grupper. Serumniveauer af PG I var også ikke signifikant forskellig mellem patienter med gastrisk cancer og raske kontroller. Serumniveauer af PG II, var imidlertid signifikant højere i gastrisk cancer gruppen end i den raske gruppe. PG I-forhold /II i mavekræft gruppen var signifikant lavere end for kontrollen med undtagelse af CAG tilfælde (tabel 1).
Serumkoncentrationer af TFFs
Den serumkoncentrationer af TFF1, TFF2, og TFF3 Hos patienter med gastrisk cancer, CAG og CNAG, og i de raske grupper, er vist i figur 1. i patienter med gastrisk cancer, var den gennemsnitlige serum TFF1-koncentrationen var 1,30 ± 0,15 ng /ml (95% CI [1,01, 1,59] ), mens der i CAG, CNAG, og den sunde gruppe var 1,07 ± 0,14 ng /ml (95% CI [0,77, 1,35]), 0,70 ± 0,08 ng /ml (95% CI [0,53, 0,87]), og 0,72 ± 0,07 ng /ml (95% CI [0,58, 0,86]) hhv. Yderligere statistiske analyse viste, at den gennemsnitlige serum TFF1 niveau i gastrisk cancer var signifikant højere end i både CNAG (P
= 0,0075) og sunde gruppe (P Salg = 0,0045) patienter, men det var ikke signifikant forskellig fra at i CAG (P
= 0,1332). Koncentrationen Den gennemsnitlige serum TFF2 hos patienter med mavekræft var 1,08 ± 0,07 ng /ml (95% CI [0,93, 1,23]), hvilket var betydeligt højere end i KAG (0,86 ± 0,07 ng /ml, 95% CI [0,71, 1.00], P
= 0,034), CNAG (0,64 ± 0,08 ng /ml, 95% CI [0,47, 0,81], P
= 0,0011), og sunde (0,63 ± 0,05 ng /ml, 95% CI [0,53, 0,74], P
< 0,0001) gruppe. Det gennemsnitlige TFF3 serum niveau i mavecancerpatienter var også signifikant højere end i de andre grupper. Faktisk koncentration de gennemsnitlige serum TFF3 i patienter med gastrisk cancer var 50.95 ± 2.31 ng /ml (95% CI [46.35, 55,55]), mens der i CAG, CNAG og sunde grupper var det 31.41 ± 1,34 ng /ml (95% CI [28.74, 34,09], P
< 0,0001), 32,30 ± 2,09 ng /ml (95% CI [28,00, 36,59], P
< 0,0001) og 30,67 ± 2,20 ng /ml (95% CI [26.22, 35.13] P
< 0,0001), hhv. Figur 1 Koncentration af serum TFFs målt ved ELISA. Koncentration af serum TFFs i patienter med gastrisk cancer var signifikant højere end de andre kontrolgrupper.
ROC-analyse af serum TFF og PG test som indikatorer for mavekræft
ROC-analyse blev udført for at evaluere nøjagtigheden af serumkoncentrationer af TFFs og PG i /II-forholdet til diagnosticering af gastrisk cancer. Arealet under kurven for TFF1, TFF2, TFF3, og PG I /II-forholdet var 0,67 (95% CI [0,56, 0,77]), 0,74 (95% CI [0,65, 0,83]), 0,81 (95% CI [ ,,,0],0,72, 0,89]) og 0,78 (95% CI [0,69, 0,87]), henholdsvis (figur 2A). Således ROC kurver indikerede et højere observerede nøjagtighed for TFF3 i sammenligning med den for PG I /II-forholdet. I modsætning til CAG, arealet under kurven for TFFs viste signifikant lavere værdier i sammenligning med den for PG I /II-forholdet (figur 2B). Figur 2 ROC kurver for koncentrationen af serum TFFs og PG I /II-forholdet til at diagnosticere gastrisk cancer eller CAG. (A) ROC kurver for koncentration af serum TFFs at diagnosticere gastrisk cancer sammenlignet med PG I /II-forholdet. Arealet under kurven for serum TFF1, TFF2, TFF3 og PG I /II-forholdet var 0,67, 0,74, 0,81 og 0,78 hhv. Resultaterne viste, at serum TFF3 har en større forudsigelseskraft for mavekræft end PG I /II-forholdet. (B) ROC kurver for koncentrationen af serum TFFs og PG I /forholdet II til diagnose CAG. Arealet under kurven for TFF1, TFF2, TFF3 og PG I /II-forholdet var 0,63, 0,61, 0,53 og 0,76 hhv. Resultaterne præsenteret, at PG I /II-forholdet er en tydeligvis bedre markør for CAG detektion end alle serum TFFs.
Cutoff værdier for TFF1, TFF2, og TFF3, som beregnet af ROC, var 1,0 ng /ml, 0,7 ng /ml og 42,0 ng /ml. Følsomheden og specificiteten af TFF1 var 58,33% og 72,97%, henholdsvis, og odds ratio var 3,78. Følsomheden og specificiteten af TFF2 var 65,28% og 70,27%, henholdsvis, og odds ratio var 4,44. Følsomheden og specificiteten af TFF3 var 66,67% og 83,78%, henholdsvis odds ratio var 10,33. Følsomheden og specificiteten af PG + var 37,5% og 81,08%, henholdsvis, og odds ratio var 2,57. Disse data tyder på, at serumkoncentrationen af TFFs, især TFF3, er signifikant associeret med mavekræft som det fremgår af de væsentligt højere odds ratio end fastlagt for PG test (tabel 2) .table 2 Sammenligning af sensitivitet og specificitet af serum TFFs og PG test for mavekræft
Kriterier
Følsomhed
Specificitet
Odds forholdet
PG test (+)
37,50%
81,08%
2,57
TFF3 (≥42ng /ml)
66,67%
83,78%
10,33
TFF2 (≥0.7 ng /ml)
65,28%
70,27 %
4,44
TFF1 (≥1.0 ng /ml)
58,33%
72,97%
3,78
Effekt af HP-infektion på ROC'er af serum TFFs
for yderligere at evaluere forudsigende magt TFFs og PG i /II, mavens kræft og sunde grupper blev yderligere opdelt i henhold til HP positivitet og derefter blev udført ROC-analyse. AUC for HP-positive mavecancerpatienter var signifikant større for TFF3 (0,83, 95% CI [0,73, 0,94]) og PG I /II-forhold (0,86, 95% CI [0,74, 0,98]) end dem, for enten TFF1 eller TFF2 (figur 3A). I modsætning hertil AUC for HP negative gruppe var lidt mindre end den for HP positiv. AUC for TFF3, TFF2, og PG I /II-forholdet var meget tæt på 0,77, 0,75 og 0,72, henholdsvis (figur 3B). Disse resultater indikerer, at TFF3 er en lidt bedre markør end PG I /forholdet II til detektering mavekræft uanset HP infektion status. Figur 3 For HP +/- patienter, ROC kurver af serum TFFs og PG I /II-forholdet. (A) For HP positive patienter, området under kurven for serum TFF1, TFF2, TFF3 og PG I /II-forholdet var 0,67, 0,72, 0,83 og 0,86, henholdsvis. Serum TFF3 og PG I /II-forholdet viste en god ROC-kurve. (B) For HP-negative patienter, arealet under kurven for serum TFF1, TFF2, TFF3 og PG I /II-forholdet var 0,64, 0,75, 0,77 og 0,72, henholdsvis.
Effekt af at kombinere måling af serum TFF3 og PG test for mavekræft bestemmelse
Vi næste analyseret nøjagtigheden af ved hjælp af både koncentrationen af TFF3 og PG test til påvisning af mavekræft. Ifølge kriterierne i PG +, blev påvist 24 af de 72 gastrisk patienter ved PG testen. Men når serum TFF3 testen blev tilsat, blev påvist 54 af de 72 mavecancerpatienter med gastrisk cancer, det vil sige yderligere 30 patienter med gastrisk cancer, som ikke blev identificeret af PG resultat alene blev plukket af serum TFF3 test . Tværtimod 6 patienter med mavekræft, som ikke blev registreret af serum TFF3 var positive ved PG testen. Således selvom følsomheden af de kombinerede test forhøjes til 75%, blev specificiteten faldet.
Forholdet mellem serum TFFs og de histologiske typer og TNM stadier af mavekræft
Koncentrationerne af serum TFFs blev sammenlignet med histologiske typer og TNM stadier af mavekræft at undersøge deres indflydelse på mavens udvikling kræft og progression. Koncentrationen af serum TFF1 ikke signifikant forskellig mellem forskellige histologiske typer eller TNM etaper. Koncentrationen af serum TFF2, var signifikant lavere hos patienter med intestinal type end diffus form mavekræft (0,87 ± 0,07 vs 1,19 ± 0,10, P
= 0,0373), men det var ikke forskellig mellem tidlige og fremskredne stadier af mavekræft. Koncentrationen af serum TFF3 hos patienter med tarm form mavekræft var signifikant lavere end i diffuse type (43,87 ± 2,74 vs 54,72 ± 3,10, P
= 0,0242), det blev også reduceret hos patienter med tidlig mavekræft end i dem, fremskreden mavekræft (42,50 ± 3,32 vs 53,36 ± 2,74, P
= 0,0497) (Figur 4). Som en kontrol, PG I /II-forhold var ikke signifikant forskellig i enten forskellige histologiske typer eller TNM stadier af mavecancer. Figur 4 Fordeling af serum TFF3 i differentieret eller udifferentieret, tidlig eller avanceret mavekræft. Koncentrationen af serum TFF3 hos patienter med differentieret gastrisk cancer var signifikant lavere end i udifferentieret gruppe (P
= 0,0273). Serum TFF3 niveau hos patienter med tidlig mavekræft var også betydeligt lavere end i fremskreden mavekræft (P
= 0,0497). Resultaterne viste, at koncentrationen af serum TFF3 har korreleret med histologiske type og TNM stadier af mavecancer.
Diskussion
mavekræft er en af de mest almindelige ondartetheder. Det er normalt opdages på et fremskredent stadium, hvor prognosen er dårlig, og overlevelse er lav. For at reducere dødeligheden sygdomsrelaterede og forbedre overlevelsen, er der behov for bedre biomarkører for screening og tidlig påvisning af mavekræft. Pepsinogen testen er blevet anvendt til gastrisk cancer screening i Japan [28, 29] og er for nylig begyndt at blive anvendt i Kina. Følsomheden af pepsinogen testen er blevet rapporteret at ligge i området fra 45-77% med specificitet i området fra 68-87% [30-32]. I den foreliggende undersøgelse sensitiviteten af pepsinogen test var 37,5%, mens dets specificitet var 81,1%, og odds-forholdet var 2,57. Den relativt lavere følsomhed af pepsinogen test i vores undersøgelse, sammenlignet med den rapporterede interval, kan være forbundet med brugen af forskellige PG immunoassay kits. Iijima K et al. [33] har tidligere rapporteret, at serum PG I-niveauer bestemmes under anvendelse af GastroPenal test (Biohit Plc) var dobbelt så høje som dem, detekteret med den japanske kit, selvom PG assays med begge kits kunne identificere stærkt signifikante korrelationer mellem PG-koncentration og gastrisk kræft. Derudover kan vores resultater blive påvirket af den højere diffuse gastriske kræft i vores undersøgelse rekrutter. Faktisk er der rapporteret serum PG II niveauer øges hos patienter med diffuse form kræft [34]. Kort sagt, ser det ud til, at PG test for mavekræft let påvirkes af forskellige faktorer, og derfor ikke opfylder de ideelle kriterier for screening.
Kaise M et al. [35] var den første til at rapportere, at serumniveauer af TFFs, især TFF3, er signifikant forbundet med tilstedeværelsen af gastrisk cancer. I vores kohorte, serumkoncentrationer af TFFs viste signifikant højere odds ratio end pepsinogen test. Af de tre TFFs, den bedste biomarkør var serum TFF3 som havde en følsomhed på 66,67%, en specificitet på 83,78%, og en odds ratio på 10,33.
Den sammenlignende analyse af de pepsinogen test- og serum TFF koncentrationer til screening af mavekræft yderligere belyse deres respektive forudsigelseskraft. Vi fandt, at 48 (66,7%) af de 72 patienter med gastrisk cancer var negative for pepsinogen test, mens serum TFF3 test identificeret yderligere 30, følsomheden af at kombinere resultaterne af serum TFF3 og pepsinogen tests var 75%, hvilket var bedre end alene enten tests.
i HP positive emner, AUC af serum TFF3 var meget tæt på den for PG i /II-forhold (0,83 vs. 0,86). I HP negative emner, men AUC af serum TFF3 var lidt større end for PG I /II-forhold (0,77 vs. 0,72). De serum TFFs og PG tests er begge baseret på histologiske forandringer i maveslimhinden fra atrofisk gastritis. I denne undersøgelse blev HP-infektion bestemt ved at måle serum-anti-HP IgG-niveauer. Imidlertid er anti-HP IgG niveauer rapporteret at falde, når atrofisk gastritis har udvidet til det meste af fundiske område af maven efter langvarig HP-infektion [36]. Således kan HP positive emner i denne undersøgelse omfatter patienter med mavekræft og ikke-kræft personer med samme omfang af sværhedsgraden af atrofisk gastritis. Efterfølgende er det vanskeligt at screene for mavecancer ved anvendelse af atrofisk gastritis beslægtede markører i denne sammenhæng. Faktisk den prædiktive effekt af HP-infektion status var mindre end enten serum TFF3 eller PG testen.
Vi vurderede også forholdet mellem TFF3 og den histologiske type og stadium i mavekræft. Vi fandt, at serumkoncentrationer af TFF2 og TFF3 hos patienter med tarm form mavekræft var lavere end hos patienter med diffuse type. Hverken serum TFF1 eller PG I /II-forholdet var signifikant associeret med enten den histologiske type eller TNM stadie. Muller et al. [37] tidligere har rapporteret en meget signifikant korrelation mellem TFF1 ekspression og af pepsinogen II, en markør for gastrisk differentiering, i gastrisk adenocarcinom væv. Der var imidlertid ingen signifikant sammenhæng mellem TFF1 ekspression og den histologiske type af mavekræft. Tilsvarende har TFF1 knockout-mus blevet vist at udvikle både gastriske adenomer og carcinomer [38]. Endvidere TFF1 er blevet vist, at være markant nedreguleret i human gastrisk cancer [39]. Disse observationer kan forklare en vis grad, hvorfor serum TFF1 og PG I /II-forholdet ikke var relateret til histologiske typer og TNM stadier i gastrisk cancer. Med hensyn til TFF2 har spasmolytisk polypeptid (TFF2) udtrykkende metaplasi (SPEM) ofte blevet observeret i maveslimhinden omgivende mavekræft og TFF2 er rapporteret at være nedreguleret (83,3%) i den primære gastrisk kræft [40]. Således det lavere niveau af serum TFF2 hos patienter med intestinal type, gastrisk cancer kan afspejle udskiftning af SPEM med intestinal metaplasi. I modsætning hertil har TFF3 blevet rapporteret at være opreguleret i de fleste maligne tumorer, herunder primær mavekræft [23-27]. Desuden har dets ekspression blevet korreleret med en særdeles aggressiv fænotype og dårlig prognose [41]. Im et al. yderligere, at TFF3 udtryk er højere hos patienter med udifferentieret form mavekræft, og at det i høj grad korreleret med fremskredne stadier [39]. Dermed er resultaterne af vores undersøgelse er meget i overensstemmelse med disse rapporter. Men ifølge den histopathogenesis af gastrisk cancer, fordi TFF3 udtrykkes kraftigt af slimceller i den normale tarm og i den intestinale metaplastisk epithel af maven, høj ekspression af TFF3 ville forventes i differential type og intestinal type, gastrisk cancer,. Yderligere undersøgelser er derfor behov for at forklare disse indbyrdes modstridende fænomener. Navnlig er andre undersøgelser nylig rapporteret, at serum TFF3 øges hos patienter med lungecancer, endometriecancer, og prostatacancer, og at TFF3 udtrykkes i vævet af disse cancere [24, 26, 27]. Således kan forhøjede serum TFF3 niveauer ikke være specifikt for mavekræft. Derfor oprindelsen af høje serum TFFs har også brug for yderligere undersøgelse.
En begrænsning af denne undersøgelse er det forudindtaget prøvetagning på grund af sin tilmelding af emner fra en klinisk serie af hospitalets sager blandet med raske mennesker fra sundhedstjekket centrum af et hospital snarere end en populationsbaseret kohorte. Antallet af studier tilfælde var også begrænset. Derfor er yderligere populationsbaserede undersøgelser eller store kliniske kohortestudier kræves for at bekræfte den stærke forudsigelseskraft af serum TFF3 såvel som for dets kombination med PG test, og for derved at beskrive muligheden for serum TFF3 som en ikke-endoskopisk biomarkør i befolkningen-baserede screening for mavekræft.
konklusioner
at vurdere deres anvendelse som potentielle biomarkører for befolkningen-baserede screening, udforskede vi den forudsigelseskraft af serum TFFs sammenlignet med PG-test til påvisning af mavekræft . Vi fandt det første kan koncentrationen af serum TFF3 være en bedre biomarkør for mavekræft end PG test. For det andet kunne kombination test af serum PG og TFF3 forbedre effekten af gastrisk kræftscreening. For det tredje, serum TFF3 niveau har en forening med differentiering type og TNM stadie i mavekræft. Vores resultater støtter derfor TFF3 serum som biomarkør for gastrisk kræftscreening
Forkortelser
TFFs:.
Serum trefoil faktorer
PG:
Pepsinogen
CAG:
Kronisk atrofisk gastritis
CNAG:
Kronisk non-atrofisk gastritis
HP:
Helicobacter pylori
Ig:
Immunoglobulin
ELISA:
enzymmaerket assay
TMB:
tetramethylbenzidin
PG +: pg positiv
ROC:
Receiver opererer karakteristiske |
AUC:.
Areal under disse kurver |
erklæringer
Tak
undersøgelsen blev støttet af Ningbo Enestående Young Health Talents Fund, Ningbo Natural Science Foundation (NO. 2012A610212), Den Videnskabelige Innovation Team Project Ningbo (NO. 2013B82010) og Klinisk Videnskabelig Research Foundation of Zhejiang Medical Association (NO. 2013ZYC-A65).
Forfattere 'oprindelige indsendt filer til Images of Nedenfor er links til forfatternes oprindelige indsendt filer til billeder. 12876_2013_1108_MOESM1_ESM.tif Forfatternes oprindelige fil til figur 1 12876_2013_1108_MOESM2_ESM.tif Forfatternes oprindelige fil til figur 2 12876_2013_1108_MOESM3_ESM.tif Forfatternes oprindelige fil til figur 3 12876_2013_1108_MOESM4_ESM.tif Forfatternes oprindelige fil til figur 4 konkurrerende interesser
Forfatterne erklærer, at de har ingen konkurrerende interesser.
Forfattere bidrag
ZH designet undersøgelsen og skrev papiret. QZ og HD deltog i skrivning af papiret. XZ, HL, LW og DW opnåede prøverne og analyseret data. Alle, der er godkendt af den endelige manuskript før indsendelse. Alle forfattere læst og godkendt den endelige manuskript.
 Tarm og orale mikrobiomer forudsiger sværhedsgraden af COVID-19
Tarm og orale mikrobiomer forudsiger sværhedsgraden af COVID-19
 Find måder at forebygge hæmorider
Find måder at forebygge hæmorider
 Mere sandsynlige komplikationer ved akut galdeblærekirurgi:Undersøgelse
Mere sandsynlige komplikationer ved akut galdeblærekirurgi:Undersøgelse
 Hvad er handlen med hepatitis C?
Hvad er handlen med hepatitis C?
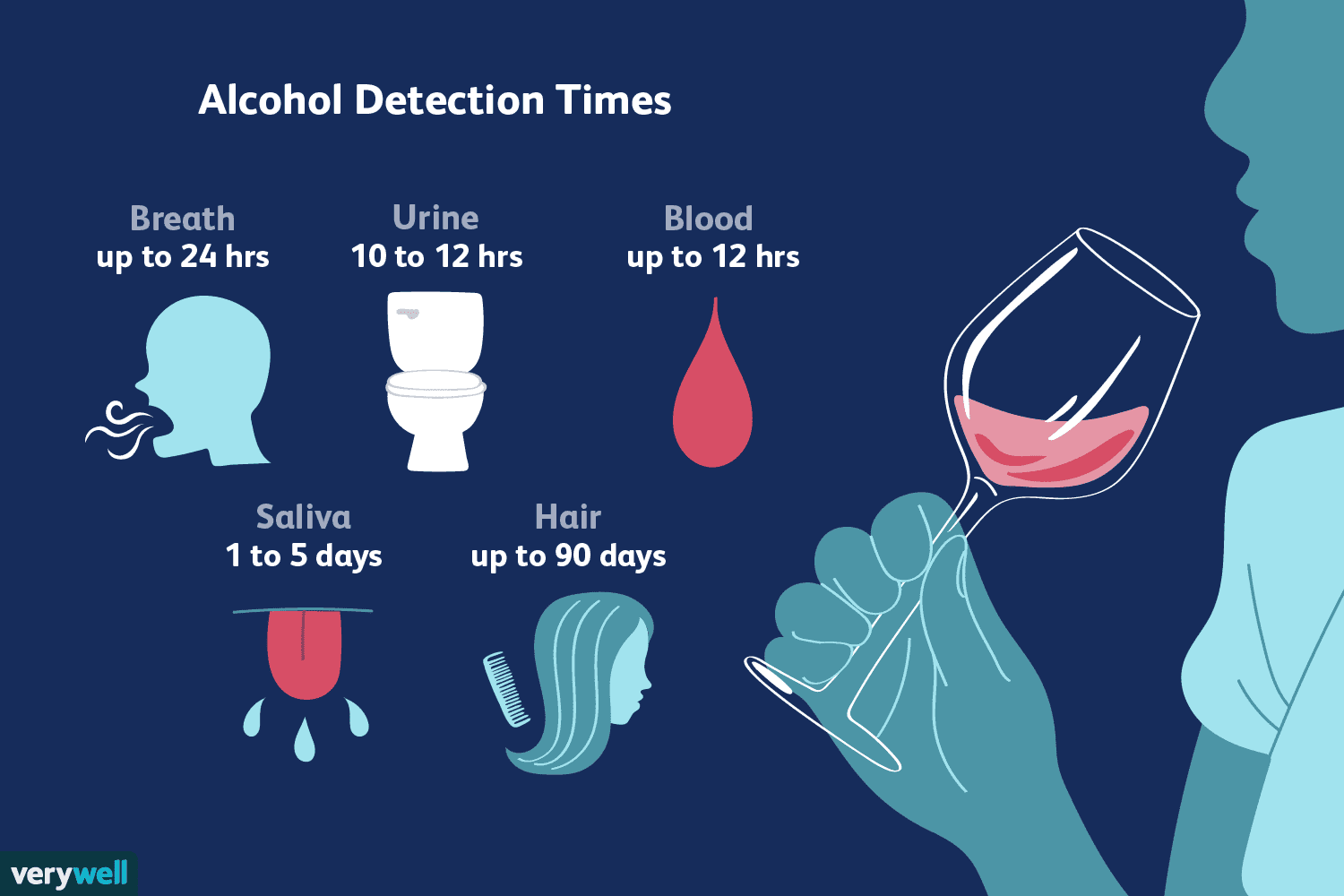 Hvor længe bliver alkohol i dit system?
Hvor længe bliver alkohol i dit system?
 Specific Carbohydrate Diet Friends Spotlight:Sherry fra SCDforLife
Specific Carbohydrate Diet Friends Spotlight:Sherry fra SCDforLife
 Perkutan endoskopisk gastrostomi (PEG)
Perkutan endoskopisk gastrostomi (PEG) center Tag Pancreatitis-quizzen Forøg fordøjelsessundheden Diashow med fordøjelsesbesvær:Problemfødevarer, der skal undgås Fakta om perkutan endoskopisk gastro
Perkutan endoskopisk gastrostomi (PEG)
Perkutan endoskopisk gastrostomi (PEG) center Tag Pancreatitis-quizzen Forøg fordøjelsessundheden Diashow med fordøjelsesbesvær:Problemfødevarer, der skal undgås Fakta om perkutan endoskopisk gastro
 The Brain Gut Connection in IBS
Dysfunktion i forbindelsen mellem hjernen og tarmen kan være en medvirkende årsag til irritabel tyktarm (IBS). IBS er langt fra simpelt, og forskere ser ud over tarmen og mod det komplekse kommunikati
The Brain Gut Connection in IBS
Dysfunktion i forbindelsen mellem hjernen og tarmen kan være en medvirkende årsag til irritabel tyktarm (IBS). IBS er langt fra simpelt, og forskere ser ud over tarmen og mod det komplekse kommunikati
 Gamle primatmikrobiomer kan give mere information om menneskelig udvikling
Gamle menneskelige mikrobiomer er under mikroskopet for det, de fortæller forskere om mennesker for længe siden. En ny undersøgelse offentliggjort i tidsskriftet Grænser i økologi og evolution i feb
Gamle primatmikrobiomer kan give mere information om menneskelig udvikling
Gamle menneskelige mikrobiomer er under mikroskopet for det, de fortæller forskere om mennesker for længe siden. En ny undersøgelse offentliggjort i tidsskriftet Grænser i økologi og evolution i feb