Abstrakt
Hintergrund
Aufgrund der geringen Toleranz gegenüber einer Chemotherapie, die maximale Anzahl der Zyklen der postoperativen adjuvanten Chemotherapie ist 4 in der adjuvanten Magen klinischen Studien. Das Ziel dieser Studie ist es, im Nachhinein die Sicherheit und Wirksamkeit von Epirubicin-basierte Triplett-Chemotherapie und Strahlentherapie bei der Behandlung von reseziert lokal fortgeschrittenem Magen-oder gastroösophagealen Übergang Adenokarzinom Adjuvans zu bewerten.
Von Januar 2004 bis Juli 2008 siebenundneunzig aufeinander folgenden Magen-oder gastroösophagealen Übergang Adenokarzinom-Patienten in Stadien T3-4 /N + wurden mit postoperativen Strahlentherapie und Chemotherapie behandelt. Die empfohlene Behandlungsplan wurde radikale Resektion von 1-2 Zyklen der adjuvanten Chemotherapie (ACT), postoperative Radiochemotherapie (CRT) gefolgt, und schließlich 4-5 Zyklen von ACT. Die Patienten wurden in zwei Gruppen eingeteilt, je nach der Anzahl der Zyklen von ACT: Gruppe 1 erhielt 4-6 Zyklen (n = 59) und Gruppe 2 erhielt 0-3 Zyklen (n = 38). Die detaillierte Gruppierung ist wie folgt: RT allein, 2; RT und CT, 18; gleichzeitige RTCT und CT, 41; und CRT, 36. Von den 97 Patienten, 77 Patienten erhielten eine begleitende Therapie (CRT, (5-Fluorouracil oder Capecitabin) und 20 erhielten Strahlentherapie allein wegen der Patient Ablehnung (n = 15) oder die Behandlung Toxizität (n = 5). Nach einem medianen Follow-up von 44 Monaten, die 3-Jahres krankheitsfreie Überleben (DFS) und Gesamtüberleben (OS) waren 66,5% und 69,5% für die Gruppe 1 und 45,5% und 50% für die Gruppe 2 (p = 0,005 und . p = 0,024) Multivariate Analyse ergab, dass 4-6 Zyklen von ACT, lymphovascular Invasion oder Peritonealdialyse Metastasen waren unabhängige prognostische Faktoren für das krankheitsfreie Überleben oder das Gesamtüberleben (p <. 0,05)
Schlussfolgerungen /Bedeutung
Diese Studie zeigt, dass die gleichzeitige Radiochemotherapie mit Adjuvans Epirubicin-basierte Triplett Chemotherapie ist möglich und erträglich für Magen-oder gastroösophagealen Übergang Karzinom-Patienten Patienten können aus mehreren Zyklen von ACT profitieren
Citation:.. Li G, Zhang Z, Ma X, Zhu J, Cai G (2013) Postoperative Radiochemotherapie in Kombination mit Epirubicin-Based Triplet Chemotherapie bei lokal fortgeschrittenem Adenokarzinom des Magens oder gastroösophagealen Übergang. PLoS ONE 8 (1): e54233. doi: 10.1371 /journal.pone.0054233
Editor: Dominique Heymann, Faculté de Médecine de Nantes, Frankreich
Empfangen: 31. Juli 2012; Akzeptiert: 11. Dezember 2012; Veröffentlicht: 25. Januar 2013
Copyright: © 2013 Li et al. Dies ist eine Open-Access-Artikel unter den Bedingungen der Lizenz Creative Commons, die uneingeschränkte Nutzung erlaubt, die Verteilung und Vervielfältigung in jedem Medium, vorausgesetzt, der ursprüngliche Autor und Quelle genannt werden
Finanzierung:. Die Autoren erklären, dass ihre Studie nicht von einem kommerziellen Sponsorings unterstützt hat. Sie fanden keine Mittel aus irgendwelchen Organisationen erhalten
Konkurrierende Interessen:. Die Autoren haben erklärt, dass keine Interessenkonflikte bestehen
Einführung
Magenkrebs ist die vierte am häufigsten diagnostizierte. Krebs weltweit und Konten für 8% aller neuen Krebsdiagnosen. Magenkrebs ist für 10% aller Todesfälle durch Krebs verantwortlich, und es ist eines der am häufigsten diagnostizierten Krebserkrankungen in Asien [1], [2]. Die meisten Patienten mit den gegenwärtigen Magenkrebs in einem fortgeschrittenen Stadium, und die Prognose schlecht bleibt, insbesondere in fortgeschrittenen Stadien [3], [4].
Chirurgie ist die primäre Magenkrebs Behandlung, aber die chirurgische Behandlung allein hat eine hohe Rate von lokoregionaler und Fernmetastasen [3], [4], und bedeutende Forschung hat sich auf die Identifizierung wirksame adjuvante Therapien fokussiert das Rezidivrisiko nach der Operation zu reduzieren. Eine Meta-Analyse der postoperativen adjuvanten Chemotherapie (ACT) zeigten eine mäßige Überlebensvorteile [5] - [9], und fünf-Jahres-Follow-up-Daten eines ACTS-GC-Studie [10] zeigten, dass die postoperative adjuvante Therapie mit S-1 Gesamtüberleben und rezidivfreie Überleben bei Patienten verbessern mit Stadium II oder III Magenkrebs, die D2 Gastrektomie unterzogen hatten. Darüber hinaus zeigte die Magen-Surgical Adjuvant Studie INT 0116 [11], dass das rezidivfreies Überleben (p < 0,001) und das Gesamtüberleben (p = 0,005) profitieren von einer adjuvanten CRT für Patienten mit einem hohen Risiko für einen Rückfall. In dieser Studie war die gleichzeitige Chemotherapie 5-Fluorouracil (5-FU) und Leucovorin, aber das Regime gedacht wird jetzt zur Verhinderung von Fernmetastasen als unzureichend. Eine Therapie mit Epirubicin, Cisplatin und 5-Fluorouracil (ECF) zunehmend wurde in fortgeschrittener Erkrankung eingesetzt und hat in der adjuvanten Therapie in Phase-II-Studien untersucht worden. Das Medical Research Council Adjuvant Gastric infusional Chemotherapie (MAGIC) Studie [12] gezeigt, dass eine perioperative Gabe von ECF Tumorgröße und Stufe verringert und eine deutlich verbesserte das progressionsfreie Überleben (PFS) und das Gesamtüberleben (OS) in funktioneller Magenkrebs oder unteren Ösophagus Adenokarzinom. Die anschließende REAL-2-Studie bestätigt, dass in der Epirubicin-basierte Triple-Therapie [Epirubicin (50 mg /m 2 am Tag 1) + Cisplatin (30 mg /m 2 an den Tagen 1-3) 5 -FU (425 mg /m 2 /Tag an den Tagen 1-5)], die Substitution von Cisplatin mit Oxaliplatin und 5-FU mit Capecitabin führte zu einer geringeren Toxizität [13]. Die vor kurzem berichtet Krebs und Leukämie Gruppe B (CALGB) 80101 Studie zeigte ein ähnliches Ergebnis mit ECF und 5-FU (ASCO 2011). Allerdings hat die Wirksamkeit von CRT mit optimalen Zyklen Chemotherapie nicht gut untersucht worden; Diese Informationen sind notwendig, um die Behandlung von lokal fortgeschrittenem Magenkrebs zu optimieren. Das Ziel dieser Studie ist es, die Wirksamkeit der adjuvanten CRT und die Wirkung der Zyklenzahl in der adjuvanten Epirubicin-basierte Chemotherapie bei Patienten mit Stadium T3-4 /N + Magen-oder gastroösophagealen Übergang Adenokarzinom zu bewerten. 1 Studienfächer Alle Daten wurden von mündigen Individuen gesammelt nach den von der Ethik Review Board an der Fudan-Universität Shanghai Cancer Center genehmigten Protokollen. Von Januar 2004 bis Juli 2008 97 aufeinander folgenden Patienten mit lokal fortgeschritten diagnostiziert und nicht metastasiertem Adenokarzinom des Magens oder gastroösophagealen Übergang wurden in die Studie eingeschlossen. Pathologische Diagnosen wurden in allen Fällen vor Staging und Behandlung erhalten. Die Aufarbeitung bestand aus einer vollständigen Anamnese, körperliche Untersuchung, Performance-Status, Blutbild, Leber- und Nierenfunktionstests, Endoskopie, Brust, Bauch-Computertomographie (CT) und Ultraschall des Beckens. Innerhalb der Kohorte, 59 Patienten (Gruppe 1) wurden nach einem institutionellen klinischen Protokoll behandelt, die von der Operation durch eine adjuvante Chemotherapie /Strahlentherapie und 4-6 Zyklen der adjuvanten Epirubicin-basierte Chemotherapie bestand. Die restlichen 38 Patienten (Gruppe 2) wurden mit der Operation durch Chemo /Strahlentherapie und 0-3 Zyklen von ACT mit dem gleichen Regime wegen der frühen Krankheitsprogression (n = 3), Patienten Ablehnung (n = 15) oder die Behandlung Toxizität behandelt, gefolgt (n = 20). Die Patientencharakteristika sind in Tabelle 1 aufgeführt; es gab keine signifikanten Unterschiede zwischen den beiden Gruppen. 2 Behandlung Details Das Behandlungsprotokoll empfohlen in unserem Institut ist die operative Entfernung Radikal, das durch 1-2 Zyklen von ACT gefolgt, postoperativen CRT und 4- 5 Zyklen von ACT, wie in Abbildung 1 gezeigt 2.1 Chirurgie. Chirurgie wurde entweder mit vollständiger oder subtotale Gastrektomie durchgeführt. Dieses Verfahren brachte die Resektion aller perigastrischen Lymphknoten und einige celiac, Milz- oder splenic-Hilus, hepaticartery und kardialen Lymphknoten, abhängig von der Lage des Tumors in den Magen. Die regionalen Lymphknoten Bereiche wurden nach den Definitionen der japanischen Forschungsgesellschaft für Magenkrebs definiert [14], [15]. Pathologische Inszenierung auf 2002 beruhte American Joint Committee on Cancer (AJCC) TNM [16]. Alle außer vier Patienten abgeschlossen adjuvante Strahlentherapie (RT) mit oder ohne ausreichend postoperativen ACT. Die vorgeschriebene Bestrahlungsdosis war 45-50,4 Gy mit 25-28 Fraktionen, 1,8 Gy pro Fraktion, fünf Tage pro Woche. Das Zielvolumen enthalten Tumorbett, anastomotischen Stoma, Magen-Rest (T3, T4), und regionalen Lymphknoten. Tumorbett durch präoperativen und postoperativen CT-Bildgebung, Barium Radiographie definiert wurde, und, in einigen Fällen, chirurgischen Klammern [11]. Perigastrischen, abdominal, lokale paraaortic, Milz-, hepatoduodenale oder Leber-Portal und pancreaticoduodenalis Lymphknoten wurden im Strahlungszielvolumen enthalten ist, und die paracardial und paraösophagealen Lymphknoten waren ebenfalls enthalten, wenn der Patient Tumoren in der gastro-Kreuzung hatte. Ausschluss der Milz- Knoten wurde bei Patienten mit antralen Läsionen erlaubt die linke Niere [17] zu schützen. Einige Patienten verwendet, um einen aktiven Atem Koordinator (ABC, n = 15) Atmung bedingte Unsicherheit bei Simulationen und Behandlungen zu reduzieren. Alle Patienten wurden mit Vakuum-Pad während der Simulation und Behandlung (CIVIC Medical Lösung, Iowa) fixiert. Die Behandlungen wurden 3-dimensionalen konformen Strahlentherapie geliefert Verwendung (3D-CRT, n = 93) oder intensitätsmodulierte Bestrahlungstherapie (IMRT, n = 4) mit einem 6-MV Photons. Simulieren CT Datensätze wurden in der CT-Simulator (Philips Medical Madison, WI) mit einer 5-mm Schichtdicke mindestens 3 Stunden nach den Mahlzeiten erworben. Alle Behandlungspläne wurden mit einem kommerziellen Bestrahlungsplanungssystem (TPS, Philips Radiation Oncology Systems, Pinnacle Version 8.0 m, Milpitas, CA) optimiert. Alle Behandlungen wurden mit einem Elekta Synergy slinear Beschleuniger geliefert mit einem elektronischen Portal Imaging-Gerät ausgestattet (EPID) und einem Kilovolt Kegelstrahl-CT-System (Elekta Synergy S, Elekta Oncology Systems, Crawley, UK). Die Toleranzen von normalen Geweben wurden wie folgt definiert: 1) weniger als 30% der Leber Aufnahme 30 Gy, mittlere Dosis an Leber weniger als 23 Gy; 2) weniger als 50% der Nieren Aufnahme 15 Gy, mittlere Dosen beider Nieren weniger als 16 Gy; und 3) weniger als 40% des Herzens, der 40 Gy. 2.3 Chemotherapie. Nach den Richtlinien des Instituts, alle Patienten empfohlen wurden Strahlentherapie mit gleichzeitiger Chemotherapie erhalten (5- Fluorouracil oder Capecitabin) und vier sechs Zyklen von Epirubicin-basierte Triplett-adjuvanten Chemotherapie sowohl vor (1-2 Zyklus) und nach (4-5 Zyklen) Chemoradiatio. 2.4 Concurrent Chemotherapie. Fluorouracil (225 mg /m 2 /Tag) mit einer kontinuierlichen intravenösen oder oralen Capecitabin (625 mg /m 2, bid) gleichzeitig mit Strahlung verabreicht wurde. 2.5 adjuvante Chemotherapie. wurden alle Patienten empfohlen, vier Minuten vor sechs weitere Zyklen von ACT (ECF) von Epirubicin bestehend erhalten (50 mg /m 2 am Tag 1), Cisplatin (30 mg /m 2 an den Tagen 1- 3), 5-FU (425 mg /m 2 /Tag an den Tagen 1-5) oder eine modifizierte ECF Schema bestehend entweder aus Epirubicin (50 mg /m 2 am Tag 1), Oxaliplatin (130 mg /m 2 am Tag 1) und 5-FU (425 mg /m 2 /Tag an den Tagen 1-5) (EOF) oder Epirubicin (50 mg /m 2 am Tag 1) , Oxaliplatin (130 mg /m 2 am Tag 1) und Capecitabin (625-825 mg /m 2 /Tag, zweimal am Tag, oral an den Tagen 1-14) (EOX). Die Patienten wurden in zwei Gruppen eingeteilt entsprechend der Anzahl von ACT-Zyklen. Die 61% (59/97) der Patienten, die 4-6 Zyklen von ACT erhielt, wurden als Gruppe 1 aufgezeichnet, und die restlichen 39% (38/97) wurden als Gruppe 2. 3 Follow-up aufgenommen Alle Patienten wurden alle 3 Monate für die ersten 3 Jahre nach Abschluss der Behandlung und alle 6 Monate für drei weitere Jahre danach beurteilt. Follow-up-Untersuchungen, einschließlich Anamnese und körperliche Untersuchung, Blutbild, Serumchemie, Ultraschall der Leber, und eine Röntgen-Thorax, wurden routinemäßig durchgeführt, entweder durch den behandelnden Onkologe oder dem Chirurgen bei jeder Nachsorgeuntersuchung. CT-Scans der Brust und Bauch und oberen Endoskopie Verdauungstrakt wurden alle 6 Monate routinemäßig durchgeführt. CT-Scans der Brust, CT-Scans oder Sonographie des Abdomens und des Beckens, Endoskopie des oberen Magen-Darm-Trakt, und /oder Positronen-Emissions-Tomographie (PET) wurden durchgeführt, sofort, wenn Symptom der Krankheit aufgetreten oder erhöhter Tumormarker Ebenen nachgewiesen. 4 Unerwünschte Wirkungen Auswertung Akute und späten Toxizitäten wurden nach CTCAE 3,0 benotet und der Radiation Therapy Oncology Group /Europäische Organisation für Forschung und Behandlung von Krebs (RTOG /EORTC) Kriterien [18], [19]. Am späten Toxizitäten wurden als Symptome definiert ersten auftretenden oder dauerhafte > 90 Tage nach dem Beginn der RT. Aufgrund der Schwierigkeiten, die zugrunde liegenden Toxizitäten von der Operation, CRT oder ACT bei der Differenzierung, wurden zusammen berichtet diese Toxizitäten. Die Seiten von Rezidiven als Lokalrezidiv eingestuft wurden, wenn ein Tumor wurde in der Strahlung CTV Volumen (chirurgische Anastomose, Rest Magen oder Magen-Bett und einige regionale Lymphknoten), als regionale erkannt, wenn ein Tumor in der Bauchhöhle (einschließlich anderer intra-abdominalen Lymphknoten und das Peritoneum) erkannt wurde, und als entfernten wenn die Metastasen außerhalb der Bauchhöhle und der Leber waren. Alle Patienten wurden in die Analyse der toxischen Wirkungen Überlebensrate enthalten. Die Intervalle, bis ein lokales Rezidiv, regionale Karzinomatose und Fernmetastasen wurden aus dem Abschluss der Operation zur dokumentierten Therapieversagen gemessen. Die Gesamtüberlebensdauer wurde leben von der Operation Fertigstellung bis zum Tod oder zum Zeitpunkt der letzten Nachuntersuchung berechnet noch für die Patienten. Die Kaplan-Meier-Methode [20] wurde verwendet, um die DFS, OS und lokale Kontrollraten zu schätzen. Die Assoziation zwischen jedem der potentiellen prognostischen Faktoren und der geschätzten lokalen Kontrollrate, DFS oder OS wurde mit dem Log-Rank-Test [21] getestet. Multivariate Analyse wurde das Cox-Regressionsmodell durchgeführt [22]. Alle statistischen Analysen wurden mit SPSS 13.0 Software. Innerhalb der Patientengruppe hatte 51 zuvor unterzogen Standard D2 Dissektion (Entfernung aller eingedrungen N2 [15] Lymphknoten) und die Rest hatte D1 Dissektionen (Entfernung aller eingedrungen N1 [15] Lymphknoten) unterzogen. Die mittlere Anzahl der entfernten Lymphknoten war 16. Positive Lymphknoten-Verhältnis (positive Lymphknoten /Gesamt Lymphknoten entfernt) zwischen jedem Patienten-Untergruppe ausgewogen war, und das mittlere positive Lymphknoten-Verhältnis in Gruppe1 und group2 waren 0,36 (0-1) und 0,33 (0-0,96), die jeweils. Die medianen Follow-up-Zeit für alle Patienten betrug 44 Monate (Bereich: 10-99 Monate). Von den 97 Patienten, 93 (95,9%) beendeten die gesamte Strahlentherapie ohne Unterbrechung, während 4 Patienten nicht die Strahlentherapie aufgrund der akuten Toxizität (Erbrechen) abzuschließen. Siebenundsiebzig Patienten abgeschlossen gleichzeitige Chemotherapie. Unter den 20 Patienten, die keine gleichzeitige Chemotherapie abgeschlossen haben, Therapie wurde in 5 wegen der akuten Toxizität abgesetzt, und die anderen weigerten gleichzeitige Chemotherapie zu unterziehen, weil die Angst vor negativen Auswirkungen. Die detaillierte Anordnung war wie folgt: RT allein, 2; RT und CT, 18; gleichzeitige RTCT und CT, 41; und CRT, 36. 1 Behandlungsergebnisse Die 3-Jahres lokale Kontrolle, DFS und OS waren 90%, 58% und 62%, bzw. (Abbildung 2). Forty-One-Patienten (42%) hatten Rezidiv (19 in Gruppe 1 und 22 in Gruppe 2) und 40 Patienten (41%) starben (18 in Gruppe 1 und 22 in Gruppe 2). Lokalrezidiv bei 5 Patienten (4%) in der CRT (CRT + ACT) Gruppe entwickelt. Insgesamt 14 Patienten hatten Fernmetastasen, 9 von ihnen hatten < 4 und 5, von denen ≥4 Zyklen von ACT hatte. Darüber hinaus, 15 und 12 Patienten regionalen Peritoneum Karzinomatose in der CRT und CRT + ACT-Gruppen, die jeweils entwickelt. Die 3-Jahres-Gesamtüberlebenszeit und krankheitsfreie Überleben waren 69,5% und 66,5% für die Gruppe 1 und 50% und 45,5% für die Gruppe 2 (p = 0,024 und p = 0,005). Die lokalen Kontrollraten waren 94% und 89% für die Gruppen 1 und 2 (p = 0,24) (Abbildung 3). Die Auswirkungen von Alter, Geschlecht, Krankheits T- und N-Kategorien, positive Lymphknoten-Verhältnis, Vollständigkeit der Operation, lymphovascular Invasion und ACT auf lokale Steuerung, Peritonealkarzinose, Fernmetastasen, DFS und OS wurden durch univariate und multivariate Analysen ausgewertet (Tabellen 2 und 3). Patientengewichtsverlust wurde in den symmetrischen Faktoren nicht berücksichtigt, da diese Studie retrospektiv und Gewichtsverlust war, konnte von vielen Faktoren ab, wie zum Beispiel Ernährung zu unterstützen und Erholungszustand von der Operation beeinflusst werden. Für Patienten unter Ernährungsrisiko, empfohlen wir Ernährung zu unterstützen. Multivariate Analyse ergab, dass die Anzahl der Zyklen von ACT (4-6 vs 0-3) und lymphovascular Invasion waren unabhängige prognostische Faktoren für DFS (p = 0,010 und p = 0,003), während Peritonealdialyse Metastasen ein unabhängiger prognostischer Faktor für OS war ( p <. 0,01) 3 Unerwünschte Wirkungen Die Toxizität, die unter den 97 Patienten beobachtet wurde, ist in Tabelle 4 Die wichtigsten toxischen Wirkungen waren hämatologische und gastrointestinale zusammengefasst. Die häufigste hämatologische toxische Wirkung war Leukopenie, die bei 30 Patienten (31%) entwickelt, während schwere Thrombozytopenie ungewöhnlich war (2%). Ein Patient (1%) starben durch eine adjuvante Chemotherapie-induzierten Leberversagen sowie febrile Neutropenie, und ein anderer Patient erlitt anastomotic Stoma Ödem 3 Monaten nach Abschluss der Radiochemotherapie. Strahleninduzierte Grad 3 oder höher akuten Verdauungs toxischen Wirkungen wie Übelkeit /Erbrechen, Dyspepsie, Diarrhöe und wurden bei 23 Patienten (23%) beobachtet. Gastrectomy-induzierte Komplikationen, wie Anastomose Fistel, Pankreasnekrose oder Wunddehiszenz, wurden nicht beobachtet. Die Behandlungsergebnisse, wie durch die DFS und OS bleiben düster für Patienten mit erweiterte Adenokarzinom des Magens. Komplette Tumorresektion mit ausreichender Lympknotendissektion ist der wichtigste Faktor für die Seuchenbekämpfung und langfristige Überleben von Patienten mit Magenkrebs. Die Clearance von lokoregionaler Erkrankung mit der Operation allein (auch D2) für die meisten Patienten nicht ausreichend ist, mit lokal Adenokarzinom des Magens fortgeschritten, und adjuvanten Behandlung ist zwingend notwendig für die weitere Tumorkontrolle zu erhöhen und die Behandlungsergebnisse zu verbessern. Verschiedene Strategien, einschließlich neoadjuvante und /oder ACT, Strahlentherapie, und deren Kombination wurden in einem Versuch untersucht die Behandlungsergebnisse zu verbessern. Lokoregionale Steuerung wurde verbessert als Strahlentherapie für Magenkrebs eine der Behandlungsmethoden geworden ist, [23] und sogar DFS und OS wurden in einer INT 0116 Studie und deren Update-Bericht mit gleichzeitiger postoperativen CRT [11], [24] erhöht. Allerdings sind nur 10% der Patienten in dieser Studie unterzog D2 Resektion, und es war unklar, ob die postoperativen CRT einfach für die ungenügende Resektion kompensiert. Zwei aktuelle Studien in Korea berichtet, dass eine adjuvante CRT nach D2 Gastrektomie deutlich die Behandlungsergebnisse bei Patienten mit nicht-metastasiertem Adenokarzinom des Magens verbessert [25], [26]. Daher ist die postoperative gleichzeitige CRT eine wirksame Behandlung für lokoregionaler fortgeschrittenem Magenkrebs. Doch in der INT 0116-Studie fand sich postoperativen CRT nicht signifikant regionalen Rezidiv oder Fern Schübe zu verringern. In der Tat, 72% der Befragten in der Chirurgie-only-Gruppe und 65% der Befragten in der Radiochemotherapie-Gruppe hatte regionalen Rückfall, und 18% der Befragten in der Chirurgie-only-Gruppe und 33% der Befragten in der Radiochemotherapie-Gruppe hatte fernen Rückfall. Die Wirksamkeit von neoadjuvante und ACT mit Epirubicin-basierten Regime wurde in der MAGIC-Studie [12] berichtet. Die Gesamtüberlebensrate betrug 36,3% und 23,0% bei Patienten mit oder ohne postoperative Chemotherapie behandelt sind. Diese Studien und die Häufigkeit der Wiederholung nach der Resektion von Magenkrebs hat uns ermutigt, die Kombination von CRT und Adjuvans Epirubicin-basierte Chemotherapie bei Patienten mit einem Adenokarzinom des Magens oder gastroösophagealen Übergang zu studieren. In der vorliegenden Studie wurde bei Patienten mit lokal fortgeschrittenem Magenkrebs (definiert als Stufe T3, T4, oder N +) wurden mit Gastrektomie gefolgt von CRT und ACT behandelt. Diese Therapien im Wesentlichen das Behandlungsergebnis verbessert, einschließlich Tumorkontrolle und Gesamtüberlebensraten. Die 3-Jahres Peritoneum Metastasierung Kontrolle und Gesamtüberlebensrate betrug 52% gegenüber 50% (p = 0,023) und 77% vs. 69,5% (p = 0,024) bei Patienten mit weniger ACT vs. mehr ACT sind. Die 3-Jahres-lokale Steuersätze für die CRT + ACT und CRT nur Gruppen waren 94% und 89% (p = 0,240), respectively. Somit sind unsere Ergebnisse mit denen früherer Studien vergleichbar. Die kürzlich berichtet Multizenterstudie der Trans-Tasman Radiation Oncology Group (TROG) [27], die eine adjuvante Therapie-Schema eines Zyklus von ECF bestehend enthalten gefolgt, angezeigt durch Strahlentherapie mit gleichzeitiger Infusion von 5-FU und dann zwei weitere Zyklen von ECF, dass die adjuvante Therapie mit ECF vor und nach der dreidimensionalen konformen Chemoradiatio machbar ist und in einer kooperativen Gruppeneinstellung sicher geliefert werden kann. Wir fanden, dass zusätzliche 4-6 Zyklen von ACT in adjuvante Chemotherapie /Strahlentherapie wurde eine signifikante prognostischer Faktor für Peritonealdialyse und Fernsteuerungs- und Gesamtüberlebenszeit und erhöht sich nicht signifikant die Häufigkeit von Langzeitkomplikationen. Nach bestem Wissen und Gewissen, unseren Bericht ist die einzige Analyse dieser Art von Behandlungsstrategie. Unsere Ergebnisse zeigten eine geringere Toxizität Raten, eine ähnliche Behandlung Compliance und höhere Gesamtüberlebenszeit im Vergleich zu denen in der TROG Studie. Die Radiochemotherapie Regime in unserer Studie verwendet wurde im Allgemeinen gut vertragen, wobei 61% der Patienten (im Vergleich zu 67% in der TROG Studie) alle Kurse der Behandlung abgeschlossen (CRT + 4-6 Zyklen von ACT) und nur 9% (6% in der TROG) von Patienten, die keine gleichzeitige CRT abgeschlossen werden, da von behandlungsbedingter Toxizität. Die hämatologische und gastrointestinale (GI) Toxizität Raten waren auch ähnlich denen in der TROG Studie. Trotzdem waren die 3-Jahres-Gesamtüberlebenszeit und krankheitsfreie Überleben höher als die in der TROG Studie (61% und 70% gegenüber 58,6% und 61,6%, respectively), die aufgrund gründlichere Behandlung chirurgische sein kann und mehr Zyklen der Chemotherapie. In unserer Studie 53 Patienten (52%) hatten zuvor formal D2 Dissektion und D1 Dissektion (Entfernung aller eingedrungen N1 Lymphknoten) unterzogen hatten in den Rest (48%) durchgeführt wurde, während in der TROG Studie, 20% unterzogen weniger als ein Lympknotendissektion D1. Darüber hinaus enthalten unsere Studie mehr Zyklen von ACT als die TROG Studie. Die Phase-III-Studie von Künstler [28] im Vergleich der postoperativen Behandlung mit Capecitabin plus Cisplatin (XP) im Vergleich zu XP plus Strahlentherapie mit Capecitabin (XP /XRT /XP); In dieser Studie haben reduzieren die Zugabe von XRT Chemotherapie XP nicht signifikant Rezidiv nach kurativer Resektion und Lymphadenektomie D2 Lymphe bei Magenkrebs. In einer Subgruppenanalyse der Patienten mit positiven pathologischen Lymphknoten, gab es einen statistisch signifikanten Anstieg der DFS in der XP /XRT /XP Arm (geschätzte 3-Jahres-DFS-Rate von 77,5%) im Vergleich zu dem XP-alone-Arm (3- Jahr DFS, 72,3%; P = 0,0365). In dieser Studie wurden 60% der Patienten statt Ib oder II, und relativ frühen Stadium Patienten haben eine bessere Prognose und kann nicht so viel von einer adjuvanten Behandlung profitieren. Dies kann auch der erhöhte DFS in dieser Studie erklären, im Vergleich zu dem in der vorliegenden Studie. Ein Französisch retrospektiven Studie [29] zu dem Schluss, dass die postoperative Cisplatin-basierte Chemotherapie gefolgt von einer konforme Strahlentherapie mit gleichzeitiger 5-FU war machbar. Die Gesamt-und krankheitsfreie Überlebensrate waren vergleichbar mit denen, die zuvor in der Literatur berichtet, mit guten lokalen und regionalen Seuchenbekämpfung. Trotz verstärkten Einsatz der postoperativen Chemotherapie mit Cisplatin, fern und Peritonealdialyse Rezidive bleiben die am häufigsten Schübe beobachtet. Die Französisch FNCLCC (Federation Nationale des Centres de Lutte Contre le Cancer) ACCORD07-FFCD 9703 randomisierten Studie [30] berichtet dass die präoperative 5-FU und Cisplatin-Chemotherapie bei Patienten mit resektablen Adenokarzinom des Magens und der unteren Speiseröhre deutlich verbessert 5-Jahres-Gesamt-und krankheitsfreie Überleben im Vergleich mit der Operation allein: 38% vs. 24% und 34% gegenüber 21% bzw. . Die CLASSIC-Studie [31] zeigten, dass eine adjuvante Chemotherapie mit Capecitabin plus Oxaliplatin (8 Zyklen) nach D2 Gastrektomie mit der Operation allein deutlich 3-Jahres krankheitsfreie Überleben auf 74% von 59,0% verbessert. Die laufende US-Inter Studie (CALGB 80101) ist eine randomisierte Phase-III-Studie mit einem ECF-basierten Regime, das dem in der TROG Studie verwendeten ähnlich ist. Die Patienten in der Studie Inter erhalten auch einen Zyklus von ECF vor Chemoradiatio und zwei Zyklen nach Radiochemotherapie. Jedoch aufgrund der hohen Rate der akuten Toxizität (wie in der TROG Studie berichtet), die Arzneimitteldosen sind in den postradiotherapy Zyklen reduziert. Wir haben eine Chemotherapie mit einer geringeren Toxizität (EOF oder EOX) für die meisten Patienten, diese Therapien ermöglichen, besser verträglich zu sein. Die Dutch /Schwedische Studie (Randomisierte Phase-III-Studie zur adjuvanten Chemotherapie oder Radiochemotherapie in resektablen Magenkrebs (KRITIKER) studieren; ClinicalTrials.gov ID NCT00407186) vergleicht drei postoperativen Kurse von Epirubicin, Cisplatin und Capecitabin-Chemotherapie gegen Chemoradiotherapie mit Capecitabin und Cisplatin bei Patienten mit Magenkrebs behandelt mit drei präoperativen Kurse von Epirubicin, Cisplatin und Capecitabin-Chemotherapie durch eine Operation mit D2 Lymphadenektomie ohne Splenektomie und Pankreatektomie. Eine Phase-III-Studie (ARTIST-II) Chemotherapie im Vergleich zu einer Chemotherapie mit RT bei Patienten mit D2 Lymphknotendissektion und pathologischen Lymphknoten-positive Krankheit zu vergleichen ist geplant, um die Vorteile der adjuvanten CRT zu bestätigen. Die TOPGEAR Studie ist untersuchen, ob die Zugabe von Chemoradiotherapie mit einer Chemotherapie ist in der neoadjuvant Einstellung zur Chemotherapie allein überlegen durch die anfängliche pathologische komplette Remission (pCR) Raten sowie nachfolgende Gesamtüberlebenszeit bei Patienten mit ausreichend Chirurgie (D1 Dissektion) für resektablen Magenkrebs zu verbessern. Einige wichtige Fragen bleiben. Erstens, weil unsere Studie eine retrospektive Studie, die Zahl der Patienten war für eine ausreichende statistische Aussagekraft gefordert wurde nicht bestimmt. Allgemeiner gesagt, wie die Rolle der neoadjuvanten und ACT in der Behandlung des fortgeschrittenen Magenkrebs klar wird, ob die Zugabe der präoperativen Chemotherapie weiterhin die Behandlungsergebnisse verbessern kann, muss bestimmt werden. Darüber hinaus ist es unklar, ob die präoperative Radiochemotherapie und postoperativen Chemotherapie unserer Methode in Bezug auf das Behandlungsergebnis und Toleranz überlegen ist. In unserer Studie beobachteten die Haupt Wiederholung war Peritoneum Metastasierung, die ergab, dass die weitere Behandlung regionalen Wiederholung zu reduzieren erforderlich war. Drittens, wenn ein Epirubicin-basierte Chemotherapie in der adjuvanten Radiochemotherapie Behandlung am effektivsten ist, Einsicht vom Künstler-Studie [28] über die Wahl der postoperativen adjuvanten Chemotherapie kann dazu beitragen, die Toxizität Rate zu senken. Schließlich ergab, multivariate Analyse, die in regionalen oder auf der Fernbedienung oder die Gesamtüberlebensraten in Bezug auf die verschiedenen prognostischen Faktoren wurden keine signifikanten Unterschiede; Jedoch zeigte die krankheitsfreie Überleben signifikante Unterschiede in der regionalen oder auf der Fernbedienung und die allgemeine Überlebensrate in Bezug auf die prognostische Faktoren, wie sie in der Log-Rank-Test bewertet. Zukünftige Studien sollten diese Fragen zu lösen wollen. Die Entwicklung einer optimalen adjuvanten Radiochemotherapie Strategie für lokal fortgeschrittenem Adenokarzinom des Magens wäre ein großer Erfolg auf dem Gebiet sein, und gemeinsame Anstrengungen zwischen den Institutionen der Krebsbehandlung sind die beste Strategie, um dieses Ziel zu erreichen. Gastrectomy mit Lymphadenektomie und CRT von ACT gefolgt ist möglich und erträglich für die Behandlung von lokal fortgeschrittenem Magenkrebs. Die Zugabe von ausreichend ACT zur postoperativen CRT deutlich verbessert 3-Jahres-Bauch Karzinomatose Kontrolle und die 3-Jahres-Gesamtüberlebensrate. Im Vergleich zum 5-FU-basierten CRT-Strategie, diese neuartige CRT-Therapie mit einer erhöhten ACT-Therapie in einer adjuvanten Therapie verwendet wird, sollte weiter in prospektiven Studien optimiert und untersucht werden, um festzustellen, ob sie weiter die endgültige Behandlungsergebnis zu verbessern.
Methoden und Materialien
2.2 Strahlentherapie.
5 Statistische Analyse
Ergebnisse |
2 Prognosefaktoren
Diskussion
Schlussfolgerungen
 Natürliche Heilmittel für Hypochlorhydrie und Achlorhydrie
Natürliche Heilmittel für Hypochlorhydrie und Achlorhydrie
 Was ist der Unterschied zwischen Fluoroskopie und Radiographie?
Was ist der Unterschied zwischen Fluoroskopie und Radiographie?
 Der traurige Zustand der amerikanischen Medizin:Warum Patienten und Ärzte leiden (und wie wir es beheben können)
Der traurige Zustand der amerikanischen Medizin:Warum Patienten und Ärzte leiden (und wie wir es beheben können)
 Sakralnervenstimulation bei Stuhlinkontinenz
Sakralnervenstimulation bei Stuhlinkontinenz
 7 Sibo-freundliche Rezepte für den Sommer
7 Sibo-freundliche Rezepte für den Sommer
 Symptome einer akuten Gastrektasie - Diagnose eines akuten Abdomens
Symptome einer akuten Gastrektasie - Diagnose eines akuten Abdomens
 Was führt dazu, dass eine Person einen Kolostomiebeutel trägt?
Was ist eine Kolostomie? Eine Kolostomie ist ein chirurgischer Eingriff, bei dem eine Öffnung vom Dickdarm durch das Abdomen gemacht wird, wodurch der Stuhl hindurchtreten kann den Bauch, anstatt d
Was führt dazu, dass eine Person einen Kolostomiebeutel trägt?
Was ist eine Kolostomie? Eine Kolostomie ist ein chirurgischer Eingriff, bei dem eine Öffnung vom Dickdarm durch das Abdomen gemacht wird, wodurch der Stuhl hindurchtreten kann den Bauch, anstatt d
 Wissenschaftler extrahieren komplettes menschliches Genom aus einem Jahrtausende alten „Kaugummi“
Kaugummi kauen scheint kein neuer Trend zu sein! Forscher haben einen Kaugummi mit 5 gefunden, 700 Jahre alt und hat Hinweise auf alte DNA geliefert. Eine Studie mit den Ergebnissen wurde in der Zeits
Wissenschaftler extrahieren komplettes menschliches Genom aus einem Jahrtausende alten „Kaugummi“
Kaugummi kauen scheint kein neuer Trend zu sein! Forscher haben einen Kaugummi mit 5 gefunden, 700 Jahre alt und hat Hinweise auf alte DNA geliefert. Eine Studie mit den Ergebnissen wurde in der Zeits
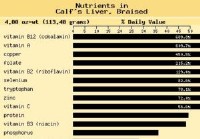 SCD-Rezept:Zitronen-Pfeffer-Lebersteak
In den letzten paar Monaten habe ich mich mehr für Organfleisch interessiert. Ich möchte mich im Laufe der Zeit auf die Qualität meiner Lebensmittel verlassen können, um alle Vitamine und Mineralstoff
SCD-Rezept:Zitronen-Pfeffer-Lebersteak
In den letzten paar Monaten habe ich mich mehr für Organfleisch interessiert. Ich möchte mich im Laufe der Zeit auf die Qualität meiner Lebensmittel verlassen können, um alle Vitamine und Mineralstoff