Sažetak pregled
Peptički ulkus je jedan od najčešćih probavnih poremećaja sa složenim etiologije. Nedavno smo proveli genoma široku studiju udruge za čir na dvanaestercu i identificirati promjene osjetljivosti bolesti u dva genetskog lokusa odgovara prostate matičnih stanica antigena Izvor. Tanikawa C, Matsuo K, Kubo M, Takahashi A, Ito H, Tanaka H, et al. (2013) Utjecaj PSCA Urednik: Giuseppe Novelli, Tor Vergata Sveučilište u Rim, Italija pregled Primljeno: 12. studenog 2012; Prihvaćeno: 7. travnja 2013; Objavljeno: 21. svibanj 2013 pregled Copyright: © 2013 Tanikawa et al. Ovo je otvorenog pristupa članak distribuirati pod uvjetima Creative Commons Imenovanje License, koja omogućuje neograničeno korištenje, distribuciju i reprodukciju u bilo kojem mediju, pod uvjetom da je izvorni autor i izvor su zaslužan financiranja. Aichi dio studije je podržan od strane grant-in-pomoći iz Ministarstva obrazovanja, kulture, športa, znanosti i tehnologije Japana [prioritetnih područja raka (br 17015018) i inovativnih područja (br 221S0001)] i od Ministarstva zdravstva, socijalne skrbi i Labours Japana [H24-3-G002 i H23-aplikacija (raka) -G002]. U financijeri nisu imali ulogu u studiju dizajna, prikupljanja i analize podataka, Odluka o objavi, ili pripremu rukopisa pregled U konkurenciji interese.. Autori su izjavili da ne postoje suprotstavljeni interesi pregled Uvod pregled peptički ulkus je najčešća bolest u gastrointestinalnom traktu sa simptomima mučnina, povraćanje i bol u trbuhu, a ponekad uzrokuje krvarenje i perforacija akutne peritonitisa. Životni vijek prevalencija peptički ulkus je 10-15% u japanskom, a 4-10% u bijelaca [1] - [3]. Oko 70% pacijenata želuca i 90% bolesnika na dvanaesniku su povezani s H. pylori pregled infekcija [4]. Od iskorjenjivanje H. pylori pregled antibioticima u kombinaciji s inhibitorom protonske pompe može učinkovito liječiti peptički ulkus [5], H. pylori pregled se pokazuje da je glavni uzrok peptički ulkus. Iako je gotovo 50% osoba na zemlji su zaražene s H. pylori, pregled, većina njih ostati bez simptoma ukazuje na to da je ishod bolesti nakon H. pylori pregled infekcija značajno varira među pojedincima. Ti me vlastite raznolikosti pod utjecajem različitih čimbenika, uključujući bakterije podvrste, odgovor domaćina i njihovih interakcija. na dvanaesniku promicanje gena pregled ( dupa pregled) u H. pylori pregled je navedeno da inducira interleukin (IL) -8 koja povećava rizik od duodenuma i smanjuje rizik od raka želuca [6], [7]. Nesteroidni protuupalni lijekovi (NSAR) i pušenje su poznati čimbenici rizika za peptički ulkus [8], [9]. Osim ovih bakterijskih i okolišnih čimbenika, domaćini genetski faktori su bili uključeni da ima neke uloge u opasnosti od peptički ulkus. Vrpca-mudar podudarnost stopa peptičkog ulkusa na jednojajčane blizance je kao visok kao 23,6% dok je u dizygotic blizanaca bila je 14,8%. Nekoliko pristupa gena kandidata otkrio moguću povezanost genetskih varijacija u IL-6 pregled, IL-8 pregled, IL-10 Netlogu [10], TNF U našem prethodnom genoma studije širom udruge (GWAS) ulkusa dvanaesnika pomoću ukupno 7,035 predmeta i 25,323 kontrole, utvrdili smo značajnu povezanost genetskih varijacija na PSCA pregled ( prostata antigena matičnih stanica pregled) i ABO pregled krvne grupe sa duodenum ulkus [13]. C alel od rs2294008 na PSCA pregled povećava rizik od čira dvanaesnika (omjer izgleda (OR) od 1,84 s P pregled vrijednost 3,92 × 10 -33) u recesivnim modelom , dok je smanjen rizik raka želuca (OR 0,79 s P pregled vrijednost 6,79 × 10 -12) kao što je prethodno opisano [14]. Naši funkcionalna analiza pokazala je da je T alel od SNP rs2294008 stvara uzvodnog pravocrtnu inicijacijski kodon i dodati signalni peptid sekvence na N-terminalnom dijelu, što rezultira promjenom protein podstanično lokaliziranje iz citoplazme u staničnoj površini. SNP rs505922 na ABO pregled je također bio povezan s čir na dvanaestercu u recesivnim modelom (OR 1,32 s P pregled vrijednost 1,15 × 10 -10). Budući da H. pylori pregled, infekcija i nesteroidni protuupalni lijekovi induciraju gastroduodenalnog sluznice ozljede koje bi ga moglo duodenalna i želuca, ispitali smo ulogu varijanti u PSCA pregled i ABO Rezultati ukupno 4,291 slučajeva čira na želucu i 22,665 kontrole bez prošlost povijesti duodenalni ulkus ili kontinuirano uzimanje NSAR su regrutirani iz BioBank Japana i Aichi Cancer Center (Tablica 1). Zatim smo genotipiziran SNP rs2294008 i rs505922 u dva slučaja kontrolni uzorak postavlja i ispituje povezanost s želučanog čira u tri genetskih modela (aditiva, recesivna i dominantna modela) (Tablica 2). Za povećanje statističku snagu ovog istraživanja, koristili smo subjekata s bilo kojim od 22 bolesti kao kontrolnih uzoraka. Stoga smo ocijenili zapanjujuće učinak kontrolnih uzoraka miksa bolesti koji se koriste u ovoj analizi. SNP-ovima rs2294008 i rs505922 nije pokazala značajnu povezanost između kontrole slučaj-mix (n = 19,884) i zdravih ispitanika (n = 2,781) (Tablica S1). Osim toga, oba SNP nije pokazao značajno odstupanje od HWE (Hardy-Weinberg ravnoteže) u svakoj skupini bolesti. Stoga kontrole mix bolest čini se da nije uvelike utjecati na rezultat pridruživanja naše analize. Pregled rezultati zajedno analiza pokazala da bolesnici želučani čir imali veću učestalost C alel na rs2294008 nego u kontrolnoj grupi u oba (39,7 % u odnosu na 36,9% i 40,1% vs 37,0%, respektivno). Meta-analiza dviju studija je pokazala značajnu povezanost rs2294008 u modelu aditiva bez dokaza o heterogenosti (p = 5,85 × 10 -7 s OR 1,13), iako je udruga nije bila statistički značajna između Aichi raka Centar kohorta vjerojatno zbog manje veličine uzorka. aleli rizik (C alela na rs2294008) u dva uzorka seta bili su u skladu između čir na dvanaestercu i čira na želucu, što ukazuje na ulogu PSCA pregled varijacije kao zajedničkih genetskih faktora za peptički ulkus. Međutim utjecaj ove varijacije na rizik želučanog ulkusa nije bila tako jaka kao i one na čir na dvanaestercu ranije izvijestili [13]. Pregled S druge ruke, SNP rs505922 pokazali nedosljedne rezultate između dvije skupine. AT alel rs505922 povećan želučane rizik čira na sva tri genetskih modela u BioBank Japanu skupini. Međutim, želuca pacijenti imaju nižu frekvenciju (53,5%) T alela nego zdravih ispitanika (55,1%) u Aichi Cancer Center skupini. Prema tome, daljnja analiza asocijacija bitno je odrediti ulogu Abo pregled, varijacija na želučani ulkus osjetljivosti. Budući da imamo genotipizacija rezultate 1.862 slučajeva čira na želucu i 17,482 kontrola analiziranim Illumina ljudskim Hap610- Quad genechip, proveli smo cijeli genom screening pomoću ovih primjera set. Iako je 62 SNP izlagao sugestivne povezanost s P Također smo istražili povezanost prethodno prijavljenih gena s čira na želucu (tablica 3). Odabrali smo 32 SNP-ova u pet gena lokusa koji su genotipiziran strane Illumina Human Hap610-Quad genechip. Kao rezultat toga, dva lokusa na LTA pregled i PTGS1 pregled pokazuje sugestivan udruge (p = 1,64 × 10 3 i 0,0376), iako te udruge nisu bile statistički značajne nakon Bonferronijev je korekcija ( P izvoznici < 0,00156 = 0,05 /32). Tako daljnje analize su potrebne kako bi se razjasnila uloga tih varijacija na želučani ulkus. Pregled Rasprava pregled Razvoj čira na želucu određuje se interakcije između lučenja želučane kiseline i mukozne otpora, međutim njihov podređeni patogeneza još nije u potpunosti razjašnjen. Želuca sluzi, želatinozni materijal izlučuju želuca mukoznih stanica, služi kao neuskomiješan sloj kroz koji se smanjuje širenje kiseline i pepsina. Mi smo ovdje otkrili da varijacije u PSCA H. pylori pregled igra važnu ulogu u razvoju gastritisa, peptičkog ulkusa i raka želuca i iskorjenjivanje H. pylori pregled je pokazala da smanjuju ponavljanje želučanog čira [26] i spriječiti pojavu raka želuca [27]. Budući da vertikalni prijenos u djetinjstvu je glavni izvor zaraze, obiteljska povijest H. pylori Ovdje smo otkrili da je PSCA pregled varijanta bila je statistički značajno povezana s čira na želucu. U našoj prethodnoj analizi, PSCA varijacija ne povezujemo s H. pylori pregled prevalencija [13]. Budući da H. pylori pregled infekcija je povezana s mnogim bolestima kao što su MALT limfom [34], idiopatski purpura trombocitopenijom [35], atrofični gastritis [36], i NSAID inducirani želučani ulkus, to je vrlo zanimljivo procijeniti učinak PSCA Metode Izjava Etika pregled Ovaj istraživački projekt je odobren od etičkih povjerenstava na Sveučilištu u Tokiju, Riken i Aichi Cancer Center. Svi sudionici pod uvjetom pismeni informirani pristanak uz odobrenje etičkih povjerenstava Sveučilišta u Tokiju i Aichi Cancer Center. Pregled Sudionici istraživanja Demografske detalji sudionika studije sažeti su u tablici 1. ukupne od 3,866 pacijenata želuca i čira na želucu 20,791 negativnim kontrolama dobivene su iz BioBank Japana koji je pokrenut 2003. godine s vlastitim sredstvima iz Ministarstva obrazovanja, kulture, športa, znanosti i tehnologije, Japanu [37]. U BioBank Japanu Projekta, DNA i serumu bolesnika s 47 bolesti prikupljeni su kroz suradnju mrežu od 66 bolnica diljem Japana. Popis bolnica koje sudjeluju prikazan je na sljedećoj internetskoj stranici (http://biobankjp.org/plan/member_hospital.html~~HEAD=pobj). Ukupno 425 slučajeva čira na želucu i 1.874 zdravih osoba dobiveni su iz Aichi Cancer Center. Dijagnoza čira na želucu temelji se na kliničkim, endoskopskih i histološke značajke. Popis kontrolnih uzoraka bolesti mix korištena u ovom ispitivanju je prikazan u tablici S1. Mi smo isključeni bolesnici s duodenalni ulkus ili raka želuca od oba slučaja i kontrole. Deregulacija PSCA zabilježeno je u mnogim vrstama, kao što su maligne bolesti prostate, gušterače, pluća, mjehura, želuca, holangiokarcinomom i rak jednjaka [14] - [16], [20], [38], [39]. Osim toga, ABO pregled locus ranije pokazalo da je povezan s raznim bolestima, kao što su infarkt miokarda i karcinoma gušterače [40], [41]. Stoga smo izostavili osobe s ove bolesti od kontrole slučaj mix. Također smo isključeni ispitanici s kontinuiranim unosom NSAID. Pregled SNP genotipa pregled genotipizacija platforme koje se koriste u ovoj studiji prikazani su u tablici 1. Ukupno 1.862 slučajeva čira na želucu i 20.791 čira na želucu uzorku negativne kontrole genotipizirane s Illumina ljudskim Hap610-Quad ili ljudskim Hap550v3. Ostali uzorci genotipizirane od Invader sustav za testiranje (treći val Technologies, Madison, WI) ili Taqman analize. Pregled Statistička analiza pregled Udruga SNP-a rs2294008 i rs505922 s čira na želucu, a testirana je hi-kvadrat test. omjeri su izgledi izračunata s obzirom na zaštitnu alel kao referentnu alela. Udruga SNP genotipiziran strane Illumina Human Hap610-Quad s čira na želucu, a testirana je multivarijatne logističke regresijske analize po prilagodbe za dob zapošljavanje i spolu koristeći plink [42]. Heterogenost preko dvije faze ispitana je Cochran Q test [43]. Pregled popratne podatke Izvori pregled Želimo zahvaliti svim pacijentima i članovima Rotary kluba Osaka-Midosuji Distrikta 2660 Rotary International u Japanu, koji je donirao svoju DNK za ovaj posao. Također zahvaljujemo Ayako Matsui i Hiroe Tagaya (University of Tokyo), a tehničko osoblje Laboratorija za genotipizacija razvoj, Centar za genomske medicine, Riken za njihovu tehničku podršku. Pregled
( PSCA
) gena i ABO krv grupe pregled ( ABO pregled) gena. Ovdje smo istražili povezanost tih varijacija s čira na želucu u dva japanska case-control uzoraka setova, ukupno 4,291 slučajeva čira na želucu i 22,665 kontrola. Kao rezultat toga, C-alel rs2294008 na PSCA pregled povećava rizik od želučanog ulkusa s omjer vjerojatnosti (OR) 1.13 ( P pregled vrijednost 5,85 × 10 -7 ) u modelu aditiva. S druge strane, SNP rs505922 na ABO
izlagao nedosljedne rezultat između dvije skupine. Naš pronalazak podrazumijeva prisutnost zajedničke genetske varijante u patogenezi želuca i dvanaesnika pregled
Varijacija na čira na želucu podložnost. PLoS ONE 8 (5): e63698. doi: 10,1371 /journal.pone.0063698 pregled
, LTA pregled [11], i cox1 pregled [12] s peptički ulkus rizika. pregled
gena na želučani ulkus rizik među japanske populacije. pregled
vrijednosti manje od 1 × 10 -4, ne SNP izbrisani genom širok značajan prag (Tablica S2 i na slici S1). Dakle, naš skup uzoraka nisu imali dovoljno statističku snagu za otkrivanje želučani ulkus osjetljivosti lokusa po GWAS. Pregled
gena značajno je povezan s čira na želucu. PSCA Najprije je identificirana kao tumorskog antigena koji je visoko izražen u prostate, mjehura, pankreasa i tkiva karcinoma [15], [16]. Budući da tumorske stanice tretirane s anti-PSCA antitijela pokazalo je porast supresijski učinak [17], [18], na površini stanice-PSCA smatra da igra važnu ulogu u proliferaciji stanica. Nasuprot tome, down-regulacija PSCA u želuca i jednjaka, tkiva raka je također zabilježena [19], [20]. Stoga je uloga PSCA u karcinogeneze je još uvijek kontroverzna [21]. Ti različiti učinci PSCA među različitim vrstama raka može se djelomično objasniti utjecajem genetskih varijacija. Osobe koje nose T alel u rs2294008 izraziti PSCA proteine s dodatnim fragment devet aminokiselina na N-terminalnom dijelu [13]. S druge strane, pojedinci koji nose C alel na rs2294008 izražavaju kraći PSCA protein kojemu nedostaje signalni peptid i predviđeni biti lokaliziran u citoplazmi, bez glikozilacije [22]. Također smo otkrili da je u citosolu kraći PSCA protein je više osjetljiv na razgradnju putem proteasoma od dugog PSCA proteina na površini stanice. Budući da su PSCA izvedene peptide izvijestila da se meta T-stanica na temelju imunoterapija za uznapredovali karcinom prostate [23], je kraće PSCA protein će uzrokovati aktivaciju CD4-pozitivne i /ili CD8-pozitivnih T-stanica, a nakon toga promovirati epitela mukozno oštećenje [24]. Nasuprot tome, duga PSCA protein na površini stanice bi se olakšalo sluznice popravak jačanjem epitelnih proliferacije stanica. Osim toga, T alel od SNP rs2294008 pokazalo se da je povezan s većim mRNA i proteina [25]. Tako je utjecaj PSCA o želuca i karcinogeneze može biti regulirana PSCA
varijacija. Pregled
infekcije ili H. pylori pregled povezani s grupom bolesti je faktor rizika za H. pylori pregled infekcija [28] - [30]. Osim toga, nedavno nakupila dokazi otkrila niz faktora rizika od raka želuca (T alela na rs2294008, krvne grupe A, smanjena želučane kiseline, unos inhibitora protonske crpke /H 2 blocker, i CagA
u H. pylori pregled [31]) ili peptički ulkus (C alela na rs2294008, krvna grupa O, NSAID unos, dupa pregled u H. pylori pregled) [32 ]. Osim toga, CYP2C19 pregled genotip povezan s odgovorom na trostruki anti H. pylori
terapiju uključujući inhibitora protonske pumpe [33]. Međutim, naša prethodna analiza pokazala je da SNP rs2294008 i rs505922 nije povezan s H. pylori pregled prevalencija [13]. Uzimajući gore navedene informacije u obzir, procjena rizika od neke bolesti i učinkovitosti lijeka će nam omogućiti da se utvrdilo odgovarajući protokol liječenja za H. pylori pregled nositelji. pregled
varijacije na ove bolesti. Nadamo se da će naši rezultati će pridonijeti rasvjetljavanju patogeneze bolesti, kao i da se uspostavi personaliziranih medicinskih tretmana u budućnosti. Pregled
Slika S1. pregled Manhattan grafički prikaz genoma širom P vrijednosti udruge. U P vrijednosti dobivene su logističke regresijske analize po prilagodbe za dob i spol. Na y-osi predstavlja -log10 P vrijednosti 480,566 SNP, a njihovi kromosomske pozicije su prikazane na osi x pregled doi:. 10,1371 /journal.pone.0063698.s001 pregled (TIF) pregled Tablica S1 , pregled genotip učestalost dva SNP u kontrolama miksa bolesti pregled doi:. 10,1371 /journal.pone.0063698.s002 pregled (docx) pregled Tablica S2. pregled Rezultat analize pridruživanja želučanog čira u GWAS pregled doi:. 10,1371 /journal.pone.0063698.s003 pregled (docx) pregled
 Kako probiotici pomažu da vaša crijeva budu zdrava
Kako probiotici pomažu da vaša crijeva budu zdrava
 7 razloga zašto ste napuhani
7 razloga zašto ste napuhani
 Staceyina priča o uspjehu u propuštanju crijeva (IBS i težina NESTAJU!)
Staceyina priča o uspjehu u propuštanju crijeva (IBS i težina NESTAJU!)
 Mit o kalorijama:knjiga koju ćete pročitati i proslijediti obitelji 2014.
Mit o kalorijama:knjiga koju ćete pročitati i proslijediti obitelji 2014.
 Vaginalne bakterije povezane s preranim rođenjem
Vaginalne bakterije povezane s preranim rođenjem
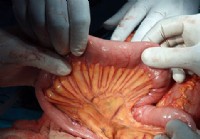 Koje su tri vrste anastomoze?
Koje su tri vrste anastomoze?
 Znanstveni simpozij u LABVOLUTION -u fokusira se na ključna pitanja znanosti o životu
Znanstveni simpozij u LABVOLUTION -u bit će usredotočen na ključna pitanja znanosti o životu. Prema tome, predviđa se visoka razina potražnje posjetitelja. Znanstveni simpozij će imati sv
Znanstveni simpozij u LABVOLUTION -u fokusira se na ključna pitanja znanosti o životu
Znanstveni simpozij u LABVOLUTION -u bit će usredotočen na ključna pitanja znanosti o životu. Prema tome, predviđa se visoka razina potražnje posjetitelja. Znanstveni simpozij će imati sv
 Istraživanja su pokazala da su mikrobi povezani sa srčanim udarima
Studija otkrivena na kongresu ESC 2019 održanom u Parizu prošlog vikenda otkriva da abnormalna populacija mikroba u tijelu može dovesti do oštećenja stabilnih koronarnih plakova i dovesti do njihovog
Istraživanja su pokazala da su mikrobi povezani sa srčanim udarima
Studija otkrivena na kongresu ESC 2019 održanom u Parizu prošlog vikenda otkriva da abnormalna populacija mikroba u tijelu može dovesti do oštećenja stabilnih koronarnih plakova i dovesti do njihovog
 Matematički model otkriva rizik od infekcije SARS-CoV-2 nakon transplantacije fekalne mikrobiote
U svom novom članku dostupnom na stranici bioRxiv* poslužitelj predispisa, Američki istraživači iz neprofitne organizacije OpenBiome upotrijebili su matematički model za simulaciju korisnosti različ
Matematički model otkriva rizik od infekcije SARS-CoV-2 nakon transplantacije fekalne mikrobiote
U svom novom članku dostupnom na stranici bioRxiv* poslužitelj predispisa, Američki istraživači iz neprofitne organizacije OpenBiome upotrijebili su matematički model za simulaciju korisnosti različ