Studija je objavljena 23. srpnja u časopisu Znanost .
HDL je uglavnom poznat po uklanjanju kolesterola u tijelu i dostavi ga u jetru radi odlaganja. No, u novoj studiji, istraživači su identificirali posebnu vrstu HDL -a zvanu HDL3 koja, kada ga proizvodi crijevo, blokira crijevne bakterijske signale koji uzrokuju upalu jetre. Ako nije blokiran, ti bakterijski signali putuju iz crijeva u jetru, gdje aktiviraju imunološke stanice koje izazivaju upalno stanje, što dovodi do oštećenja jetre.
Iako se HDL smatrao dobrim kolesterolom, 'Lijekovi koji povećavaju ukupnu razinu HDL -a pali su posljednjih godina zbog kliničkih ispitivanja koja nisu pokazala nikakvu korist kod kardiovaskularnih bolesti. No, naša studija sugerira da povećanje razine ove specifične vrste HDL -a, i posebno podizanje u crijevima, može obećati zaštitu od bolesti jetre, koji, poput bolesti srca, također je veliki kronični zdravstveni problem. "
Gwendalyn J. Randolph, Doktor znanosti, Viši autor, ugledni profesor imunologije Emil R. Unanue
U studiji, istraživači su pokazali da HDL3 iz crijeva štiti jetru od upale kod miševa.
Bilo koja vrsta oštećenja crijeva može utjecati na to kako skupina mikroba koja se naziva gram-negativna bakterija može utjecati na tijelo. Takvi mikrobi proizvode upalnu molekulu zvanu lipopolisaharid koja može putovati u jetru putem portalne vene. Portalna vena je glavna žila koja opskrbljuje krv jetrom, a većinu hranjivih tvari prenosi u jetru nakon što se hrana apsorbira u crijevima. Tvari iz crijevnih mikroba mogu putovati zajedno s hranjivim tvarima iz hrane kako bi aktivirale imunološke stanice koje izazivaju upalu. Na ovaj način, elementi crijevnog mikrobioma mogu potaknuti bolest jetre, uključujući masnu bolest jetre i fibrozu jetre, u kojem jetra razvija ožiljno tkivo.
Randolph se za ovu temu zainteresirao u suradnji s dva kirurga sa sveučilišta Washington, Emily J. Onufer, DOKTOR MEDICINE, kirurški stažist, i Brad W. Warner, DOKTOR MEDICINE, doktorica Jessie L. Ternberg, DOKTOR MEDICINE, Uvaženi profesor dječje kirurgije i glavni kirurg u dječjoj bolnici St. Louis, oboje koautori studije. Neka nedonoščad razviju stanje opasno po život koje se naziva nekrotizirajući enterokolitis, upala crijeva koja može zahtijevati kirurški odstranjivanje dijela crijeva. Čak i nakon uspješne operacije crijeva, takve bebe često razviju bolest jetre, a Onufer i Warner željeli su razumjeti zašto.
"Proučavali su ovaj problem na mišjem modelu stanja:uklonili su dio tankog crijeva kod miševa i proučavali fibrozu jetre koja je rezultirala, "Randolph je rekao." U literaturi je bilo naznaka da bi HDL mogao ometati imunološke stanice u otkrivanju lipopolisaharida i da bi receptor za lipopolisaharid mogao biti povezan s bolešću jetre nakon operacije crijeva.
"Međutim, nitko nije mislio da će se HDL izravno premjestiti iz crijeva u jetru, što zahtijeva da uđe u portalnu venu, "rekla je." U drugim tkivima, HDL putuje kroz drugu vrstu žile koja se naziva limfna žila koja, u crijevima, ne povezuje se s jetrom. U našem laboratoriju imamo vrlo lijep alat koji nam omogućuje da osvijetlimo različite organe i pratimo HDL iz tog organa. Tako, htjeli smo osvijetliti crijeva i vidjeti kako HDL odlazi i kamo odatle odlazi. Tako smo pokazali da HDL3 odlazi samo kroz portalnu venu kako bi otišao izravno u jetru. "
Dok HDL3 prolazi ovim kratkim putovanjem niz portalnu venu, veže se za protein zvan LBP - protein koji veže lipopolisaharid - koji se veže za štetni lipopolisaharid. Kad se štetni lipopolisaharid veže za ovaj kompleks, blokirano je aktiviranje imunoloških stanica koje se zovu Kupfferove stanice. To su makrofagi koji se nalaze u jetri i, kada se aktivira lipopolisaharidom, može izazvati upalu jetre.
Kao kompleks proteina i masti, HDL3 koristi svoje partnerstvo s LBP -om za vezanje na lipopolisaharid. Kada je LBP dio kompleksa HDL3, sprječava da štetna bakterijska molekula aktivira Kupfferove stanice jetre i izazove upalu, prema eksperimentima koje je proveo prvi autor Yong-Hyun Han, Doktor znanosti, kad je bio postdoktorski istraživač u Randolphovom laboratoriju. Han je sada na fakultetu Nacionalnog sveučilišta Kangwon u Južnoj Koreji.
"Mislimo da je LBP, samo kada je vezan za HDL3, fizički stoji na putu, pa lipopolisaharid ne može aktivirati upalne imunološke stanice, "Rekao je Han." HDL3 u osnovi skriva štetnu molekulu. Međutim, ako se LBP veže za lipopolisaharid, a HDL3 nije prisutan, LBP nije u stanju stati na put. Bez HDL3, LBP će izazvati jaču upalu. "
Istraživači su pokazali da je ozljeda jetre gora kada se HDL3 iz crijeva smanji, poput kirurškog uklanjanja dijela crijeva.
"Čini se da operacija uzrokuje dva problema, "Rekao je Randolph." Kraće crijevo znači da stvara manje HDL3, i sama operacija dovodi do ozlijeđenog stanja u crijevima, što omogućuje izlijevanje više lipopolisaharida u portalnu krv. Kad uklonite dio crijeva koji stvara najviše HDL3, dobijete najgori ishod jetre. Kad imate miša koji genetski ne može stvoriti HDL3, upala jetre je također gora. Također smo htjeli vidjeti je li ta dinamika prisutna u drugim oblicima crijevnih ozljeda, pa smo pogledali mišje modele prehrane bogate mastima i alkoholne bolesti jetre. "
U svim tim modelima ozljede crijeva, istraživači su otkrili da je HDL3 zaštitni, vezanje za dodatni lipopolisaharid koji se oslobađa iz ozlijeđenog crijeva i blokira njegove nizvodne upalne učinke u jetri.
Istraživači su nadalje pokazali da su isti zaštitni molekularni kompleksi prisutni u uzorcima ljudske krvi, sugerirajući da je sličan mehanizam prisutan i kod ljudi. Također su upotrijebili spoj lijekova za povećanje HDL3 u crijevima miševa i otkrili su da štiti od različitih vrsta ozljeda jetre. Iako je lijek dostupan samo za istraživanje na životinjama, studija otkriva nove mogućnosti liječenja ili sprječavanja bolesti jetre, dolazi li od oštećenja crijeva uzrokovanog dijetom s visokim udjelom masti, pretjerana upotreba alkohola ili tjelesne ozljede, kao na primjer od operacije.
"Nadamo se da HDL3 može poslužiti kao meta u budućim terapijama bolesti jetre, "Randolph je rekao." Nastavljamo s istraživanjem kako bismo bolje razumjeli detalje ovog jedinstvenog procesa. "
 Endometrioza povezana s većim rizikom od Crohnova, kolitisa
Endometrioza povezana s većim rizikom od Crohnova, kolitisa
 Odabir bolesti s toliko toga što je ostalo za dati
Odabir bolesti s toliko toga što je ostalo za dati
 Je li operacija uvijek potrebna za upalu slijepog crijeva kod djece?
Je li operacija uvijek potrebna za upalu slijepog crijeva kod djece?
 Kako znate da je trovanje hranom?
Kako znate da je trovanje hranom?
 Može li gastroenteritis uzrokovati visok broj bijelih krvnih stanica?
Može li gastroenteritis uzrokovati visok broj bijelih krvnih stanica?
 Znanstvenici dokazuju ulogu mikrobioma u pretilosti
Znanstvenici dokazuju ulogu mikrobioma u pretilosti
 Novi lijek za IBS nekima olakšava bolove u želucu i proljev:studija
Posljednje vijesti o probavi Kada transplantacija bubrega ne uspije pokušati je ponovno Ne dopustite da vam žgaravica pokvari blagdansku gozbu Potražnja za transplantacijom jetre naglo raste Niske do
Novi lijek za IBS nekima olakšava bolove u želucu i proljev:studija
Posljednje vijesti o probavi Kada transplantacija bubrega ne uspije pokušati je ponovno Ne dopustite da vam žgaravica pokvari blagdansku gozbu Potražnja za transplantacijom jetre naglo raste Niske do
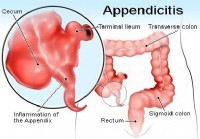 Je li to upala slijepog crijeva ili nešto drugo?
Medicinski autor:Benjamin C. Wedro, dr. med., FAAEMMedicinska urednica:Melissa Conrad Stöppler, dr. med. U medicini uvijek postoje nepostavljena pitanja. Pacijenti s pritužbom posjećuju liječnika na
Je li to upala slijepog crijeva ili nešto drugo?
Medicinski autor:Benjamin C. Wedro, dr. med., FAAEMMedicinska urednica:Melissa Conrad Stöppler, dr. med. U medicini uvijek postoje nepostavljena pitanja. Pacijenti s pritužbom posjećuju liječnika na
 Dijeta s niskim sadržajem FODMAP-a
Slijeđenje plana prehrane s niskim sadržajem FODMAP-a može se činiti zastrašujućim, ali ne mora se tako osjećati. Uz malo znanja ili pomoć dijetetičara (plus današnji pristup širokom rasponu voća, pov
Dijeta s niskim sadržajem FODMAP-a
Slijeđenje plana prehrane s niskim sadržajem FODMAP-a može se činiti zastrašujućim, ali ne mora se tako osjećati. Uz malo znanja ili pomoć dijetetičara (plus današnji pristup širokom rasponu voća, pov