Az egyik ilyen szilárd daganat, amely jól alkalmazkodik a hipoxiához, a PDAC, a hasnyálmirigyrák agresszív típusa. Ez a rákos megbetegedések egyik leggyakoribb oka, rendkívül rossz túlélési rátával. Mivel a specifikus génexpressziós profilok különböző tulajdonságokat biztosítanak, amelyek elősegítik a tumor növekedését, az intratumorális variációk megértése rávilágít a PDAC patogenezisének alapjául szolgáló komplex molekuláris mechanizmusokra. Míg a daganatszöveteken végzett hagyományos szekvenáló vizsgálatok betekintést nyújtanak a tumor génexpressziós mintázatába, nem világítanak a daganat különböző régiói közötti térbeli különbségekre, más néven "intratumorális heterogenitás". Ráadásul, a hipoxia ilyen variációra gyakorolt hatása továbbra is rosszul ismert.
Most, a Tianjin Orvostudományi Egyetem Rákkutató Intézetének és Kórházának (Kína) kutatói egy lépéssel továbbmentek a hipoxia által kiváltott génexpressziós variációk megértésében a PDAC-ban, "térbeli transzkriptómia" (ST) használatával. Ez a technika lehetővé teszi a tumor egyes régióinak szekvenálását. Megmagyarázza a ben megjelent munkájuk motivációját Rákbiológia és orvostudomány , Jihui Hao professzor és Baocun Sun, a megfelelő szerzők, mond, "Sok PDAC -beteg végül meghal a betegségben a hatékony kezelések hiánya miatt. A kezelés által kiváltott hypoxia káros változásokat okozhat a rákos sejtekben; azonban, e változások térbeli eloszlását eddig nem vizsgálták. "
A kutatók egy "xenograft" egérmodell kifejlesztésével kezdték, az emberi PDAC beültetésével az ischaemiás hátsó végtagokba (amelyek a vérellátás hiányából állnak, hipoxiás állapotot eredményez) az állatok. A daganatokat összegyűjtötték és különböző szakaszokra vágták, megfelel a daganat különböző régióinak. Ezeket a szekciókat ezután feldolgozták és a „rögzítési területekhez” csatolták, amelyek különböző génekre és komplementer transzkriptumokra specifikus nukleotidszondákat tartalmaztak. Ezeket a lemezeket tovább inkubáltuk a reakciókamrákban amplifikáció és szekvenáló könyvtár előállítása céljából. Következő, "RNS szekvenálás" elnevezésű technikát végeztünk, hogy azonosítsuk a differenciális génexpressziós mintázatokat a hipoxiás állapotoktól izolált daganatokban, szemben a kontrollokkal. A kapott adatokat a hipoxiás és a kontroll csoport specifikus klasztereire osztották fel, a korábbi irodalom génfunkciója alapján.
Érdekes módon, a sejtciklusban részt vevő gének, proliferáció, migráció, és a metasztázisok felül voltak szabályozva a kontroll alcsoportokban, a hipoxiás alcsoportokhoz képest. A tumor invazív frontjáról izolált egyik domináns hipoxiás alcsoporthoz ezek a tulajdonságok kapcsolódtak, a stresszválaszhoz kapcsolódó géneken kívül, anyagcsere, és a hasnyálmirigy normál működését. Nevezetesen, a hipoxiával kapcsolatos gének expressziója az alcsoportokban változó volt, kiemelve összefüggésüket a rákos megbetegedésekkel. Ez arra utal, hogy hipoxiás körülmények között, a rákos sejtek bizonyos alpopulációi tovább élnek, és ellenállnak a hipoxiás stressznek.
A kutatók tovább igazolták eredményeik klinikai relevanciáját azáltal, hogy összefüggésbe hozták az expressziós mintákat a beteg prognózisával. A hipoxikus génexpressziós minta valóban az volt, rosszabb prognózissal jár. Eredményeik azt is sugallták, hogy a "PI3K" jelátviteli út vonható be a legagresszívebb hipoxiás alcsoportba. Az ezen alcsoport génszignatúrájú daganatai és így, reagál a PI3K -gátlókkal történő kezelésre.
Átfogó, a tanulmány kiemeli, hogy a hipoxia jelentős szerepet játszik a PDAC intratumorális heterogenitásában, és tisztázza a PDAC térbeli molekuláris variációit. A PDAC molekuláris térképének megértése megkönnyítheti a célzott kezelések tervezését a jövőben.
Leírásaik klinikai következményeinek leírása, Jihui Hao professzor és Baocun Sun arra a következtetésre jutottak, " Eredményeink kombinálják a PDAC szövettani és transzkriptómiai variációit, feltárja a gyógyszerrezisztencia néhány mechanizmusát és a lehetséges terápiás célokat a hasnyálmirigyrák -kezelők számára t. "
 Életkezelés az irritábilis bél szindrómával
Életkezelés az irritábilis bél szindrómával
 Hogyan lehet tudni, hogy a sápadt vagy agyagszínű széklet jelenthet problémát?
Hogyan lehet tudni, hogy a sápadt vagy agyagszínű széklet jelenthet problémát?
 Mi a teendő, ha az élet összeomlik?
Mi a teendő, ha az élet összeomlik?
 Az élet tesztjei hiedelmek feltárására szolgálnak
Az élet tesztjei hiedelmek feltárására szolgálnak
 Miért van szüksége mindenkinek, aki cöliákiában szenved, égetően D-vitaminra?
Miért van szüksége mindenkinek, aki cöliákiában szenved, égetően D-vitaminra?
 A tűz almabor és az oximelek tudománya az egészség javítására
A tűz almabor és az oximelek tudománya az egészség javítására
 Az emberi nyelv mikrobiomjának részletes térképe
Új tanulmány jelent meg a folyóiratban Cellajelentések 2020 márciusában beszámol a fejlett és gyors spektrális képalkotó technikák használatáról az emberi nyelven található mikrobiális közösségek ré
Az emberi nyelv mikrobiomjának részletes térképe
Új tanulmány jelent meg a folyóiratban Cellajelentések 2020 márciusában beszámol a fejlett és gyors spektrális képalkotó technikák használatáról az emberi nyelven található mikrobiális közösségek ré
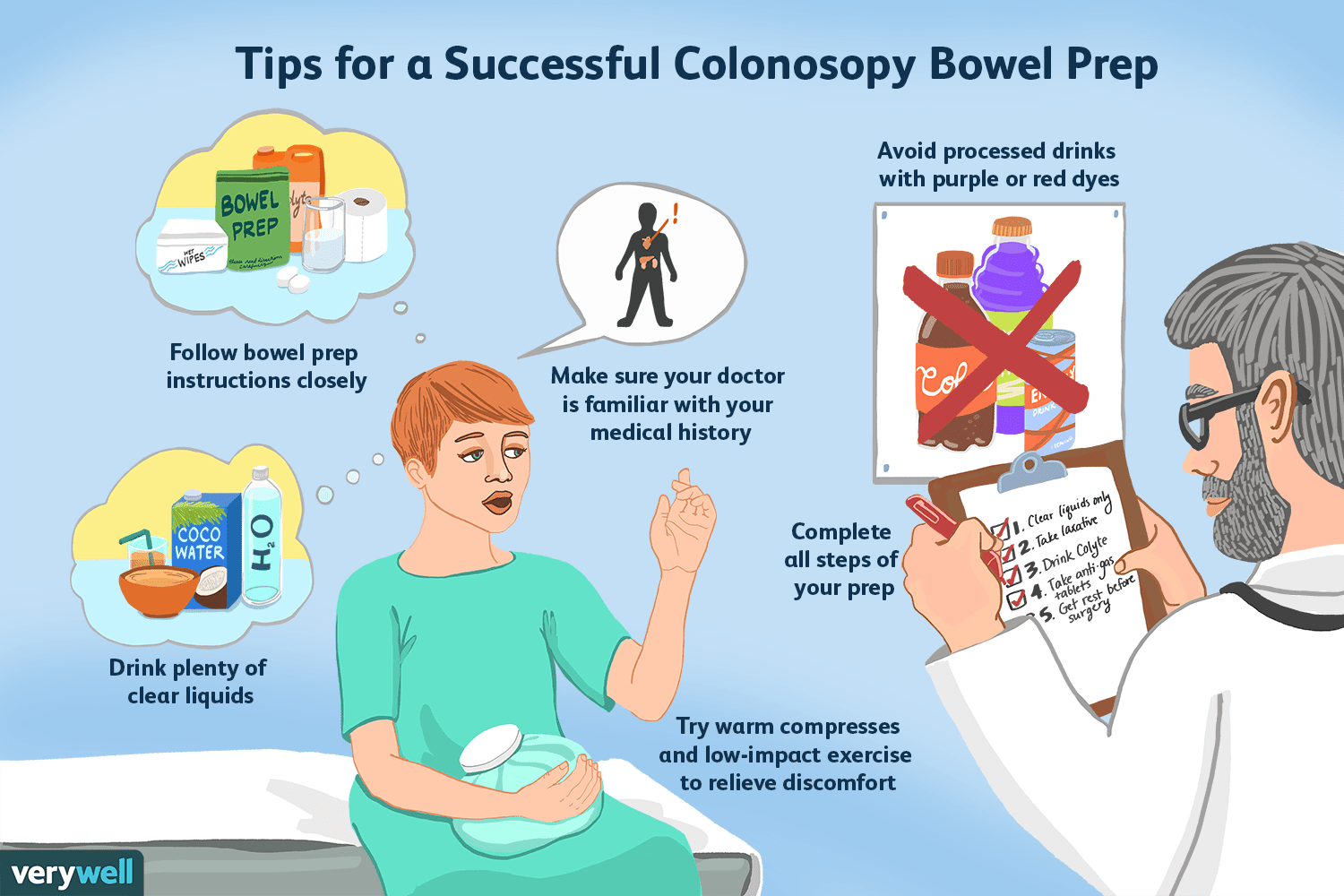 Hogyan lehet tudni, hogy a bél előkészítése befejeződött?
A bél előkészítése olyasvalami, amit el kell végeznie a vastagbél tisztítására, mielőtt kolonoszkópiát végezne. A kolonoszkópia egy olyan orvosi vizsgálat, amely a vastagbelet (vastagbelet) és a végbe
Hogyan lehet tudni, hogy a bél előkészítése befejeződött?
A bél előkészítése olyasvalami, amit el kell végeznie a vastagbél tisztítására, mielőtt kolonoszkópiát végezne. A kolonoszkópia egy olyan orvosi vizsgálat, amely a vastagbelet (vastagbelet) és a végbe
 A matematikai modell feltárja a SARS-CoV-2 fertőzés kockázatát a széklet mikrobiota transzplantációja után
Új lapjukban elérhető a bioRxiv* preprint szerver, Az OpenBiome nonprofit szervezet amerikai kutatói matematikai modellt használtak a székletminták különböző tesztelési stratégiáinak hasznosságának
A matematikai modell feltárja a SARS-CoV-2 fertőzés kockázatát a széklet mikrobiota transzplantációja után
Új lapjukban elérhető a bioRxiv* preprint szerver, Az OpenBiome nonprofit szervezet amerikai kutatói matematikai modellt használtak a székletminták különböző tesztelési stratégiáinak hasznosságának