Per 22 anni, Kibow ® si è concentrata sulla ricerca e sullo sviluppo di integratori alimentari per la salute dei reni basati sul concetto di compensazione della funzione renale inefficace utilizzando il microbioma del BOWel (da cui il nome KIBOW) per rimuovere le tossine. Questo si basa sulle proprietà di probiotici e prebiotici altamente specifici e selettivi del ceppo per diverse applicazioni di modulazione intestinale. Kibow ® è ben noto per il suo prodotto di punta Renadyl™ (un pre/probiotico per la salute dei reni), Kibow Fortis ® (un multifibra per il benessere), Kibow Flora™ (un probiotico per la salute immunitaria) per l'uomo, e Azodyl™, un prodotto veterinario per l'insufficienza renale progettato appositamente per cani e gatti (concesso in licenza esclusiva a Vetoquinol USA dal luglio 2006). L'azienda sta inoltre esplorando lo sviluppo di nuovi prodotti di integratori alimentari mirati alla funzione degli organi, ampliando così il proprio portafoglio di prodotti nel prossimo anno.
Il Kibow attualmente commercializzato ® gli integratori per l'uomo e gli animali domestici sono classificati dalla FDA statunitense come integratori alimentari. Sebbene i prodotti siano stati sviluppati con convalida di tipo farmaceutico (https://kibowbiotech.com/rd/) (https://kibowbiotech.com/journal-publications/) nell'arco di due decenni, il potenziale utilizzo di questi prodotti è limitato dalle normative FDA/FTC statunitensi, in quanto non possono essere presentate richieste di assistenza sanitaria o di trattamento della malattia. Anche, Questi prodotti, come integratori alimentari, non sono qualificati per ottenere il rimborso medico. In considerazione di queste limitazioni e del desiderio di raggiungere e aiutare un maggior numero di pazienti con reni cronici, Kibow ® ha sviluppato una nuova e più avanzata formulazione di Live Bitherapeutic (LBP) per essere scientificamente avanzata come prodotto farmaceutico approvato dalla FDA degli Stati Uniti e convalidato clinicamente.
Poiché i probiotici sono microbi vivi, questo nuovo prodotto rientrerà nei farmaci Live Biotherapeutic Product (LBP) del Center for Biological Evaluation Research (CBER) e nelle normative della FDA statunitense. Questo sarà il primo farmaco LBP per i pazienti con CKD negli Stati Uniti e si qualificherebbe per il rimborso medico. L'azienda sta avviando il processo IND e sta pianificando le sperimentazioni cliniche necessarie. Al completamento con successo della proposta randomizzata, studi clinici controllati in pazienti con CKD III/IV e presentazione dei dati alla FDA per la revisione e l'approvazione, Kibow ® si attrezzerà per lanciare il suo prodotto farmaceutico LBP nel 2023 negli Stati Uniti e in altri paesi. Ciò contribuirà a garantire che molti più pazienti possano accedere e permettersi questa nuova opzione di trattamento.
Kibow ® sta inoltre pianificando ulteriori studi clinici in pazienti sottoposti a dialisi per esplorare risultati migliori e il potenziale di riduzione della durata e/o della frequenza della dialisi. Anche questo studio clinico dovrebbe essere completato prima del 2023. Kibow ® attende con impazienza questa prossima pietra miliare che potrebbe apportare enormi benefici ai pazienti in dialisi e ridurre considerevolmente le spese di Medicare per il sistema sanitario statunitense di diversi miliardi di dollari. Kibow ® Il lancio da parte di Biotech della sua divisione farmaceutica interamente controllata e la sua azione per andare avanti per cercare lo status di farmaco LBP è in linea con la missione del programma HHS/ASN KidneyX (https://www.kidneyx.org/) recentemente creato, nonché ordine esecutivo firmato dal presidente per promuovere la salute dei reni (https://www.whitehouse.gov/presidential-actions/executive-order-advancing-american-kidney-health/).
 Trattamento della sindrome dell'intestino irritabile (IBS) del dolore addominale
Trattamento della sindrome dell'intestino irritabile (IBS) del dolore addominale
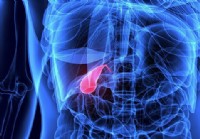 Quali sono i primi segni di una cattiva cistifellea?
Quali sono i primi segni di una cattiva cistifellea?
 2015:l'anno dell'azione
2015:l'anno dell'azione
 Un nuovo metodo di modellazione computazionale prevede come i microbi intestinali cambiano nel tempo
Un nuovo metodo di modellazione computazionale prevede come i microbi intestinali cambiano nel tempo
 Quali alimenti provocano la colite ulcerosa?
Quali alimenti provocano la colite ulcerosa?
 Capito:i punti salienti di The Gut Stuff
Capito:i punti salienti di The Gut Stuff
 Che cos'è l'appendicectomia transvaginale?
Cosè lappendicectomia transvaginale? Nel trattamento dellappendicite acuta, lappendicectomia transvaginale, che comporta la rimozione dellappendice attraverso la vagina, è unopzione. Lappendicec
Che cos'è l'appendicectomia transvaginale?
Cosè lappendicectomia transvaginale? Nel trattamento dellappendicite acuta, lappendicectomia transvaginale, che comporta la rimozione dellappendice attraverso la vagina, è unopzione. Lappendicec
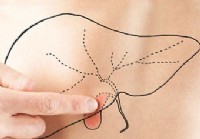 Calcoli biliari:trattamento, sintomi e cause
Un adulto maschio che indica un contorno di fegato e si dipinge una cistifellea sulladdome. Definizione e fatti di Gallstone I calcoli biliari sono calcoli che si formano nella cistifellea o nei dott
Calcoli biliari:trattamento, sintomi e cause
Un adulto maschio che indica un contorno di fegato e si dipinge una cistifellea sulladdome. Definizione e fatti di Gallstone I calcoli biliari sono calcoli che si formano nella cistifellea o nei dott
 Stile di vita SCD sulle onde radio
Sei disposto a rispondere alle domande IN DIRETTA su un programma radiofonico nazionale? Diamine sì! Le ultime settimane sono state un vero spasso. Abbiamo fatto una presentazione di fantasia, una r
Stile di vita SCD sulle onde radio
Sei disposto a rispondere alle domande IN DIRETTA su un programma radiofonico nazionale? Diamine sì! Le ultime settimane sono state un vero spasso. Abbiamo fatto una presentazione di fantasia, una r