Kadangi intensyviai stengiamasi kovoti su virusu, naujas tarptautinės mokslininkų grupės tyrimas praneša apie netikėtą bakterijos sėkmę moduliuojant imuninį atsaką kvėpavimo takuose ir apsaugant ląsteles nuo infekcijos šiuo virusu.
 Tyrimas:Dolosigranulum pigrum moduliuoja imunitetą nuo SARS-CoV-2 kvėpavimo takų epitelio ląstelėse. Vaizdo kreditas:creativeneko / Shutterstock
Tyrimas:Dolosigranulum pigrum moduliuoja imunitetą nuo SARS-CoV-2 kvėpavimo takų epitelio ląstelėse. Vaizdo kreditas:creativeneko / Shutterstock Komandos išvados buvo paskelbtos žurnale Patogenai .
SARS-CoV-2 patenka į ląstelę šeimininkę per angiotenziną konvertuojantį fermentą 2 (ACE2), ekspresuojamas kvėpavimo epitelio ir plaučių ląstelėse. Sunkiais atvejais, liga yra susijusi su plačiu plaučių pažeidimu ir ūminiu kvėpavimo distreso sindromu (ARDS), ir daugelio organų pažeidimas, kartais priveda prie mirties.
Manoma, kad ligos sunkumą lemia ne tik virusinis citopatinis viruso poveikis užkrėstoms ląstelėms, bet dar daugiau, dėl hiperaktyvios uždegiminės reakcijos. Atrodo, kad virusas slopina I ir III tipo interferonų (IFN) išsiskyrimą, taip pat antivirusiniai veiksniai, skatinti sunkią infekciją.
Be to, infekcijos sukelta epitelio ląstelių mirtis sukelia uždegiminių tarpininkų išsiskyrimą ir uždegiminių imuninių ląstelių migraciją į pažeistus kvėpavimo takų audinius. Visa tai išskiria daugiau chemokinų ir citokinų, ir susidaro užburtas didėjančio uždegimo ratas.
Bandydamas atremti šiuos destruktyvius procesus, naudojami priešuždegiminiai ir antivirusiniai vaistai; taip pat imunomoduliuojantys vaistai. Naujasis dokumentas suteikia dar vieną galimybę, naudojant kvėpavimo takų mikrobiomą viruso poveikiui sumažinti.
Tyrimas, kuriame dalyvavo sunkumo spektro COVID-19 pacientai, parodė, kad ne mažiau kaip 60 bakterinių operacinių taksonominių vienetų (OTU) buvo nustatyta tik pacientams, sergantiems SARS-CoV-2, daugiausia iš prieglobsčio Bakteroidai ir Firmicutes . Be to, Prevotella buvo labiausiai paplitusi bakterijų gentis, aptikta tik sunkiais COVID-19 sergančiais pacientais, tuo tarpu Dolosigranum rūšių buvo nustatyta lengvo COVID-19, atvirkščiai proporcingai Prevotella .
Atsižvelgiant į tai, dabartiniai tyrėjai anksčiau parodė teigiamą šios bakterijos poveikį įgimtam imuniniam atsakui kvėpavimo takuose. Vartojant į nosį, bakterija D. pigrum 040417 ne tik greičiau pašalino virusą, bet ir užkirto kelią plaučių pažeidimams dėl uždegimo. Jie taip pat nustatė, kad naudingas bakterijos poveikis būdingas jų naudojamai padermei.
Pelėms, nosies vartojimas D. pigrum 040417 moduliavo įgimtą imuninį atsaką ir pagerino atsparumą tiek pneumokokų, tiek kvėpavimo takų sincitinio viruso (RSV) infekcijoms.
Šiame dokumente, jie naudojo Calu-3 ląsteles, žmogaus plaučių epitelio ląstelių linija. Kai inkubuojama su D. pigrum 040417, epitelio ląstelės kultūroje nebuvo neigiamai paveiktos. Tačiau, padidėjo IFN-β ir IL-6 gamyba, tausojantis CXCL8. Šio efekto nebuvo matyti D. pigrum 030918.
Šis eksperimentas grindžiamas tuo, kad dvigubos grandinės ribonukleino rūgštis (dsRNR) yra tarpinė medžiaga koronaviruso replikacijos ir transkripcijos metu. Tai nustatoma naudojant ląstelių antivirusinę apsaugą kvėpavimo epitelyje, sukelia citokinų išsiskyrimą.
Konkrečiai, modelio atpažinimo receptoriai (PRR) šeimininke atpažįsta viruso dsRNR, dėl to gaminami I ir III tipo interferonai, pirminė antivirusinė gynyba. Tai sukelia interferono stimuliuojamo geno (ISG) ekspresiją, o tai savo ruožtu suaktyvina kitas antivirusines sistemas.
Koronavirusai gali pasislėpti nuo šių gynybos sistemų. Iš tiesų, anti-dsRNR sistemos yra mažiau aktyviai veikiamos SARS-CoV-2 nei su Sindbis virusu, bet daugiau nei ankstesnio Artimųjų Rytų kvėpavimo sindromo koronaviruso (MERS-CoV) atveju. Tai gali reikšti, kad SARS-CoV-2 nėra toks geras kaip kiti į SARS panašūs virusai, kad išvengtų nuo dsRNR priklausomų imuninių takų.
Jei taip, interferono kelias galėtų būti naudojamas ankstyvai antivirusinei gynybai sustiprinti, siekiant apriboti viruso replikaciją su šiuo virusu.
Po inkubacijos su bakterija D. pigrum , ląstelės padidino IFN-β kiekį, IL-6 ir CXCL8 pradžioje. Kai vėliau stimuliuojamas į „Toll“ panašų receptorių 3 (TLR3) agonistą, polinozininė:policididilo rūgštis poli (I:C), kuris atitinka dsRNR, tiek kontrolinėse, tiek apdorotose ląstelėse IFN-β ir IL-6 koncentracija padidėjo keturis ar penkis kartus.
Chemokinų CCL5 ir CXCL10 pradžioje nebuvo, bet buvo pagaminti po stimuliacijos.
IFN-β ir IL-6 padidėjimas buvo žymiai didesnis ląstelėms, iš anksto apdorotoms D. pigrum 040417 pradžioje ir po stimuliacijos, palyginti su kontroliniais. Ir atvirkščiai, CXCL8 kilimas, CCL5 ir CXCL10 koncentracijos buvo mažesnės D. pigrum 040417 apdorotos ląstelės.
D. pigrum 030918 nesukėlė jokių citokinų lygio pokyčių, palyginti su kontroliniais.
Tyrėjai taip pat nustatė, kad po to SARS-CoV-2 replikacija Calu-3 ląstelėse buvo lėtesnė D. pigrum Išankstinis apdorojimas 040417, kartu su sumažėjusiu LDH kiekiu. LDH yra ląstelių pažeidimo žymuo. Vėlgi, D. pigrum 030918 neparodė jokio teigiamo poveikio.
Neapdorotose ląstelėse, IFN-β ir IL-6 koncentracija padidėjo po infekcijos praėjus 48 valandoms po infekcijos, kaip ir CXCL8, CCL5 ir CXCL10. Tačiau, Pirmasis išliko tame pačiame lygyje po 72 valandų, pastarųjų ir toliau daugėjo.
Po inkubacijos su D. pigrum 040417, kartu su replikacijos vėlavimu, citokinų profilis taip pat parodė reikšmingus pokyčius. Nors IFN-β ir IL-6 pakilo į aukštesnį lygį, CXCL8 lygis sumažėjo ir po 48, ir po 72 valandų, tuo tarpu CCL5 ir CXCL10 sumažėjo 72 val.
Pirmą kartą, šis tyrimas parodė, kad nosies vartojimas D. pigrum 040417 moduliuoja įgimtą nosies epitelio imuninį atsaką į TLR3 stimuliaciją poli (I:C) ir SARS-CoV-2 infekciją. Gali būti, kad naudingų komensinių bakterijų buvimas keičia kvėpavimo epitelio imunologines savybes ir taip padidina jų atsparumą kai kuriems patogenams.
Patobulinta IFN-β gamyba su D. pigrum 040417 gali būti atsakingas už mažesnį SARS-CoV-2 replikacijos greitį, nurodant padidėjusį dsRNR antagonizmo efektyvumą ląstelės šeimininkės imuniniais keliais.
Vėlyvas interferono atsakas yra susijęs su intensyviu uždegimu ir audinių pažeidimu. Iš tiesų, kai kurie tyrimai parodė, kad SARS-CoV-2 sukelia uždegimą ankstyvoje infekcijos stadijoje, su dideliu kiekiu chemokinų, įskaitant CXCL8.
Didelis šių citokinų kiekis būdingas sunkiam ar kritiniam COVID-19, tai rodo nereguliuojamą uždegiminį atsaką tiek kvėpavimo, tiek sisteminiu lygiu. CXCL8 sumažėjimas, CCL5 ir CXCL10 epitelio ląstelėse, iš anksto apdorojus D. pigrum 040417 gali, galbūt, rodo, kad ši bakterija gali padėti išvengti tokių uždegiminių pažeidimų.
Tyrimas taip pat nurodo, kad reikia nustatyti naudingiausias bakterijų padermes, nes visi jie nėra vienodo veiksmingumo. Papildomai, pažymėtina, kad D. pigrum 040417 turėjo tik dalinį poveikį viruso replikacijai. Taigi, reikia nustatyti, kurios bakterijų padermės ir gentys veikia kartu, kad apsaugotų nuo infekcijos ar simptominės ligos.
 Keturi dalykai, kurie sukelia skrandžio skausmus | Arshad Malik, MD
Kiekvienas žmogus retkarčiais patiria pilvo skausmą, nesvarbu, ar tai valgo kažką, kas jūsų organizmui nepatinka, ar menstruacijų skausmai (moterims). Tačiau jei pilvo skausmus jaučiate reguliariai, t
Keturi dalykai, kurie sukelia skrandžio skausmus | Arshad Malik, MD
Kiekvienas žmogus retkarčiais patiria pilvo skausmą, nesvarbu, ar tai valgo kažką, kas jūsų organizmui nepatinka, ar menstruacijų skausmai (moterims). Tačiau jei pilvo skausmus jaučiate reguliariai, t
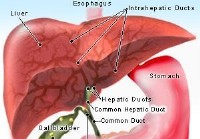 ERCP (endoskopinė retrogradinė cholangio-pankreatografija)
Faktai, kuriuos turėtumėte žinoti apie ERCP Viršutinės virškinimo trakto sistemos, tulžies pūslės, kepenų ir kasos vaizdas ERCP yra diagnostinė procedūra, skirta kepenų, tulžies latakų ir kasos ligom
ERCP (endoskopinė retrogradinė cholangio-pankreatografija)
Faktai, kuriuos turėtumėte žinoti apie ERCP Viršutinės virškinimo trakto sistemos, tulžies pūslės, kepenų ir kasos vaizdas ERCP yra diagnostinė procedūra, skirta kepenų, tulžies latakų ir kasos ligom
 Inkstų nepakankamumas
Moteris jaučia silpnumą ir dusulį. Inkstų nepakankamumo apibrėžimas ir faktai Inkstai yra organai, kurie filtruoja atliekas iš kraujo. Jie taip pat dalyvauja reguliuojant kraujospūdį, elektrolitų pus
Inkstų nepakankamumas
Moteris jaučia silpnumą ir dusulį. Inkstų nepakankamumo apibrėžimas ir faktai Inkstai yra organai, kurie filtruoja atliekas iš kraujo. Jie taip pat dalyvauja reguliuojant kraujospūdį, elektrolitų pus