 Foto van een man met pancreaskanker door iStock
Foto van een man met pancreaskanker door iStock Pancreaskanker veroorzaakt meestal geen symptomen totdat het is gegroeid, dus het wordt meestal gediagnosticeerd in gevorderde stadia in plaats van vroeg in de loop van de ziekte. In sommige gevallen kan geelzucht (een gelige verkleuring van de huid en het wit van de ogen) zonder pijn een vroeg teken zijn van alvleesklierkanker. Andere symptomen die kunnen optreden bij een verder gevorderde ziekte zijn:
Bleke ontlasting, rugpijn, buikpijn, donkere urine, opgeblazen gevoel in de buik, diarree en vergrote lymfeklieren in de nek kunnen ook aanwezig zijn.
Lees meer over symptomen van alvleesklierkanker »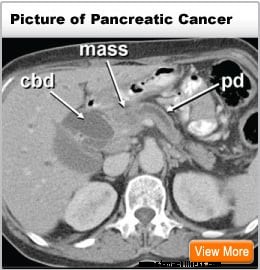
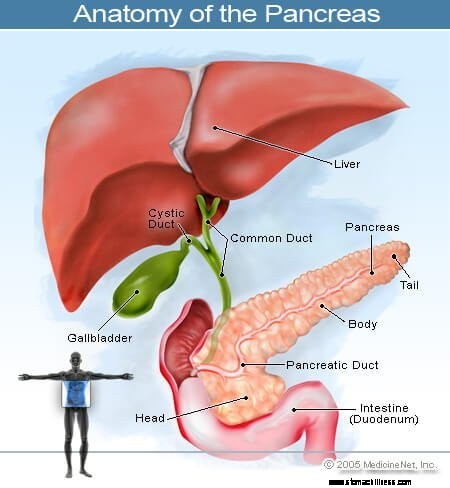 Kanker die in de alvleesklier begint, wordt alvleesklierkanker genoemd. Deze foto van de alvleesklier toont zijn locatie aan de achterkant van de buik, achter de maag.
Kanker die in de alvleesklier begint, wordt alvleesklierkanker genoemd. Deze foto van de alvleesklier toont zijn locatie aan de achterkant van de buik, achter de maag. De alvleesklier is een hormoonproducerend orgaan in de buik dat voor de wervelkolom boven het niveau van de navel zit. Het heeft twee hoofdfuncties:
De enzymen helpen de spijsvertering door eiwitten, vetten en koolhydraten in kleinere delen te hakken, zodat ze gemakkelijker door het lichaam kunnen worden opgenomen en kunnen worden gebruikt als bouwstenen voor weefsels en voor energie. Enzymen verlaten de pancreas via een systeem van buizen die "kanalen" worden genoemd en die de pancreas verbinden met de darmen waar de enzymen zich vermengen met ingenomen voedsel.
De alvleesklier zit diep in de buik en bevindt zich dicht bij veel belangrijke structuren zoals de dunne darm (de twaalfvingerige darm) en de galwegen, evenals belangrijke bloedvaten en zenuwen.
Elke seconde van elke dag vindt er in ons lichaam een enorm proces van vernietiging en herstel plaats. Het menselijk lichaam bestaat uit biljoenen cellen en elke dag verslijten of worden miljarden cellen vernietigd. Elke keer dat het lichaam een nieuwe cel aanmaakt om een versleten cel te vervangen, probeert het lichaam een perfecte kopie te maken van de cel die afsterft, meestal door vergelijkbare gezonde cellen te laten delen in twee cellen omdat die stervende cel een taak had te doen , en de nieuw gemaakte cel moet in staat zijn om diezelfde functie uit te voeren. Ondanks opmerkelijk elegante systemen om fouten in dit proces weg te werken, maakt het lichaam dagelijks tienduizenden fouten bij de normale celdeling, hetzij als gevolg van willekeurige fouten of door omgevingsdruk in het lichaam. De meeste van deze fouten worden gecorrigeerd, of de fout leidt tot de dood van de nieuw gemaakte cel en er wordt dan weer een nieuwe cel gemaakt. Soms wordt een fout gemaakt die, in plaats van het vermogen van de cel om te groeien en te overleven, te remmen, de nieuw gemaakte cel op een ongereguleerde manier laat groeien. Wanneer dit gebeurt, wordt die cel een kankercel die in staat is om te delen, onafhankelijk van de checks and balances die de normale celdeling regelen. De kankercel vermenigvuldigt zich en er ontstaat een kankergezwel of kwaadaardige tumor.
Tumoren vallen in twee categorieën:"goedaardige" tumoren en "kwaadaardige" of kankerachtige tumoren. Wat is het verschil? Het antwoord is dat een goedaardige tumor alleen groeit in het weefsel waaruit hij voortkomt. Goedaardige tumoren kunnen soms behoorlijk groot of snel groeien en ernstige symptomen veroorzaken. Een vleesboom in de baarmoeder van een vrouw kan bijvoorbeeld bloedingen of pijn veroorzaken, maar zal nooit buiten de baarmoeder reizen, omliggende weefsels binnendringen of groeien als een nieuwe tumor elders in het lichaam (uitgezaaid). Vleesbomen hebben, net als alle goedaardige tumoren, niet het vermogen om cellen in het bloed en de lymfesystemen af te scheiden en kunnen niet naar andere plaatsen in het lichaam reizen en groeien. Aan de andere kant kan een kankercel cellen van de oorspronkelijke tumor afstoten die als paardenbloemzaden in de wind door de bloedbaan of lymfevaten kunnen drijven, in weefsels ver van de tumor terechtkomen en zich ontwikkelen tot nieuwe tumoren in andere delen van het lichaam. Dit proces, metastase genaamd, is het bepalende kenmerk van een kankergezwel. Pancreaskanker is helaas een bijzonder goed model voor dit proces. Pancreaskanker kan op deze manier vroeg uitzaaien naar andere organen. Ze kunnen ook rechtstreeks groeien en aangrenzende structuren binnendringen, waardoor chirurgische verwijdering van de tumor vaak onmogelijk wordt.
Kankers worden genoemd door de weefsels waaruit de primaire tumor voortkomt. Daarom is een longkanker die zich naar de lever verplaatst geen "leverkanker", maar wordt beschreven als uitgezaaide longkanker, en een patiënt met borstkanker die zich uitbreidt naar de hersenen wordt niet beschreven als een "hersentumor" maar eerder als een patiënt met uitgezaaide borstkanker.


Wat is polycythaemia vera?
Meer informatie op
Een kanker die zich in de pancreas ontwikkelt, valt in twee hoofdcategorieën:(1) kankers van de endocriene pancreas (het deel dat insuline en andere hormonen maakt) worden "eilandcel" of "pancreas neuro-endocriene tumoren of PNET's" genoemd en (2) kankers van de exocriene pancreas (het deel dat enzymen maakt). Eilandcelkankers zijn zeldzaam en groeien doorgaans langzaam in vergelijking met exocriene pancreaskankers. Eilandceltumoren geven vaak hormonen af in de bloedbaan en worden verder gekenmerkt door de hormonen die ze produceren (insuline, glucagon, gastrine en andere hormonen). Kankers van de exocriene pancreas (exocriene kankers) ontwikkelen zich uit de cellen die het systeem van kanalen bekleden die enzymen aan de dunne darm afleveren en worden gewoonlijk pancreasadenocarcinomen genoemd. Plaveiselcelcarcinoom van de alvleesklier is zeldzaam. Adenocarcinoom van de pancreas omvat bijna alle ductale kankers van de alvleesklier en is het hoofdonderwerp van deze review.
Cellen die de kanalen in de exocriene pancreas bekleden, delen zich sneller dan de weefsels die hen omringen. Om redenen die we niet begrijpen, kunnen deze cellen een fout maken wanneer ze hun DNA kopiëren terwijl ze zich delen om andere stervende cellen te vervangen. Op deze manier kan een abnormale cel worden gemaakt. Wanneer een abnormale ductale cel zich op een ongereguleerde manier begint te delen, kan er een groei ontstaan die bestaat uit abnormaal uitziende en functionerende cellen. De abnormale veranderingen die onder de microscoop kunnen worden herkend, worden 'dysplasie' genoemd. Vaak kunnen dysplastische cellen in de loop van de tijd extra DNA-fouten ondergaan en zelfs nog abnormaler worden. Wanneer deze dysplastische cellen door de wanden van het kanaal van waaruit ze ontstaan in het omringende weefsel binnendringen, is de dysplasie een kanker geworden.
In een in 2016 gepubliceerde studie rapporteerden onderzoekers analyse van de genen in 456 ductale adenocarcinomen van de pancreas. Daaropvolgende expressie-analyse van deze adenocarcinomen maakte het mogelijk ze te definiëren in vier subtypes. Deze subtypes zijn niet eerder onderscheiden. De subtypen omvatten:
Deze nieuwe bevindingen kunnen toekomstige kankerpatiënten mogelijk maken om specifieker te worden behandeld, afhankelijk van hun subtype en, hopelijk, effectiever. Het immunogene subtype zou bijvoorbeeld mogelijk kunnen reageren op therapie waarbij het immuunsysteem opnieuw wordt ontworpen om dit soort kankercellen aan te vallen.
Pancreaskanker moet niet worden verward met de term pancreatitis. Pancreatitis wordt eenvoudigweg gedefinieerd als een ontsteking van de alvleesklier en wordt voornamelijk veroorzaakt door alcoholmisbruik en/of galsteenvorming (ongeveer 80% tot 90%). Niettemin wordt chronische pancreatitis geassocieerd met alvleesklierkanker.
Ongeveer 53.670 gevallen van alvleesklierkanker komen jaarlijks voor in de Verenigde Staten. De meeste mensen die alvleesklierkanker krijgen, doen dit zonder predisponerende risicofactoren. Maar misschien is de grootste risicofactor het ouder worden; ouder zijn dan 60 brengt een persoon een groter risico met zich mee. Zelden kunnen er familiale of erfelijke genetische syndromen zijn die het gevolg zijn van genetische mutaties die in families voorkomen en individuen een hoger risico opleveren, zoals BRCA-2 en, in mindere mate, BRCA-1-genmutaties. Familiaire syndromen zijn ongebruikelijk, maar het is belangrijk om een arts te laten weten of bij iemand anders in de familie kanker is vastgesteld, met name alvleesklierkanker. Bovendien wordt gedacht dat bepaalde gedragingen of aandoeningen het risico van een persoon om alvleesklierkanker te ontwikkelen licht verhogen. Afro-Amerikanen lopen bijvoorbeeld mogelijk een groter risico, evenals personen met naaste familieleden bij wie eerder de diagnose pancreaskanker is gesteld. Andere gedragingen of aandoeningen die mensen in gevaar kunnen brengen, zijn onder meer tabaksgebruik, obesitas, een zittende levensstijl, een voorgeschiedenis van diabetes, chronische pancreasontsteking (pancreatitis) en een vet (of westers) dieet. Voorafgaande maagoperaties kunnen het risico matig verhogen, evenals bepaalde chronische infecties zoals hepatitis B en H. pylori (een bacteriële infectie van het maagslijmvlies). Bepaalde geneesmiddelen (sitagliptine [Januvia], exenatide [Byetta], liraglutide [Victoza] en metformine en sitagliptine [Janumet]) zijn in verband gebracht met de ontwikkeling van alvleesklierkanker. Sommige soorten pancreascysten kunnen individuen het risico geven om pancreaskanker te ontwikkelen. Een paar onderzoekers suggereren dat het drinken van koffie en frisdrank het risico op alvleesklierkanker verhoogt. Wanneer pancreaskanker begint, begint het meestal in de cellen die de kanalen van de pancreas bekleden en wordt het pancreasadenocarcinoom genoemd. of exocriene alvleesklierkanker . Ondanks de hierboven genoemde risico's, wordt bij de meeste mensen die alvleesklierkanker krijgen geen aanwijsbare oorzaak gevonden.
Door op 'Verzenden' te klikken, ga ik akkoord met de algemene voorwaarden en het privacybeleid van MedicineNet. Ik ga er ook mee akkoord e-mails van MedicineNet te ontvangen en ik begrijp dat ik me op elk moment kan afmelden voor MedicineNet-abonnementen.
Omdat de alvleesklier diep in de buik voor de wervelkolom ligt, groeit alvleesklierkanker vaak maandenlang stil voordat het wordt ontdekt. Vroege kankersymptomen en/of eerste tekenen kunnen afwezig of heel subtiel zijn. Gemakkelijker identificeerbare symptomen ontwikkelen zich zodra de tumor groot genoeg wordt om op andere nabijgelegen structuren te drukken, zoals zenuwen (die algemene pijn en/of rugpijn veroorzaken), de darmen (die de eetlust beïnvloeden en misselijkheid veroorzaken samen met gewichtsverlies), of de galwegen (die geelzucht of geelverkleuring van de huid veroorzaken en verlies van eetlust en jeuk kunnen veroorzaken). Symptomen bij vrouwen verschillen zelden van die bij mannen. Zodra de tumor kankercellen in de bloed- en lymfesystemen afstoot en uitzaait, ontstaan er meestal aanvullende symptomen, afhankelijk van de locatie van de metastase. Frequente plaatsen van metastase voor alvleesklierkanker zijn de lever, de lymfeklieren en het slijmvlies van de buik (het buikvlies genoemd; ascitesvocht kan zich ophopen bij uitgezaaide alvleesklierkanker). Helaas worden de meeste pancreaskankers gevonden nadat de kanker is gegroeid of voorbij de pancreas is gevorderd of is uitgezaaid naar andere plaatsen.
Over het algemeen kunnen de tekenen en symptomen van alvleesklierkanker worden geproduceerd door exocriene of endocriene kankercellen. Veel van de tekenen en symptomen van exocriene pancreaskanker zijn het gevolg van verstopping van het kanaal dat door de pancreas loopt van de lever die gal naar de darm vervoert. Symptomen van exocriene pancreaskanker zijn onder meer
De tekenen en symptomen van endocriene pancreaskanker zijn vaak gerelateerd aan de overmatige hormonen die ze produceren en bijgevolg aan een verscheidenheid aan verschillende symptomen. Dergelijke symptomen zijn gerelateerd aan de hormonen en zijn als volgt:
Niet-functionerende neuro-endocriene tumoren maken geen overtollige hormonen aan, maar kunnen groot worden en zich uit de pancreas verspreiden. Symptomen kunnen dan lijken op elk van de hierboven beschreven endocriene pancreaskankers.
De meeste mensen hoeven niet te worden gescreend op alvleesklierkanker, en de tests die beschikbaar zijn voor screening zijn vaak complex, riskant, duur of ongevoelig in de vroege stadia van de kanker. Degenen die mogelijk in aanmerking komen, hebben meestal een reeks factoren die het risico op pancreaskanker verhogen, zoals pancreascysten, eerstegraads familieleden met pancreaskanker of een voorgeschiedenis van genetische syndromen die verband houden met pancreaskanker. De meeste screeningstesten bestaan uit CT-scans, echografieën, magnetische resonantie cholangiopancreatografie (MRCP), endoscopische retrograde cholangiopancreatografie (ERCP) of endoscopische echografie. Helaas is vroege detectie van alvleesklierkanker moeilijk omdat er weinig of geen symptomen zijn.
De meeste mensen met alvleesklierkanker gaan eerst naar hun huisarts met klachten over niet-specifieke symptomen (zie het gedeelte over symptomen hierboven). Enkele waarschuwingssignalen zijn pijn, gastro-intestinale symptomen, gewichtsverlies, vermoeidheid en toegenomen buikvocht. Deze klachten leiden vaak tot een evaluatie, waaronder een lichamelijk onderzoek (meestal normaal), bloedonderzoek, röntgenfoto's en een echografie. Als alvleesklierkanker aanwezig is, is de kans dat een echografie een afwijking in de alvleesklier aan het licht brengt ongeveer 75%. Als een probleem wordt geïdentificeerd of vermoed, wordt vaak een computertomografie (CT)-scan uitgevoerd als de volgende stap in de evaluatie; sommige clinici geven de voorkeur aan een MRI. Als een alvleeskliermassa wordt gezien, roept dat de verdenking op alvleesklierkanker op en een arts voert vervolgens een biopsie uit om een diagnose te stellen.
Er kunnen verschillende strategieën worden gebruikt om een biopsie van de vermoedelijke kanker uit te voeren. Vaak zal een naaldbiopsie van de lever door de buikwand (percutane leverbiopsie) worden gebruikt als blijkt dat de kanker is uitgezaaid naar de lever. Als de tumor gelokaliseerd blijft in de pancreas, wordt meestal direct een biopsie van de pancreas uitgevoerd met behulp van een CT. Een directe biopsie kan ook worden gemaakt via een endoscoop die in de keel en in de darmen wordt geplaatst. Met een camera op de punt van de endoscoop kan de endoscopist de endoscoop in de darm voortbewegen. Een ultrasoon apparaat aan de punt van de endoscoop lokaliseert het gebied van de pancreas dat moet worden gebiopteerd, en een biopsienaald wordt door een werkkanaal in de endoscoop geleid om weefsel van de vermoedelijke kanker te verkrijgen. Uiteindelijk is een weefseldiagnose de enige manier om de diagnose met zekerheid te stellen, en het team van artsen werkt aan een zo eenvoudig mogelijke weefseldiagnose.
Naast radiologische tests kan een vermoeden van pancreaskanker ontstaan door de verhoging van een "tumormarker", een bloedtest die abnormaal hoog kan zijn bij mensen met pancreaskanker. De tumormarker die het vaakst wordt geassocieerd met pancreaskanker wordt de CA19-9 genoemd. Het wordt vaak in de bloedbaan afgegeven door pancreaskankercellen en kan verhoogd zijn bij patiënten die onlangs pancreaskanker hebben ontdekt. Helaas, hoewel de CA19-9-test kankergerelateerd is, is deze niet specifiek voor alvleesklierkanker. Andere vormen van kanker en sommige goedaardige aandoeningen kunnen ervoor zorgen dat de CA 19-9 verhoogd is. Soms (ongeveer 20% van de tijd) zal de CA19-9 op normale niveaus in het bloed zijn ondanks een bevestigde diagnose van alvleesklierkanker, dus de tumormarker is niet perfect. Het kan echter nuttig zijn om tijdens de ziekte te volgen, aangezien de opkomst en ondergang ervan kunnen correleren met de groei van de kanker en helpen bij het begeleiden van de juiste therapie.
Zodra pancreaskanker is gediagnosticeerd, wordt het 'geënsceneerd'. Pancreaskanker wordt opgedeeld in vier stadia, waarbij stadium 1 het vroegste stadium is (stadium 0 wordt niet meegeteld) en stadium IV het verst gevorderd is (gemetastaseerde ziekte). Dit zijn de stadia van alvleesklierkanker volgens het National Cancer Institute:
Fase 0 :Kanker komt alleen voor in het slijmvlies van de ductus pancreaticus. Stadium 0 wordt ook wel carcinoma in situ genoemd.
Fase I :Kanker heeft zich gevormd en bevindt zich alleen in de alvleesklier.
Fase II :Kanker is mogelijk uitgezaaid of gevorderd naar nabijgelegen weefsel en organen en lymfeklieren in de buurt van de pancreas.
Fase III :Kanker is uitgezaaid of gevorderd naar de belangrijkste bloedvaten in de buurt van de pancreas en is mogelijk uitgezaaid naar nabijgelegen lymfeklieren.
Fase IV :Kanker kan elke grootte hebben en is uitgezaaid naar verre organen, zoals de lever, long en buikholte. Het kan ook zijn uitgezaaid naar organen en weefsels in de buurt van de pancreas of naar lymfeklieren. Dit stadium wordt ook wel eindstadium pancreaskanker genoemd.
In tegenstelling tot veel vormen van kanker, worden patiënten met pancreaskanker echter meestal gegroepeerd in drie categorieën, die met lokale ziekte, die met lokaal gevorderde, niet-reseceerbare ziekte, en die met gemetastaseerde ziekte. De initiële therapie verschilt vaak voor patiënten in deze drie groepen.
Van patiënten met stadium I en stadium II kankers wordt gedacht dat ze lokale of "reseceerbare" kanker hebben (kanker die volledig kan worden verwijderd met een operatie). Patiënten met stadium III kankers hebben een "plaatselijk gevorderde, niet-reseceerbare" ziekte. In deze situatie is de kans op genezing verloren gegaan, maar lokale behandelingen zoals bestralingstherapie blijven opties. Bij patiënten met stadium IV pancreaskanker wordt chemotherapie meestal aanbevolen als middel om de symptomen die verband houden met de kanker onder controle te houden en de levensduur te verlengen. Hieronder bespreken we veelvoorkomende behandelingen voor de drie groepen pancreaskanker (reseceerbare, lokaal gevorderde inoperabele en gemetastaseerde pancreaskanker).
Als een alvleesklierkanker in een vroeg stadium (stadium I en stadium II) wordt gevonden en lokaal in of rond de alvleesklier zit, kan een operatie worden aanbevolen (reseceerbare pancreaskanker). Chirurgie is de enige potentieel curatieve behandeling voor alvleesklierkanker. The surgical procedure most commonly performed to remove a pancreatic cancer is a Whipple procedure (pancreatoduodenectomy or pancreaticoduodenectomy). It often comprises removal of a portion of the stomach, the duodenum (the first part of the small intestine), pancreas, a portion of the main bile duct, lymph nodes, and gallbladder. It is important to be evaluated at a hospital with lots of experience performing pancreatic cancer surgery because the operation is a big one, and evidence shows that experienced surgeons better select people who can get through the surgery safely and also better judge who will most likely benefit from the operation. In experienced hands, the mortality from the surgery itself is less than 4%.
After the Whipple surgery, patients typically spend about one week in the hospital recovering from the operation. Complications from the surgery can include blood loss (anemia), leakage from the reconnected intestines or ducts, or slow return of bowel function. Recovery to presurgical health often can take several months.
After patients recover from a Whipple procedure for pancreatic cancer, treatment to reduce the risk of the cancer returning is a standard recommendation. This treatment, referred to as "adjuvant therapy (chemotherapy)," has proven to lower the risk of recurrent cancer. Typically, physicians recommend six months of adjuvant chemotherapy, sometimes with radiation incorporated into the treatment plan.
Some patients with pancreatic cancer experience blockage of bile and/or pancreas ducts and thus may need a surgeon to place a stent to allow drainage through the stent.
Unfortunately, only about 20 people out of 100 diagnosed with pancreatic cancer are found to have a tumor that is amenable to surgical resection or is borderline resectable. The rest have pancreatic tumors that are too locally advanced to completely remove or have metastatic spread at the time of diagnosis. Even among patients whose cancers are amenable to surgery, statistical data suggest that only 20% live 5 years. Most pancreatic cancer patients do not qualify for a pancreas transplant because of their advanced disease; most pancreas transplants are done in patients with diabetes that results from the removal of the endocrine portion of the pancreas and not for pancreatic cancer. Consequently, remission rates are fair to poor.
If a pancreatic cancer is found when it has grown into important local structures but not yet spread to distant sites, this is described as locally advanced, unresectable (inoperable) pancreatic cancer (stage III). The standard of care in the United States for the treatment of locally advanced cancer is a combination of low-dose chemotherapy given simultaneously with radiation treatments to the pancreas and surrounding tissues. Radiation treatments are designed to lower the risk of local growth of the cancer, thereby minimizing the symptoms that local progression causes (back or belly pain, nausea, loss of appetite, intestinal blockage, jaundice). Radiation treatments are typically given Monday through Friday for about five weeks. Chemotherapy given concurrently (at the same time; FOLFOX combination therapy) may improve the effectiveness of the radiation and may lower the risk for cancer spread outside the area where the radiation is delivered. When the radiation is completed and the patient has recovered, more chemotherapy often is recommended. Recently, newer forms of radiation delivery (proton therapy, stereotactic radiosurgery, gamma knife radiation, Nanoknife, CyberKnife radiation) have been utilized in locally advanced pancreatic cancer with varying degrees of success, but these treatments can be more toxic and are, for now, largely experimental; individuals should discuss with their doctors what treatment(s) are best for their condition.
Once a pancreatic cancer has spread beyond the vicinity of the pancreas and involves other organs, it has become a problem through the system. As a result, a systemic treatment is most appropriate and chemotherapy (for example, nab-paclitaxel [Abraxane] in combination with gemcitabine [Gemzar]) is recommended. Chemotherapy travels through the bloodstream and goes anywhere the blood flows and, as such, treats most of the body. It can attack a cancer that has spread through the body wherever it is found. In metastatic pancreatic cancer, chemotherapy is recommended for individuals healthy enough to receive it. It has been proven to both extend the lives of patients with pancreatic cancer and to improve their quality of life. These benefits are documented, but unfortunately the overall benefit from chemotherapy in pancreatic cancer treatment is modest and chemotherapy prolongs life for the average patient by only a few months. Chemotherapy options for patients with pancreatic cancer vary from treatment with a single chemotherapy agent like Tarceva or Onivyde to treatment with as many as two or three chemotherapy agents or immunotherapy agents given together (for example, capecitabine plus ruxolitinib). The aggressiveness of the treatment is determined by the cancer doctor (medical oncologist) and by the overall health and strength of the individual patient.
Side effects of treatment for pancreatic cancer vary depending on the type of treatment. For example, radiation treatment (which is a local treatment) side effects tend to accumulate throughout the course of radiation therapy and include fatigue, nausea, and diarrhea. Chemotherapy side effects depend on the type of chemotherapy given (less aggressive chemotherapy treatments typically cause fewer side effects whereas more aggressive combination regimens are more toxic) and can include fatigue, loss of appetite, change in taste, hair loss (although not usually), and lowering of the immune system with risk for infections (immunosuppression). While these lists of side effects may seem worrisome, radiation doctors (radiation oncologists) and medical oncologists have much better supportive medications than they did in years past to control any nausea, pain, diarrhea, or immunosuppression related to treatment. The risks associated with pancreatic cancer treatment must be weighed against the inevitable and devastating risks associated with uncontrolled pancreatic cancer and, if the treatments control progression of the cancer, most patients feel better on treatment than they otherwise would.
Pancreatic cancer is a difficult disease. Even for surgically resectable (and therefore potentially curable) pancreatic tumors, the risk of cancer recurrence and subsequent death remains high. Consequently, the prognosis of pancreatic cancer usually ranges from fair to poor. Only about 20% of patients undergoing a Whipple procedure for potentially curable pancreatic cancer live five years, with the rest surviving on average less than two years. For patients with incurable (locally advanced unresectable or metastatic) pancreatic cancer, survival is even shorter; typically, it is measured in months. With metastatic disease (stage IV), the average survival is just over six months. The American Cancer Society statistics suggest that for all stages of pancreatic cancer combined, the one-year survival rate is 20% and the mortality rate is 80%, while the five-year survival rate is 6% with a mortality rate of 94%. These rates are mainly based on patients diagnosed between 1985 and 2004 and are representative of those patients according to the American Cancer Society (ACS). These data-based survival rates are what are available currently, but they are only estimates and are not predictive about what may happen to each individual. Currently, the ACS advises patients to discuss their individual situation and prognosis with their treatment team of physicians. Doctors around the world continue to study pancreatic cancer and strive to improve treatments, but progress has been difficult to achieve.
Doctors and researchers all over the world are hard at work developing better treatments for pancreatic cancer. Cooperative cancer research led by centers of excellence in this country and many others continue daily to test new surgical techniques, radiation strategies, chemotherapy agents, and alternative therapies in an effort to improve care. Given the slow progress experienced over the last quarter century, many doctors feel that every eligible patient with pancreatic cancer should be offered enrollment in a research trial. New cytotoxic combinations of drugs are being tried in clinical trials. For example, Folfirinox, a new combination regimen consisting of four different chemicals has shown increased survival times for patients in clinical trials. In addition, patients who received one of two vaccines, GVAX and CRS-207, showed about a doubling of survival time compared to patients that did not receive the vaccine; this vaccine protocol is still undergoing clinical trials. For a complete list of clinical trials in pancreatic cancer treatment, please check online at http://www.cancer.gov.
Complimentary or alternative medicine is of unclear benefit in pancreatic cancer treatment. No specific complimentary or alternative therapy has been proven beneficial, but many adjunctive treatments have been tried. Compounds such as curcumin, the principle ingredient in turmeric, have shown efficacy in nonhuman research and are being tested in clinical trials in pancreatic cancer. Given the modest benefit derived from chemotherapy and radiation in this disease, alternative approaches in the treatment of pancreatic cancer in conjunction with (rather than instead of) standard treatment is warranted.
At this time, there is no known surveillance strategy to reduce the risk of pancreatic cancer for the general population. With only 48,900 new diagnoses a year, screening blood tests or X-rays have never been proven to be cost effective or beneficial. Additionally, doctors do not routinely screen individuals with family members diagnosed with pancreatic cancer aside from the rare instance where a known genetic risk factor is present. Some researchers suggest vitamin D blood levels above 40 ng/ml may reduce the risk of pancreatic cancer.
There are many fine organizations helping to provide support for individuals and families battling pancreatic cancer. Many hospitals provide support networks utilizing the expertise of trained social workers with experience in caring for people with cancer. Additionally, the Pancreatic Cancer Action Network (PANCAN) and the American Cancer Society both provide information and support for people living with pancreatic cancer. Visit their web sites at http://www.pancan.org and http://www.cancer.org. Diet recommendations can be found at ACS Guidelines on Nutrition and Physical Activity for Cancer Prevention.
Again, both PANCAN and the American Cancer Society are excellent resources for additional information regarding pancreatic cancer. The American Society of Clinical Oncology web site (http://www.cancer.net) also boasts a wealth of information for patients, family members, and professionals interesting in learning more about this disease. November is Pancreatic Awareness Month with the goal to make pancreas care an everyday event (http://daysofyear.com/pancreatic-cancer-awareness-month/).
 Constipatie en hoe je het kunt verslaan!
Constipatie en hoe je het kunt verslaan!
 Histamine-intolerantie:8 oorzaken, symptoomchecklist en vandaag nog verlichting
Histamine-intolerantie:8 oorzaken, symptoomchecklist en vandaag nog verlichting
 Divertikelziekte en diverticulitis
Divertikelziekte en diverticulitis
 Leaky Gut Takeover:Week 1 Recap
Leaky Gut Takeover:Week 1 Recap
 Spijsverteringsstoornissen:redenen waarom je maag pijn doet
Spijsverteringsstoornissen:redenen waarom je maag pijn doet
 Studie koppelt consumptie van gefermenteerde groenten aan lage COVID-19-sterfte
Studie koppelt consumptie van gefermenteerde groenten aan lage COVID-19-sterfte
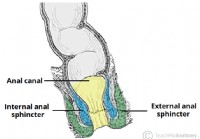 Het anale kanaal
1 anatomische positie 2 Anatomische structuur 2.1 anale sluitspieren 2.2 Interne structuur 3 Anatomische relaties 4 Neurovasculaire toevoer en lymfevaten 5 Klinische relevantie – aambeien Het ana
Het anale kanaal
1 anatomische positie 2 Anatomische structuur 2.1 anale sluitspieren 2.2 Interne structuur 3 Anatomische relaties 4 Neurovasculaire toevoer en lymfevaten 5 Klinische relevantie – aambeien Het ana
 Voedingsmiddelen die diarree veroorzaken (maar zo lekker smaken)
Hey bro, jij daar? zei ik met een vermoeide en zwakke stem. Het was 1 uur s nachts en voor de 8e keer in de afgelopen 4 uur had ik explosieve diarree. Ik pakte mijn telefoon en belde Jordan. Ik had
Voedingsmiddelen die diarree veroorzaken (maar zo lekker smaken)
Hey bro, jij daar? zei ik met een vermoeide en zwakke stem. Het was 1 uur s nachts en voor de 8e keer in de afgelopen 4 uur had ik explosieve diarree. Ik pakte mijn telefoon en belde Jordan. Ik had
 week 1 review over het 8-weekse bloedsuikerdieet
Het is de eerste week van Dr. Michael Mosley s programma, Het 8-weekse bloedsuikerdieet . In een poging om het gewicht te verliezen dat ik ben aangekomen door Small Intestinal Bacterial Overgrowth (SI
week 1 review over het 8-weekse bloedsuikerdieet
Het is de eerste week van Dr. Michael Mosley s programma, Het 8-weekse bloedsuikerdieet . In een poging om het gewicht te verliezen dat ik ben aangekomen door Small Intestinal Bacterial Overgrowth (SI