Pancreaticogastrostomy in pure laparoscopische pancreaticoduodenectomie-A novel pancreas-gastric anastomose techniek -
Abstracte achtergrond
Hoewel veel chirurgische procedures worden nu routinematig laparoscopisch uitgevoerd, pure laparoscopische pancreaticoduodenectomie (LPD) wordt niet vaak uitgevoerd vanwege de technische problemen resectie van pancreas en de bijbehorende procedures reconstructie. Verschillende pancreas-enterische anastomose technieken voor LPD zijn gemeld, maar de meeste zijn aanpassingen van openbare procedures. Om pure LPD te bereiken, achten wij het noodzakelijk om nieuwe alvleesklier-enterische anastomose technieken die specifiek zijn ontwikkeld voor LPD en zijn veilig en haalbaar is om uit te voeren vast te stellen.
Resultaten
Eén patiënt ontwikkelde een postoperatieve pancreas fistel (International Study Group of alvleesklier Fistula criteria, klasse B) en de latere postoperatieve vertraagde maaglediging (International Study Group van de pancreas Chirurgie criteria, klasse C). Geen andere grote complicaties opgetreden. We ontwikkelden een nieuwe alvleesklier-gastric anastomose techniek die ons in staat om pure LPD veilig uit te voeren. De belangrijkste ductus pancreaticus werd een stent met een 4-Fr polyvinyl katheter tijdens pancreas resectie. Een klein gat werd gemaakt in de achterwand van de maag en werd botweg verwijd. Een 5-cm insnijding gemaakt in de voorste maag en de pancreas afvoerbuis werd overgegaan in de maag door het gat in de achterwand. Het restant pancreas werd getrokken in de maag, en is eenvoudig te plaatsen en vastgezet op zijn plaats met slechts 4-6 hechtingen tussen de alvleesklier capsule en het maagslijmvlies. We gebruikten deze techniek om pure LPD uit te voeren op de vijf patiënten die tussen december 2012 en juli 2013.
Conclusies
Onze nieuwe techniek is technisch eenvoudig en biedt een veilige fixatie tussen de maagwand en de alvleesklier. Deze techniek vereist geen grote ductus pancreaticus dilatatie, en het risico van intra-abdominale abcesvorming door postoperatieve pancreatische fistula geminimaliseerd worden. Hoewel deze techniek verder onderzoek omdat het de kans op een vertraagde maaglediging kan toenemen vereist, kan het een bruikbare methode voor het uitvoeren van pancreaticogastrostomy in pure LPD
Trial registratie &ISRCTN16761283 zijn.. Geregistreerd 16 januari 2015.
Sleutelwoorden
Laparoscopy pancreaticoduodenectomie pancreas chirurgie laparoscopische pancreaticoduodenectomie Pancreaticogastrostomy Pancreatic-enterische anastomose Achtergrond
Hoewel veel chirurgische procedures worden nu routinematig laparoscopisch uitgevoerd, pure laparoscopische pancreaticoduodenectomie (LPD) wordt niet op grote schaal uitgevoerd als gevolg van de technische moeilijkheidsgraad van pancreatische resectie en de complexiteit van reconstructie procedures. Als postoperatieve alvleesklier naadlekkage draagt een verhoogd risico op intra-abdominale bloeding en een hoog sterftecijfer [1, 2], sommige chirurgen vermijden intracorporeal wederopbouw, en het gebruik van een hybride laparoscopische-open benadering van de veiligheid en de haalbaarheid van de alvleesklier anastomose [verhogen ,,,0],3, 4]. Hoewel een hybride benadering operatierisico kan verminderen, resulteert ook verlies van de potentiële voordelen van minimaal invasieve chirurgie. Verschillende rapporten hebben beschreven technieken voor laparoscopische pancreaticojejunostomie (PJ), maar de meeste zijn aanpassingen van openbare procedures [5-10]. Evenals in open chirurgie, LPD tot een verhoogd risico op postoperatieve pancreatische fistelvorming bij patiënten met zachte pancreas textuur of een klein ductus pancreaticus. Dit verhoogde risico kan worden toegeschreven aan de technische problemen bij het uitvoeren van de traditionele kanaal naar mucosa anastomose in de pancreas-enterische reconstructie. Vergroting laparoscopie kan nuttig zijn voor deze buis naar mucosa anastomose, maar de bewegingsbeperking van laparoscopische tang maakt het soms moeilijk om de anastomose te voeren. Er zijn een toenemend aantal robotic PD die uitvoering van complexe reconstructie kan vergemakkelijken, maar robotachtige PD is alleen mogelijk voor zeer geselecteerde patiënten [11]. Wij achten het daarom noodzakelijk om nieuwe alvleesklier-enterische anastomose technieken die eenvoudig, haalbaar is om uit te voeren, zorgen voor een veilig fixatie tussen het enterisch muur en de alvleesklier zijn, en zijn specifiek ontwikkeld voor LPD vast te stellen. We beschrijven hier onze nieuwe alvleesklier-gastric anastomose techniek (PG) in pure LPD.
Methods
Van december 2012 tot juli 2013, hebben we onze techniek die gebruikt wordt op de vijf patiënten. Patiënten kwamen in aanmerking voor deze procedure als zij waren niet-obese zonder eerdere bovenste abdominale chirurgie. Drie patiënten hadden intraductal papillaire mucinous gezwellen, één had carcinoom van de papil van Vater, en men had solide pseudopapillary neoplasma. Voor de operatie werden de tumoren volledig geëvalueerd door abdominale computertomografie, magnetische resonantie beeldvorming en endoscopische echografie. Alle tumoren werden beperkt tot de pancreaskop of periampullaire regio. De patiënten waren drie mannen en twee vrouwen met een mediane leeftijd van 64 jaar (range, 47-76 jaar) en een gemiddelde body mass index van 22,2 kg /m
2 (bereik, 17,4-25,5 kg /m 2). De patiënten waren allemaal Oost-Azië en woonde in het oostelijk deel van Japan. De voor- en nadelen, en de potentiële risico's van de chirurgische ingreep werden de patiënten uitgelegd en geïnformeerde toestemming werd verkregen. Gegevensregistratie en evaluatie werd goedgekeurd door de ethische commissie van Toranomon ziekenhuis en was in overeenstemming met de Verklaring van Helsinki.
Techniek
Chirurgie onder algemene verdoving werd uitgevoerd met de patiënt in rugligging met de benen uit elkaar. De eerste 12-mm umbilical trocar ingebracht was een electrolaparoscope (LTF-VH, Olympus Medical Systems, Tokyo, Japan) met een mini-laparotomie techniek en een pneumoperitoneum opgericht met een CO 2 druk van 10 mmHg. Drie 12-mm trocar (links subcostal en bilaterale supraumbilical pararectal) en een 5 mm trocar (rechts subcostal) werden in de buikwand. De chirurg stond aan de rechterzijde van de patiënt tijdens de reconstructie. Na mobilisatie van de kop van de pancreas, werd een tunnel gevormd tussen het achterste deel van de hals van de pancreas en de superieure mesenterische en portale aderen. Indien mogelijk, is de tunnel verlengd 2-3 cm naar het lichaam van de pancreas als voorbereiding op eenvoudige reconstructie. Het lichaam van de alvleesklier werd vervolgens langzaam en voorzichtig ontleed met behulp van laparoscopische coagulatie scharen (SonoSurg ™, Olympus Medical Systems). De belangrijkste ductus pancreaticus werd geïdentificeerd en werd dwars helft van zijn breedte met een schaar en een stent met een 4-Fr polyvinyl katheter (MD-41513 ductus pancreaticus buis, 65 cm; Sumitomo Bakelite, Tokyo, Japan). De buis werd stevig bevestigd aan het distale alvleesklier op twee plaatsen met 3-0 absorbeerbare hechtingen (Vicril ™ 3-0, Ethicon).
Wederopbouw
Na excisie van het proximale gedeelte van de pancreas, werd het monster verwijderd via de navelstreng trocar site, die werd verlengd tot 3 cm. Het distale gedeelte van het restant pancreas werd ontleed uit de milt slagader, ader milt en bindweefsel laparoscopische scharen coagulatie, tot 3 cm voorbij de doorsnijding vlak, als voorbereiding op invaginatie in de maag. Twee verankeren hechtingen (Ti-Cron ™ 3-0, Covidien) werden geplaatst in het overblijfsel alvleesklier, 2 cm distaal van de doorsnijding vlak (afb. 1 en Aanvullende bestandsinformatie 1). Na het bepalen van de plaats van de anastomose (meestal de achterwand van het onderlichaam van de maag), werd een klein gat in de maag serosa van de geplande anastomotische plek door elektrocauterisatie en het gat werd bot verwijd met een pincet (Fig. 2 en Aanvullende bestandsinformatie 2). Een 5 cm verticale incisie werd vervolgens in de voorste wand van de maag alleen ventraal van de geplande anastomotische plek laparoscopische coagulatie schaar (fig. 3 en aanvullende bestandsinformatie 3). De verankering twee hechtingen en stenting buis werden door het gat aan de anastomotische plek en getrokken in de maag met behulp van pincet ingebracht door de incisie maag. Het restant pancreas werd dan getrokken in de maag door het gat aan de anastomotische plek en op zijn plaats met de verankering hechtingen vast, het verzorgen van de alvleesklier (afb. 4 en Extra file 4) niet te verwonden. Na het trekken van de rest pancreas 2-3 cm in de maag, waren 4-6 onderbroken hechtingen (Vicril ™ 3-0, Ethicon) geplaatst tussen de alvleesklier capsule en het maagslijmvlies (Fig. 5 en extra file 5). De stenting buis werd door de incisie in de voorste wand van de maag en de incisie werd gesloten met een doorlopende absorbeerbare hechtdraad (PDS ™ 4-0, Ethicon). De stenting buis werd vervolgens door de buikwand (meestal links subcostal) een gastrostomie (fig. 6) te vormen. Fibrinelijm werd geplaatst rond de PG ter bescherming. Een profylactische drainage buis (Multi-Channel ™ Drainage Set 6,5 mm, Covidien) werd geplaatst op de pancreas anastomose. Fig. 1 Twee verankering hechtingen werden in het overblijfsel pancreas, 2 cm distaal van de doorsnijding vlak. De belangrijkste alvleesklierbuis reeds een stent met een 4-Vr polyvinyl katheter. A: foto, B: illustratie
Fig. 2 Een klein gat werd gemaakt in de maag serosa op het geplande anastomotische site, en werd botweg verwijd met een tang. A: foto, B: illustratie
Fig. 3 Een 5-cm verticale incisie gemaakt in de voorste wand van de maag alleen ventraal van de geplande anastomotische plek, middels coagulatie laparoscopische scharen. A: foto, B: illustratie
Fig. 4 De twee verankering hechtingen en het plaatsen van een stent buis werden doorgegeven door het gat, en het overblijfsel alvleesklier werd vervolgens getrokken in de maag en vastgezet. A: foto, B: illustratie
Fig. 5 Na het trekken van de rest pancreas 2-3 cm in de maag werden 5:56 onderbroken hechtingen geplaatst tussen de pancreas capsule en het maagslijmvlies. A: foto, B: illustratie
Fig. 6 De stenting buis werd door de buikwand van een gastrostomie vormen. A: foto, B: illustratie
Resultaten
Alle procedures werden uitgevoerd door dezelfde chirurg (tabel 1). De pancreas textuur was zacht bij alle patiënten. De mediane schatting bloedverlies was 100 ml (range, 0-400 ml) en de mediane operatieduur was 492 min (range, 435-739 min). De mediane opnameduur was 35 dagen (bereik, 19-57 dagen). De externe afvoerbuis werd achtergelaten in de plaats voor een mediaan van 20 dagen na de operatie (range, 18-22 dagen) en de afvoerbuis aan de anastomotische plek werd achtergelaten in de plaats voor een mediaan van 24 dagen na de operatie (bereik, 17- 41 dagen). Eén patiënt ontwikkelde een postoperatieve pancreas fistel van International Study Group van Pancreatic Fistula (ISGPF) rang B [12] op postoperatieve dag 7, en vervolgens ontwikkeld postoperatieve vertraagde maaglediging van International Study Group of pancreas Chirurgie (ISGPS) rang C [13]. Beide complicaties opgelost conservatieve behandeling. Geen grote complicaties opgetreden bij de andere patiënten, en de postoperatieve follow-up periode was saai (range, 7,7-15,5 maanden). Alle resectie marges waren tumorvrij op bevroren sectie examination.Table 1 Patiënten demografie en chirurgische resultaten
Case
Diagnose
ope tijd (min)
bloedverlies ( ml)
stenting buis
PF (ISGPF)
DGE (ISGPS)
Lengte van het verblijf (dagen)
1
ampullaire ca
492
0
internal
B
C
50
2
IPMN
739
350
external
0
A
57
3
IPMN
599
400
external
0
A
35
4
IPMN
435
100
external
0
A
29
5
SPN
450
100
external
0
0
19
Ampullaire ca
carcinoom van de ampulla van Vater, IPMN
intraductal papillaire mucinos neoplasma, SPN
stevige pseudo-papillaire neoplasma, PF
pacreatic fistel, DGE
vertraagde maaglediging
Discussie
De incidentie van postoperatieve pancreatische fistula varieert van 2 tot meer dan 20% na een open pancreaticoduodenectomie [13], en 1,8-20% na LPD [6, 7, 9, 10]. Het is belangrijk om een goede pancreas-enterische anastomose te realiseren, omdat een postoperatieve pancreatische fistula kan leiden tot ernstige complicaties, langdurige ziekenhuisopname en mortaliteit [1, 2]. Minilaparotomy is geadviseerd om veilige anastomose te garanderen. Hoewel een hybride laparoscopische open techniek operatierisico kan verminderen, resulteert ook verlies van de potentiële voordelen van minimaal invasieve chirurgie. We ontwikkelden een nieuwe PG techniek om veilig wederopbouw in pure LPD in te schakelen.
Hoewel PG heeft een aanvaardbare methode van de wederopbouw werd overwogen na pancreaticoduodenectomie in de afgelopen 50 jaar, is er nog steeds controverse over de relatieve superioriteit van PG versus PJ in termen van uitkomsten. Weller et al. gemeld dat PG was superieur aan PJ qua postoperatieve pancreatische fistelvorming beoordeeld volgens de criteria ISGPF [14]. Ook de recente meta-analyse uitgevoerd op PJ vs PG na PD gebleken dat PG lijkt superieur PJ in vermindering van de incidentie van pancreatische fistelvorming en intra-abdominale vloeistofverzamelsysteem [15-17]. Ondernemingen De standaard pancreas-enterische anastomose uitgevoerd tijdens de LPD is PJ. Slechts één geval bericht heeft reconstructie beschreven PG in LPD [18]. In die zaak werd het overblijfsel alvleesklier geïnvagineerde in de maag en is vastgezet met twee continue purse-string hechtingen rond de incisie in de maagwand met behulp van zelf-behoud monofilament hechtingen (V-Loc 180 3-0, Covidien). Onze techniek is relatief eenvoudiger uit te voeren. We hebben een klein gaatje in de achterwand van de maag en verwijde het bot. Het restant pancreas werd vervolgens getrokken in de maag en eenvoudig te plaatsen, zodat slechts een enkele hechtingen nodig waren tussen de pancreas capsule en maagslijmvlies te zijn plaats te houden.
LPD, is reconstructie meestal uitgevoerd door end-to-side PJ met duct naar mucosa anastomose [5-7]. Evenals in open chirurgie, LPD tot een verhoogd risico op alvleesklier fistelvorming bij patiënten met een kleine ductus pancreaticus. Dit verhoogde risico kan worden toegeschreven aan de technische problemen bij het uitvoeren van het kanaal naar mucosa anastomose gedeelte van de pancreas-enterische reconstructie. Bij deze patiënten kan vergroting laparoscopie nuttig zijn voor het uitvoeren duct te mucosa anastomose, maar de bewegingsbeperking van laparoscopische tang maakt dit soms moeilijk anastomose. Onze techniek geen kanaal naar mucosa anastomose vereisen, en kan gemakkelijk worden gebruikt bij patiënten met een kleine ductus pancreaticus.
Onze techniek kan ook het risico van intra-abdominale abcessen verlagen door geringe lekkage van pancreassap van gewonden alvleesklier capsule, omdat de hechtingen tussen de pancreas en de maagwand worden geplaatst in de maag. Schade aan de pancreas capsule buiten de maag te voorkomen, kan deze techniek veilig bij patiënten met een zachte pancreas textuur zijn.
Eén patiënt in onze serie ontwikkelden een postoperatieve pancreatische fistels (ISGPF klasse B). Bij deze patiënt werden slechts twee hechtingen geplaatst tussen de pancreas capsule en het maagslijmvlies, die waarschijnlijk onvoldoende en kan hebben bijgedragen tot fistelvorming. Om het risico op postoperatieve pancreas fistula na PG te verminderen, raden wij de plaatsing van een voldoende aantal hechtingen tussen de alvleesklier capsule en het maagslijmvlies.
Deze patiënt kreeg ook slechts een korte interne plastic stent over de PG website. Een meta-analyse van gerandomiseerde klinische trials bleek dat plaatsing van een stent in de ductus pancreaticus niet de incidentie van postoperatieve pancreatische fistels niet verminderen. Echter, subgroep analyse bleek dat het gebruik van een externe stent significant de incidentie van postoperatieve pancreas fistel [19]. Andere gerandomiseerde klinische studies bleek dat externe kanaal stenting na pancreaticoduodenectomie verminderde het risico van klinisch relevante postoperatieve pancreas fistel vorming [20, 21]. Het merendeel van de geselecteerde patiënten van deze studies gebruikt PJ wederopbouw en subgroepanalyse externe buis stent in PG werd niet gemeld. Plaatsing van een externe stent in de PG anastomose is niet noodzakelijk een essentieel onderdeel van PG, maar kan worden gebruikt aanhangsel van het risico van pancreatische fistelvorming verminderen.
Een van de nadelen van onze techniek is dat dit kan leiden tot vertraagde gastrische legen, dat is een van de meest voorkomende postoperatieve complicaties pancreatische chirurgie, optreedt in 19-57% van de patiënten [13]. Bij patiënten met PG, maag peristaltiek wordt verstoord omdat de achterwand van de maag wordt vastgehouden door de PG anastomose. Bovendien insnijding van de voorste wand van de maag verhoogt het risico van vertraagde maaglediging [22]. In onze techniek, wordt de voorste wand van de buik ingesneden, gehecht, en aan de buikwand van de gastrostomie die vertraagde maaglediging kan veroorzaken. Ondernemingen De langdurige en oncologische chirurgische resultaten na gebruik van onze procedure voldoet onderzocht, en toekomstig onderzoek moet onderzoeken of LPD biedt significante voordelen ten opzichte van andere methoden voor het uitvoeren van pancreaticoduodenectomy. Het is moeilijk om elk geluid conclusies over de veiligheid of de beperkingen van onze techniek met zo weinig informatie over de selectie van patiënten te trekken, maar we beschouwen onze techniek een relatief eenvoudige methode voor de wederopbouw in pure LPD. De techniek kan ook een alternatieve reconstructiemethode voor gebruik in een hybride procedure. Wederopbouw PG LPD nog een nieuwe techniek, verdere klinische evaluatie resultaten vergelijken tussen het gebruik van PG en PJ LPD gerechtvaardigd.
Conclusies
Wij presenteren een nieuwe pancreas-gastrische anastomose techniek specifiek voor LPD . Onze nieuwe techniek is technisch eenvoudig en biedt een uitstekende fixatie tussen de maagwand en de alvleesklier. Alvleesklier duct dilatatie is niet vereist, en het risico van intra-abdominale abcesvorming wordt geminimaliseerd. Hoewel de verdere klinische evaluatie nodig is, deze techniek is direct klinisch toepasbaar en kan dienen als basis voor aanvullend onderzoek
Afkortingen
LPD.
Laparoscopische pancreaticoduodenectomie
PJ:
pancreaticojejunostomie
PG:
Pancreaticogastrostomy
ISGPF:
International Study Group van Pancreatic Fistula
ISGPS:
International Study Group of pancreas Chirurgie
verklaringen
Extra bestanden
Extra file 1: Twee verankering hechtingen werden geplaatst het overblijfsel pancreas, 2 cm distaal van de doorsnijding vlak. De belangrijkste alvleesklierbuis reeds een stent met een 4-Vr polyvinyl katheter. Extra file 2: Een klein gat werd gemaakt in de maag serosa op het geplande anastomotische site, en werd botweg verwijd met een tang. Extra bestand 3: Een 5-cm verticale incisie gemaakt in de voorste wand van de maag alleen ventraal van de geplande anastomotische plek, middels coagulatie laparoscopische scharen. Extra bestand 4: De twee verankering hechtingen en het plaatsen van een stent buis werden doorgegeven door het gat, en het overblijfsel alvleesklier werd vervolgens getrokken in de maag en op zijn plaats vast. Extra bestand 5: Na het trekken van de rest pancreas 2-3 cm in de maag, 05:56 onderbroken hechtingen geplaatst tussen de pancreas capsule en het maagslijmvlies. Tegenstrijdige belangen Ondernemingen De auteurs verklaren dat ze geen concurrerende belangen. Bijdragen
Authors '
MM, SH, HS, en KS voerde de chirurgische procedures. MM en KS verzamelde gegevens, bereid het manuscript en vergrootten de analyse en interpretatie van de resultaten. GW bijgedragen tot de analyse en interpretatie van de resultaten. Alle auteurs gelezen en goedgekeurd het definitieve manuscript.
 Hoe voorkom je een opgeblazen gevoel, zure oprispingen en meer voor de feestdagen
Hoe voorkom je een opgeblazen gevoel, zure oprispingen en meer voor de feestdagen
 Dieet en voeding beïnvloeden het microbioom in het colonslijmvlies
Dieet en voeding beïnvloeden het microbioom in het colonslijmvlies
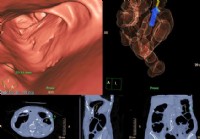 Virtuele colonoscopie
Virtuele colonoscopie
 Gezondheidsvoordelen van slapen met een wigkussen
Gezondheidsvoordelen van slapen met een wigkussen
 Hoe maak je thuis 24-uurs yoghurt met geitenmelk (stap voor stap met afbeeldingen)
Hoe maak je thuis 24-uurs yoghurt met geitenmelk (stap voor stap met afbeeldingen)
 kip yakitori spiesjes met regenboog bloemkoolrijst
kip yakitori spiesjes met regenboog bloemkoolrijst
 orale sorbitol
Diavoorstelling over constipatiemythen en feiten Aambeien Diavoorstelling Afbeeldingen Constipatie:te eten voedsel, te vermijden voedsel Wat is orale sorbitol? Wat zijn de toepassingen van orale sor
orale sorbitol
Diavoorstelling over constipatiemythen en feiten Aambeien Diavoorstelling Afbeeldingen Constipatie:te eten voedsel, te vermijden voedsel Wat is orale sorbitol? Wat zijn de toepassingen van orale sor
 Habba-syndroom Symptomen en behandeling
Habba-syndroom is een term bedacht door Saad F. Habba, MD Dr. Habba heeft de theorie gepostuleerd dat diarree-dominante IBS (IBS-D) en functionele diarree zijn catch-all termen voor andere identificee
Habba-syndroom Symptomen en behandeling
Habba-syndroom is een term bedacht door Saad F. Habba, MD Dr. Habba heeft de theorie gepostuleerd dat diarree-dominante IBS (IBS-D) en functionele diarree zijn catch-all termen voor andere identificee
 Is een luscolostoma permanent?
Wat is een colostoma? Een colostoma is een chirurgische ingreep waarbij een stoma of opening in de dikke darm wordt gemaakt die via door de buik gaan. Bij een luscolostoma is de hele lus van de dik
Is een luscolostoma permanent?
Wat is een colostoma? Een colostoma is een chirurgische ingreep waarbij een stoma of opening in de dikke darm wordt gemaakt die via door de buik gaan. Bij een luscolostoma is de hele lus van de dik