Et høyt nivå av TMB (TMB-H), som gjenspeiler forhøyet totalt antall ikke-synonyme somatiske mutasjoner per kodende område av et tumorgenom og normalt avledet fra genpaneltesting, er anerkjent som en lovende biomarkør for ICI -behandlinger av forskjellige solide kreftformer. Derimot, i klinisk praksis, det er ikke mulig å utføre genpaneltesting for alle kreftpasienter.
Dr. Yoshifumi Shimada og kolleger fra divisjonen for fordøyelses- og generell kirurgi, Graduate School of Medical and Dental Sciences, Niigata University, betraktet TMB-H fra en spesifikk CRC-pasientundergruppe, som en mer robust markør for å forutsi effekten av ICI, og utviklet et konvolusjonelt neuralt nettverk (CNN) - basert algoritme for å forutsi TMB -H CRC direkte fra de histopatologiske egenskapene, spesielt, TIL, hentet fra hematoksylin og eosin (H&E) fargede objektglass. Et representativt mikroskopisk bilde av H &E-farget svulstmutasjonell byrdehøy kolorektal kreftsvulst er vist i den medfølgende figuren, demonstrere tilstedeværelse av tumorinfiltrerende lymfocytter i signifikant forhøyet nivå sammenlignet med normalt omkringliggende vev.
Digital informasjon fra slike neoplastiske og ikke-neoplastiske bilder hentet fra JP-CRC-kohort blir transformert og normalisert for å bygge en prediktiv Convoluted Neural Network-modell som bruker Inception V3-læringsmodell, av Dr. Shimada -gruppen. Den CNN-baserte modellen utviklet av Dr. Shimada og kolleger har potensial til ikke bare å redusere byrden med riktig diagnose på patologer, men også gi den nødvendige informasjonen om pasientenes respons på ICI-baserte terapier, uten bruk av dyre, tidkrevende og ikke lett tilgjengelig genpaneltesting. Denne studien av Dr. Shimada og kolleger er publisert i en nylig utgave av Journal of Gastroenterology (2021; bind 56:s. 547-559; https:/
I tillegg, studiene av Dr. Shimada-gruppen ga også midler til å forutsi TMB-H CRC bare ved å bruke TIL-informasjonen fra H &E-lysbildene fra pasientenes tumorvev. Derimot, med tanke på at pasientene i den studerte kohorten ikke ble behandlet med noen ICI, ingen konklusjoner kunne trekkes om deres ICI-respons etter TMB-H-diagnosen, og det ble foreslått at fremtidige kliniske studier må utføres for å ta opp om TIL alene kan være nyttig som en prediktiv biomarkør for effekten av ICI.
Dr. Shimada sier om den nåværende studien:" Vi har utviklet kunstig intelligens for å forutsi genetiske endringer i tykktarmskreft ved dyp læring ved bruk av hematoksylin og eosin -lysbilder. Denne kunstige intelligensen er viktig for å løse kostnadsproblemene knyttet til genetisk analyse og tilrettelegge for personlig medisin mot tykktarmskreft . "
Alt i alt, studiene av Dr. Shimada og medarbeidere gir en kostnadseffektiv og tidseffektiv og pålitelig metode for å informere klinikerne om CRC-pasienten de administrerer kan ha nytte av Immune Checkpoint Inhibitor (inkludert hemmere av PD-1-proteinet og dets ligand, PD-L1) terapi, uten å implisere bruken av genpanel.
 Oral sex kan utløse bakteriell vaginose
En ny studie publisert i tidsskriftet PLOS Biologi har avslørt forskjellige mikrobielle populasjoner som kan lette vaginal kolonisering av patogener, som igjen kan forlenge egenskapene til bakteriel
Oral sex kan utløse bakteriell vaginose
En ny studie publisert i tidsskriftet PLOS Biologi har avslørt forskjellige mikrobielle populasjoner som kan lette vaginal kolonisering av patogener, som igjen kan forlenge egenskapene til bakteriel
 Menn som spiser yoghurt to ganger i uken er mindre sannsynlig å utvikle tarmkreft
Ny forskning har avslørt at menn som spiser to eller flere porsjoner yoghurt per uke, kan redusere risikoen for å utvikle kreft før kreft som kan føre til tarmkreft. Hvis resultatene kan replikeres, y
Menn som spiser yoghurt to ganger i uken er mindre sannsynlig å utvikle tarmkreft
Ny forskning har avslørt at menn som spiser to eller flere porsjoner yoghurt per uke, kan redusere risikoen for å utvikle kreft før kreft som kan føre til tarmkreft. Hvis resultatene kan replikeres, y
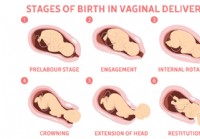 Hva er bedre? Naturlig fødsel, eller en keisersnitt?
Gratulerer, du skal ha en baby, og det er nå på tide å planlegge ankomsten av gledesbunten din. Fødselslegen din kan ha tilbudt deg valget mellom en naturlig (vaginal) fødsel eller et elektivt keisers
Hva er bedre? Naturlig fødsel, eller en keisersnitt?
Gratulerer, du skal ha en baby, og det er nå på tide å planlegge ankomsten av gledesbunten din. Fødselslegen din kan ha tilbudt deg valget mellom en naturlig (vaginal) fødsel eller et elektivt keisers