O DIBSS-C foi desenvolvido pelo Grupo de Trabalho da Síndrome do Cólon Irritável (IBS) do Consórcio PRO para apoiar os parâmetros de eficácia baseados em sintomas em ensaios clínicos para produtos destinados ao tratamento de IBS com predominância de constipação (IBS-C) em adultos. A qualificação do DIBSS-C representa um marco importante para o Grupo de Trabalho IBS e é a quarta avaliação de resultados clínicos (COA) do Consórcio PRO a ser qualificado através do Programa de Qualificação COA dentro do Centro de Avaliação e Pesquisa de Medicamentos da FDA.
"A colaboração de várias partes interessadas dentro do Consórcio PRO do Critical Path Institute, inclusive de patrocinadores, pacientes, especialistas em medição e a FDA têm sido fundamentais para permitir a incorporação da voz do paciente no desenvolvimento de medicamentos IBS e na rotulagem de produtos.
A disponibilidade do DIBSS-C para uso em ensaios IBS-C é uma grande vitória para os pacientes, uma vez que visa avaliar o impacto do tratamento nos sintomas que são importantes para eles e informar sua tomada de decisão de tratamento para esta condição onerosa, "afirmou Robyn T. Carson, MPH, Vice presidente, Pesquisa de Resultados Centrada no Paciente, na AbbVie e co-presidente do Grupo de Trabalho IBS do PRO Consortium.
A SII é um distúrbio intestinal funcional crônico caracterizado por episódios recorrentes de dor abdominal associada a alterações nos movimentos intestinais. Diagnóstico de distúrbios intestinais funcionais, como IBS, baseia-se em critérios de sintomas porque não existem biomarcadores diagnósticos consistentes e confiáveis. Como esses sintomas estão sujeitos à variabilidade natural, o DIBSS-C foi desenvolvido como um diário baseado em eventos para facilitar a coleta de dados confiáveis em ensaios clínicos que avaliam tratamentos para essa condição.
A qualificação do DIBSS-C exemplifica o compromisso da FDA com as necessidades da comunidade de doenças gastrointestinais. É uma indicação clara de que as vozes dos pacientes estão sendo ouvidas e uma grande vitória para a comunidade como um todo. O IFFGD tem orgulho de fazer parte do Grupo de Trabalho IBS do PRO Consortium e estamos entusiasmados em ver a ênfase contínua em atender às verdadeiras necessidades dos pacientes, ouvindo as vozes dos pacientes . "
Ceciel T. Rooker, Presidente da Fundação Internacional para Doenças Gastrointestinais e Participante do Grupo de Trabalho IBS, Critical Path Institute
O DIBSS-C significa um avanço importante na avaliação PRO no desenvolvimento de medicamentos para IBS-C e reflete o compromisso da FDA com o desenvolvimento de medicamentos com foco no paciente por meio da qualificação de COAs que capturam válidos, de confiança, e dados significativos. Stephen Joel Coons, Ph.D., o Diretor Executivo do Consórcio PRO, afirmou que, "A qualificação do DIBSS-C é uma conquista incrivelmente gratificante para o PRO Consortium. É o resultado de uma quantidade substancial de tempo e esforço investidos pela C-Path, nossos parceiros da indústria, consultores clínicos e de medição, FDA, e os pacientes que participaram deste projeto muito valioso. O DIBSS-C tem o potencial de mudar o paradigma de medição atual para avaliar o benefício clínico em ensaios de tratamento para IBS-C. "
 30 receitas SIBO para o Dia da Austrália
30 deliciosas receitas amigáveis da SIBO para o Dia da Austrália Se você é como eu, seu Dia da Austrália será repleto de churrascos e celebrações de piquenique. É um ótimo momento para descontrair,
30 receitas SIBO para o Dia da Austrália
30 deliciosas receitas amigáveis da SIBO para o Dia da Austrália Se você é como eu, seu Dia da Austrália será repleto de churrascos e celebrações de piquenique. É um ótimo momento para descontrair,
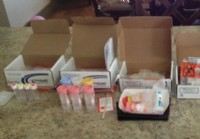 Como encontrar a causa raiz de seus problemas digestivos
Esta é uma foto do meu regime anual de re-teste. Inclui uma variedade de exames de sangue da melhor qualidade, exames de urina, exames de saliva e exames de fezes... OH MY! Este ano, isso me custou
Como encontrar a causa raiz de seus problemas digestivos
Esta é uma foto do meu regime anual de re-teste. Inclui uma variedade de exames de sangue da melhor qualidade, exames de urina, exames de saliva e exames de fezes... OH MY! Este ano, isso me custou
 Como alimentar sua microbiota intestinal com as fibras necessárias
Todos nós já ouvimos que a fibra é essencial para nossa microbiota intestinal e, portanto, para nossa saúde geral, mas isso significa que toda vez que comemos um lanche rico em fibras, estamos realmen
Como alimentar sua microbiota intestinal com as fibras necessárias
Todos nós já ouvimos que a fibra é essencial para nossa microbiota intestinal e, portanto, para nossa saúde geral, mas isso significa que toda vez que comemos um lanche rico em fibras, estamos realmen