Um novo estudo publicado na revista
Natureza mostra que existem literalmente centenas de vírus grandes o suficiente para consumir bactérias, e com propriedades que são típicas de um organismo vivo, em vez dos pacotes não vivos auto-replicantes de DNA / RNA que os vírus costumam ser considerados.
p Esses vírus são chamados de bacteriófagos - literalmente, comedores de bactérias - e fagos, para abreviar. Embora os fagos já existam há muito tempo, esses novos fagos são surpreendentes em termos de tamanho e sistemas biologicamente complexos. Muitos de seus genes são geralmente encontrados em bactérias e são usados para atacar as bactérias hospedeiras.
O processo
p Onde os cientistas encontraram esses fagos enormes e raros? Eles se debruçaram sobre um vasto banco de dados de sequências de DNA obtidas de uma ampla e diversa gama de ambientes na Terra. Esses quase 30 microbiomas abrangem o espectro de uma fonte termal no Tibete, por meio de biorreatores na África do Sul, ao intestino de uma mulher carregando um bebê no útero. Outros locais incluem furos subterrâneos, oceanos, lagos, e o intestino de um bebê prematuro.
p A pesquisadora Jill Banfield vem fazendo isso há mais de uma década e meia. Ela calcula as sequências de todos os bits de DNA em qualquer amostra que obtém de um local na Terra. Ela então ajusta as peças do quebra-cabeça para obter a sequência genômica.
p Na maioria dos casos, ela obtém um esboço do genoma, mas alguns foram confirmados como genomas de micróbios inteiramente novos. Alguns desses micróbios são regulados por minúsculos genomas que, na verdade, parecem incapazes de sustentar a vida de forma independente, e, em vez disso, são totalmente dependentes de outras formas de vida, nomeadamente, archaea e bactérias.
Fagos de genoma grande
p Há um ano ela relatou a descoberta de fagos grandes, que ela apelidou de fagos de Lak, no intestino e na boca humanos. Esses fagos comem bactérias na saliva e no intestino.
p No novo jornal, ela relata o isolamento de mais de 350 fagos muito grandes com genomas que são, com comprimentos de 200, 000 bases, quatro vezes maior do que a sequência genética média de qualquer bacteriófago conhecido até agora (50 kb). Comentários Banfield, "Estamos explorando os microbiomas da Terra, e às vezes acontecem coisas inesperadas. "
p O maior sequenciado até agora tem um genoma que abrange 735 surpreendentes, 000 pares de bases, que é cerca de 15 vezes o tamanho do genoma médio do fago, e de fato, marcadamente maior do que muitos genomas bacterianos. Mas poderia ser maior ainda, uma vez que eles sequenciaram apenas 175 desses grandes fagos até agora.
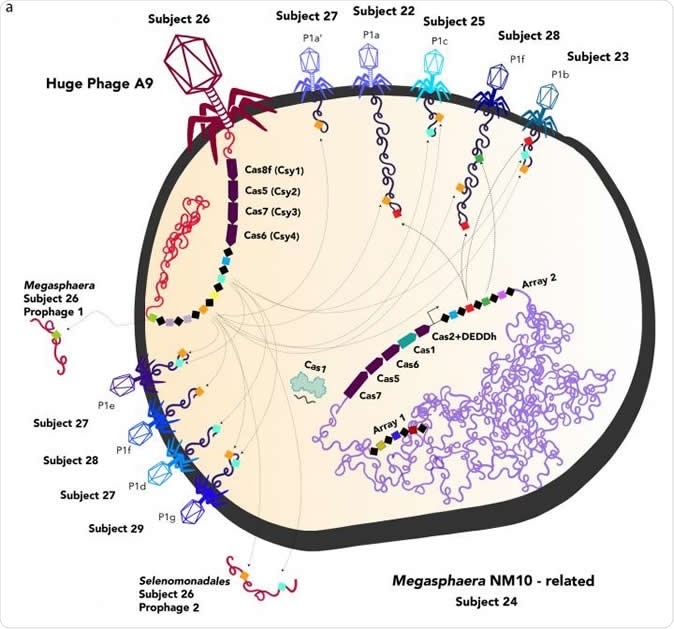 Representação de fagos enormes (vermelho, esquerda) e fagos normais que infectam uma célula bacteriana. O enorme fago injeta seu DNA na célula hospedeira, onde as proteínas Cas - parte do sistema imunológico CRISPR normalmente encontrado apenas em bactérias e arquéias - manipulam a resposta da célula hospedeira a outros vírus. A equipe da UC Berkeley ainda não fotografou nenhum fago enorme, então todos são representados parecendo o tipo mais comum de fago, T4. Crédito da imagem:imagem da UC Berkeley cortesia do laboratório Jill Banfield
Representação de fagos enormes (vermelho, esquerda) e fagos normais que infectam uma célula bacteriana. O enorme fago injeta seu DNA na célula hospedeira, onde as proteínas Cas - parte do sistema imunológico CRISPR normalmente encontrado apenas em bactérias e arquéias - manipulam a resposta da célula hospedeira a outros vírus. A equipe da UC Berkeley ainda não fotografou nenhum fago enorme, então todos são representados parecendo o tipo mais comum de fago, T4. Crédito da imagem:imagem da UC Berkeley cortesia do laboratório Jill Banfield Um murmúrio de fagos
p Esses grandes fagos foram classificados em dez clados ou grupos. Cada um foi denominado "Big fago", embora use idiomas diferentes, ou palavras diferentes no mesmo idioma. Os idiomas são os do país de origem dos pesquisadores. Assim, existe um clado Mahaphage, um Biggiephage, um Judaphage, um Kaempephage, um Dakhmphage, um Jabbarphage e um Kabirphage, bem como um Enormefago, Whopperphage, e clado Kyodaiphage - em sânscrito, Inglês australiano, Chinês, Dinamarquês, Árabe (os próximos três), Francês, Inglês americano, e japonês!
Armas bacterianas dentro de vírus?
p Os genes bacterianos dentro desses fagos contêm alguns elementos CRISPR, edição de genes que codificam segmentos de proteína, que são usados por bactérias para resistir ao ataque viral. Os cientistas acham que esses elementos devem se tornar parte do sistema CRISPR do hospedeiro, capacitando as bactérias a resistir a outros vírus para que esses grandes fagos possam desfrutar de sua refeição sem interrupções. Outro pesquisador, Basem Al-Shayeb, explica que esses fagos usam este sistema para seu próprio benefício, "para alimentar a guerra entre esses vírus."
p Outro elemento fascinante em um desses novos fagos é uma proteína que desempenha o mesmo papel que a proteína Cas-9, uma parte integrante da ferramenta de edição de genes CRISPR-Cas9 amplamente usada, introduzida pela primeira vez por Doudna e Charpentier. Esta nova proteína foi chamada de CasØ - a letra Ø, ou phi (em grego), é o símbolo de um fago. Isso faz parte da família Cas-12, mas esses fagos também têm outros elementos CRISPR bacterianos como Cas-9, Cas-X, e proteínas Cas-Y.
p Alguns desses fagos também têm matrizes CRISPR muito grandes. Isso se refere à presença de matrizes compostas de fragmentos de DNA viral, matrizes de memória que permitem o rápido reconhecimento de um ataque repetido por qualquer um desses vírus. Esse, por sua vez, desencadeia reações Cas instantâneas, permitindo o direcionamento específico desses vírus.
Vida ou não vida?
p Outra descoberta surpreendente foi a ocorrência de genes que codificam proteínas ribossomais. O ribossomo é a organela da célula que lê o mRNA e o usa para fazer proteínas específicas. Esta é uma das primeiras ocorrências de genes ribossomais em vírus.
p Eles também encontraram genes que codificam para RNAs de transferência, que são as moléculas que captam os aminoácidos certos para serem incorporados na sequência da proteína. Existem genes reguladores para tRNAs, genes para ligar o processo de síntese de proteínas, e até mesmo alguns segmentos ribossomais. Esses genes são encontrados apenas em formas de vida, uma vez que têm a ver com a fabricação de componentes de proteínas - o que é diferente do que qualquer outro vírus pode fazer, e que é uma capacidade que significa vida.
p O investigador Rohan Sachdeva diz que esta é "uma das principais características definidoras que separam vírus e bactérias, não-vida e vida ”. Ele chama isso de“ confundir um pouco a linha ”.
p Por que esses genes estão lá? Os pesquisadores acham que podem ser usados para sequestrar os ribossomos para começar a replicar as proteínas virais, em vez das bacterianas do hospedeiro. Uma descoberta adicional é a presença de códigos genéticos alternativos, ou o uso de mais de um código genético para denotar o mesmo aminoácido. Esse recurso poderia muito bem desviar o ribossomo bacteriano e levá-lo a decodificar o RNA viral em vez do próprio RNA do hospedeiro.
Implicações
p A descoberta de novas ferramentas usadas na luta entre bactérias e vírus oferece muitas possibilidades para encontrar novas ferramentas de edição de genes. Muitos dos novos genes ainda precisam ser explorados para suas funções, e pode muito bem ser que essas novas proteínas sejam úteis em várias aplicações na indústria, as ciências médicas, ou na agricultura.
p Existem perigos, também. Os vírus transferem genes de uma bactéria para outra - alguns dos quais podem ser responsáveis pela resistência aos antibióticos ou pela virulência (a capacidade de causar doenças). Essa propriedade dos fagos recém-descobertos pode significar que existe o risco de transferir alguns desses genes prejudiciais para o microbioma humano, uma vez que os fagos ocorrem junto com as bactérias.
p Uma vez que o número de genes transportados por esses grandes fagos é marcadamente maior do que os fagos comuns, eles têm uma capacidade maior de mover genes que podem prejudicar outras células. Por sua vez, isso aumenta o risco de que alguns desses genes sejam adquiridos por genes no ambiente humano.
Conclusão
p Completamente, os pesquisadores estão fascinados com a presença de fagos com genomas enormes em uma variedade de microbiomas em toda a Terra. A relação entre esses grandes fagos é interpretada como significando que eles vêm de uma antiga família de vírus de genoma grande.
p Diz Banfield, "Ter grandes genomas é uma estratégia de sucesso para a existência. Esses vírus de bactérias fazem parte da biologia, de replicar entidades, sobre os quais sabemos muito pouco. "
p É verdade. Esses fagos são de um tamanho que os faz caber em algum lugar na lacuna entre as arquéias (os primeiros parentes das bactérias), e fagos comuns que se parecem com coisas não vivas. Banfield os descreve como "estratégias de existência bem-sucedidas que são híbridas entre o que consideramos vírus tradicionais e organismos vivos tradicionais".
 Representação de fagos enormes (vermelho, esquerda) e fagos normais que infectam uma célula bacteriana. O enorme fago injeta seu DNA na célula hospedeira, onde as proteínas Cas - parte do sistema imunológico CRISPR normalmente encontrado apenas em bactérias e arquéias - manipulam a resposta da célula hospedeira a outros vírus. A equipe da UC Berkeley ainda não fotografou nenhum fago enorme, então todos são representados parecendo o tipo mais comum de fago, T4. Crédito da imagem:imagem da UC Berkeley cortesia do laboratório Jill Banfield
Representação de fagos enormes (vermelho, esquerda) e fagos normais que infectam uma célula bacteriana. O enorme fago injeta seu DNA na célula hospedeira, onde as proteínas Cas - parte do sistema imunológico CRISPR normalmente encontrado apenas em bactérias e arquéias - manipulam a resposta da célula hospedeira a outros vírus. A equipe da UC Berkeley ainda não fotografou nenhum fago enorme, então todos são representados parecendo o tipo mais comum de fago, T4. Crédito da imagem:imagem da UC Berkeley cortesia do laboratório Jill Banfield  Gastroenterologista em Fort Pierce, Flórida
Quando se trata de sua saúde, é importante escolher um médico que tenha não apenas uma educação qualificada, mas também experiência e histórico comprovado de tratamento bem-sucedido de pacientes. Nest
Gastroenterologista em Fort Pierce, Flórida
Quando se trata de sua saúde, é importante escolher um médico que tenha não apenas uma educação qualificada, mas também experiência e histórico comprovado de tratamento bem-sucedido de pacientes. Nest
 Agradecimentos, elogios e motivação
Ahh aquela sensação de quando está tudo bem. A camisa, restaurante ou parceiro certo. Não tenho certeza se as palavras podem descrevê-lo adequadamente. É apenas um saber que está bem no fundo. Apost
Agradecimentos, elogios e motivação
Ahh aquela sensação de quando está tudo bem. A camisa, restaurante ou parceiro certo. Não tenho certeza se as palavras podem descrevê-lo adequadamente. É apenas um saber que está bem no fundo. Apost
 Pesticidas e seu microbioma intestinal
As toxinas ambientais estão em toda parte; de pesticidas a PFAS, VOCs a metais pesados, toxinas ambientais invadiram todos os cantos de nossas vidas. E muitos são cancerígenos, desreguladores endócrin
Pesticidas e seu microbioma intestinal
As toxinas ambientais estão em toda parte; de pesticidas a PFAS, VOCs a metais pesados, toxinas ambientais invadiram todos os cantos de nossas vidas. E muitos são cancerígenos, desreguladores endócrin