Študija primerov in kontrol o vplivu Apolipoprotein E genotipi želodca tveganje za nastanek raka in napredovanje
abstraktnih
Ozadje
apolipoprotein E (ApoE) je večnamenski protein igrajo tako pomembno vlogo pri presnovi holesterola in trigliceridov in popravilo tkiva in vnetja. V ApoE
gen (19q13.2) ima tri glavne izooblike s ε2, ε3 in ε4 alelov kodirane z alel ε4 povezano s hiperholesterolemijo in alel ε2 z nasprotnim učinkom. Obratnem sorazmerju ravni holesterola in raka želodca (PK) je bila pred tem poročali, čeprav je razmerje med APOE
genotipov in GC ni bila doslej raziskana.
Metode
raka sto petdeset in šest želodca primerov in 444 bolnišničnih kontrole so genotipizacijo za ApoE polimorfizem (ε2, ε3, ε4 alelov). Razmerje med GC in domnevnih dejavnikov tveganja je bila izmerjena z uporabo prilagojene razmerje obetov (OR) in njihove 95% intervali zaupanja (CIS) iz logistično regresijsko analizo. Gen-okolje analize interakcije bila izvedena. Vpliv genotipa ApoE na preživetje iz GC je raziskati z analizo Kaplan-Meier in Cox proporcionalne regresije nevarnosti modelu.
Rezultati
subjektov, ki opravljajo vsaj eno APOE
ε2 alel pomembno 60% zmanjšanje GC tveganja (OR = 0,40, 95% IZ: 0,19-0,84) v primerjavi z ε3 homozigoti. No pomembne interakcije so nastale med ε4 ali alel ε2 in okoljske izpostavljenosti, niti ε2 ali ε4 alelov so vplivali na mediano časa preživetja, tudi po popravku za starost, spol in stadiona.
Sklepi
Naša raziskava poročila za prvič zaščitni učinek alel ε2 pred GC, ki bi lahko delno pripisuje višje antioksidativne lastnosti ε2 v primerjavi z ε3 ali ε4 alelov. Glede na velikost vzorca Študija je, so potrebne nadaljnje študije za potrditev naših ugotovitev.
Ključne besede
Rak želodca Apolipoprotein E Genetic epidemiologija polimorfizma genov, interakcije z okoljem Ozadje
apolipoprotein E (ApoE) je majhen glikoprotein, ki ima velik vlogo pri potrditvi krvnega holesterola bogati delcev, znan kot Preostali lipoproteini [1]. Poleg svoje prepoznavna vloga v presnovo lipidov, ApoE je bilo dokazano, da se vključijo v številnih patofizioloških procesov, vključno antioksidant in imunskih dejavnosti, kot tudi moduliranega učinek na angiogenezo rast tumorskih celic in indukcijo metastaz [2]. Za strukturni gen (19q13.2) za ApoE
polimorfna z dvema ločenima nukleotidnih polimorfizmov (SNP) v regiji kodiranja, ki izhaja v treh različnih alelov (ε2, ε3, ε4) in šest APOE
genotipov (tri homozigoti ε4 /ε4, ε3 /ε3 in ε2 /ε2, in tri heterozigoti ε4 /ε3, ε3 /ε2, ε4 /ε2), vsak, ki prikazujejo sposobnosti različnih receptorjev za vezavo [3, 4]. Metaanaliza poročali skoraj linearno razmerje med APOE
genotipi in ravni skupnega in LDL serum holesterola (LDL-C), ko se šest genotipi naročenih takole: ε2 /ε2, ε2 /ε3, ε2 /ε4, ε3 /ε3, ε3 /ε4, ε4 /ε4 [5]. Na splošno, v primerjavi s posamezniki z alel ε3, raven skupnega in LDL-C so ponavadi nižje za tiste z alel ε2 in višji za ε4 prevoznikov [6]. V zadnjih dveh desetletjih, so presečne in prihodnje študije poročajo, da so nizko raven holesterola v serumu povezano z višjo non-kardiovaskularno tveganje, še posebej raka tveganja [7-10], zato bolniki z vseh ravni holesterola nizke serumu so bolj verjetno, da trpijo zaradi raka. Do danes je točen razlog za takšno ugotovitev še vedno ni jasno. Različne razlage se lahko daje kot: (i) bi to združenje teoretično odražajo neposredno vzročno vlogo holesterola v raka etiologijo, ali pa je posledica (ii) da se nekaj zavajajočih dejavnikov, ki povzročajo tako nizko raven holesterola in raka, ali (iii) " povratne vzročno zvezo ", saj lahko nizke ravni holesterola preprosto učinek raka in ne vzrok [11].
Da bi v celoti odgovoriti na vprašanje, ali obstaja vzročna zveza med nizko raven holesterola in raka, alternativni epidemioloških pristop, imenovan" Mendelian popačenja "se lahko uporablja za reševanje problema povratne vzročnosti in zavajajoče. V skladu s tem pristopom, genetske variacije (npr apoE
), ki služi kot trden približek za okoljsko spremenljivi izpostavljenosti (npr serum ravni holesterola) se lahko uporablja, da bi vzročnih sklepati o bolezni [12]. Benn et al. [13] sta nedavno pokazala, da je nizek holesterol LDL trdno povezana z rakom v velikem danski kohortni študiji, medtem ko je zmanjšanje LDL s SNP povzročil, vključno apo E
, ni bilo. S sprejetjem pristopa Mendlovo naključnih Benn ugotovila, da so njegovi rezultati v skladu s tistimi, ki so nastale iz kohorte starejših osebah, zdravljenih z pravastatin [14], in od tveganja ateroskleroze v skupnosti kohorte študija [15], vse kaže na nizko raven LDL holesterola so verjetno posledica v predklinični fazi raka in per se
ne povzročajo raka.
vlogo APOE
genotipov na raka želodca (GC) etiologija ni bil doslej exlpored, kot Benn et al. [13] obravnavajo vse raka v prebavilih brez posebnim poudarkom na GC. Do danes, štiri kohorte študije [10, 16-18] raziskati odnos serumsko raven holesterola in razvoj GC med. Med njimi sta dve japonski trdno povezanih raziskav [10, 18] in švedska študija [16] je poročal, da so nizko raven holesterola v serumu neodvisni dejavniki tveganja za nastanek raka na želodcu, predvsem v črevesju histotype. Ne združenje, pa je bilo v veliki finski študiji kohorte [17]. Ker je vprašanje, ali je hypocholesterolemia predispozicijski dejavnik za GC ali predklinični fazi GC ni bil v celoti rešen, si prizadeva naša študija primerov in kontrol, ki temeljijo bolnišnica odpraviti to težavo, ki neposredno gledamo na odnos med APOE
genotipov in GC, kakor tudi njihove interakcije z morebitnimi prilagajanje učinek.
Rezultati
splošne značilnosti študijske populacije, vključno s 156 primeri GC in 444 kontrol, so predstavljene v tabeli 1. porabe alkohola je bila povezana s povečanim tveganjem GC z oddaljenih regij 1,84 (95% CI = 1,10-3,07) in 3,29 (95% IZ = 1,36-7,98) za zmerno in težkih pivcev, oz. Skoraj podvojila GC tveganja (OR = 1,95, 95% IZ: 1,06-3,60) je bila odkrita med posamezniki kajenje več kot 25 pakiranj let. Poleg tega je družinsko anamnezo raka želodca je povzročilo, da je povezana s povečanim tveganjem za GC (OR = 3,14, 95% IZ: 1.17 - 8.44; tabela 1). Tabela 2 prikazuje porazdelitev šestih APO
E genotipov med primerih GC in kontrol, s ε3 /ε2 genotip pa redkeje zastopane v primerih (9,87%) kot v kontrolni skupini (15,67%). Tabela 1 razmerij obetov (95 % CI) za raka želodca glede na izbrane spremenljivke in njihovo distribucijo frekvence med 156 želodca primerov raka in 444 kontrol
primeri
kontrol
ALI (95% CI) †
n (%)
n (%)
Age (povprečje ± SD)
67,05 ± 11,33
59.04 ± 16.00
Moški spol
82 (53,2)
261 (58,8)
0.50 (0.30-0.83)
alkohola pivci
0-6 g /dan
60 (40,5)
251 (57,6)
1 *
7-29 g /dan
71 (48,0)
163 (37,4)
1,84 (1.10- 3.07)
> = 30 g /dan
17 (11,5)
22 (5,0)
3,29 (1.36- 7,98)
kajenje
Nikoli
78 (50,7)
238 (54,2)
1 *
Ever
76 (49,3)
201 (45,8)
1.51 (0.94- 2.45)
Pack-let kajenja
0
74 (51,7)
245 (57,0)
1 *
25/01
31 (21,7)
111 (25,8)
1,40 (0.78- 2.50)
> 25
38 (26,6)
74 (17.2)
1,95 (1.06- 3.60)
sadja in zelenjave vnosa
Visoka ‡
41 (27,5)
116 (27.2)
1 *
Nizka
108 (72,5)
310 (72,8)
1,18 (0.70- 1,98)
meso na žaru
Nizka ^
106 (75,7)
314 (81,1 )
1 *
Visoka
34 (24,3)
73 (18,9)
1,25 (0.72- 2,15)
Telesna dejavnost
Vse
29 (18,6)
93 (20,9)
1 *
Nič
127 (81,4)
351 (79,1)
0,81 (0.45- 1.45)
Družinska anamneza raka
Ne
87 (62,2)
291 (71,2)
1 *
Družinska anamneza raka želodca
10 (7.1)
14 (3.4)
3.14 (1.17- 8.44)
Družinska anamneza drugega raka
43 (30,7)
104 (25,4)
1,09 (0.66- 1,81)
alel frekvenca ApoE
ε3
130 (85,5)
322 (80,1)
ε2
8 (5.3)
39 (9,7)
ε4
14 (9.2)
41 (10,2)
† ALI prilagoditi glede na starost, spol , uživanje alkohola (kot stalna spremenljivke), packyears kajenja, na žaru porabe mesa in zgodovino družinskih raka.
* referenčna kategorija.
‡ vsaj treh obrokov sadja in zelenjave na dan.
^ manj kot štirikrat /mesec.
Tabela 2 Porazdelitev APOE polimorfizma med primerih želodca raka in kontrol
Ohišja ‡
kontrole ^
Vsi primeri
črevesne (n = 79)
difuzna (n = 57)
n (%)
n (%)
OR (95% CI) †
OR (95% CI) †
OR (95% CI) †
ε3 /ε3
109 (71,71)
253 (62,94)
1 *
1 *
1 *
ε3 /ε2
15 (9,87)
63 (15.67)
0,43 (0,21 -0.91)
0,34 (0,13 - 0.92)
0,57 (0,23-1,40)
ε3 /ε4
27 (17.76)
75 (18,66)
0,70 (0,37 - 1,30)
0,75 (0,35 - 1,60)
0,64 (0,27-1,47)
ε2 /ε2
0 (0,00)
5 (1,24)
NC
NC
NC
ε2 /ε4
1 (0,66)
5 (1,24)
1.25 (0,10-15,10)
2,54 (0,21-31,17)
NC
ε4 /ε4
0 (0,00)
1 (0.25)
NC
NC
NC
ε3 /ε2 ali ε2 /ε2
15 (12.10)
68 (21.18)
0,40 (0.19 - 0.84)
0,31 (0,11-0,83)
0,53 (0,21-1,30)
ε3 /ε4 ali ε4 /ε4
27 (19.85)
76 (23.10)
0,68 (0,36 - 1,26)
0,71 (0,34-1,53)
0,62 (0,27 - 1,43).
‡ Apolipoprotein genotip je bil izmerjen v 152 primerih
^ Apolipoprotein genotip je bil izmerjen v 402 kontrol
† ALI prilagojena glede na starost. .. spol, uživanje alkohola (kot stalna spremenljivke), packyears kajenja, na žaru uživanje mesa in družinsko anamnezo raka želodca
* Reference kategorija
NC: ne izračunavajo zaradi nekaj številnih vrednot
Pogostost ApoE.
genotipi spoštovali Hardy-Weinberg Equilibrium (HWE) v kontrolni skupini (p
-vrednost > 0,05, podatki niso prikazani). Iz Večvariantna analiza imela posamezniki imajo najmanj en APOE
alel ε2 precejšnje 60% zmanjšala nevarnost GC (OR = 0,40, 95% CI: 0,19 - 0,84), v primerjavi s tistimi homozigotna za divjega tipa (ε3 /ε3) (tabela 2). Ko so rezultati razvrščeni v razrede po histologijo tumorja je pomembna povezava med APOE
alelov ε2 nosilci in rakom želodca, se zdi, da je omejen na črevesno tipa, z ali 0,31 (95% IZ: 0,11-0,83; tabela 2). kontrole kakovosti so pokazali 100% skladnost med polimorfizem dolžin restrikcijskih fragmentov (RFLP) metoda in DNA sekvenciranje.
Rezultati analize interakcije genov, okolja so predstavljeni v tabeli 3. Statistično pomembnih interakcij pojavile med ε4 ali alel ε2 (p-
vrednost za interakcijo > 0,05), spol, starost, uživanje alkohola ali sadja in zelenjave intake.Table 3 interakcije med APOE genotipov in izbranih demografskih in življenjskega sloga spremenljivke v zvezi z GC izpostavljeno nevarnosti
spremenljivk
zadevah
Controls
Vse E2
Ohišja
Controls
Vse E4
OR (95% CI) †
OR (95% CI) †
Spol
Ženska, e3 /e3
51 ( 34.69)
96 (65,31)
1 *
51 (34.69)
96 (65,31)
1 *
Ženska, varianta
8 (27.59)
21 (72.41)
0,58 (0,20-1,65)
12 (24.00)
38 (76.00)
0,55 (0,23 - 1,32)
Moški, e3 /e3
57 (26.64)
157 (73,36)
0,48 (0,27-0,88)
57 (26.64)
157 (73.36)
0,49 (0,27 - 0,89)
Moški, varianta
7 (12.96)
47 (87,04)
0,49 (0,11 - 2.18)
14 (26.92)
38 (73.08)
1,52 (0,44 - 5,27)
P vrednosti za interakcija °
0,347
0,660
Starost
< 60 let, e3 /e3
25 (17,73)
116 (82,27)
1 *
25 (17,73)
116 (82,27)
1 *
< 60 let, varianta
4 (12.50)
28 (87.50)
0,35 (0,07-1,68 )
7 (21.21)
26 (78.79)
0,70 (0,18 - 2,66)
≥ 60 let, E3 /e3
84 (38.01)
137 (61,99 )
2,85 (1,53-5,28)
84 (38.01)
137 (61,99)
2,84 (1,54-5,26)
≥ 60 let, varianta
11 (21.57)
40 (78.43)
1,24 (0,21-7,26)
20 (28.57)
50 (71,43)
0,97 (0,21 - 4,36)
P vrednost za interakcijo
0,807
0,964
alkohol pitje
Nikoli, e3 /e3
45 (24.06)
142 (75,94)
1 *
45 (24.06)
142 (75,94)
1 *
Nikoli, varianta
5 (12.50)
35 (87.50)
0,29 (0,08-1,04)
12 (18.18)
54 ( 81,82)
0,62 (0,28-1,37)
kdaj, e3 /e3
64 (36.57)
111 (63,43)
1,59 (0,88-2,86)
64 ( 36.57)
111 (63,43)
1,46 (0,81-2,62)
kdaj, varianta
10 (23.26)
33 (76,74)
1,78 (0,37-8,50)
15 (40,54)
22 (59.46)
1,28 (0,35 - 4,66)
P vrednost za interakcijo
0,468
0,707
Kajenje
Nikoli, E3 /e3
54 (29,03)
132 (70,97)
1 *
54 (29,03)
132 (70,97)
1 *
Nikoli, varianta
8 (20.51)
31 (79,49)
0,48 (0,18-1,28)
13 (20.00)
52 (80.00)
0,53 (0,23 - 1,23)
Ever, e3 /e3
54 (31.40)
118 (68,60)
1,41 (0,80-2,50)
54 (31.40)
118 (68.60)
1,39 (0,79 - 2,45 )
Ever, varianta
7 (16.28)
36 (83,72)
0,68 (0,15-2,98)
13 (36.11)
23 (63.89)
1,98 (0,59 - 6.73)
P vrednost za interakcijo
0,609
0.271
sadja in zelenjave vnosa
Low, e3 /e3
28 (29.47)
67 (70.53)
1 *
28 (29.47)
67 (70.53)
1 *
Low, varianta
2 (9.09)
20 (90.91)
0,14 (0,02 - 0,87)
9 (32.14)
19 (67.86)
0,84 (0,28 - 2,49)
visoko, E3 /E3
78 (31.08)
173 (68,92)
1,17 (0,61-2,23)
78 (31.08)
173 (68,92)
1,12 (0,59-2,13)
visoka, varianta
11 (19.30)
46 (80.70)
2,83 (0,38-21,05)
16 (22.86)
54 (77.14)
0,62 (0,16 - 2,37)
P vrednost za interakcijo
0,309
0,487
† ALI prilagojena glede na starost, spol, uživanje alkohola (kot neprekinjeno spremenljivke), packyears kajenja, na žaru poraba mesa in zgodovina družinica raka želodca.
* referenčni kategoriji.
° s testom razmerje verjetnosti.
Mediana časa preživetja iz želodca je bila 19 mesecev brez statistično pomembnih razlik za ApoE
ε2 ali ε4 alelov prevoznikov (p-
vrednost log-rank testa > 0,05), četudi je analiza omejena na 1 leto in 2 leti po kirurškem posegu (podatki niso prikazani). Cox regresijska analiza ni pokazala pomembne razlike glede na APOE
po prilagoditvi za starost, spol in stadiona, tudi po stratifikacije s raka histotype.
Razprava
Naša primerov in kontrol študiji 156 želodca primerov raka in 444 bolnišnici ki temeljijo na kontrole ocenjene prvič učinek APOE
genotipov in njihove interakcije z izbranimi demografskimi in življenjskega sloga dejavnikov na tveganje za raka želodca med italijanskim prebivalstvom. Glede na naše rezultate, je na APOE
ε2 alel povezan s 60% statistično značilno zmanjšalo tveganje za GC v primerjavi z divjim tipom ε3 alel. Ta zaščitni učinek je še posebej močan črevesne histotype. Nismo mogli, pa je zaznati pomembne interakcije med APOE
alelov in dejavniki življenjskega sloga. Poleg tega se ne pojavljajo APOE
genotipi vplivati na čas preživetja po kirurškem posegu, tudi če je bila analiza omejena na posebne tumorske histotypes.
Pred razlagi naše rezultate je treba nekatere omejitve raziskave je treba upoštevati. Prvič, na podlagi razširjenosti v APOE
alelov v naši kontrolne populacije, ta študija je a priori
90% moči, da zazna ali 0,40 za vpliv na APOE
alel ε2 (na 5% raven pomembnosti). Velikost vzorca Študija je omejuje možnost za odkrivanje statistično pomembne gene-okoljskih interakcij, pa moramo povečati velikost vzorca, da bi potrditev naše rezultate. Drugič, podatki o serumske ravni holesterola niso na voljo v naši raziskavi populaciji, čeprav bi bila njihova uporabnost omejena zaradi dejstva so prizadeti takšne vrednosti, ki jih je rak sam.
Učinek APOE
genotipov je že prej raziskovali v zvezi z rakom dojk, debelega črevesa, žolčevodov, prostate, raka glave in vratu, in hematoloških malignih obolenj [19-24], z nasprotujočimi si rezultati. Nedavno objavljena Mendlovo študija naključnost obravnavali Nerešeno vprašanje o vzročni vlogi holesterola v raka etiologiji s pregledom, če nekateri SNP vključno APOE
, vsi povezani z vseživljenjsko zmanjša plazemski LDL-C, so vzročno povezani s povečanim tveganjem za raka med dve veliki danski splošna populacijske študije [13]. Rezultati kažejo obratno sorazmerje med incidenco raka ali stopenj umrljivosti in holesterola, medtem ko ni bilo učinka dokazana v APOE
alelov. Tudi z nekaterimi omejitvami za izbrani kohorte, avtorji ugotavljajo, da obstaja velika pomanjkanja vzročne učinek holesterola na tveganje za nastanek raka, vključno raka prebavil. Zato je očitno nasprotje med rezultati, ki se nanašajo raven plazemskega holesterola in tveganje za nastanek raka v zvezi z apo E
, lahko nakazujejo predklinični fazi raka, ki vključuje povečano stopnjo holesterola iz krvi za rast celic in orožja, s čimer znižuje hiperholesterolemije pred diagnozo klinično raka.
Kot je za rakom na želodcu, dva japonska študije kohorte [10, 18] in švedski študiji kohorte [16] poroča močno inverzno povezavo med ravnmi holesterola v serumu in tveganje za raka želodca. Japonski študije, pa ugotovi, da je društvo precej manj močnejši po izključitvi primerov zgodnjih 3-letno nezgod in naprednih primerih, kar kaže na razvoj raka na želodcu sam nagiba k znižanju celotnega holesterola. Da bi rešili vprašanja v zvezi z vzvratno vzročno zvezo ali zavajajočih ga dejavniki življenjskega sloga, smo se odločili, da pojasni vlogo ravni holesterola v GC tveganja z uporabo Mendelovi pristop naključnih in sicer z neposrednim študijem vpliva na APOE
genotipov na velike serije italijanskih primerov GC in nadzora. Naši rezultati kažejo statistično značilna 60% zmanjšalo tveganje za GC, povezano z alel ε2.
Ker imajo ε2 prevozniki nižji serum hiperholesterolemije kot ne- ε2 prevozniki, naša ugotovitev je v nasprotju z že poročali ugotovitev, da nizko raven holesterola v serumu poveča GC tveganje [10, 16, 18]. ApoE pa ima številne druge funkcije, poleg svoje znane vloge v metabolizmu lipidov, ki so potencialno vpletene v tveganju za raka, kot je vključena v popravilo tkiva, vnetnega in imunskega odziva, rast celic in angiogenezo [2], in kaže antioksidant lastnosti [25]. Pomembno, ApoE protein ima določene antioksidativne lastnosti, z zmanjšanjem antioksidativno aktivnost v red ε2 > ε3 > ε4 alelov [25]. Tudi če molekularnih mehanizmov, ki so odgovorni za antioksidativnih lastnosti APOE
še ni pojasnjeno, številne študije so preučiti mehanizme, prek katerih bi lahko APOE
genotipi vplivajo na mediatorje oksidacijske stanja odvisnega ali biomarkerjev oksidativnega stresa [26 -28]. ApoE
posamezniki ε2-nosilec za kajenje, ki so izpostavljeni nikotinu, pomemben vir oksidativnega stresa, ima skoraj 30% večjo skupno stanje antioksidantov v primerjavi z ApoE
ε3-prevoznikov, merjena kot sposobnost, da zavira s peroksidazo pogojenega oblikovanje od 2,2-azino-bis-3-ethylbensthiazoline-6-sulfonska kislina (ABTS +) radikalom, medtem ko APOE
ε4 predmeti kažejo 30% povečala oksidiran LDL [26].
oksidativni stres ki jo neravnovesje med povečane proizvodnje reaktivnih kisikovih zvrsti in znatno zmanjšanje zmogljivosti antioksidant funkcij. Proizvodnja peroksidov in prostih radikalov povezana s spremembami v normalnem redoks stanju tkiv lahko povzroči toksične učinke, vključno z oksidativno poškodbo DNA, ki skupaj s hipoksijo in acidoza, lahko močno vpletena v patogenezo GC saj se lahko šteje vzrok kakor tudi zaradi napredovanja tumorja [29, 30]. Nekateri dokazi v primerjavi z zdravimi posamezniki, kot je razvidno iz zvišanih vrednosti lipidov izdelkov peroksidacijo in izčrpavanje encimov in neencimskih antioksidantov [31, 32] je pokazala širok obseg oksidativnega stresa v primerih GC. Glede na vse te ugotovitve, rezultati naše raziskave, ki poroča zaščitni učinek na APOE
alel ε2 na GC, lahko razložimo z izboljšanimi antioksidativnim alele ε2 v primerjavi z ε3 ali ε4 alelov, in to dokaz je lahko še posebej velja za GC, katerega patogenezo ki je povezano s kajenjem oksidativnim stresom [33] močno prizadela. Če je naš model velja, bi pričakovali, da je komunikacija med APOE
statusa alelov ε2 in kajenje, lahko pa omejeno moč naše analize interakcije so jo zakrita.
Sklepe
Skratka, naša študija predvideva prvič dokazov o morebitni zaščitni učinek alel ε2 proti GC. Nadaljnje raziskave so potrebne za potrditev naše rezultate in da ugotovimo, če je zaščitni učinek posredovana preko znižan nivo holesterola ali boljših antioksidativne lastnosti.
Metod
Študija prebivalstva
bili izbrani Študijski predmeti v skladu s sodno kontrolo študija zasnovo kot je opisano predhodno [34-36]. Na kratko, so bili primeri zaporednih primarni bolnikov adenokarcinomom želodca, z histološke potrditve, ki je prestal kurativni želodca v "A. Gemelli" učni bolnišnici v obdobju 2002-2010. Kontrole so bili izbrani izmed rakavih bolnikih brez, s široko paleto diagnoz, sprejeti v isti bolnišnici v času enakem časovnem obdobju.
V tesnejše podrobnosti, približno 50% naše kontrolne populacije je izdelan darovalcev krvi, medtem ko je druga polovica je izdelan iz bolnikih z kirurških posegov, kot laparoskopsko holecistektomijo ali slepiča ali dimeljsko kilo in manjši del bolnikov s kroničnimi boleznimi, kot so hipertenzija ali kronično obstruktivno pljučno boleznijo (KOPB) doživlja občasno check-up prizadela.
Vsi predmeti so bili belci rojen Italija. Velikost Študija Vzorec je zajemal 156 primerov in 444 kontrol, s stopnjo udeležbe 98% med primerov in 93% med kontrolami. Po klasifikaciji Lauren, je bila večina (58,1%) primerov raka želodca črevesne [37]. Tumorji so se nahajala v antruma (44,5%), v korpusu (14,8%), v antruma /korpusa (21,1%), v Kardije (3,1%), štorov (5,5%), v fundum (1,6% ) v Cardia /korpusa (6,3%) in celotnega želodca (3,1%). Temelji na citoloških in arhitekturnih atypisms, kot tudi poročila o histo-patoloških [38], tumorji bolnikov so bile ustrezno razvrstijo: 70,0% komaj razlikuje (G3), 27,6% zmerno razlikuje (G2), 3,4% dobro diferencirani-(G1 ), 51,7%, medtem ko so potekali I-II in 48,3% uprizorjena III-IV.
Pisna privolitev je bila pridobljena iz vseh študijskih predmetov, po katerem je vsak predmet, ki venski krvni vzorec, ki so zbrani v-EDTA obloženih cevi. Ta študija je bila izvedena v skladu s Helsinško deklaracijo in je bil odobren s strani odbora za etiko v Katoliška univerza Srca Jezusovega.
Genotipizacije
DNA je bila vzeta iz limfocitov periferne krvi in je bila izvedena genotipizacijo APOE
uporabo polimorfizem dolžin restrikcijskih fragmentov (RFLP). Na kratko, 20ng genomske DNK pomnožili z uporabo oligonukleotidnih primerjev 5'-TCC AAG GAG CTG OAS GCG GCG CA-3 'in 5' GCC CCG GCC TGG TAC ACT GCC A-3 ". Reakcije smo denaturirali 3 minute pri 95 ° C, čemur sledi 35 dvostopenjskega ciklov, ki so sestavljeni iz 10 sekund pri 95 ° C, nato 10 sekund pri 66 ° C. Potem ko so cikli zaključena končno razširitev 5 minut pri 95 ° C je bila opravljena. 10-ul alikvot vsake RFLP izdelka smo razgradili s 5 U AFL
III in ločeno 10 ml alikvot smo razgradili s 5 U Hae
II. Oba APOE
ε2 in APOE
ε3 alelov smo razrezali z AFL
III, da dobimo izdelke 50 in 168 bp, medtem ko je APOE
ε4 alel ostaja nerazrezani na 218 bazičnih točk. Uporaba Hae
II, tako apoE
ε3and apoE ε4 alelov dobimo izdelke 23 in 195 bp, medtem ko je APOE
ε2 alel ostaja nerazrezani na 218 bazičnih točk. Šest možni genotipi so bili dodeljeni na podlagi analize vzorcev, ki jih proizvaja omejitev izvlečku. Kot je za nadzor kakovosti, je bilo zaporedje tudi 5% vzorcev, pri standardnih vzorcev DNK za vsakega APOE
genotipa s Seripa et al poslano. [39] zbiranja podatkov.
Torbice in kontrole so bili opravljeni pogovori usposobljeni zdravniki s pomočjo strukturiranega vprašalnika za zbiranje podatkov o demografskih podatkov, kajenje cigaret, pitje zgodovine, prehranjevalnih navad, telesne aktivnosti in družinsko anamnezo raka, ki imajo poseben poudarek na raka želodca. Udeleženci so bile pozvane, da se osredotoči na eno leto pred diagnozo (za nadzor leto pred datumom razgovora), ko odgovarja na vprašanja o življenjskih navad. Kajenje je kategoriziran kot še nikoli in vedno kadilci (vključno s sedanjih in nekdanjih kadilcev). Pack-let smo izračunali kot leta kadili pomnoži s trenutno številko (ali prejšnje številke, za tiste, ki so nehal) od pokajenih cigaret na dan, deljeno s 20.
sadja in zelenjave vnos je bil kategoriziran kot visoka, če vsaj tri dele sadje in zelenjava so bile porabljene na dan, ko je bila na žaru vnos meso, opredeljeno kot nizko, če je poraba manj kot 4-krat /mesec. Družinsko anamnezo raka iz starši, sorojenci in potomcev. Podatki v zvezi prejšnjega Helicobacter pylori
okužbe so na voljo samo za primerov raka želodca. Stopnja odgovora za dokončanje intervju je bil 92%, za primere, in 97% za nadzor, z izjemo podatkov, ki se nanašajo na žaru vnosa mesa (neznani v 10% primerov in 12,8% kontrol) in družinsko anamnezo raka (znan 10% primerov in 8% kontrol).
Statistična analiza
razmerje med rakom želodca in domnevnih dejavnikov tveganja so bile izmerjene z uporabo prilagojene razmerje obetov (OR) in njihovo 95% interval zaupanja (CI), ki izhajajo iz logistike regresijska analiza s pomočjo stata programske opreme (različica 10.0). Možni dejavniki tveganja, ki so menili, da je nagnjenost, če dodajanje te spremenljivke v model spremenili oziroma za 10% ali več, in ko je bila ugotovljena confounder o vseh ocenah glavnega učinka, je bila shranjena v vseh modelih. Na podlagi teh kriterijev, smo pod nadzorom za starost, spol, alkohol in na žaru porabo mesa, kajenje cigaret (pakiranj let) in družinsko anamnezo raka želodca. Χ
2-test Hardy-Weinberg Equilibrium (HWE) Za tri APOE
alelov je bila izvedena med kontrolami. Da bi preverili, če je bil učinek izbranih polimorfizmov spremenjene nekatere vplive iz okolja, je bila izvedena slojevito logistična regresijska analiza, prilagoditev za confounders predhodno ugotovljene. Gen-okolje analize interakcije je bila opravljena s pomočjo tistih, ki nosi homozigoti divjega tipa genotip (ε3 /ε3 povezanih z ApoE
ε3 izo-oblike) kot referenčno skupino. V tej analizi so bile genotipov razvrščena takole: prisotnost vsaj enega APOE
alel ε2 ali prisotnosti vsaj ene APOE
alel ε4 (genotip ε2 /ε4 ni bila vključena v vsaki kategoriji), saj zagotavlja . drugi dve APOE
izooblike (apo E
2 in apo E
4)
V tej analizi je bila starost razvrščeni binomski (< stara 60 in ≥ 60 let), kadilski status je veljal za nikoli /nikoli kadilci cigaret, in uživanje alkohola, kot pivci /ne-pivcev (ta vključuje tudi posameznike, katerih alkohol vnos je bil manjši od 7 g /dan). Da bi testirali za interakcijo med dvema spremenljivkama izpostavljenosti, je bil uporabljen test razmerja verjetnosti, s posamezniki homozigotno za divjim genotipom (ε3 /ε3) in niso izpostavljeni spremenljivk interesa, ki se uporablja kot referenčno skupino.
Splošno krivulje preživetja so izračunani z mejno izdelek metodi Kaplan-Meier od dneva diagnoze do smrti. Če pacient ni bil mrtev, je bilo preživetje cenzurirano ob zadnjem obisku. Test Dnevnik Stopnja je bila uporabljena za oceno razlik med podskupinami. Tveganje za smrt v zvezi z ApoE izooblik je ocenil Cox sorazmernih tveganj modela. razmerja ogroženosti (HR) so bili prilagojeni za starost, spol in stadiona, z genotipom divjega tipa (ε3 /ε3) kot referenčno skupino. Poleg tega so bile analize razvrščeni v razrede po histotype raka (črevesno /difuzno)
Vir podpore
, da ni na voljo sredstva razglasiti
Kratice
ALI:..
Razmerje obetov
 Ameriška preventivna delovna skupina svetuje preglede raka debelega črevesa pri 45 letih
Zrela ženska V posvetovanju z zdravnico, ki sedi na kavču za preglede v pisarni Ameriško združenje za boj proti raku od leta 2018 poziva prebivalstvo, naj se pregleda za raka debelega črevesa pri 45 l
Ameriška preventivna delovna skupina svetuje preglede raka debelega črevesa pri 45 letih
Zrela ženska V posvetovanju z zdravnico, ki sedi na kavču za preglede v pisarni Ameriško združenje za boj proti raku od leta 2018 poziva prebivalstvo, naj se pregleda za raka debelega črevesa pri 45 l
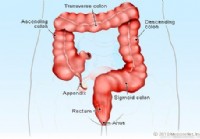 Simptomi in zdravljenje analne razpoke
Kaj moram vedeti o analnih razpokah? Slika anusa Kaj je analna razpoka? Analna razpoka je rez ali raztrganina, ki se pojavi v anusu (odprtina, skozi katero blato prehaja iz telesa), ki sega navzgor
Simptomi in zdravljenje analne razpoke
Kaj moram vedeti o analnih razpokah? Slika anusa Kaj je analna razpoka? Analna razpoka je rez ali raztrganina, ki se pojavi v anusu (odprtina, skozi katero blato prehaja iz telesa), ki sega navzgor
 Mikrobe na jeziku bi lahko uporabili za diagnosticiranje raka trebušne slinavke
Raziskovalci na Medicinski fakulteti Univerze Zhenjiang, Kitajska je ugotovila, da bi lahko motnje v mikrobni sestavi jezikovne obloge služile kot biomarker za zgodnji stadij raka trebušne slinavke.
Mikrobe na jeziku bi lahko uporabili za diagnosticiranje raka trebušne slinavke
Raziskovalci na Medicinski fakulteti Univerze Zhenjiang, Kitajska je ugotovila, da bi lahko motnje v mikrobni sestavi jezikovne obloge služile kot biomarker za zgodnji stadij raka trebušne slinavke.