"Detta är den första kända rapporten som visar att inom det komplexa tarmmikrobiomet, specifika mikrober har kapacitet att påverka normal skeletttillväxt och mognad, sa Chad M. Novince, D.D.S., Ph.D., en biträdande professor vid högskolorna för medicin och tandläkare, som studerar mikrobiomets inverkan på osteoimmunologi och skelettutveckling.
Novince-labbet fokuserar på post-pubertetsfasen av skelettutveckling, det kritiska fönstret av plasticitet som stöder ackumulering av cirka 40% av en persons maximala benmassa. Nyligen genomfört arbete från labbet visade att tarmmikrobiomet ökar immunsvaret i lever- och benmiljön, som försämrar skelettets benmassa. SFB har visats av andra grupper för att aktivera immunsvaret för TH17-celler på ett interleukin-17A (IL-17A) beroende sätt. Forskningen syftade till att koppla samman dessa aspekter av SFB-medierad immunitet avgör om specifika tarmmikrober har förmågan att påverka skeletthälsan.
För att studera effekterna av SFB och tarmmikrobiomet på skeletthälsan, Novince -labbet använde en musmodell med en definierad mikrobiota. Denna forskning underlättades av MUSC:s gnotobiotiska djurkärna, som regisseras av Caroline Westwater, Ph.D., medförfattare och professor vid College of Dental Medicine. Tillgänglig genom den unika djurkärnan, bakteriefria möss (ingen mikrobiota) och gnotobiotiska möss (definierad mikrobiota) ger en utmärkt modell för att studera mikrobiomens bidrag till skelettutveckling.
När vi tänker på ben, det är alltid balansen mellan osteoblaster och osteoklaster; osteoblasterna bildar benet, och osteoklasterna resorberar benet. SFB -kolonisering orsakade en förskjutning på båda sidor av axeln:osteoklastaktiviteten gick upp, och osteoblastaktiviteten gick ner, vilket är skadligt för skelettet. "
Chad M. Novince, biträdande professor vid högskolorna för medicin och tandläkare, MUSK
För att börja sina studier, Novince-labbet jämförde bakteriefria möss med SFB-monoassocierade möss. Möss som hade SFB uppvisade en 20% minskning av trabekulär benvolym - den typ av ben som genomgår höga hastigheter av benmetabolism. Ytterligare undersökning av dessa möss visade att SFB-kolonisering ledde till ökade IL-17A-nivåer i tarmen och cirkulation, och förbättrad osteoklastpotential.
Nästa, Novince -labbet undersökte om förekomsten av SFB i en komplex tarmmikrobiota kan påverka normal skelettutveckling. De jämförde Taconic-specifika-patogenfria möss som hade SFB som en del av sitt mikrobiom med Taconic-specifikt-patogenfria möss som saknade SFB.
Närvaron av SFB i en komplex mikrobiota ledde till minskad trabekulär benvolym, vilket tillskrevs ökad osteoklastaktivitet och minskad osteoblastaktivitet. SFB -kolonisering ledde till ett proinflammatoriskt immunstatus i tarmen, med ökat antal myeloid-härledda suppressorceller (MDSC) och M1-makrofager i lymfkörtlarna associerade med tarmen. Dessutom, SFB-kolonisering ökade IL-17A-nivåerna i tarmen och cirkulationen.
Intressant, SFB -närvaron i en komplex tarmmikrobiota stimulerade också starkt hepatisk immunitet. SFB -kolonisering uppreglerade proinflammatoriska immunfaktorer i levern och ökade TH17 -celler i levern som tömmer lymfkörtlar. Vidare, förekomsten av SFB ledde till högre nivåer av akuta fasreaktanter - immunfaktorer som bildas i levern och utsöndras i cirkulationen. Lipocalin-2 (LCN2) var särskilt intressant eftersom det är en antimikrobiell peptid som påverkar benmetabolismen.
SFB-kolonisering resulterade i ökade cirkulerande nivåer av IL-17A och LCN2, som båda är faktorer som stöder osteoklastaktivitet och undertrycker osteoblastaktivitet. Tagen tillsammans, dessa data visar att SFB spelar en avgörande roll för att reglera immunsvaret i både tarmen och levern som har betydande effekter på skelettet och ger starkt stöd för att tarmmikrobiotiska verkningar på skelettet delvis medieras genom en tarm-lever-benaxel .
Dessutom, SFB:s bidrag till skeletthälsan kan ha betydande kliniska konsekvenser.
"Om vi kan förhindra koloniseringen eller tömma specifika mikrober som SFB från mikrobiomet, det finns en klinisk potential att optimera benmassauppsamling under skelettutveckling efter puberteten, sa Novince.
Det är känt att kost, probiotika och antibiotika har betydande effekter på mikrobiomets sammansättning, inklusive SFB -kolonisering. En majoritet av en persons benmassa tillkommer under tonåren, eller efteråt. När människor åldras, de börjar sakta förlora benmassa, vilket utsätter dem för risk för frakturer och osteoporos. Modulation av SFB, genom icke-invasiva ingrepp som dieter eller probiotika, kan möjliggöra uppbyggnad eller optimering av maximal benmassauppsamling under tonåren. Detta skulle begränsa risken för åldrande i samband med låg benmassa och relaterade frakturer.
Sammanfattningsvis, Novinces grupp har visat att inom det komplexa mikrobiomet, en specifik kommensal mikrobe, SFB, har kapacitet att kritiskt förändra hur mikrobiomet interagerar med värdens immunsystem och skelett. Detta immunsvar, förmedlas genom en tarm-lever-benaxel, inducerar en pro-osteoklast och anti-osteoblast miljö i benet, som försämrar normal skeletttillväxt och mognad. Det starka bidraget från leverimmuniteten motiverar ytterligare undersökning av hur akutfasprodukterna kan ha en återkopplingseffekt på mikrobiomet eller ytterligare effekter på värden.
 Varför polyfenoler är viktiga och hur de matar dina magbuggar
Det är sällsynt att jag träffar utövare som Få det – som har gått så djupt som jag har gjort i kaninhålen av mat, tarmhälsa och övergripande kroppshälsa. Det är ännu mer sällsynt att dessa människor
Varför polyfenoler är viktiga och hur de matar dina magbuggar
Det är sällsynt att jag träffar utövare som Få det – som har gått så djupt som jag har gjort i kaninhålen av mat, tarmhälsa och övergripande kroppshälsa. Det är ännu mer sällsynt att dessa människor
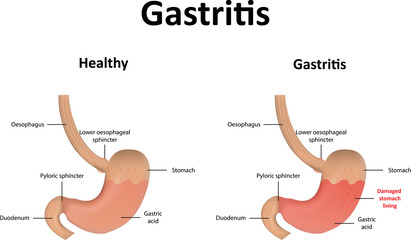 Gastrit
Gastrit är sur skada på magslemhinnan leder till övergående inflammation eftersom det sker genombrott i epitelet i slemhinnan efter erosion av slemskiktet ovanför slemhinneepitelet. Gastrit kan vara a
Gastrit
Gastrit är sur skada på magslemhinnan leder till övergående inflammation eftersom det sker genombrott i epitelet i slemhinnan efter erosion av slemskiktet ovanför slemhinneepitelet. Gastrit kan vara a
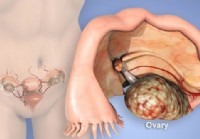 Symtom, tecken, stadier av äggstockscancer
Vad är äggstockscancer? Äggstockscancer är en malignitet i äggstockarna, de kvinnliga könsorganen som producerar ägg och gör hormonerna östrogen och progesteron. Behandlingarna för äggstockscancer f
Symtom, tecken, stadier av äggstockscancer
Vad är äggstockscancer? Äggstockscancer är en malignitet i äggstockarna, de kvinnliga könsorganen som producerar ägg och gör hormonerna östrogen och progesteron. Behandlingarna för äggstockscancer f