Los investigadores, que publicaron sus hallazgos el 17 de agosto en Cell, demostró que las ILC3 tienden a reducirse drásticamente y alterarse funcionalmente en personas con cáncer colorrectal. Más lejos, Demuestran que la alteración experimental de las funciones de las ILC3 en ratones conduce a un cáncer de colon agresivo y reduce en gran medida la eficacia de las inmunoterapias contra el cáncer.
El cáncer colorrectal es el cuarto cáncer más común en los Estados Unidos, con unos 150, 000 casos nuevos cada año y alrededor de 50, 000 muertes. Si bien la detección temprana de estos cánceres o pólipos precancerosos con colonoscopias de detección es muy eficaz, Los tratamientos para los tumores colorrectales avanzados siguen siendo un desafío importante con opciones terapéuticas limitadas. Los oncólogos están particularmente preocupados por la resistencia relativa de estos tumores a las inmunoterapias, tratamientos que funcionan bien contra algunos otros cánceres al estimular la capacidad del sistema inmunológico para atacar las células malignas.
"Estos hallazgos sugieren nuevas posibilidades para el enfoque clínico del cáncer colorrectal, y también ayudar a explicar por qué este tipo de cáncer a menudo no responde a las inmunoterapias, "dijo el autor principal, el Dr. Gregory Sonnenberg, profesor asociado de microbiología e inmunología en medicina en la División de Gastroenterología y Hepatología y miembro del Instituto Jill Roberts de Investigación en Enfermedad Inflamatoria Intestinal de Weill Cornell Medicine.
Un factor que influye en la resistencia a las inmunoterapias puede ser el microbioma intestinal, la población de bacterias y otras especies microbianas que residen en los intestinos y normalmente ayudan a la digestión, Apoyar varias funciones metabólicas y desempeñar un papel en la regulación del sistema inmunológico. El cáncer colorrectal se asocia con inflamación intestinal crónica y una alteración importante del microbioma normal. Más lejos, Estudios recientes sugieren que los microbiomas de los pacientes juegan un papel clave en el control del resultado de las inmunoterapias contra el cáncer y pueden explicar por qué lo hacen los cánceres de algunos pacientes. o no, responden bien al tratamiento.
En el nuevo estudio, Dr. Sonnenberg y colegas, incluido el autor principal, el Dr. Jeremy Goc, un investigador asociado en el laboratorio del Dr. Sonnenberg, examinó el papel de las ILC3, que residen en los intestinos y se sabe que ayudan a mediar en la relación entre el sistema inmunológico y los microbios intestinales.
Las células linfoides innatas del grupo 3 normalmente juegan un papel clave en el mantenimiento de un diálogo saludable entre el microbioma y el entorno inmunológico en la parte inferior del intestino. En estrecha colaboración con el Dr. Manish Shah, el Profesor de la Familia Bartlett de Oncología Gastrointestinal, director del Programa de Oncología Gastrointestinal de la División de Hematología y Oncología Médica, y miembro del Centro Oncológico Sandra y Edward Meyer en Weill Cornell Medicine, el grupo de investigación analizó tumores colorrectales y pólipos precancerosos de humanos y ratones. Descubrieron que las ILC3 de los tejidos cancerosos estaban relativamente agotadas en comparación con los tejidos sanos y además se modificaron fundamentalmente en sus funciones.
Este es un hallazgo emocionante que podría tener amplias implicaciones para nuestra comprensión de las vías que controlan la patogénesis, progresión y capacidad de respuesta terapéutica de las neoplasias gastrointestinales ".
Dr. Manish Shah, coautor del estudio, jefe del Servicio de Oncología de Tumores Sólidos y codirector del Centro de Atención Digestiva Avanzada del NewYork-Presbyterian / Weill Cornell Medical Center
Entre esta pérdida de la actividad normal de ILC3 en el intestino, los autores observaron además que la capacidad de las ILC3 para regular un subconjunto de células inmunitarias específicas llamadas células T se vio significativamente alterada. Esta interrupción del diálogo entre las ILC3 y las células T condujo aún más a un aumento de la inflamación en el intestino que posteriormente modifica el microbioma intestinal. Estos cambios en los microbios intestinales, a su vez, inducen una disminución en los niveles de células T que son buenas para combatir los tumores.
Esos resultados colectivos tienen importantes consecuencias en el desarrollo de tumores, los investigadores mostraron. En ratones que desarrollan cánceres de colon, el bloqueo de la señalización de ILC3 condujo al crecimiento de tumores anormalmente invasivos y más agresivos con mal pronóstico. Y cuando se implantaron tumores de colon en ratones con señalización ILC3 bloqueada, los tumores no respondieron relativamente a una inmunoterapia contra el cáncer llamada bloqueo de puntos de control anti-PD-1, mientras que el mismo tipo de tumor, implantado en ratones con señalización ILC3 normal, respondió bien a la terapia.
Finalmente, en tejidos colorrectales biopsiados de pacientes con enfermedad inflamatoria intestinal (EII), los investigadores encontraron anomalías relacionadas con ILC3 similares a las de los pacientes con cáncer colorrectal. El trasplante de microbios de pacientes con EII a ratones confirió resistencia a la terapia, mientras que los ratones trasplantados con microbios de donantes humanos sanos aún respondieron bien al bloqueo del punto de control anti-PD-1.
"Comprender mejor la contribución del microbioma al desarrollo del cáncer y la capacidad de respuesta al tratamiento podría revolucionar las estrategias de manejo del paciente. Este estudio ilumina un mecanismo de resistencia a la terapia impulsado por la desregulación del microbioma que no se ha apreciado hasta ahora". "Dijo el Dr. Goc." Sugiere, por ejemplo, que algún día podríamos tomar muestras de la microbiota intestinal para predecir la progresión del tumor y la respuesta a la inmunoterapia, e incluso utilizar una microbiota saludable para mejorar la respuesta al tratamiento ".
Los investigadores ahora están trabajando para identificar las especies de bacterias intestinales que son más beneficiosas a este respecto. Esta investigación está respaldada en parte por un mecanismo de financiación novedoso del Instituto de Investigación del Cáncer que fue otorgado al Dr. Sonnenberg en 2019, el año inaugural del programa.
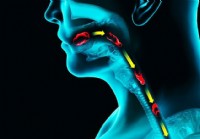 ¿Cuál es la diferencia entre odinofagia y disfagia?
¿Qué son la odinofagia y la disfagia? La diferencia entre odinofagia y disfagia es que la disfagia es dificultad para tragar y la odinofagia es dolor al tragar. La disfagia es un término médico
¿Cuál es la diferencia entre odinofagia y disfagia?
¿Qué son la odinofagia y la disfagia? La diferencia entre odinofagia y disfagia es que la disfagia es dificultad para tragar y la odinofagia es dolor al tragar. La disfagia es un término médico
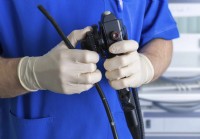 Los diferentes tipos de procedimientos de endoscopia
Una endoscopia es un procedimiento médico que se usa para ver los órganos internos de una manera no quirúrgica. Estos a menudo se denominan procedimientos mínimamente invasivos, ya que son formas meno
Los diferentes tipos de procedimientos de endoscopia
Una endoscopia es un procedimiento médico que se usa para ver los órganos internos de una manera no quirúrgica. Estos a menudo se denominan procedimientos mínimamente invasivos, ya que son formas meno
 Aprobación de Afinitor ampliada para incluir tumores renales benignos
Últimas noticias sobre medicamentos Los hospitales planean producir sus propios medicamentos genéricos El compuesto de marihuana altera los niveles de la droga anticonvulsiva Aprobado por Briviact pa
Aprobación de Afinitor ampliada para incluir tumores renales benignos
Últimas noticias sobre medicamentos Los hospitales planean producir sus propios medicamentos genéricos El compuesto de marihuana altera los niveles de la droga anticonvulsiva Aprobado por Briviact pa