Cromoendoscopia en la cápsula endoscópica guiada magnéticamente
Resumen Antecedentes
Diagnóstico de metaplasia intestinal y displasia vía endoscópica convencional se caracteriza por la concordancia entre baja y pobre correlación con los hallazgos histopatológicos. Cromoendoscopia mejora significativamente la visibilidad de las irregularidades de la mucosa, como la metaplasia y displasia de la mucosa. Magnéticamente guiado cápsula endoscópica (MGCE) ofrece una tecnología alternativa para el examen del tracto gastrointestinal superior. Esperamos que las dificultades de diagnóstico de neoplasia en la endoscopia convencional para transferir a MGCE. Por lo tanto, nuestro objetivo es trazar un camino para la aplicación de la cromoendoscopia en MGCE a través de un estudio ex vivo animal.
Métodos
se propone un protocolo de preparación modificado que añade una etapa de tinción para el protocolo de preparación MGCE existente. Una concentración óptima de tinción se determina cuantitativamente para diferentes tipos de manchas y patologías. A tal fin 190 muestras de tejido de estómago de cerdo con y sin imitaciones de lesión fueron teñidas con diferentes concentraciones de colorante. se introducen criterios visuales cuantitativos para medir la calidad de la tinción con respecto a la mucosa y la visibilidad de la lesión. Thusly
determinaron las concentraciones óptimas se ponen a prueba en un experimento estómago de cerdo ex vivo bajo la orientación magnética de una cápsula endoscópica con el protocolo modificado. Resultados
Hemos encontrado que la modificación protocolo propuesto no afecta la visibilidad en el estómago o la maniobrabilidad de la cápsula endoscópica. Una concentración de tinción óptimo promedio para el protocolo propuesto se encontró en el 0,4% en el caso de metileno azul y carmín de índigo. La visibilidad de la lesión se mejora mediante la concentración de colorante óptimo obtenido con anterioridad.
Conclusiones
Llegamos a la conclusión de que la cromoendoscopia se puede aplicar en MGCE y mejora la mucosa y la lesión visibilidad. La evaluación sistemática proporciona información importante sobre la concentración de tinción adecuada. Sin embargo, más animal y humana in vivo son necesarios estudios. Antecedentes
Palabras clave
azul de metileno índigo carmín tinción
Aunque la incidencia y mortalidad del cáncer están disminuyendo, gástrico, con 738.000 casos en todo el mundo en el año 2008 es el segundo más letal digestivo neoplasia en el mundo [1]. metaplasia intestinal y displasia son precursores de cáncer [2]. La identificación de estas lesiones y el seguimiento de los pacientes afectados podrían conducir a un diagnóstico y tratamiento tempranos, y por lo tanto mejorar la supervivencia de los pacientes [3, 4]. La endoscopia digestiva alta (EGD) es el procedimiento más común para el diagnóstico y el tratamiento. Sin embargo, para la detección de la metaplasia y displasia EGD convencional se caracteriza por la concordancia entre baja y pobre correlación con los hallazgos histopatológicos [5, 6].
Están disponibles diversas técnicas para mejorar y poner de relieve las irregularidades de la mucosa y para aumentar la visibilidad de las estructuras que mentir bajo la superficie de la mucosa. Los métodos más importantes incluyen imágenes de banda estrecha, endomicroscopía láser confocal, endoscopia de magnificación, la tomografía de coherencia óptica y cromoendoscopia [7-10]. Estas técnicas a menudo han sido comparados uno contra el otro, o en combinación en términos de su impacto en la precisión de diagnóstico (por ejemplo, en [11, 12]). Sin embargo una diferencia sustancial entre la cromoendoscopia y todas las técnicas de la competencia radica en la falta de hardware adicional. Cromoendoscopia no requiere ninguna modificación del hardware del sistema de imagen en sí.
Además, cromoendoscopia en EGD y la colonoscopia se ha demostrado para mejorar significativamente la visibilidad de las irregularidades de la mucosa, como metaplasia y displasia [13]. Cromoendoscopia consiste en la aplicación tópica de diferentes manchas para mejorar la visibilidad del tejido, la localización y caracterización con el fin de un mejor diagnóstico. Cromoendoscopia por lo general consta de cuatro pasos para manchas de absorción y tres pasos para las manchas de contraste: (1) La aplicación de una solución de ácido para disolver el moco gástrico, (2) la aplicación local de una mancha, (3) (sólo para las manchas de absorción) de lavado de la región respectiva con agua y (4) la inspección visual de las regiones teñidas con fines de diagnóstico. En (1) - (3) la aplicación de tinte se realiza localmente mediante el canal de trabajo del endoscopio y diferentes catéteres pulverización (método directo), bajo la dirección visual del endoscopio. Para colonoscopia la aplicación pasiva de mancha con una cápsula llena de tinte en polvo también se ha descrito [14, 15]. En este procedimiento se da una cápsula con polvo de colorante para el paciente después de la administración de una solución de limpieza del intestino tales como PEG. Entre la administración del colorante y la colonoscopia es necesario un tiempo de espera. La aplicación del tinte en la mañana y el examen de la tarde se informó como un lapso de tiempo suficientemente grande [14]. Aunque se encontró el procedimiento para ser factible, las dificultades se han reportado debido a la aplicación no homogénea de la mancha [16]. La aplicación oral de tinte para el examen del estómago sin utilizar un catéter de pulverización (método indirecto) se ha descrito en [15, 17].
Recientemente, diferentes enfoques para endoscopios magnéticamente guiadas en cápsula (MGCE) para gástrico y exámenes del intestino delgado se presentaron [18-23]. En un estudio clínico en seres humanos, MGCE mostró la viabilidad de la exploración gástrico con un endoscopio cápsula guiada [18, 19]. En este estudio específico el estómago estaba lleno de agua y la cápsula se navega desde el exterior usando un campo magnético externo. Un operador puede controlar el movimiento de la cápsula durante el examen utilizando la retroalimentación de imágenes gástrica en tiempo real proporcionada por dos sensores de la cámara de la cápsula. Por lo tanto, se podría obtener un número suficiente de imágenes de la superficie del estómago con valor diagnóstico.
Esperamos que las dificultades conocidas en el diagnóstico de la neoplasia, con respecto a la concordancia entre observadores en la endoscopia convencional, la transferencia a MGCE. MGCE podría, por lo tanto, beneficiarse de la cromoendoscopia de la misma manera endoscopia clásico hace. Sin embargo, en comparación con la aplicación directa de la mancha en EGD y la mayoría de los procedimientos de colonoscopia, en MGCE única aplicación indirecta es posible. No preparación de ácido y el lavado de la mucosa gástrica es posible. Además, el agua en la que se maniobra la cápsula, no debe ser manchado a niveles que reducen la visibilidad global. métodos de la competencia, como la imagen de banda estrecha en el diagnóstico de la neoplasia colorrectal son difíciles de integrar en una cápsula endoscópica [11]. Además, como en muchas de las técnicas endoscópicas todavía no se han establecido el impacto exacto de cromoendoscopia y los detalles técnicos [24, 25]. Por ejemplo, en la literatura ([5, 26, 27]) se pueden encontrar tres diferentes concentraciones de colorante azul de metileno y tiempos de aplicación para el examen de neoplasia gástrica. La búsqueda de una concentración óptima para un procedimiento de tinción en los ensayos con animales y humanos se ha reportado un par de veces, pero sin el apoyo de un análisis exhaustivo. En [28] una concentración óptima para la tinción endomicroscopía láser confocal simultánea y cromoendoscopia con violeta de cresilo se evalúa en Ratones, pero sin un criterio objetivo. En [29] se accedió a una concentración óptima para la tinción de endocytoscopy en un estudio ex-vivo animal en el que se examinaron recién resecado esófago porcino, estómago y colon. contraste de la imagen y el estado de la tinción se evaluaron por expertos para cada órgano para determinar la mejor concentración. Los resultados se transfieren a los órganos humanos resecados. El problema de la falta de un estudio sistemático de la cromoendoscopia clásico en las transferencias de estómago a MGCE y se vuelve más severa a través de los desafíos de la aplicación indirecta de la mancha.
En este trabajo se evalúa la posible aplicación de la cromoendoscopia para MGCE en un ex-vivo estudio en animales. En primer lugar, se propone una modificación del protocolo de preparación MGCE con el fin de incorporar un procedimiento de tinción para cromoendoscopia. En segundo lugar, se presenta un método para evaluar sistemáticamente una concentración óptima de colorante para la modificación del protocolo propuesto. La optimización se lleva a cabo en experimentos utilizando muestras de tejido de estómago de cerdo y con respecto a la mejor visibilidad de tejido de diferentes histológica o naturaleza patológica. En tercer lugar, que la transferencia de estos resultados a un experimento estómago de cerdo ex vivo bajo la orientación magnética de una cápsula endoscópica. Estos experimentos deben determinar: a) el total visibilidad bajo el agua después de que el protocolo de tinción pasiva propuesta; y b) la mucosa y la visibilidad de la lesión con la concentración de colorante optimizada.
El imán orientación es técnicamente similar a la utilizada para el estudio en seres humanos [18, 19]. Todas las funciones de navegación de este estudio están también disponibles en nuestra configuración. El sistema es un desarrollo conjunto de Siemens Healthcare y Olympus Medical Systems Corp. Sus principales componentes son: (1) Un imán orientación que consiste en un conjunto de bobinas electromagnéticas que definen un volumen de trabajo y permite al operador controlar un endoscopio cápsula con 5 grados de la libertad (DOF). La densidad de flujo magnético tiene un máximo de 100 militeslas. (2) Una cápsula endoscópica de una longitud de 31 mm fabricado por Olympus Medical Systems Corp. con una acumulación de imán permanente y dos cámaras CCD cada una transmisión de 2 imágenes por segundo en tiempo real a un receptor externo conectado al cuerpo del paciente. (3) Una pantalla que muestra las imágenes de la cápsula para el operador. (4) Un conjunto de palancas de mando que permiten al operador maniobrar la cápsula en el interior del estómago. La orientación de un campo electromagnético (EM) orienta la cápsula en el estómago. El campo EM junto con un gradiente de campo EM generar fuerzas sobre el endoscopio cápsula de menos de 1 milinewton. Estos son suficientes para movimientos de traslación. Más detalles sobre el diseño del hardware y software del imán guía se pueden encontrar en [30]. La orientación de la cápsula se realiza sobre la base de imágenes en tiempo real proporcionada por la cápsula endoscópica en el interior del estómago de cerdo. Hoteles en [31] un estudio estómago de cerdo se presentó para mejorar la visibilidad en la mucosa MGCE usando azul de metileno. Este estudio se limitó a sólo unos pocos casos y un solo colorante. La manejabilidad sólo magnético se simuló utilizando un soporte de plástico y no había ninguna evaluación sistemática de una concentración de colorante optimizado antes de los experimentos. Mientras que en el presente trabajo la capacidad de dirección magnética se consigue con un imán orientación cápsula. El estudio se llevó a cabo con un gran número de estómagos de cerdo y conduce a una evaluación sistemática de los dos tipos de colorantes óptimas.
Métodos
Modificación del protocolo de preparación para MGCE México La preparación protocolo establecido utilizado para el estudio MGCE humana existente con 43 pacientes consiste en tres administraciones de agua del grifo antes de examinar: [18, 19]
existente protocolo de preparación MGCE
E.1 500 ml de agua limpia a temperatura ambiente una hora y 15 minutos antes del examen y después de una noche en ayunas.
E.2 400 ml de agua limpia a temperatura ambiente 15 minutos antes del examen seguido de ejercicios ligeros.
E.3 400 ml de agua clara a la temperatura corporal cercano, inmediatamente antes del examen .
Todas las aplicaciones se administran por vía oral. Pasos E.1 y E.2 están destinados principalmente para la limpieza del estómago. Paso E.3 tiene por objeto ampliar el estómago con el fin de obtener suficiente espacio para la cápsula a ser maniobrado y para la visibilidad completa de la mucosa del estómago sin pliegues gástricos se solapan entre sí y, finalmente, ocultando partes de la mucosa pertinentes. Paso E.3 no se puede modificar ya que es crucial para la orientación de la cápsula en el interior del estómago. Esperamos que el agua que se tiñó en una medida tal que la visibilidad en general se reduce cuando la mancha se aplica directamente antes de E.3. Por lo tanto, proponemos para adaptarse a una etapa de tinción entre los pasos E.1 y E.2 del protocolo de preparación existente. Con el fin de llevar a cabo más experimentos con animales fantasmas de la siguiente protocolo se adoptó para estómagos de cerdo: protocolo de preparación MGCE
Modificado para estómagos de cerdo
M.1 2000 ml de agua limpia a temperatura ambiente que se vacía del estómago inmediatamente después de la administración. El propósito de este paso es todavía la limpieza del estómago de moco y /o restos de comida.
M.2 100 ml de colorante, seguido de 5 minutos de masaje y amasando el estómago para simular el movimiento peristáltico, seguido de vaciado de la estómago del tinte. Este paso se aplica el tinte de las paredes del estómago. Masaje y amasando el estómago simula el movimiento peristáltico y se lleva a cabo bajo el supuesto de que el colorante se dispersa naturalmente sobre todas las áreas anatómicas del estómago en el caso natural. La simulación de la peristalsis digestiva a través de masaje una bolsa Stomacher o un sistema de poleas para crear movimiento peristáltico en un modelo mecánico de estómago se informó en [32, 33].
M.3 500 ml de agua clara a temperatura ambiente, que permanece en el estómago durante 5 minutos y se después vaciado. Este paso es similar a E.2 del procedimiento MGCE estándar, pero esta vez también se evacua el tinte restante.
M.4 2000 ml de agua clara a la temperatura corporal cercano, inmediatamente antes del examen (mismo propósito que E.3 ).
Todas las aplicaciones se realizan a través del esófago y la intención de simular la aplicación oral de agua y colorante. Usando una combinación de agua, para expandir el estómago, y el tinte, al mismo tiempo se supuso que era incompatible con MGCE ya que la visibilidad de la cápsula se deterioraría. El vaciado se realiza apretando suavemente el estómago e imita la evacuación natural de contenido del estómago hacia el intestino delgado. La cantidad de agua para el lavado y la expansión del estómago (paso M.1 y M.4) se configura con valores más grandes debido al mayor tamaño del estómago de un cerdo.
Objetivo lesión y lesión imitaciones
para evaluar los beneficios de cromoendoscopia en MGCE el método propuesto se prueba en la mucosa sana e imitaciones de lesiones neoplásicas. Las lesiones de un posible cáncer gástrico temprano (CGT) se subdividen en 3 categorías principales: sobresaliente (0-I), que no sobresale y no excavado (0-II), excavado (0-III) con cada uno de estos tipos tiene múltiples sub -Tipos [34]. Dos tipos de lesiones se consideran con el fin de evaluar los beneficios de la cromoendoscopia con el protocolo modificado propuesto: Seudopólipos para simular una lesión que sobresale (0-lp) y lesiones que no sobresale ligeramente deprimidas del tipo 0-IIc. En [35] se describe un método para crear un pseudopolyp utilizando un dispositivo de ligadura variceal esofágica. Se utilizó un enfoque similar pero empleó una sutura para realizar una ligadura de la mucosa del estómago con el fin de crear un pseudopolyp. Para la simulación de las lesiones 0-IIc no sobresalen se aplicó una solución de HCl 10% a la mucosa del estómago durante 15 segundos y se lavó con agua del grifo. Ocho imágenes de ejemplo (cuatro de 0-LP y cuatro de 0-IIc) de las imitaciones de las lesiones creadas se muestran en la Figura 1. Figura 1 lesión imitaciones: Figura 1 (A): Cuatro ejemplos de que no sobresale ligeramente lesiones deprimidas-(0 -IIc) contorneada con líneas oscuras, la Figura 1 (B): cuatro ejemplos de pseudopólipos (marcados con flechas) para simular una lesión que sobresale (0-lp)
manchas
Durante EGD o colonoscopia, se utilizan diferentes manchas. para cromoendoscopia. Se clasifican como de absorción, el contraste o reactiva [24]. En nuestros experimentos usamos una mancha de absorción (azul de metileno) y una mancha de contraste (Indigo carmín). Azul de metileno, es absorbida por determinados tipos de células y pone de relieve, por lo tanto, a través de la absorción preferencial. Índigo carmín no es absorbente y pone de relieve la mucosa, poniendo en común mecánicamente en cuellos de útero entre las células epiteliales, grasa o lesiones deprimidas y otras irregularidades. Las imitaciones de lesiones de tipo 0-IIc (temprana del cáncer gástrico) se tiñeron con índigo carmín como se describe en [36]. . Para la tinción de los detalles finos de la mucosa azul de metileno se utiliza
criterios visuales de una concentración óptima de manchas
Un procedimiento de tinción para cromoendoscopia en MGCE tiene retos adicionales en comparación con cromoendoscopia clásico que implica un endoscopio flexible: La aplicación local de la mancha tal como se utiliza en EGD y la colonoscopia no es posible en MGCE, ni es una preparación de ácido de la mucosa o el lavado de la mucosa gástrica después de la aplicación de la mancha. La concentración óptima de colorante se evalúa cuantitativamente y de manera sistemática y se aplica aún más en el protocolo modificado propuesto. Para ello, un gran número de imágenes a partir de muestras de tejido de estómago de cerdo se tiñe con diferentes concentraciones de colorante con el fin de determinar una concentración óptima de tinción (véanse las Figuras 2 y 3). Dado que hemos encontrado que la simple inspección visual no es suficiente para juzgar con precisión la concentración óptima de manchas, definimos dos parámetros visuales objetivas para evaluar la concentración aplicada a la mucosa sana e imitaciones de lesión 0-IIc: la figura 2 de metileno tinción con azul: parches de estómago de cerdo derivadas de diferentes estómagos tiñeron con concentración de 0% a 1,4% azul de metileno. (A): no tinción, (B): 0,2%, (C): 0,4%, (D): 0,6%, (E): 0,8%, (F): 1%, (G): 1,2%, ( H): 1,4%. Imagen de 2 x 2 cm parches estómago de cerdo se recorta a 1,8 x 1,8 cm.
Figura 3 parches estómago de cerdo de imitación de la lesión manchado con diferentes concentraciones de índigo carmín. (A) no tinción, (B) 0,2%, (C) 0,4%, (D) 0,6%, (E) 0,8%, (F) 1%. Que no sobresale ligeramente lesiones deprimidas-(0-IIc) están contorneados con contornos rojos. Imagen de 2 x 2 cm parches estómago de cerdo se recorta a 1,8 x 1,8 cm
1.-Lesión a cambio de fondo:. El contraste de imagen puede ser definida como la diferencia cuantitativa, en términos de color y la intensidad, entre varios espacial vecina regiones de imagen u objetos dentro de una imagen. Para las imágenes endoscópicas de contraste se puede interpretar como la diferencia cualitativa local en color y /o la intensidad entre el tejido patológico y sano vecino. Una concentración óptima de manchas para la visualización de una lesión sería, por lo tanto, ser definida por una concentración que conduce a un contraste máximo entre patológica y mucosa sana. Cromoendoscopia tiene como objetivo mejorar este contraste tanto como sea posible por el colorante aplicada y los cambios resultantes en la coloración de los diferentes tipos de mucosa. Asignamos una puntuación numérica I
c
la que informalmente se puede definir como la diferencia promedio entre tejido de la lesión y el tejido sano.
Para el cálculo de la puntuación de contraste I
c
dos regiones R
l
y R
h
se defina para cada área de imagen con las lesiones y el tejido sano, respectivamente. Dado que el contraste de una imagen que puede ser descrito como la diferencia cuantitativa entre diferentes áreas de imagen. Una medida del contraste I
c
entre ambas regiones, por tanto, puede ser denota I
c
=
g
(
R
l
)
-
g
(
R
h
) gratis (1) donde g gratis (·) se refiere a la conversión de escala de grises de la imagen en color original. Calcular una puntuación de este medio de contraste, para cada imagen las dos regiones R
l
y R
h ¿Cuáles son elegidos de forma manual dentro de una región con lesiones y el tejido sano. Este proceso de etiquetado no segmento de la frontera exacta entre el tejido sano y enfermo. la segmentación manual está siempre sujeto a la experta. Más en particular una segmentación exacto es relativamente poco importante, en comparación con el contraste general entre dos regiones de imagen. Por lo tanto una segmentación región exacta no es necesario. La Figura 4 muestra un ejemplo de una región de tejido enfermo segmentado manualmente. El valor de una imagen de escala de grises en el se encuentra entre 0 y 255. Por lo tanto, la puntuación para el contraste de la lesión a fondo que también se encuentran entre estos dos valores, donde un valor pequeño implicaría un contraste pobre y un alto valor indicaría una imagen con alta contraste entre la lesión y el fondo. En [29] se definió un enfoque de este tipo para determinar el contraste óptimo entre el citoplasma y los núcleos para endocytoscopy. Figura 4 Etiquetado ejemplo del método: la figura 2 (A): Sin etiquetas. La figura 2 (B): La región de tejido enfermo segmentado está delimitada por una línea roja. Los puntos de la línea roja muestran los puntos de segmentación seleccionados manualmente
2. varianza textura global:. Varias medidas de textura son conocidos de la visión por ordenador en general y en particular de procesamiento de imágenes médicas con el fin de segmentación automática, clasificación o contenido basado recuperación de imágenes [37, 38].
Image textura puede ser descrito como una medida de la disposición espacial y la distribución de intensidad y /o color en una imagen. Dentro de estas disposiciones y distribuciones de la varianza se puede medir. Para las imágenes en la endoscopia esta puede ser la diferencia cuantitativa global en color y /o la intensidad entre el tejido de diferente histológico o naturaleza patológica y la varianza de intensidad /color entre estas áreas de tejido. Una imagen que muestra una alta textura es una imagen con una cantidad considerable de variación de la intensidad /color de distinguibles. Si al mismo tiempo la imagen presenta una alta varianza entre estas áreas de imagen que traducir esto a una imagen con textura de alta varianza. Cromoendoscopia tiene como objetivo mejorar la varianza global de la textura, poniendo de relieve las áreas de tejido en la mucosa gástrica con diferentes características lo más claramente posible. Un colorante óptima sería, por lo tanto, al máximo mejorar las áreas de tejido diferentes realmente existentes y causaría alta varianza en contraste entre estos diferentes texturas.
Una característica popular para describir la textura es el patrón local de binario (LBP) [39]. Este método ha sido aplicado ampliamente en el procesamiento de imágenes médicas y tiene, entre otras variaciones, ha ampliado para cuantificar la variación de la textura global de una imagen [40]. Asignamos una puntuación numérica v
un
r gratis (R
, N
) g
la que informalmente se puede definir como la variación de contraste en la imagen de textura.
El cálculo de v
un
r gratis (R
, N
) g
es el siguiente: El principio básico de la LBP es una caracterización discreto de los barrios de píxeles . Cada píxel de una imagen se le asigna un valor en función de cómo se relaciona con sus píxeles vecinos en términos de intensidad. El vecindario es generalmente definida por dos parámetros, que son el número de píxeles que se tienen en cuenta y la distancia entre el centro del píxel y sus vecinos. En LBP los vecinos están dispuestos en un círculo alrededor de un píxel central y por lo tanto la distancia simplemente puede ser definido por el radio del círculo. Cada píxel en este círculo se le asigna el valor 0, si su intensidad está por debajo de la intensidad del píxel central y el valor 1 si el valor de intensidad es mayor que la del píxel central. Para un píxel central con 8 vecinos que resultarían, por ejemplo, en un número binario de 8 dígitos que conduce a el nombre original de un patrón binario lineal. Un modelo LBP binaria en un centro de píxel p
c
en la posición (c
x
, c
y
) con su extremo N
vecinos píxels P _
n
a un radio R
por consiguiente, puede describirse como LBP (
R
,
N
)
(
c
x
, España c
y
)
= Σ
i
=
1 | N
b
(
p
n
(
i
)
-
p
c
x
, España c
y
)
×
2
N
(
d
→
 Los desinfectantes domésticos podrían contribuir al riesgo de obesidad en los niños
Los desinfectantes domésticos podrían contribuir al riesgo de obesidad en los niños
 ¿Puedes comer huevos cuando tienes diarrea?
¿Puedes comer huevos cuando tienes diarrea?
 Alergias relacionadas con un mayor consumo de comida chatarra,
Alergias relacionadas con un mayor consumo de comida chatarra,
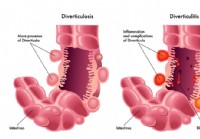 Enfermedad diverticular y diverticulitis
Enfermedad diverticular y diverticulitis
 ¿Qué elimina rápidamente la acidez estomacal?
¿Qué elimina rápidamente la acidez estomacal?
 ¿Qué debo comer cuando tengo acidez estomacal?
¿Qué debo comer cuando tengo acidez estomacal?
 Síntomas de hemorragia gastrointestinal crónica
El sangrado gastrointestinal crónico es un sangrado que generalmente es lento y puede continuar durante mucho tiempo o comenzar y detenerse en un corto período de tiempo. Los síntomas del sangrado
Síntomas de hemorragia gastrointestinal crónica
El sangrado gastrointestinal crónico es un sangrado que generalmente es lento y puede continuar durante mucho tiempo o comenzar y detenerse en un corto período de tiempo. Los síntomas del sangrado
 Cómo deshacerse de las náuseas y los vómitos
Náuseas y vómitos definición y hechos Las náuseas y los vómitos son síntomas de una enfermedad subyacente y no se deben a una enfermedad específica. Las náuseas y los vómitos son síntomas de una
Cómo deshacerse de las náuseas y los vómitos
Náuseas y vómitos definición y hechos Las náuseas y los vómitos son síntomas de una enfermedad subyacente y no se deben a una enfermedad específica. Las náuseas y los vómitos son síntomas de una
 Estudio de vaciamiento gástrico
¿Qué es un estudio de vaciamiento gástrico? El dolor abdominal puede ser un síntoma de vaciado gástrico lento. El tipo más común de estudio de vaciamiento gástrico es un procedimiento realizado por
Estudio de vaciamiento gástrico
¿Qué es un estudio de vaciamiento gástrico? El dolor abdominal puede ser un síntoma de vaciado gástrico lento. El tipo más común de estudio de vaciamiento gástrico es un procedimiento realizado por