LIM facteur de transcription à homéodomaine Isl1 dirige le développement du pylore normale en ciblant Gata3
Anomalies de résumé de l'arrière-plan dans le développement du pylore ou dans la fonction contractile de la cause reflux pylore du duodénum contenu dans l'estomac et augmentent le risque de métaplasie gastrique et le cancer. Anomalies de la région du pylore sont également liés à des malformations congénitales telles que la sténose relativement commune néonatale hypertrophique du pylore, et le reflux duodéno primaire. Par conséquent, la compréhension du développement du pylore est d'une grande importance clinique. Résultats de Ici, nous avons étudié le rôle du facteur de transcription LIM homéodomaine Isl1 dans le développement du pylore.
examen d'expression Isl1 dans le développement de l'estomac de la souris par immunohistochimie, toute la montagne de l'hybridation in situ de et PCR quantitative en temps réel ont démontré que Isl1 est fortement exprimé dans le développement de l'estomac de souris, principalement dans la couche musculaire lisse du pylore. expression Isl1 a également été examinée par immunofluorescence dans la sténose hypertrophique du pylore humaine où la majorité des cellules musculaires lisses ont été trouvés pour exprimer Isl1. Isl1 fonction dans le développement de l'estomac embryonnaire
a été étudiée en utilisant un modèle de souris knock-out tamoxifène inductible Isl1
. La carence Isl1 du conduit à une absence presque totale de la couche pylore musculaire longitudinale externe au jour embryonnaire 18,5, ce qui est cohérent avec Gata3 du phénotype de souris nulle. Immunoprécipitation de la chromatine, essais luciférase, et retard sur gel a révélé que Isl1 assure le développement du pylore normal en ciblant directement Gata3
.
Conclusions
Cette étude démontre que l'axe régulation de la transcription de l'Isl1-Gata3 est essentiel pour le développement du pylore normal. Ces résultats sont très cliniquement pertinentes et peuvent aider à mieux comprendre les voies menant à la maladie du pylore.
Mots-clés
muscle lisse α-actine Gata3 Isl1 Pylore Contexte
L'intestin vertébré est une structure remarquable qui ingère et digère la nourriture, absorbe les nutriments, et élimine les déchets. L'intestin provient d'une structure tubulaire simple, composé de trois couches germinales, y compris un endoderme sous-jacente, un mésoderme splanchnique entourant, et une ectoderme [1-3]. Dans les embryons de souris, l'intestin devient modelé le long de la dorsale-ventrale, gauche-droite antérieur-postérieur et axes radiaux. Le tube de l'intestin se compose de l'intestin antérieur, mésentéron et hindgut le long de son axe antéro-postérieur [4, 5]. Mesure que le développement progresse, l'intestin antérieur donne lieu à l'œsophage, l'estomac, le foie, les poumons et le pancréas. La forme mésogastre de l'intestin grêle et le gros intestin se développe dans le gros intestin [1, 5-8].
L'estomac est dérivé de l'intestin antérieur postérieur. L'estomac différencie morphologiquement du tube de foregut autour du jour embryonnaire 9,5 (de E9.5) et l'expansion du mésenchyme pré-gastrique permet le domaine de l'estomac pour être visible au début E10.5 [9]. Les cellules mésenchymateuses de l'estomac se différencient en quatre couches concentriques distinctes, y compris la lamina propria, muscularis mucosae, et le muscle lisse circulaire et longitudinale à différents stades du développement embryonnaire [10]. Par E11.5, l'estomac est nettement plus grande échelle. L'estomac muscle lisse différencie au E13, avec une couche distincte de l'actine α-muscle lisse (α-SMA) cellules -positifs apparaissant et une couche de muscle circulaire formant dans tout l'estomac [11]. La couche de muscle lisse épaissit dans la région resserrée du potentiel sphincter pylorique à environ E14.5 [2, 9]. Au'a 18,5, le sphincter pylorique commence à fonctionner en empêchant le reflux du contenu duodénal dans l'estomac [9].
La partie postérieure ou une partie pylorique de l'estomac est la jonction anatomique entre l'estomac et le duodénum. À l'extrémité du pylore, les volets valvulaires distincts du sphincter pylorique peut voir [2]. Dans des conditions physiologiques normales, l'estomac dépend de sa contraction péristaltique à broyer et la poussée des aliments partiellement digérés et le pylore repose sur le sphincter pylorique épaissie pour contrôler l'écoulement de nourriture dans l'intestin grêle. Anomalies du développement du pylore ou dans la fonction contractile du pylore provoquer le reflux du contenu du duodénum dans l'estomac et augmentent le risque de cancer gastrique et la métaplasie [12, 13]. Anomalies du pylore sont liés à des malformations congénitales [14-16]. Par conséquent, beaucoup d'attention a été accordée aux éléments de régulation et les voies de développement de l'estomac, en particulier le pylore et le développement du sphincter du pylore.
Données antérieures au poussin suggéré que la protéine morphogénétique osseuse (BMP) de signalisation régule l'expression mésenchymateuses de Nkx2.5
et Sox9
, ce qui affecte le caractère de l'épithélium pylore mais n'a aucun effet sur le muscle lisse du pylore [5, 17], ce qui suggère que la signalisation mésenchymateuses par des facteurs inconnus affecte le phénotype épithélial pylore. Chez la souris, les mécanismes moléculaires de la formation du pylore sont peu compris, avec relativement peu de facteurs nécessaires au développement du pylore normale ayant été identifiée. Ceux qui ont été incluent Sox9
[17], Six2
[9], Bapx1
[18], Nkx2.5
[3, 17], Gremlin
[9], et Gata3
[19, 20]. L'ablation du facteur de transcription à homéodomaine, Six2
exprimé dans l'estomac postérieur, perturbe l'épaississement de la couche de muscle lisse pylorique et atténue la constriction du sphincter pylorique. En outre, la perte de Six2
élimine Sox9 de l'expression, et réduit Nkx2.5
et Gremlin de l'expression dans le pylore, bien que cette expression recouvre plus tard [9], ce qui suggère que Six2
, Sox9
, Nkx2.5
et Gremlin
sont nécessaires pour le développement du pylore. En outre, Nkx2.5
, Sox9
et Gata3
sont co-exprimées dans la dorsale pylore de la couche musculaire longitudinale externe (OLM) qui vient à échéance entre E14.5 et E16,5. Après la suppression de Nkx2.5
ou Gata3
, la dorsale OLM pylore est presque absente et la constriction du sphincter du pylore est atténué [20].
La homéodomaine LIM (LIM-HD) facteur de transcription Isl1 était à l'origine trouvé pour fonctionner comme une protéine de liaison de l'activateur du gène de l'insuline [21]. Isl1 est composé de deux domaines tandem LIM et un homéodomaine. L'homéodomaine, avec sa structure hélice-tour-hélice, se lie à des séquences d'ADN régulatrices de gènes cibles, tandis que les domaines LIM sont principalement impliquées dans les interactions protéine-protéine qui régulent l'activité de la MFR-HD [22]. Isl1 joue un rôle critique dans la détermination cellulaire, la prolifération et la différenciation dans le système nerveux [23, 24], le coeur [25], et l'hypophyse [26]. En outre, l'expression Isl1 a été détectée dans mésenchyme gastrique [27, 28] et de l'épithélium gastro-intestinal chez les souris embryonnaires et adultes [29]. Toutefois, le rôle de Isl1 dans le développement de l'estomac n'a pas encore été exploré. Dans la présente étude, nous avons examiné l'expression Isl1 dans l'estomac. Isl1 a été fortement exprimé dans l'estomac postérieur dans les premiers stades de développement et est principalement restreinte aux cellules musculaires lisses de la pylore. Pour examiner la fonction Isl1 de dans le développement de l'estomac, nous avons utilisé un modèle de souris KO tamoxifène-inductible. Un modèle inductible était nécessaire parce que Isl1 - /-
mutants meurent à environ E10.5 en raison de défauts dans la formation du cœur. Nos résultats montrent que Isl1 est vital pour la formation de la couche d'OLM pylore pendant l'organogenèse de l'estomac.: Résultats
Isl1 est exprimé dans l'estomac de souris embryonnaires
Nous avons examiné les niveaux d'ARNm de Isl1 dans l'estomac de souris embryonnaires par réel PCR quantitative en temps (RT-qPCR) et monter l'ensemble dans l'hybridation (RÊVES) de situ. Isl1 de l'ARNm a été initialement détecté à E11.5 par RT-qPCR. Isl1
atteint le plus haut niveau à E13.5, suivie d'une forte baisse à E14.5, et a eu aucun changement significatif à l'âge adulte (fichier supplémentaire 1: Figure S1a). Ce résultat est semblable à un précédent rapport [29]. La localisation de l'expression de l'ARNm de Isl1 a été étudiée en utilisant WISH. Nous avons effectué Isl1 de la WISH dans l'estomac embryonnaire à E11.5, E13.5 et E14.5. À E11.5, Isl1
a été localisée à la moitié postérieure de l'estomac (fichier supplémentaire 1: Figure S1b). Cependant, le signal de Isl1 WISH était beaucoup plus forte et condensé dans le pylore par E13.5 (figure 1A). Comme le développement de l'estomac a progressé, le pylore ont continué à exprimer
Isl1 et l'expression de Isl1
étendue au sphincter pylorique prospective à E14.5 (fichier additionnel 1: Figure S1b). Cependant, le Isl1 de signal WISH affaibli considérablement de E13.5 à E14.5. Ces Isl1 de résultats WISH souscrit aux résultats Isl1
RT-qPCR. Figure 1 Isl1 est exprimée dans le développement de l'estomac de la souris. (A) Embryonic analyse WISH de l'estomac a démontré que Isl1 de l'expression était limitée à la pylore à E13.5 (flèche). (B) de coloration immunohistochimique pour Isl1 dans l'estomac. Les articles à partir d'embryons ont été disposés en rostrale à la séquence caudale à E11.5 et E13.5, et l'expression Isl1 était principalement localisée au mésenchyme de l'estomac postérieur. A E14.5 et'a 18,5, Isl1 a été fortement exprimé dans les cellules musculaires lisses du pylore, bien qu'il y ait certaines cellules Isl1 positif dans la lamina propria (pointes de flèches). images agrandies dans les régions en boîte sont présentés ci-dessous des images originales. D duodénum; Liv, le foie; Pa, du pancréas; St, de l'estomac. Les barres d'échelle des images originales: 100 um; barres d'images agrandies à l'échelle:. 50 pm
Nous avons ensuite évalué Isl1 expression de la protéine par immunohistochimie. Les résultats ont démontré que Isl1 était principalement localisée dans le mésenchyme de l'estomac postérieur de E11.5 à E13.5, puis Isl1 a été exprimé dans les cellules musculaires lisses du pylore (Figure 1B et fichiers supplémentaires 1: Figure S1c), et a également été détectée dans le lamina propria (Figure 1B, pointes de flèches). Dans l'estomac de souris adultes, seulement quelques cellules Isl1-positifs ont été observés dans la couche de muscle lisse. (Fichier supplémentaire 1: Figure S1c)
cellules Isl1 positives sont co-exprimées avec α-actine musculaire lisse dans l'estomac de souris embryonnaires
pour voir si l'expression Isl1 était liée à lisser le développement musculaire du pylore, nous avons examiné l'expression de Isl1 et par immunofluorescence premiers marqueurs musculaires lisses α-SMA. Les résultats ont montré que la proportion de cellules positives exprimant Isl1 α-SMA a progressivement augmenté (figure 2). À E11.5, pas de cellules α-SMA-positives ont été détectées, bien que Isl1 a été fortement exprimé dans le mésenchyme de l'estomac postérieur. À E14.5, un sous-ensemble de cellules Isl1-positives, principalement celles dans le muscle circulaire interne (ICM) du pylore, étaient α-SMA positif. Par E16,5, pylore OLM a déjà fait l'objet d'une différenciation [20]. À'a 18,5, la majorité des cellules positives Isl1 dans le pylore étaient α-SMA positif. expression Isl1 a persisté dans ICM pylore mature et OLM, et les cellules de la lamina propria a également exprimé Isl1 (fichier additionnel 1: Figure S2). En outre, l'expression Isl1 a été examiné dans des échantillons humains de la sténose hypertrophique du pylore par immunofluorescence, et les résultats ont démontré que Isl1 a également été exprimé dans les cellules musculaires lisses humaines du pylore (fichier additionnel 1: Figure S3). Par conséquent, ces résultats suggèrent que Isl1 peut participer à la formation du sphincter pylorique. Figure 2 Double immunomarquage pour Isl1 et α-actine musculaire lisse dans la souris des cellules musculaires lisses de la pylore dorsale. Isl1 et α-SMA co-expression dans les cellules musculaires lisses à E11.5, E14.5 et'a 18,5. pointillés jaunes marquent la membrane basale épithéliale, des lignes pointillées épaisses blanches indiquent ICM et OLM limite, et les lignes pointillées blanches indiquent OLM et la limite du pancréas. coloration rouge est Isl1, coloration verte est l'a-SMA, et contre-coloration nucléaire DAPI (ADN) est bleu. α-SMA, α-actine musculaire lisse; ICM, muscle circulaire intérieure; OLM, muscle longitudinal externe; Pa, du pancréas; St, de l'estomac. Barres d'échelle:. 50 um expression Isl1 est effectivement de ablatée dans Isl1
MCM /F
souris knockout inductible par
Pour étudier les effets de Isl1 de l'ablation sur le développement de l'estomac, nous avons utilisé Isl1
MCM /F
inductible par Cre (Isl1
MCM /Del
) souris (figure 3A) et Isl1
F /+ m
glace étaient utilisés comme témoins [30, 31]. Les embryons ont été génotypés par PCR à'a 18,5 (fichier additionnel 1: Figure S4) et intacte ou mutant Isl1 de l'ARNm a été distingué par PCR semi-quantitative (figure 3B). Figure 3 Efficacité de Isl1 ablation dans les estomacs de Isl1 MCM /Del estomacs de souris mutante à'a 18,5. (A) Tamoxifen-inductible recombinase Cre excise des séquences d'ADN flanqué par deux sites loxP de
. Les niveaux d'ARN de (B) Isl1 ont été ablater dans Isl1
estomacs mutantes de MCM /Del vu par PCR semi-quantitative. Isl1
F /+ m
glace a montré un produit de paire 592 de base alors que la souris de Isl1
MCM /Del généré un produit de 303 paires de base. (C) Isl1 était significativement régulée à la baisse sur les taux de protéines dans les estomacs mutantes de Isl1
MCM /Del comme indiqué par western blot. Expression d'embryons à E11.5 a été utilisé comme témoin positif. (D) Isl1 expression de la protéine dans Isl1
F /+ a
nd Isl1
MCM /pylore embryonnaire
Del. l'expression Isl1 était significativement réduite dans Isl1 de MCM /estomacs embryonnaires de Del, comme on le voit par immunofluorescence. Images à Isl1
F /+ a
nd Isl1
MCM /Del
ont été traitées sur la même lame et photographié à la même exposition. images agrandies des zones encadrées sont indiquées sur le côté droit des images fusionnées. flèches jaunes montrent les cellules Isl1 positives représentatives, et des pointes de flèches blanches montrent les cellules Isl1 négatif représentatives. pointillés jaunes marquent la membrane basale épithéliale. Barres d'échelle:. analyses 50 um
Western blot ont montré que les niveaux de protéines dans l'estomac Isl1 embryonnaire de Isl1
MCM /les souris Del de étaient significativement plus faibles que ceux de Isl1
F /+ m
glace (figure 3C). les résultats d'immunofluorescence démontré significativement réduit Isl1 coloration dans le pylore de Isl1
MCM /Del de les souris par rapport aux témoins (Figure 3D). Ces données démontrent que Isl1 de l'expression était effectivement régulée à la baisse dans Isl1
MCM /Del
Les estomacs mutantes.
Anomalies pyloriques dans Isl1
mutants de MCM /F
Pour étudier les effets de Isl1 de l'ablation sur le développement de l'estomac, nous avons comparé les différences morphologiques et histologiques entre Isl1
MCM /Del
et Isl1
F /+ s
tomachs à'a 18,5. A'a 18,5, liquide jaune a été observée dans Isl1
MCM /Del de l'estomac, mais pas dans les estomacs de Isl1
F /+ l
ittermates (figure 4A, astérisque) . L'examen histologique a démontré que la couche de muscle lisse dorsale du pylore était beaucoup plus mince dans le pylore de Isl1
Les souris de MCM /Del par rapport aux témoins (figure 4B). Nous avons examiné l'expression et la distribution des α-SMA dans les deux Isl1
MCM /mutants Del et de Isl1
F /+ p
ylorus. les résultats d'immunofluorescence ont montré que la carence en Isl1 a conduit à une absence presque complète de la couche d'OLM pylore à'a 18,5, et les cellules restantes ont été mal organisés (figure 5A, astérisques). En outre, la constriction du sphincter du pylore a été atténuée dans Isl1
MCM /estomacs mutantes de Del en comparaison avec constriction dans Isl1
F /+ s
tomachs (figure 5B) . En outre, nous avons analysé l'expression de la protéine spécifique du muscle lisse calponin-1 à'a 18,5 et immunofluorescence résultats ont démontré que la perte de Isl1 a également abouti à une quasi-absence de calponine-1 expression dans la couche OLM pylore dorsale, semblable au résultat d'α- SMA (fichier supplémentaire 1: Figure S5). Sox9 est exprimé à la fois épithélium et mésenchyme [9] et est nécessaire pour le développement des OLM et la formation de pylore sphincter constriction [20]. Nos résultats d'immunofluorescence ont montré que Sox9 est restée à des niveaux normaux dans l'épithélium de l'estomac de Isl1
la souris de MCM /Del à E14.5 et'a 18,5 (Figure 6, pointes de flèches), mais la zone du muscle lisse pylorique exprimant Sox9 a été significativement réduite dans Isl1
MCM /mutants Del de chez E14.5 (Figure 6A, astérisques) et absents à'a 18,5 (figure 6B, astérisques). Ainsi, Isl1
était nécessaire pour Sox9 de l'expression dans les cellules OLM pyloriques dorsales. Ces résultats indiquent que Isl1 est essentielle pour la régulation du développement de la souris muscle lisse pylorique. Figure 4 Morphologique et les changements histologiques dans le développement de l'estomac des mutants Isl1 MCM /Del. (A) brut et des preuves microscopiques pour les défauts de l'estomac chez les souris de Isl1
MCM /Del. Le total des points de vue à monter'a 18,5 en Isl1
F /+ Les estomacs de souris
un
e Isl1
MCM /Del. Isl1
MCM /estomacs mutants Del manquait un sphincter pylorique fonctionnel (pointe de flèche), permettant ainsi le reflux de fluide comme observé dans les embryons mutants. fluide jaune est désigné par astérisque. (B) hématoxyline et éosine de Isl1
F /+ un pylore de la souris
nd Isl1
MCM /Del au'a 18,5. La dorsale muscle lisse pylore (noir région encadré) était importante dans Isl1
F /+ e
mbryos, mais était beaucoup plus mince dans les embryons de Isl1
MCM /Del. Le reste du pylore est histologiquement normal. pointillés verts marquent la membrane basale épithéliale. images agrandies dans les régions en boîte sont présentés ci-dessous des photos originales. Barres d'échelle de photos originales: 200 um; barres d'échelle des images agrandies: 50 pm. H &. E, hématoxyline et éosine
Figure 5 Perte de Isl1 perturbe la formation de la dorsale du pylore muscle longitudinal externe. (A) Immunofluorescence de Isl1 et α-SMA dans Isl1
F /+ a
nd Isl1
MCM /pylore embryonnaire Del au'a 18,5. Perte de Isl1 a entraîné la perte de presque complète des cellules a-SMA-positif dans le OLM pylore dorsale (astérisques). pointillés jaunes marquent la membrane basale épithéliale et les lignes pointillées blanches indiquent ICM et OLM limite. coloration rouge est Isl1, coloration verte est l'a-SMA, et contre-coloration nucléaire DAPI (ADN) est bleu. Barres d'échelle: 50 um. (B) α-SMA immunofluorescence de Isl1
F /+ a
nd Isl1
MCM /pylore embryonnaire Del au'a 18,5. Par rapport à Isl1
F /+ e
mbryos, le sphincter constriction pylore était plus large dans les animaux de Isl1
MCM /Del. mesures sphincter de constriction sont présentés. Les barres jaunes délimitent le pylore et mettent en évidence la différence marquée de largeur entre Isl1
F /+ a
nd Isl1
échantillons
MCM /Del. Les données sont la moyenne ± SEM (n = 6
souris par groupe), * P
< 0,05 (t de Student
-test). Barres d'échelle: 50 um. α-SMA, α-actine musculaire lisse; ICM, muscle circulaire intérieure; OLM, muscle longitudinal externe.
Figure 6 Perte de Isl1 élimine le pylore longitudinal expression Sox9 musculaire externe dorsale. (A) Double immunomarquage pour Isl1 et Sox9 dans le pylore dorsal à E14.5. En l'absence de Isl1, le domaine des cellules mésodermiques (astérisques) exprimant Sox9 était plus petite. (B) Double immunomarquage pour Isl1 et Sox9 dans le pylore dorsale au'a 18,5. Inductible KO Isl1 effectivement éliminé l'expression Isl1, avec perte concomitante de l'expression dans les cellules Sox9 dorsale OLM (astérisques). expression Sox9 était normale dans l'épithélium de l'estomac aux deux étapes (pointes de flèches). pointillés jaunes marquent la membrane basale épithéliale et les lignes pointillées blanches ICM séparée et OLM. coloration rouge est Isl1, coloration verte est Sox9, et contre-coloration nucléaire DAPI (ADN) est bleu. Barres d'échelle: 50 um. ICM, muscle circulaire intérieure; OLM, muscle longitudinal externe. De l'expression et de la distribution du produit du gène de la protéine 9,5 (de PGP9.5), un marqueur du système nerveux entérique [32], était intacte au'a 18,5 en Isl1
MCM /Del
estomacs mutantes (fichier supplémentaire 1: Figure S6). gène pancréatique et duodénal homeobox 1 (Pdx1) est exprimé dans les cellules epitheliales du segment antrale-pylore et le duodénum rostrale [33]. Nos résultats d'immunofluorescence ont montré que l'expression de Pdx1 était similaire dans Isl1
MCM /Del
souris par rapport aux témoins à'a 18,5 (fichier additionnel 1: Figure S7). En outre, l'estomac de souris et de l'épithélium limite duodénale a été établie entre E14.5 et E16,5 [34], cette période coïncidant avec le développement de la couche de OLM [20]. Nous avons testé l'intégrité de l'intestin frontière pylore épithéliale de l'estomac-petit à'a 18,5 en examinant l'expression d'un marqueur épithélial Cdx2 spécifique de l'intestin [19]. Nos résultats d'immunohistochimie ont démontré que la position de la frontière du pylore épithéliales dans Isl1
souris
MCM /Del était similaire à celle des témoins (fichier supplémentaire 1: Figure S8). Ces résultats indiquent que la perte de Isl1 n'a aucune incidence sur l'innervation ou le développement épithélial du pylore.
Perte de Isl1 n'a aucune incidence sur la prolifération ou l'apoptose des pylore muscle circulaire interne et les cellules musculaires longitudinales extérieures
Pour voir si l'expression Isl1 était liée la prolifération cellulaire du pylore, nous avons examiné la co-localisation de la bromodésoxyuridine et Isl1 proliférative marqueur (BrdU) à l'aide immunofluorescence Isl1
F /+ m
glace. Nos résultats ont montré que les cellules positives à la BrdU étaient denses à E11.5 et dispersés dans les régions ICM et OLM à E14.5 et'a 18,5 (fichier supplémentaire 1: Figure S9a). En outre, la proportion de cellules proliférantes ICM et OLM n'a pas été significativement différent entre Isl1
MCM /Del
et Isl1
F /+ m
glace à'a 18,5 ( fichier supplémentaire 1:. Figure S9b)
Pour évaluer un impact potentiel sur l'apoptose, nous avons examiné clivé Caspase 3 expression à'a 18,5, et nos résultats d'immunofluorescence a montré qu'il n'y avait pas Caspase 3 positif cellules dans ICM pylore ou la couche OLM de Isl1
MCM /Del
et Isl1
F /+ m
glace (fichier supplémentaire 1: Figure S10). Ces données indiquent que l'ablation Isl1 n'a aucune incidence sur la prolifération ou l'apoptose des ICM pylore et les cellules OLM.
Perte des résultats Isl1 en diminution de l'expression de Gata3
, Gremlin
et Nkx2.5
Depuis un nombre de facteurs, y compris Bapx1
[18], Barx1
[35], Gata3
[19, 36], Gremlin
[5], Nkx2.5
[2] et Six2
[9], ont été signalés à être impliqué dans la régulation du développement du pylore, nous avons examiné les effets de la perte de Isl1 sur l'expression de ces gènes à E14.5 et'a 18,5. résultats RT-qPCR ont montré que la perte de Isl1
n'a pas d'incidence sur l'expression de Bapx1
ou Barx1
soit à E14.5 ou'a 18,5 (figure 7A, B). A'a 18,5, α-SMA
et les taux d'ARNm de Six2 étaient significativement plus faibles dans Isl1
souris
MCM /Del par rapport aux témoins (Figure 7B). A la fois les taux d'ARNm de Gremlin dans l'estomac de Isl1 E14.5 et'a 18,5, Nkx2.5
, Gata3
et
Les souris de MCM /Del étaient inférieurs contrôles (figure 7A, B). Les taux d'ARNm de GATA3 ont diminué d'environ 70% dans les deux étapes examinés (figure 7A, B). Sur la base de ces résultats, nous avons étudié Isl1
, Gata3
, Gremlin
et Nkx2.5 de l'expression dans Isl1
MCM /F
mutant et Isl1 F /+ s
tomachs utilisant WISH. Les résultats ont démontré que l'expression de chacun de ces gènes était principalement limitée à la région du pylore, comme prévu; L'expression Gata3 de plus a été réduit dans les estomacs mutantes; et Gremlin
et Nkx2.5
seulement eu des changements subtils (Figure 7E, F).
Isl1 et Gata3 de l'expression ont été les plus fortement touchés (Figure 7C, D). Ces résultats concordent avec les données RT-qPCR et suggèrent que Isl1 régule l'expression de Gata3
, Gremlin
et Nkx2.5
. Figure 7 d'expression génique Aberrant en hindstomach mutants Isl1 MCM /Del. (A) Analyse par RT-PCR quantitative des taux d'ARNm de facteurs de transcription enrichis hindstomach à E14,5 indique une réduction significative des α-SMA
, Six2 Nkx2.5
, Gata3
et Gremlin de l'ARNm dans Isl1 de MCM /estomacs mutantes de Del (n
= 4). Tous les résultats ont été normalisés à des niveaux de Gapdh de l'ARNm. (B) Analyse par RT-PCR quantitative des taux d'ARNm de facteurs de transcription enrichis en hindstomach'a 18,5 indique une réduction significative de Nkx2.5
, Gata3
et Gremlin de l'ARNm dans le Isl1
MCM /estomacs mutantes de Del (n
= 4). Tous les résultats ont été normalisés à des niveaux de Gapdh de l'ARNm. Les données sont la moyenne ± SEM (n = 6
souris par groupe). * P
< 0,05 par rapport Isl1
F /+
; ** P
< 0,01 par rapport Isl1
F /+
(t de Student
-test). (CF) analyse WISH d'ARNm a confirmé la perte de Isl1
, Gata3
, Gremlin
et expression Nkx2.5
ARNm à E14.5 dans le mutant du Isl1
MCM /Del estomacs. Isl1
et Gata3 de l'ARNm ont été sévèrement régulés à la baisse dans les souris de Isl1
MCM /Del, alors que Gremlin
et Nkx2.5 de l'expression ont été légèrement réduits. Les flèches pointent vers le sphincter pylorique.
Isl1 cible Gata3
et active sa transcription
Gata3
est exprimé sélectivement dans le pylore de l'embryon de souris en développement [19, 20]. Expression des deux Isl1
et Gata3 de l'ARNm a été observée dans le pylore à E14.5, mais si Gata3 et Isl1 sont exprimés dans les mêmes cellules n'a pas été explorée. Par conséquent, nous avons examiné l'expression de Isl1 et Gata3 par analyse immunofluorescence. Les résultats ont démontré que les protéines et Isl1 GATA3 ont été co-exprimés dans les mêmes cellules du pylore à E14,5 et dans'a 18,5 Isl1
F /+ c
ontrôle estomacs (figure 8). En outre, la zone exprimant Gata3 était significativement plus faible dans Isl1
MCM /Del de couche de muscle mutant pylore lisse à E14.5 (figure 8A) et il a été perdu à'a 18,5 dans la couche d'OLM pylore (figure 8B). Ainsi, Isl1
était nécessaire pour Gata3 de l'expression dans la couche dorsale OLM pylore. Afin de déterminer si Isl1 régule le développement de pylore en régulant directement Gata3
, nous avons effectué l'analyse bioinformatique du locus génomique Gata3. le gène de la souris Gata3 contient plusieurs éléments de réponse Isl1 putatifs (ATTA /TAAT), à -2,832 paires de bases (pb) à 1002 pb à partir des sites d'initiation de transcription [37]. Nous avons identifié 10 zones qui contenaient place (Figure 9A) liant un Isl1 putative, et 10 paires d'amorces correspondantes ont été conçues pour amplifier ces régions suivantes immunoprécipitation de la chromatine (ChIP) études utilisant l'anticorps à Isl1. L'ADN génomique immunoprécipité a été obtenu auprès pyloriques régions d'embryons de souris à E14.5. Sur les 10 zones de liaison Isl1 putatifs, deux régions discrètes, dans le -2558 pb à -2303 pb (région P1) et -1081 pb à -855 pb (région P6), étaient occupées par des protéines Isl1. Ce résultat a été confirmé par PCR semi-quantitative (figure 9B) et le procédé d'enrichissement de pliage (figure 9C). Figure 8 Perte de Isl1 élimine le pylore muscle longitudinal externe Gata3 expression dorsale. (A) Double immunomarquage pour Isl1 et Gata3 dans le pylore dorsal à E14.5. La région de cellules mésodermiques (astérisques) exprimant Gata3 était plus petit dans le pylore du Isl1
MCM /Del que Isl1
Fl +
. (B) Double immunomarquage pour Isl1 et Gata3 dans le pylore dorsale au'a 18,5. Inductible KO Isl1 effectivement éliminé l'expression Isl1, avec perte concomitante d'expression dans les cellules Gata3 dorsale OLM (astérisques). pointillés jaunes marquent la membrane basale épithéliale et les lignes pointillées blanches indiquent la limite ICM et OLM. arrowhead blanc indique la tache non spécifique. Tous les auteurs ont lu et approuvé le manuscrit final.
 Un test sanguin pour l'ADN microbien pourrait mettre en garde contre le cancer
Un test sanguin pour l'ADN microbien pourrait mettre en garde contre le cancer
 La greffe de selles apaise la colite difficile à traiter dans une étude
La greffe de selles apaise la colite difficile à traiter dans une étude
 Comment fonctionne un shunt portosystémique intrahépatique transjugulaire ?
Comment fonctionne un shunt portosystémique intrahépatique transjugulaire ?
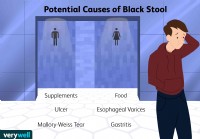 Quelles sont les causes des selles noires ?
Quelles sont les causes des selles noires ?
 Combattre le ballonnement d'été
Combattre le ballonnement d'été
 Le stress peut être dur pour votre estomac
Le stress peut être dur pour votre estomac
 essai routier d'un service de livraison à domicile sibo
Bonne nouvelle ! il existe désormais un service Sibo de livraison à domicile de plats cuisinés à Melbourne Il y a plusieurs semaines, jai été contacté par Tracey Sisson de Yardmill, propriétaire et f
essai routier d'un service de livraison à domicile sibo
Bonne nouvelle ! il existe désormais un service Sibo de livraison à domicile de plats cuisinés à Melbourne Il y a plusieurs semaines, jai été contacté par Tracey Sisson de Yardmill, propriétaire et f
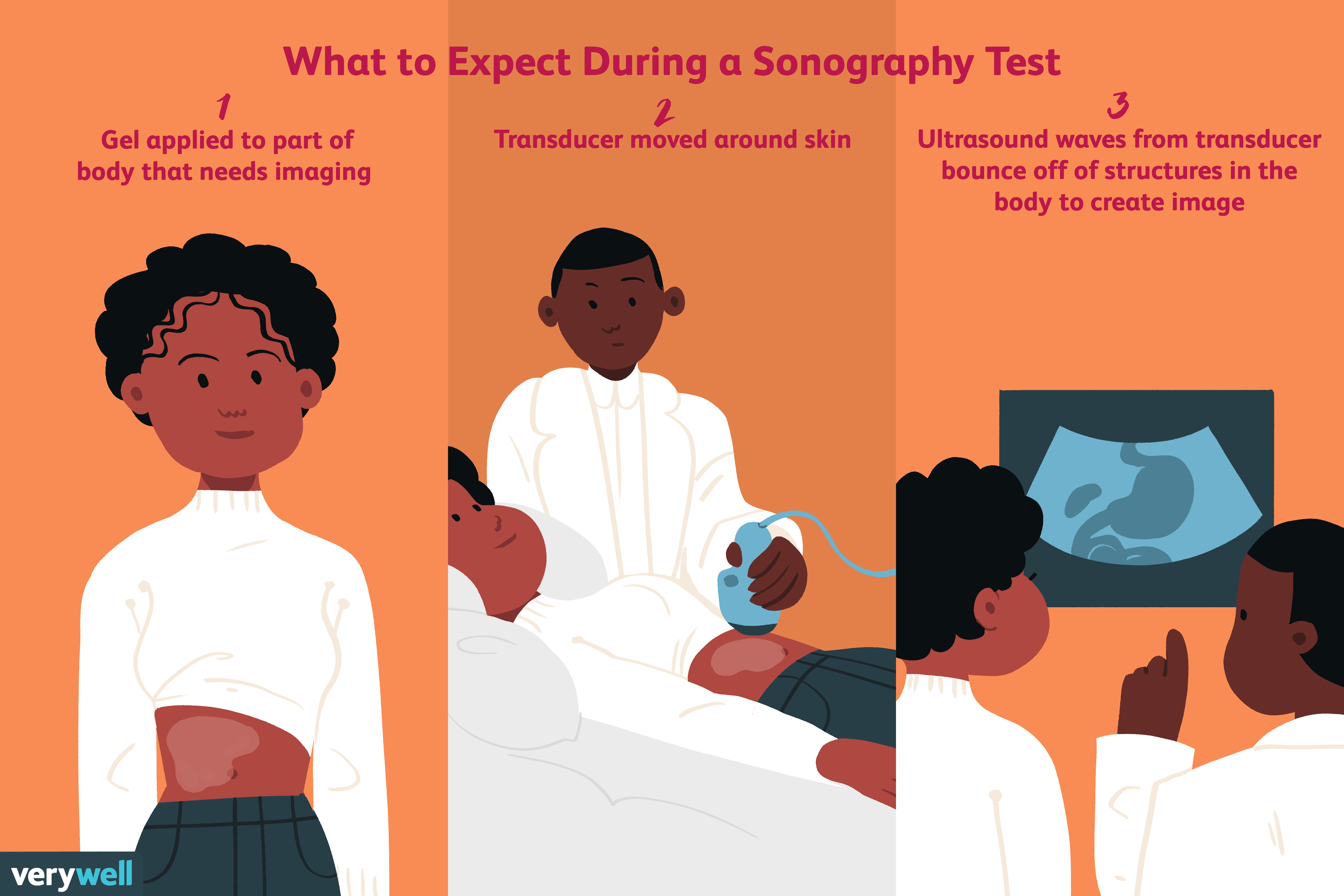 Qu'est-ce que l'échographie ?
Léchographie est un test médical de diagnostic qui utilise des ondes sonores à haute fréquence, également appelées ondes ultrasonores, pour rebondir sur les structures du corps et créer une image. À j
Qu'est-ce que l'échographie ?
Léchographie est un test médical de diagnostic qui utilise des ondes sonores à haute fréquence, également appelées ondes ultrasonores, pour rebondir sur les structures du corps et créer une image. À j
 Votre microbiome intestinal – Où commence votre santé
Le dernier grand sujet de santé est le microbiome intestinal et ses effets sur notre santé. Je suis sûr que vous avez entendu dautres médecins le mentionner à plusieurs reprises, alors jai pensé comme
Votre microbiome intestinal – Où commence votre santé
Le dernier grand sujet de santé est le microbiome intestinal et ses effets sur notre santé. Je suis sûr que vous avez entendu dautres médecins le mentionner à plusieurs reprises, alors jai pensé comme