Stress bidrar til en rekke forskjellige sykdommer og forstyrrelser slik som depresjon og magesår. Denne studien forsøkte å undersøke sammenhengen mellom stress sår og depresjon i patogenesen og behandling ved hjelp av kronisk stress depresjon (CSD), kronisk psykologisk stress sår (SUKP) og vann nedsenking begrense spennings modeller i rotter. Våre data viser at den sårindeks av dyrene etter CSD eksponering var signifikant høyere enn for kontrollene. Depresjon-lignende atferd ble observert hos rotter etter CPSU eksponering. Fluoxetinhydroklorid betydelig redusert sårindeks av rotter eksponert for CPSU stress, mens ranitidin hemmet depresjon-lignende oppførsel av dyrene i CSD gruppe. Såret indeks av rotter administrert med mifepriston etter CPSU stresset ble kraftig redusert i forhold til CPSU gruppe, selv om det var ingen signifikant forskjell i depresjon-lignende oppførsel mellom mifepriston behandlet CSD gruppe og naive kontroller. Vi fant også at rotter eksponert for CPSU eller CSD stresset vises et lavere nivå av kortikosteron enn naive kontroller, men det akutt stress (AS) gruppen viste en motsatt resultat. I tillegg, for å studere betydningen av H 2-reseptorer og depresjon, behandlet vi CSD gruppe med cimetidin og famotidin respektivt. Dataene viste at cimetidin hemmet depresjon-lignende oppførsel i CSD rotter, og famotidin hadde ingen innvirkning på depresjon. Samlet våre data antydet at hypothalamus-hypofyse-binyre (HPA) aksen dysfunksjon kan være en nøkkelrolle i å utløse depresjon og stress sår. Syre-undertrykkende midler og antidepressiva kan brukes for behandling av depresjon og stress sår henholdsvis. Forekomsten av depresjon kan inhiberes ved å blokkere den sentrale H 2-reseptorer relasjon:. Zhang S, Xu Z, Y Gao, Wu Y, Z Li Liu H, et al. (2012) Toveis Høring mellom stress-indusert magesår og depresjon etter kronisk stress. PLoS ONE 7 (12): e51148. doi: 10,1371 /journal.pone.0051148 Redaktør: Andrzej T. Slominski, University of Tennessee, USA mottatt: 28 juni 2012; Godkjent: 29 oktober 2012; Publisert: 12.12.2012 Copyright: © 2012 Zhang et al. Dette er en åpen-tilgang artikkelen distribueres under betingelsene i Creative Commons Attribution License, som tillater ubegrenset bruk, distribusjon og reproduksjon i ethvert medium, forutsatt den opprinnelige forfatteren og kilden krediteres Finansiering:. Dette arbeidet ble støttet av National Basic Research Project (973 program) (2012CB518200), General program (81100979, 81070741, 30900830) of Science Foundation of China Natural, og spesiell nøkkel programmer for Science and Technology of China (2012ZX09102301-016). Finansiører hadde ingen rolle i studiedesign, datainnsamling og analyse, beslutning om å publisere, eller utarbeidelse av manuskriptet Konkurrerende interesser:.. Forfatterne har erklært at ingen konkurrerende interesser eksisterer Innledning hans Selye var en klinisk endokrinolog og eksperimentell biolog som fokuserer sin innsats på studier av stressresponser [1]. Han først introdusert begrepene stress, stressor, eustress, nød, og "Generelt Adaptation Syndrome" (GAS). Han definerte stress som den mislykkede svar av en person til en følelsesmessig eller fysisk trussel [2] - [6]. Kronisk fysisk og psykisk stress har alvorlige skadelige effekter på et individ, og stressrelaterte lidelser har blitt en betydelig folkehelseproblem. De vanligste stress-relaterte lidelser påvirker fordøyelsessystemet, inkludert stress-sår og irritabel tarmsyndrom [7], samt i sentralnervesystemet, inkludert psykiatriske forstyrrelser slik som depresjon og angst [8]. Selv magesår var forårsaket av forstyrrelser i mage mucosal defensiv barriere [9], [10], er depresjon en komplisert følelsesmessig og fysisk reaksjon som den underliggende mekanismen var fortsatt ikke forstått. Faktorer som induserer enten stressmavesår eller depresjon kan inneholde kirurgi, traumer og følelsesmessig stress. Hypothalamus-hypofyse-binyre (HPA) aksen er en vesentlig del av det nevroendokrine system som gjenkjenner påkjenninger og styrer reaksjoner. Stressresponsen av HPA-aksen innebærer frigjøring av flere hormoner med ulike kognitive, fysiske, følelsesmessige og atferdsmessige konsekvenser. En undersøkelse av 104 pasienter med ulike krefttyper identifisert varierende kortikosteroid nivå som var nært korrelert med depresjon, smerte og tretthet [11]. Gastrisk blødning hos rotter eksponert for akutt nedsenking i vann og tilbakeholdenhet er knyttet til redusert gastrisk pH og forhøyet adrenokortikotropt hormon (ACTH) nivåer [12], [13], som tyder på rollen til HPA-akse i stressmavesår dannelse og utvikling. Selv om flere studier har blitt viet til å forstå de nevroendokrine komponentene av stress sår og depresjon, forblir mye ukjent. Grunnleggende ubesvarte spørsmål omfatte om induksjon av stress sår og utbruddet av depresjon deler en felles etiologi, og om farmakologisk intervensjon av en stressrelaterte lidelse påvirker andre eller vice versa. H 2-reseptoren antagonister er en klasse av medikamenter som cimetidin (Cim), ranitidin, famotidin og nizatidin som hemmer mavesyre-sekresjon fra parietalceller, for derved å beskytte den gastriske mucosa. Imidlertid har rollen som hjernen H 2 reseptorer, spesielt knyttet til depresjon og depresjon lignende atferd ikke blitt offentliggjort ennå. Histamin er kjent for å aktivere HPA-akse ved å påvirke H 2-reseptoren i hjernen, noe som fører til økning i serum kortikosteronnivået og indusere depresjon-lignende oppførsel. Ranitidin, cimetidin og famotidin er H 2-reseptorantagonister mye brukt i klinisk praksis. I tillegg til deres virkninger på fordøyelsessystemet, kan ranitidin og cimetidin passere over blod-hjernebarrieren (BBB) og trolig komme i kontakt med hjernen H 2-reseptorer, men famotidin ikke har muligheten til å få tilgang til sentralnervesystemet ved å penetrere BBB. I dette scenariet, vil H 2-reseptorantagonister tjene til å undertrykke depresjon-lignende atferd. Støtte denne hypotesen, kliniske observasjoner av den mentale tilstanden til pasientene led av magesår rapporterte at angst og depresjon skala ble betydelig forbedret sammenlignet med placebo etter 4 ukers behandling med ranitidin ( P Dyr Voksne Sprague-Dawley (SD) rotter som veide 200 -220 g, ble kjøpt fra Animal Senter Laboratory (Laboratory Animal Centre, Military Academy of Medical Sciences). Hver 9 dyr ble plassert i polyetylen bur (485 mm × 350 mm × 200 mm) under vanlige boforhold (12/12 timers lys-mørke-syklusen starter på 7:00, temperatur 22 ± 2 ° C, fri tilgang til mat og vann) i 6-7 dager før initiering av eksperimentet. Alle forsøk ble gjennomført for å redusere dyrs lidelser etter forslag fra International Ethical Retningslinje for Biomedical Research (CIOMS /OMS, 1985). Voksen SD hannrotter ble tilfeldig delt inn i 10 grupper ( n = 9 per gruppe): kontrollgruppen fikk saltløsning (3 ml, po); kronisk psykologisk stress (sår forming, omtalt som CPSU, behandlet med saltvann, 3 ml, p.o.); kronisk stress (som fører til depresjon, CSD, behandlet med saltløsning, 3 ml, p.o.); akutt stress (AS); CPSU behandlet med ranitidin (histamin H 2-reseptorantagonist, 150 mg /kg, p.o.); CPSU behandlet med fluoksetin-hydroklorid (selective serotonin gjenopptak-inhibitor, 1,8 mg /kg, p.o.); CPSU behandlet med mifepriston (glukokortikoidreseptorantagonist, 65 mg /kg, p.o.); CSD behandlet med fluoksetin-hydroklorid (1,8 mg /kg, p.o.); CSD behandlet med ranitidin (150 mg /kg, p.o.); og CSD behandlet med mifepriston (65 mg /kg, p.o.). Et andre sett av undersøkelser ble utført hvori SD-rotter ble utsatt for kronisk stress depresjon i nærvær av cimetidin (150 mg /kg, p.o. n = 9) og famotidin (150 mg /kg p.o. n = 9). Legemidler ble oppløst i saltvann. Alle legemiddel løsninger ble tilberedes og administreres en time før reke eksponering. Restraint ble brukt til å indusere CPSU. Kort sagt ble naive rotter anbragt i en regulerbar akryl hemi-sylindrisk plastrør (5 cm diameter og 12 cm i lengde), som tidligere rapportert [15]. Rottene ble begrenset individuelt og eksponert i en periode på 4 t om dagen i 28 dager etter hverandre. Den store fordelen med immobilisering er at den produserer både uunngåelig fysisk og psykisk stress [16]. Rotter ble utsatt for vann nedsenking holdenhet stresset (WIRS) hvor behersket i rustfritt stål bur og nedsenket til sin xifoid i et vannbad som ble holdt ved 23 ± 2 ° C. Etter eksponering i fire timer ble dyrene avlivet [17]. CSD ble utført som beskrevet med noen endringer [18]. Rotter ble utsatt for en av ni randomisert stressfaktorer gang daglig i de neste tjue-åtte dager. Disse involvert mat deprivasjon i 48 timer; vann deprivasjon i 24 timer; hale klype (1 cm fra hverandre fra enden av halen) i 5 minutter; overheng i 5 min; dag og natt omvendt; 12 ° C kaldt vann svømming for 5 min; risting-trengsel i 1 time; eller 23 ± 2 ° C vann svømming for 10 min. Tvungen Svømming Test Tvungen svømmetest (FST) ble utført som beskrevet [19]. Kort fortalt forsøket besto av to tvinger svømme økter. På den første dag, ble rottene individuelt plassert i test sylinder (60 cm i høyde og 30 cm i diameter) fylt til en dybde på 20 cm med vann (25 ° C) i 15 min. Dyrene ble anbragt i et pleksiglassboks i 30 minutter under en 60-W-pære for å tørke av etter fjerning fra vannet og håndkletørking. Tjuefire timer etter den første økten, ble dyrene plassert tilbake i sylinderen individuelt for 6 min. Den totale periode med immobilitet ble registrert i løpet av de siste 4 minutter av testen. Sylindrene ble tømt og rengjort mellom hvert dyr. Dyr ble først behandlet for å konsumere en spiselig, svak (1%) sukrose løsning. Trening bestod av en innledende 48 timers eksponering for sukrose i stedet for vann, etterfulgt av fem 1-h tester der sukrose ble presentert. På dag 28 etter kronisk stress, var sukrose forbruket målt ved bestemmelse av massen av flasken som inneholder sukrose-løsning før og etter forsøksperioden. Sukrose preferanse ble beregnet som:. (Sukrose forbruk) /(total væske forbruk) [20] Serum Corticosterone Analyse Blod ble samlet inn fra halshugget rotter mellom 09:00 og 11:00 AM førtiåtte timer etter stresset behandling og separert i en nedkjølt sentrifuger ved 4 ° C (3000 rpm x 10 min). Serum ble lagret ved -80 ° C inntil de ble utført. Serumet corticosterone (CORT) ble kvantifisert ved radio-immunoassay (RAI) i henhold til produsentens protokoller (PLA General Hospital, RIA Technology Development Center, Kina). På slutten av hvert forsøk ble dyrene avlivet ved dyp bedøvelse med 10% kloralhydrat (350 mg /kg, ip). De magene ble fjernet, oppblåst ved injisering av 2 ml 1% formalin, og åpnet langs den store kurvatur. Området (mm 2) for hver hemoragisk lesjon ble målt under et dissekere mikroskop med 10 × forstørrelse, oppsummerte per mage og brukes som lesjonen poengsum. Statistiske analyser ble utføres ved hjelp av SPSS 13,0 programvare. Alle data er presentert som gjennomsnitt ± standardavvik. Den Kolmogorov-Smirnov Z metoden ble tatt i bruk for normal test, mens studentens t Resultater Association of Stress Sår med depresjon Innledende studier ble utført for å avgjøre om en sammenheng eksisterer mellom genereringen av stress-sår og tilhørende utbruddet av depresjon. De SD-rotter ble utsatt for en 28 dagers kronisk psykologisk stress-protokollen. På dag 28 ble rottene undersøkt ved tvungen svømmetest og sukrose forbruk test (SCT). Etter fullførelse av testingen, ble rottene avlivet, ble serum samlet og sårindeks ble kvantifisert. Resultatene av sukrose preferanse og immobilitet tidspunktet for tvungen svømmetest av kronisk psykologisk stress ulcus gruppe viste ingen betydelige forskjeller med kontrollgruppen ( P Rotter eksponert for CSD vises betydelig økt immobilitet tid for tvungen svømmetest i forhold til naive kontrolldyrene som forventet ( P administrasjon av selektive serotonin reuptake inhibitor (SSRI) antidepressant fluoksetin hydroklorid betydelig redusert mageslimhinnefunksjon hos rotter med CPSU eller CSD, sammenlignet med kontroll dyr ( P Rotter eksponert for CSD ble administrert med ranitidin, en felles H 2 reseptor antagonist, eller placebo. Ranitidin hemmet depresjon-lignende oppførsel i CSD rotter. Det ble ikke observert signifikante forskjeller i immobilitet tiden av tvungen svømmetest eller sukrose preferanse fra CSD rotter som ble gitt med ranitidin i forhold til naive kontrollrotter ( P Mifepristone Hindrer Depresjon hos kronisk stress modeller i rotter eksponert for enten CPSU eller CSD, administrasjon av glukokortikoid reseptor antagonist mifepriston redusert sår indeksen i forhold til CPSU behandling alene ( P Serum kortikosteronnivået ble målt etter stressbehandlinger. Rotter eksponert for akutt stress vises betydelig høyere kortikosteron nivåer enn naive kontroller ( P H 2-reseptorantagonister har uensartede Konsekvenser for Depression-lignende atferd og Serum Corticosterone Ingen signifikante forskjeller i immobilitet tiden av tvungen svømmetest ( P for å få en bedre forståelse av de morfologiske forandringer av forskjellige grupper med behandlinger, den diffuse lunger, erosjon og blødning i kjertelmagen slimhinnene i SD-rotter kunne sees i figur 7. diskusjon stressrelaterte lidelser har blitt mer viktig og alvorlig i dagens samfunn. Det er økende interesse for å tyde den rollen stress-indusert faktorer i stress sår og depresjon. I denne studien har vi funnet toveis crosstalk mellom stress sår sykdom og depresjon samt felles mekanisme for patogenesen. Det er kjent at H 2-reseptorantagonister er en klasse av legemidler som hemmer mage syresekresjon som vanligvis brukes i klinisk praksis, noe som blokkerer H 2-reseptorer på parietalceller spiller en rolle i å beskytte den gastriske mucosa. Ranitidin, cimetidin og famotidin er mye brukt H 2-reseptorantagonister. Det har blitt vist at ingen depresjon-lignende adferd er presentert i ranitidin-behandlede rotter med CSD; derfor spekulere vi at H 2-reseptorer i hjernen spiller en viktig rolle i prosessen med forekomst og utvikling av depresjon, i samsvar med tidligere rapporter [21]. Utfyllende intervensjoner med cimetidin og famotidin ble gjennomført for videre validering. Dataene viste at cimetidin som lett kan gå på tvers av blod-hjerne-barrieren hadde en signifikant undertrykkende effekt på depresjon-lignende adferd, men ikke for famotidin. Som famotidin har en dårlig lipofilisitet, dens evne til å trenge gjennom blod-hjerne-barrieren er svakere enn de andre H 2-reseptorantagonister. Det er foreslått at effektiviteten på depression- atferd av cimetidin og ranitidin er relatert til H 2-reseptoren i hjernen. Selv om mekanismen er fremdeles uklar, er det blitt rapportert at H 2-reseptor-antagonist hindrer forekomsten av depresjon. For å forstå de underliggende mekanisme for dette fenomen, undersøkte vi serum kortikosteronnivået av rotter eksponert for CSD og behandlet med ranitidin eller cimetidin som er betydelig lavere enn den til rottene eksponert for CSD og som fikk placebo. Cerebral histamin er produsert av mastocyttene som kan aktivere HPA-aksen etter stimulering [22]. Det er mulig at H 2-reseptorantagonister slik som ranitidin og cimetidin kan påvirke histamin å aktivere HPA akse gjennom å blokkere H 2 reseptor i hjernen, noe som reduserer serum kortikosteronnivået og undertrykke depresjon-lignende atferd. Chandishwar Nath fant at sentrale histamin spiller en tilrettelegger rolle i forekomsten av depresjon hos dyr. Administrasjon med histamin kan forbedre immobilitet i svømmefortvilelse i mus [21]. Noen forskere konkluderte med at sentrale histamin H 2 reseptoren letter aggressiv oppførsel [23]. Det så ut til at H 2-reseptor-antagonister kan spille en viktig rolle i å undertrykke depresjon-lignende adferd via reduksjon av HPA akse-aktivering og inhibering av histamin ved å blokkere den H 2-reseptoren i sentralnervesystemet. Dermed våre data gir nye ledetråder til mekanismen av depresjon for videre fordypning. En pilotstudie har vært gjennomført som viste at erosjon og blødning i CSD gruppen ble observert i kjertelmageslimhinnene med sår indeksen signifikant høyere enn kontrollgruppen, viste og depresjon oppførsel test en betydelig depresjon-lignende oppførsel. Våre resultater viste at rotter med depresjon-lignende oppførsel led av en alvorlig mageslimhinnefunksjon. I mellomtiden depresjon-lignende oppførsel i CPSU gruppen var ikke signifikant forskjellig fra kontrollgruppen, noe som antyder at stressmavesår ikke nødvendigvis ledsaget av forekomst av depresjon. Resultatene er i overensstemmelse med tidligere studier [24], [25], selv om andre forfattere rapporterte et annet resultat [26]. Det er kjent at depresjon er relatert til defekt funksjon av 5-hydroksytryptamin. Kronisk restraint stress er forbundet med forbedret postsynaptiske adferds følsomhet overfor 5-hydroksytryptamin-agonist 5-metoksy-N, N-dimetyltryptamin [24], [25]. Mottakelighet for kronisk stress påvirkes av flere faktorer som døgnrytme, alder, kjønn, stamme eller genomisk makeup [27] - [30]. I konklusjonen, er det antatt at viss relevans eksisterer mellom stress sår og depresjon, og at depresjon ofte går med stressmavesår mens stressmavesår ikke nødvendigvis ledsages av forekomsten av depresjon. Forrige studien indikerte at gjentatt forbehandling med antidepressiva citalopram viste en betydelig magesekk effekt i kaldt beherskelse modell [31]. Antidepressiva har vært antatt å lindre mageslimhinnen funksjon via redusere utskillelsen av magesyre og reparasjon av slim-bikarbonat barriere. Suleyman funnet at administrering av antidepressiva øket ekspresjon av antioksidant indikatorer, inkludert glutation og superoksiddismutase, samtidig redusere ekspresjonen av oksydative indikatorer, for eksempel hydrogenperoksyd, malondialdehyd og myeloperoksidase [32]. Fluoksetin er antatt å virke som en SSRI og ofte brukt til å behandle depresjon [33]. Det kunne øke kortikal gamma-aminosmørsyre (GABA) nivåer hos stressede rotter [34], og magesekkbeskyttende aktivitet av GABA synes å være mediert ved økning av gastrisk mucosal blodstrømning ble avhengig av sensorisk neuron og ingen systemer [35]. En mer plausibel mekanisme ble presentert ved Kanof, noe som tyder på at antidepressiva kunne beskytte mageslimhinnen via interaksjoner med H 2-reseptorer i hjernen [36]. Som H 2-reseptorantagonister som passerer over BBB var i stand til å påvirke depresjon, våre data også gitt ytterligere bevis for dette problemet. Omfavner alle disse mulighetene, ble en mulig mekanisme foreslått i Figur 8. stressors aktivere paraventricular kjernen, som gir opphav til utslipp av kortikotropin frigjørende hormon (CRH). CRH virker på hypofysen og stimulerer sekresjonen av ACTH som fremmer glukokortikoider frigjøring fra binyrebarken [37]. Glukokortikoider er sluttproduktet av HPA akse referert til som kortisol i human og kortikosteron i gnagere [38]. Årsakssammenheng mellom glukokortikoider og depresjon er fortsatt uklart. Forskere på om stressfaktorer vil indusere frigjøring av glukokortikoider er inkonsekvent. Noen studier tyder på at stress utløser depresjon med økende produksjon av glukokortikoider [39], [40]. I motsetning til disse papirer, anser en annen teori at stress-indusert nedgang i glukokortikoider utgangs innebærer i patogenesen av depresjon [41]. Våre resultater viste at nivået av kortikosteron ble betydelig øket i rotter eksponert for AS, tvert imot rottene eksponert for kronisk stress (CPSU eller CSD) viste tydelig lavere enn kortikosteron naive kontroller. Denne situasjonen kan anses som påvirkning av timingen i HPA-akse. Sanne H Booij påpekes at "når kronisk stress først begynner, det er en første aktivering av HPA-akse, noe som resulterer i forhøyede konsentrasjoner av ACTH og kortisol. Men funnene tyder på at ettersom tiden går, minsker denne aktiviteten, og kortisol sekresjon returer til under normal "[42]. Glukokortikoider er utgitt som svar på mange stressfaktorer som en beskyttende hormonet, effekten av noe som er normaliseringen av stressrespons, som tjener som adaptive faktorer for å understreke hendelser eller omstendigheter. Undersøkelser viste at opplevelsen av gjentatt eller kronisk stress kan føre til hypo-aktiv tilstand av HPA akse [43]. Vi spekulert at nedgangen i serum kortikosteronnivået kan representere en adaptiv reaksjon på stress. I tillegg kan høyt nivå av glukokortikoider bli indusert av stress, noe som øker følsomheten til den negative feedback i hypofysen [44], [45]. Det er generell enighet om at store mengder av glukokortikoider kan indusere eller forverre magesår. Glukokortikoider kan ikke bare forstyrre vevsreparasjon, heve nivåene av magesyre og pepsin, men også redusere utskillelsen av gastrisk slim, og til slutt nedsette gastrisk slimhinnebarriere som fører til magesår. Videre depresjon er karakterisert med redusert neurogenesis, hovedsakelig i hippocampus [46]. Høyden av glukokortikoider kan interferere med en rekke uønskede strukturelle og cellulære endringer, inkludert neuronal skade i hippocampus [47], føre til økt sekresjon av hypothalamus CRH, og resultere i nedsatt reaktivitet for å understreke [42], [48]. Åpenbart nevroendokrine system som regulerer stressresponsen er ekstremt kompleks. Våre data antyder HPA-aksen er vesentlig involvert i kronisk stress-indusert sårdannelse og utbruddet av depresjon via flere mekanismer, hvorav den formidler de strukturelle og cellulære forandringer i hippocampus, og følgelig endringer induserer hippocampus skade, som kan øke risikoen av depresjon. Videre har disse data indikerer at intervensjon på nivået av HPA akse kan tilveiebringe alle nødvendige beskyttelse av kronisk stresslidelse De ovennevnte forsøk har bekreftet at stressmavesår ikke korrelerer med depresjon. Antidepressiva kan sannsynligvis anvendes for behandling av stressmavesår og syre-undertrykkende midler kan anvendes for å behandle depresjon, noe som tyder på at disse to sykdommer kan dele en felles mekanisme for patogenesen. Mifepriston er et glukokortikoid reseptor og progesteron reseptor antagonist testes nå som potensiell antidepressiv [49]. Vi brukte mifepriston for bedre å forstå samspillet mellom stress sår og depresjon på HPA-aksen. Våre data viste at rotter som ble gitt med mifepriston i de to gruppene (SUKP og CSD) ikke lider av alvorlig mage mucosal skade. Sammenlignet med kontrollgruppen var det ingen forskjell i undertrykk-lignende oppførsel i CSD gruppe, som ble gitt mifepriston. Disse resultatene antydet at mifepriston reduserer depresjon-lignende oppførsel og forekomst av stressmavesår i kroniske stressede rotter, i samsvar med en antidepressiv virkning betydelig. Forrige studien antydet at mifepriston lindre akutt stress-indusert depresjon-lignende oppførsel ved å målrette den glukokortikoid reseptoren [50]. Siden kroniske stressfaktorer i CPSU og CSD dyremodeller kunne forstås som integrering av ulike akutte stressfaktorer, mifepriston blokkerer glukokortikoid reseptor og ugyldig sluttproduktet av HPA-aksen, og til slutt utøver en positiv effekt på å redusere depresjon-lignende oppførsel og beskyttelse av mageslimhinnen. Resultatene har vist at glukokortikoid spiller en viktig rolle i forekomsten av stressmavesår og depresjon som vi kan konkludere med at samspillet mellom disse to sykdommene eksisterer på HPA-aksen. Det er en viss sammenheng mellom stress og depresjon sår. Stressmavesår ikke nødvendigvis er ledsaget av forekomst av depresjon mens depresjon ofte går med stressmavesår. Antidepressiva og syre-undertrykke medikamenter kan sannsynligvis anvendes for behandling av henholdsvis stressmavesår og depresjon. Akutt stress Actives HPA-aksen og kronisk stress kan føre til redusert HPA-aksen aktivering. Interaksjon eksisterer mellom forekomst av depresjon og stress sår på HPA akse, i mellomtiden H 2-reseptoren i hjernen spiller en viktig rolle ved depresjon.
< 0,05) [14 ]. Derfor, i denne studien, beregnet vi å illustrere sammenslutning av stressmavesår generasjon og utbruddet av depresjon utnytte rottemodeller av kronisk stress. Resultatene kan gi nye strategier for å behandling for vanlige kroniske stressrelaterte lidelser.
Materialer og metoder
Behandlinger
Kronisk psykisk stress Sår
Akutt stress
kronisk stress depresjon
Sukrose Forbruk Test
Sår Index Kvantifisering
statistikker
-test ble brukt til å identifisere signifikante forskjeller mellom to prøver. P
. ≪ 0,05 ble anerkjent som statistisk signifikant
> 0,05) (figur 1A.). I motsetning til dette ble arrdannelse på overflaten av mageslimhinnen hos rotter etter CPSU. Videre analyser viste diffuse lunger, erosjon og blødning av magekjertler, med en sårindeks vesentlig høyere enn det som ble observert i den ubehandlede kontrollgruppen ( P
< 0,01) (Fig. 2A). I sammendraget, ble mageslimhinnen av dyr utsettes for CPSU betydelig svekket, men ingen depresjon lignende atferd ble observert.
< 0,01) (fig. 1B). Tilsvarende sukrose preferanse var betydelig lavere i disse rotter i forhold til naive kontroller ( P
< 0,01) (Fig. 1a). Imidlertid stiplet og lineal erosjon, blødning og sårdannelse ble klart observert på overflaten av den gastriske slimhinne i rotter eksponert for CSD. Det ble ikke observert mucosal skade primært innenfor kjertelmagen, og den sårindeks var signifikant høyere sammenlignet med kontrollgruppen ( P
< 0,01) (figur 2B.). I motsetning til CPSU, CSD resulterte i både depresjon-lignende oppførsel, så vel som gastrisk mucosal sårdannelse, noe som tyder på at depresjon kan være forbundet med sårdannelse på dyrene.
Antidepressiva Inhibit sårdannelse i både CPSU og CSD modeller
< 0,05) (fig. 2). Fluoxetine hydrochloride fullstendig eliminert mageblødning, med bare noen få spredte områder av blødning og erosjon ble observert i kjertelmagen. Såret indeks over fluoksetin behandlede rotter eksponert for CPSU eller CSD var betydelig lavere enn rotter som ikke får medisiner ( P
< 0,01 for hver protokoll) (Fig. 2A). Disse dataene indikerer at inntak av antidepressiva fluoksetin hydroklorid beskytter mot stress-indusert mage mucosal skade.
H 2-reseptorantagonister Impact Depresjon
> 0,05 for hver test). (Fig. 1)
. < 0,01 for hver) (figur 2). Interessant, vi ikke observere signifikante forskjeller i immobilitet tid av tvungen svømmetest av mifepriston-behandlede rotter eksponert for CSD sammenlignet med naive kontroller ( P
> 0,05) (figur 1B.). I tillegg har vi også gjorde ikke observere noen signifikant forskjell i andelen av sukrose preferanse mellom mifepriston behandlet og CSD eksponert rotter og naiv kontrollgruppe ( P
> 0,05) (Fig. 1a). Disse resultatene indikerer at mifepriston kan forhindre forekomsten av depresjon-lignende oppførsel hos rotter.
Serum kjemi Etter Stress
< 0,05) (Fig. 3). I motsetning til rotter utsatt for enten CPSU eller CSD vises betydelig lavere corticosterone enn naiv kontrollrotter ( P
< 0,05). (Fig. 3)
> 0,05) ble observert eller prosentandelen av sukker preferanse mellom cimetidin behandlede rotter med CSD og naive kontroller som vist i Figur 4 og Figur 5 ( P
> 0,05). Imidlertid immobilitet tiden for tvungen svømmetest av famotidin-behandlede rotter var betydelig høyere ( P
< 0,01), mens prosentandelen av sukrose preferanse i denne gruppen ble betydelig redusert sammenlignet med naive kontrollrotter som vist i figur 4 og figur 5 ( P
< 0,01). I sammendrag, tyder disse data på at H 2-reseptor-antagonist, cimetidin, som er i stand til å passere på tvers av BBB, har en betydelig inhiberende virkning på depresjon-lignende oppførsel; mens famotidin, som ikke kan krysse BBB, tilbyr ikke innvirkning på depresjon. Serumkjemi analyse viste at ingen signifikante forskjeller i kortikosteron-nivåer mellom famotidin-behandlede rotter og rotter med CSD som vist i figur 6 ( P
> 0,05). Men serum kortikosteron nivåer i CSD-eksponerte rotter behandlet med ranitidin eller cimetidin var betydelig lavere enn disse i kontrollgruppen alene med CSD ( P
< 0,05). (Fig. 6)
Konklusjoner
 Den spesifikke karbohydratdietten støttes av 124 år med forskning og testing
På begynnelsen av 1900-tallet jobbet forskere febrilsk med å forstå rollen til fett, proteiner og karbohydrater hos pasienter med cøliaki. Først ble det teoretisert at protein var problemet; da var f
Den spesifikke karbohydratdietten støttes av 124 år med forskning og testing
På begynnelsen av 1900-tallet jobbet forskere febrilsk med å forstå rollen til fett, proteiner og karbohydrater hos pasienter med cøliaki. Først ble det teoretisert at protein var problemet; da var f
 9 måter å gjøre det lettere å leve med Acid Reflux Disease
Selv om du kan ha blitt diagnostisert med gastroøsofageal reflukssykdom (GERD), betyr det ikke at du ikke kan nyte livet ditt til det fulle. Det er måter å kontrollere GERD på som ikke nødvendigvis få
9 måter å gjøre det lettere å leve med Acid Reflux Disease
Selv om du kan ha blitt diagnostisert med gastroøsofageal reflukssykdom (GERD), betyr det ikke at du ikke kan nyte livet ditt til det fulle. Det er måter å kontrollere GERD på som ikke nødvendigvis få
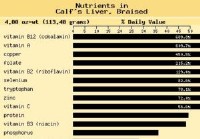 SCD-oppskrift:Lemon Pepper-leverbiff
De siste par månedene har jeg blitt mer interessert i orgelkjøtt. Jeg vil gjerne over tid kunne stole på kvaliteten på maten jeg spiser for å få tak i alle vitaminene og mineralene jeg trenger. Da håp
SCD-oppskrift:Lemon Pepper-leverbiff
De siste par månedene har jeg blitt mer interessert i orgelkjøtt. Jeg vil gjerne over tid kunne stole på kvaliteten på maten jeg spiser for å få tak i alle vitaminene og mineralene jeg trenger. Da håp