Os testes de diagnóstico continuam a ser uma ferramenta crucial na luta contra a pandemia COVID-19. Os testes padrão para a detecção de SARS-CoV-2 envolvem a amplificação do RNA viral para níveis detectáveis usando uma técnica chamada PCR de transcrição reversa quantitativa (RT-qPCR). Mas primeiro, o RNA deve ser extraído da amostra. Os fabricantes de kits de extração de RNA tiveram dificuldade em acompanhar a demanda durante a pandemia de COVID-19, dificultando a capacidade de teste em todo o mundo. Com o surgimento de novas variantes de vírus, a necessidade de melhor, testes mais rápidos são melhores do que nunca.
Uma equipe liderada por Robert B. Hufnagel, M.D., Ph.D., chefe da Unidade de Genética Médica e Genômica Oftálmica da NEI, e Bin Guan, Ph.D., um colega do Laboratório de Genômica Oftálmica do NEI, usou um agente quelante feito pela empresa de suprimentos de laboratório Bio-Rad, chamado de resina Chelex 100, para preservar o RNA SARS-CoV-2 em amostras para detecção por RT-qPCR.
"Usamos amostras de nasofaringe e saliva com várias concentrações de vírions para avaliar se elas poderiam ser usadas para detecção direta de RNA, "disse Guan, o autor principal de um relatório sobre a técnica, que foi publicado esta semana na iScience. "A resposta foi sim, com sensibilidade marcadamente alta. Também, esta preparação inativou o vírus, tornando mais seguro para o pessoal do laboratório lidar com amostras positivas. "
A equipe de Hufnagel fez sua descoberta testando uma variedade de produtos químicos usando amostras sintéticas e humanas para identificar aqueles que poderiam preservar o RNA em amostras com degradação mínima, permitindo a detecção direta do vírus por RT-qPCR.
Para validar o teste, Blake M. Warner, do NIDCR, D.D.S., Ph.D., M.P.H., e sua equipe coletou amostras de pacientes (no Protocolo de Pesquisa NIH IRB 20-D-0094) e as armazenou em qualquer meio de transporte viral, ou o recém-desenvolvido tampão de resina quelante no NIH Symptomatic Testing Facility.
As amostras em meios de transporte viral foram testadas pela equipe de testes COVID-19 no Centro Clínico do NIH, liderado por Karen M. Frank, M.D., Ph.D., usando extração de RNA convencional e teste RT-qPCR. As amostras no tampão de resina quelante foram aquecidas e o RNA viral foi, então, testado por RT-qPCR. A nova preparação aumentou significativamente o rendimento de RNA disponível para teste, em comparação com o método padrão.
Achamos que esta nova metodologia tem benefícios claros de aumentar a sensibilidade, economia de custos e tempo para testes. O método estabiliza o RNA à temperatura ambiente para facilitar o transporte, armazenar, e manuseio em ambientes clínicos. "
Robert B. Hufnagel, M.D., Ph.D., Chefe da Unidade de Genética Médica e Genômica Oftálmica da NEI
NEI protegeu a propriedade intelectual em torno desta tecnologia e está procurando parceiros para co-desenvolvimento / licenciamento. Entre em contato com [email protected] para mais informações ..
 Como diagnosticar a colite ulcerativa?
Como diagnosticar a colite ulcerativa?
 Mais carne bovina recuperada devido à salmonela:USDA
Mais carne bovina recuperada devido à salmonela:USDA
 O que desencadeia crises de diverticulite?
O que desencadeia crises de diverticulite?
 Mensageiros de proteínas do microbioma humano lançam luz sobre a saúde humana
Mensageiros de proteínas do microbioma humano lançam luz sobre a saúde humana
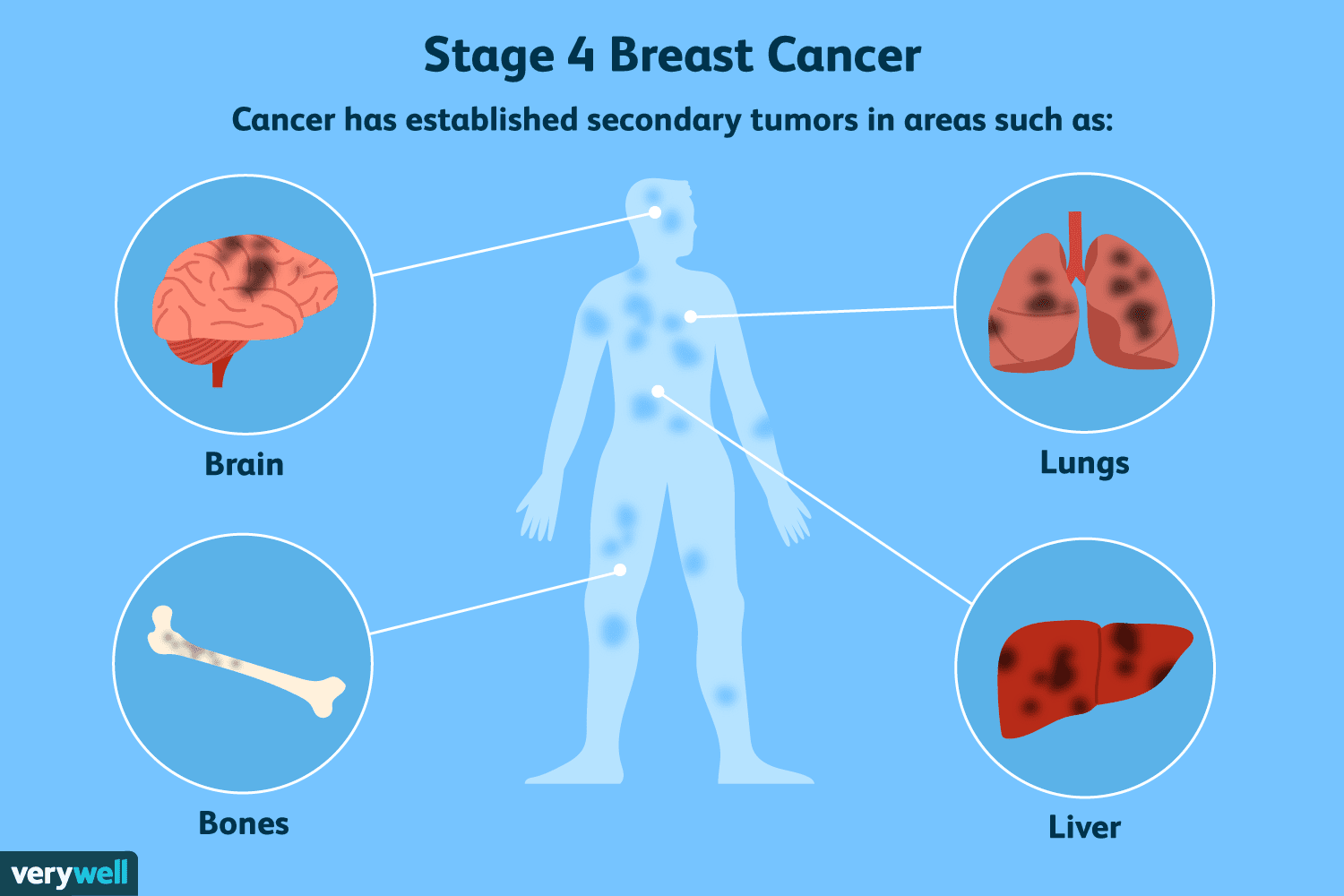 Uma visão geral do estágio 4 do câncer de mama
Uma visão geral do estágio 4 do câncer de mama
 Nutrição e sensibilidade ao trigo não celíaca
Nutrição e sensibilidade ao trigo não celíaca
 O tipo de bactéria das vias aéreas superiores pode influenciar a gravidade da asma
Um novo estudo levanta a possibilidade de modular os sintomas da asma por meio de bactérias que comumente vivem nas vias aéreas superiores. O trabalho, que foi publicado em 16 de dezembro, 2019, no jo
O tipo de bactéria das vias aéreas superiores pode influenciar a gravidade da asma
Um novo estudo levanta a possibilidade de modular os sintomas da asma por meio de bactérias que comumente vivem nas vias aéreas superiores. O trabalho, que foi publicado em 16 de dezembro, 2019, no jo
 Você está interessado em ajudar as pessoas e ser pago?
Sem lucro, perdemos US$ 14.876 e eu chorei. Eu odiava meu trabalho diário e a SCD Lifestyle ainda estava perdendo dinheiro. Eu estava doente e cansado de trabalhar 80-100 horas por semana. E Jorda
Você está interessado em ajudar as pessoas e ser pago?
Sem lucro, perdemos US$ 14.876 e eu chorei. Eu odiava meu trabalho diário e a SCD Lifestyle ainda estava perdendo dinheiro. Eu estava doente e cansado de trabalhar 80-100 horas por semana. E Jorda
 Infecção por Clostridioides difficile
O trato digestivo humano abriga cerca de 500 a 1.000 espécies diferentes de microrganismos, a maioria dos quais são inofensivos, ou mesmo útil, e viver em harmonia. No entanto, se algo perturbar o equ
Infecção por Clostridioides difficile
O trato digestivo humano abriga cerca de 500 a 1.000 espécies diferentes de microrganismos, a maioria dos quais são inofensivos, ou mesmo útil, e viver em harmonia. No entanto, se algo perturbar o equ