gástrica Uma assinatura de três gene como um potencial biomarcador preditivo de sensibilidade irinotecan no câncer gástrico
Resumo Objetivo
quimioterapia personalizada baseada em biomarcadores moleculares podem maximizar anticancerígeno eficiência. O nosso objectivo é investigar biomarcadores preditivos capazes de predizer a resposta ao tratamento à base de irinotecano no câncer gástrico.
Métodos
Nós examinados expressão gênica de APTX, BRCA1, ERCC1, ISG15, Topo1 e metilação de SULF2 em incluídas em parafina fixado em formalina incorporado tecidos de câncer gástrico de 175 pacientes e avaliaram a associação entre os níveis de expressão de genes ou estado de metilação e sensibilidade in vitro
de irinotecano. Utilizou-se análise de regressão linear múltipla para desenvolver um modelo gene-expressão para predizer sensibilidade irinotecan em câncer gástrico e validado este modelo in vivo
.
Resultados níveis de APTX, BRCA1 expressão Gene vitro
ee ERCC1 foram significativamente mais baixos em amostras de cancro gástrico irinotecano-sensíveis do que as amostras de irinotecano-resistente (P
< 0,001 para todos os genes), enquanto ISG15 (P = 0,047
) e Topo1 (P = 0,002
) foram significativamente maiores. Com base nesses genes, uma assinatura de três genes foram estabelecidas, que foi calculado da seguinte forma: Índice = 0,488 - 0,020 nível de APTX + 0,015 nível de Topo1 × expressão × expressão - nível de BRCA1 0,011 × expressão. A assinatura de três gene foi significativamente associada com sensibilidade irinotecan (rho = 0,71, P Art < 0,001). A sensibilidade e especificidade para a predição de sensibilidade irinotecano com base na assinatura de três genes atingiu 73% e 86%, respectivamente. Em outro conjunto de testes independente, as taxas de inibição de irinotecano em amostras gástricas com sensível à assinatura eram muito mais elevados do que aqueles com resistente à assinatura (65% vs 22%, P Art < 0,001). Irinotecano terapia com 20 mg /kg por semana para ratinhos imunodeficientes portadores de xenoenxertos com sensível à assinatura preso dramaticamente o crescimento de tumores (P
< 0,001), mas não tiveram efeito em ratos portadores de xenoenxertos com resistente a assinatura
. conclusões
A assinatura de três gene aqui estabelecido é um potencial biomarcador preditivo de sensibilidade irinotecan no câncer gástrico.
Palavras-chave
quimioterapia personalizado irinotecano gástrica câncer HDRA imunodeficientes ratos Introdução
O câncer gástrico continua sendo uma das principais causas de morte por câncer em todo o mundo [1, 2]. Não existe um "padrão ouro" quimioterapia para o cancro gástrico avançado até agora. Nos últimos anos, de novos agentes de quimioterapia geração, tais como o docetaxel, oxaliplatina, irinotecano, capecitabina e S-1 foi estudada em estudos de fase III [3]. No entanto, a sobrevivência média permaneceu inferior a um ano [2], e a taxa de resposta foi de apenas cerca de 30% -50% [4]. O irinotecano (CPT-11) é um derivado semi-sintético da camptotecina (CPT) que interfere com a replicação do ADN e a divisão celular através da sua interacção com o potente enzima topoisomerase I (Topo1). Ambos irinotecano e CPT pertencem aos inibidores Topo1. O irinotecano é usado principalmente em cancro colo-rectal e também frequentemente utilizados no tratamento do cancro gástrico, que mostra as taxas de resposta variam de 14% a 23% de agente único e aproximadamente 50% em combinação [5].
Um número de biomarcadores moleculares capazes de prever a probabilidade de resposta a agentes quimioterapêuticos têm sido investigados ao longo das últimas décadas [6]. Nossos estudos anteriores identificaram gene de suscetibilidade ao câncer de mama 1 (BRCA1) como potencial biomarcador preditivo de cisplatina e sensibilidade docetaxel [7, 8], a timidilato sintase (TS) de 5-FU e raltitrexed [9, 10], e reparação de excisão transversal complementando 1 (ERCC1) de platina [11]. No entanto, tem havido progressos limitados na identificação de biomarcadores capazes de predizer a resposta ao tratamento à base de irinotecano no câncer gástrico. Topo1 regula supercoiling DNA durante a replicação através da maneira de causar quebras de cadeia simples e religação [12]. Irinotecano e seu metabolito activo SN-38 induz danos no ADN através da estabilização de um complexo covalente transiente entre o DNA e Topo1, o que resulta na quebra de cadeia de ADN, prisão de replicação, e a apoptose [13]. Os níveis elevados de proteína de tumor Topo1 foram recentemente descritos para identificar um subgrupo de doentes com cancro colorrectal metastático, com boa resposta ao irinotecano [14]. Reparação de danos no DNA irinotecan-associado e Topo1 mediada requer a remoção do Topo1 parado ea resolução da quebra de DNA associado. Durante este processo, uma variedade de proteínas de reparação, incluindo aprataxin (APTX), BRCA1 e ERCC1, estão envolvidos, alguns dos quais podem ter um potencial clínico como biomarcadores preditivos [15].
Além dos biomarcadores candidatos mencionado acima, estudos recentes sugerido que a metilação de 6-o-endosulfatase promotor de sulfato de heparano (SULF2) foi associada com a sensibilidade a inibidores Topo1 em Non-Small Cell Lung Cancer-(NSCLC) [16]. regulador de INF-indutível da ubiquitinação (ISG15) pode bloquear a via da ubiquitina /26S proteossómica levando a acumulação de danos no ADN induzida por CPT que resultou num aumento da apoptose [17]. metilação SULF2 (SULF2M) e alta ISG15 expressar linhas de células NSCLC mostrou sensibilidade 134 vezes a CPT que SULF2 unmethylation (SULF2U) e ISG15 linhas celulares que expressam baixos [16].
Com base nas evidências acima, a hipótese de que APTX, BRCA1 , ERCC1, ISG15, SULF2 e Topo1 ou sua combinação pode desempenhar um papel importante na previsão de sensibilidade irinotecan no câncer gástrico. No presente estudo, nós investigamos cada gene como biomarcador preditivo por si só, e, em seguida, estabelecido algoritmo combinando os genes juntos para predizer com mais precisão a sensibilidade irinotecano. Nós também validou o modelo em outro conjunto independente de amostras de câncer gástrico e duas coortes de modelos de ratinhos imunodeficientes. O objetivo deste estudo foi identificar uma assinatura de classificação clinicamente útil que poderia prever a sensibilidade irinotecan no câncer gástrico.
Materiais e métodos
As amostras dos pacientes
Todas as amostras e dados clínicos relevantes foram obtidos do Departamento de Oncologia e cirurgia geral, Drum Tower Hospital Filiado à Faculdade de Medicina da Universidade de Nanjing, no período de agosto de 2010 a junho de 2012. as amostras incluem 175 tumores recém-removidos gástricos, que foram classificados aleatoriamente ou como conjunto de treinamento (n = 100) ou conjunto de testes (n = 75) usando números aleatórios gerados por computador. Cada tecido tumoral foi dividido em duas partes, uma vez que removido na cirurgia: (1) uma parte foi mantido em solução salina equilibrada de 4 ° C de Hanks com 1% de penicilina /estreptomicina e detectada a quimiossensibilidade in vitro
pelo ensaio de resposta à droga histocultura (HDRA); (2) a parte restante foi deixado em formalina e fez em blocos (FFPE) de tumores embebidos em parafina e fixados em formalina para a observação patológica e a detecção do gene. Diagnóstico de pacientes com tumor gástrico foi confirmado por exame histopatológico. Os dados clínicos e histopatológicos, incluindo idade, sexo, histologia, local do tumor, estágio, grau histológico e metástases em linfonodos foram todos recolhidos. As características clínicas dos pacientes foram resumidos na tabela 1. O consentimento informado foi obtido de todos os pacientes e os protocolos para este estudo foram aprovados pelo Comitê de Investigação de protecção Humana da Drum Tower Hospital Filiado à Faculdade de Medicina da Universidade de Nanjing. Todos os experimentos com animais foram realizados de acordo com a Comissão de Coordenação chinesa sobre os Regulamentos de investigação do cancro para o bem-estar dos animais e à protecção animal Law.Table 1 Características dos pacientes
Característica
conjunto de treinamento (N = 100)
conjunto de teste
Independent (N = 75) Loja Online em total (N = 175)
Idade, y mediana (intervalo)
63 (29-83)
63 (29-83)
63 (29-83)
≥ 63
51 (51%)
40 (53%)
91 (52%) Art < 63
49 (49%)
35 (47%)
84 (48%) Sexo seguro
Masculino
74 (74%)
57 (76%)
131 (75%)
Feminino
26 (26%)
18 (24%)
44 (25%)
Tumor site
estômago distal
34 ( 34%)
28 (37%)
62 (35%)
estômago proximal
41 (41%)
29 (39%)
70 (40%)
estômago inteiro de 25 (25%)
18 (24%)
43 (25%)
Stage
I
13 (13%)
7 (9% )
20 (11%)
II
20 (20%)
21 (28%)
41 (23%)
III
65 (65%)
45 (60%)
110 (63%)
IV
2 (2%) Página 2 (3%) página 4 (3%)
grau histológico
2
20 (20%)
16 (21%)
36 (21%) Sims 3
47 (47%)
34 (46%)
81 (46%)
Mixed 1-2 Sims 3 (3%) Sims 3 (4%)
6 (3%)
Mixed 2-3
30 (30%)
22 (29%)
52 (30%)
metástase linfática
Sem
21 (21%)
19 (25%)
40 (23%)
Sim 79 (79%)
56 (75%)
135 (77%)
HDRA
HDRA procedimentos foram realizados como descrito anteriormente [18]. Resumidamente, os tecidos de tumor frescas foram lavadas e picadas em pequenos pedaços de aproximadamente 0,5 mm de diâmetro, que foram, então, colocados em colagénio preparada (Health Design, Rochester, NY, EUA) As superfícies em microplacas de 24 poços. Houve 8 poços de cultura paralela para teste de sensibilidade irinotecano e 8 poços de cultura paralelos para controle. Após incubação durante 7 dias a 37 ° C (em atmosfera húmida contendo 95% de ar, 5% de CO
2) na presença de fármacos dissolvidos com meio RPMI 1640 contendo 20% de soro fetal de vitelo, 100 ul de tipo I colagenase ( 0,1 mg /mL, Sigma) e de MTT (5 mg /ml, Sigma) foram adicionados a cada poço de cultura e incubou-se durante mais 16 horas. Concentração de irinotecano foi de 20 ug /ml de acordo com o seu pico de concentração plasmática (PPC) em pacientes [19]. Após extracção com sulfóxido de dimetilo (DMSO, Sigma), a absorvância da solução em cada poço foi lida a 540 nm. Absorvância por grama de tecido de tumor em cultura foi calculada a partir da absorvância média de tecido a partir de 8 poços de cultura paralelas, e o peso do tumor de tecido foi determinada antes da cultura. A taxa de inibição foi calculada utilizando a seguinte fórmula: Inibição
taxa
%
=
1 | -
T
/Tablet C
×
100
%
T é a absorvância média dos tratados tumor /Peso
C é a absorvância média dos tumores de controlo /Peso
detecção do nível de expressão de ARNm
extração de RNA total a partir de tecido FFPE
Seis secções de 7 ^ m foram preparadas a partir de blocos tumorais FFPE que continham células de tumor, pelo menos, 80%. Após a coloração com hematoxilina-eosina, as partes cancerosas foram microdissecadas e transferido para um tubo de microcentrífuga. O ARN foi isolado de acordo com um processo patenteado (Patente Europeia número EP1945764-B1). Resumidamente, a parafina foi removida por xileno, e MICRODISSECADO partes cancerosas foram lisadas num de proteinase K contendo tampão a 60 ° C durante 16 h. O ARN foi purificado por extrações com fenol e clorofórmio seguido de precipitação com isopropanol na presença de acetato de sódio à temperatura de -20 ° C. O sedimento de ARN foi lavado em 70% de etanol e ressuspenso em 53 ul de água livre de RNase, seguida por tratamento com ADNase I (Life Technologies).
QPCR avaliação da expressão do gene
M-MLV Kit de Transcriptase Reversa (Invitrogen) foi aplicado para gerar ADNc para quantitativa de reacção em cadeia da polimerase (qPCR) para detectar a β-actina (ACTB), APTX, BRCA1, ERCC1, ISG15 e Topo1. Cada lote de reacção incluído um controlo positivo de comercial de pulmão humano e ARN do fígado (Stratagene, La Jolla, CA, EUA) como calibradores e controlos negativos sem ARN e transcriptase inversa. O RNA total foi 1 ug utilizada para cada reacção de RT. Molde de ADNc foi amplificado com os iniciadores e sondas específicos para ACTB, APTX, BRCA1, ERCC1, ISG15 e Topo1 usando Taqman Universal Master Mix (Applied Biosystems, Foster City, CA). O ensaio identificações (Applied Biosystems, Foster City, CA) para os iniciadores e sondas foram como se segue: Hs99999903_m1 (ACTB), Hs00214452_m1 (APTX), Hs00157415_m1 (ERCC1), Hs00192713_m1 (ISG15), Hs00243257_m1 (Topo1), BRCA1 (NM_007294) : para a frente 5 'GGCTATCCTCTCAGAGTGACATTTTA 3', inverta 5 'GCTTTATCAGGTTATGTTGCATGGT 3', e 6FAM sonda -5 'CCACTCAGCAGAGGG 3' MGB. QPCR foi realizada para quantificar a expressão de genes utilizando o Prism 7900HT Sequence Detection System ABI (Applied Biosystems). As condições de PCR foram 50 ° C durante 2 min, 95 ° C durante 15 min, seguido de 40 ciclos a 95 ° C durante 15 s e 60 ° C durante 1 min. quantificações de expressão gênica relativa foram calculados de acordo com o método Ct comparativo utilizando ACTB como um controle endógeno, com base na nossa experiência anterior comparando diferentes genes housekeeping [7, 20], e RNAs de pulmão e fígado humanos comerciais (Stratagene, La Jolla, CA, EUA ) como calibradores, o que permite-nos comparar os níveis de expressão de genes entre diferentes pacientes. Os resultados finais foram determinados pela expressão de mRNA fórmula level = 2 - (amostra em DCT dCt calibrador) (dCt = Ct gene- Ct ACTB) [7, 21] e foram analisados com a análise Stratagene software.
detecção da metilação de DNA
extracção de ADN e de modificação
Três secções de 7 mícrons foram preparados a partir de blocos de tumor primárias que continham células de tumor, pelo menos, 80%. Após a coloração com hematoxilina-eosina, as partes cancerosas foram microdissecadas e transferido para um tubo de microcentrífuga. O ADN foi isolado rotineiramente e, em seguida, foi quimicamente modificado por bissulfito de sódio para converter todas as citosinas não metiladas em uracilos, enquanto deixando inalterada methylcytosines [16]. Em seguida, eles foram armazenadas a -20 ° C para posterior análise.
Reacção em cadeia da polimerase-metilação específico (MSP)
MSP foi realizada para determinar a metilação de SULF2 utilizando o Prism 7300HT Sequence Detection System ABI (Applied Biosystems). Cada reacção de PCR continha ADN genómico de 2 uL, SYBR Verde mistura de PCR (Takara, Japão) 10 ul, 7,7 ul de água, e primers 0,15 uL (10 umol /L). As condições de PCR foram 95 ° C durante 10 min, seguido de 45 ciclos a 59 ° C durante 30 s, 72 ° C durante 30 s e 95 ° C durante 30 s. Os iniciadores para PCR SULF2 metilado (Takara, Japão) foram como se segue: directo 5 'TAAGTGTTTTTTTTATAGCGGC 3', reverso 5'TACCGTAATTTCCGCTATC 3 '. Os iniciadores para PCR não metilado SULF2 (Takara, Japão) foram como se segue: transmitir a 5 'GTTTATAAGTGTTTTTTTATAGTGGT3', reverso 5'TACCATAATTTCCACTATCCCT 3 '. Cada lote de reacção incluíram um controlo positivo de metiltransferase (M.SssI) tenha sido tratada com DNA genómico humano (totalmente metilado), um controlo negativo a partir de amostras de DNA que foi confirmado não metilado e outro controle negativo sem ADN. Todos os testes foram realizados em duplicata.
A criação e validação do modelo gene-expressão para a previsão sensibilidade irinotecan
Adotamos análise de regressão linear múltipla para estabelecer o modelo gene-expressão otimizado com base no conjunto de formação de 100 cancros gástricos [22]. De acordo com os resultados de regressão passo a passo (entrada: α = 0,10, remova: α = 0,15), o modelo consistiu em APTX, Topo1 e BRCA1 é a única otimizada. Nós atribuído a cada paciente um índice de acordo com a combinação linear do nível do ARNm ponderado pelo coeficiente de regressão a partir das amostras de formação expressão. O índice do modelo gene-expressão foi calculado da seguinte forma: Índice = 0,488 - 0,020 nível de APTX + 0,015 nível de Topo1 × expressão × expressão - nível de BRCA1 0,011 × expressão. Este modelo foi posteriormente validado em outro conjunto de testes independente de 75 pacientes com câncer gástrico. No conjunto de testes, os pacientes foram classificados de acordo com seu índice de gene assinatura e divididos em grupos sensíveis à assinatura e resistentes a assinatura usando o índice mediano como ponto de corte. A sensibilidade irinotecano destes dois grupos foram testadas pelo HDRA e comparados uns com os outros. Em
viv
O validação do modelo do gene-expressão de sensibilidade irinotecano predição
Para estabelecer modelos de ratinhos imunodeficientes com gástrica derivados de paciente xenoenxertos de cancro, cada tecido tumoral cirúrgica recém-removido foi cortado em pedaços de 3 x 3 x 3 milímetros 3, que foram transplantadas dentro de 30 min a 12 ratinhos atímicos imunodeficientes, designado por "grupo" [23]. Em cada grupo, quando o tumor cresceu até um tamanho de 50-100 mm 3, ratinhos com xenoenxertos foram distribuídos aleatoriamente para tratamento com irinotecano 20 mg /kg /w, IP (n = 6) ou sem tratamento como controlo ( n = 6). Os volumes tumorais individuais (V) foram calculadas pela fórmula "V = (comprimento x largura x largura) /2" e comparados com os valores no início do tratamento para se obter o volume relativo do tumor. Os ratinhos foram observados todos os dias durante o crescimento do tumor.
A fim de avaliar a inibição consistente de irinotecan nos ratinhos sensíveis à assinatura, três semanas após a primeira administração, todos os tumores foram separados a partir de ratinhos de primeira geração e passados para a segunda geração ratos. Na segunda geração, nenhuma droga foi administrada. Os ratos foram observados todos os dias por mais duas semanas.
Análise estatística of the Mann-Whitney U-teste eo teste de Kruskal-Wallis foram utilizados para testar a associação entre os níveis de expressão de mRNA e características clínicas, ea associação entre irinotecan sensibilidade e os parâmetros clínico dos pacientes. método de classificação de Spearman foi utilizado para avaliar a correlação dos níveis de expressão de mRNA entre diferentes genes, bem como a correlação entre os níveis de mRNA e in vitro
sensibilidade irinotecan. O U-teste de Mann-Whitney foi utilizado para comparar a sensibilidade irinotecan entre os grupos SULF2M e SULF2U, pacientes irinotecano sensíveis e resistentes ao irinotecano e entre sensível à assinatura e grupos resistente à assinatura. operating characteristic (ROC) Receptor foram gerados para calcular a sensibilidade e especificidade da predição baseada em genes diferentes e o modelo de expressão genética em termos de sensibilidade irinotecano. O teste t de Student pareado foi utilizado para avaliar as diferenças entre os tamanhos dos tumores dos ratos sensíveis à assinatura ou camundongos resistentes à assinatura e controles. A P Art < 0,05 foi considerado estatisticamente significativo (frente e verso). A análise estatística foi realizada através do SPSS, versão 16.0.
Resultados
características do paciente
Características de todos os pacientes são apresentados na Tabela 1. Nos 175 pacientes, a maioria dos pacientes eram do sexo masculino (75%), e a histologia de cada amostra foi de adenocarcinoma. Em 62 (35%) pacientes, o tumor estava localizado no estômago distal, em 70 (40%) no estômago proximal, e em 43 (25%) no estômago inteiro. Cento e dez (63%) pacientes apresentavam doença estágio III da doença. metástase ganglionar estava presente em 135 (77%) pacientes. níveis de expressão do gene
Os níveis de expressão de mRNA de APTX, BRCA1, ERCC1, ISG15 e Topo1 foram detectados em todos os tumores, com nível de expressão genética média em relação ao serviço de limpeza ACTB de 4,32 para APTX (faixa de 0,26-17,99, 95% de intervalo de confiança (IC): 3,78-5,19), 7,91 para BRCA1 (faixa de 0,37-29,04, 95% CI: 7,07-9,51), 14,03 por ERCC1 (intervalo ,33-46,30 , IC 95%: 13,01-17,07), 5,07 para ISG15 (faixa de 0,04-34,24, 95% CI: 3,94-6,21) e 7,51 para Topo1 (faixa de 1,07-37,81, 95% CI: 6,38-9,17) (Figura 1) . Observou-se uma associação significativa entre os níveis de mRNA APTX de expressão e grau histológico (P
= 0,03), e mRNA ISG15 e sexo (P
= 0,017). Nenhuma outra associação entre características clínicas e níveis de mRNA tumor foi encontrado (Tabela 2). No entanto, foi observada uma forte correlação entre os níveis de expressão de mRNA de APTX e BRCA1 (rho = 0,53, P Art < 0,001), APTX e ERCC1 (rho = 0,73, P Art < 0,001), BRCA1 e ERCC1 (rho = 0,48, P
< 0,001) no tumor. Figura níveis de expressão de um gene de APTX, BRCA1, ERCC1, ISG15 e Topo1 em 175 pacientes analisados por RT-PCR quantitativo. Os valores de expressão do gene foram calculados de acordo com o método Ct comparativo utilizando ACTB como um controle endógeno. A linha azul representava média com 95% CI.
Tabela 2 A associação das expressões de genes e características patológicas
Característica
No. de Pacientes
mRNA APTX
BRCA1 mRNA
ERCC1 mRNA
ISG15 mRNA
Topo1 mRNA
média ± SD
média ± SD
média ± SD
média ± SD
média ± SD
Idade , y
≥ 63
91 (52%)
4,81 ± 3,78
8,61 ± 5,73
15,28 ± 10,01
4,48 ± 3,69
8,03 ± 7,30 Art < 63
84 (48%)
4,09 ± 3,76
7,90 ± 5,95
14,75 ± 9,28
5,79 ± 6,90
7,47 ± 5,81 Sexo seguro
Masculino
131 (75%)
4,77 ± 3,33
8,41 ± 5,57
15,74 ± 10,19
5,54 ± 5,62
7,95 ± 7,17
Feminino
44 (25%)
3,58 ± 3,29
7,92 ± 6,67
12,77 ± 7,30
3,53 ± 4,27 *
7,21 ± 4,62
Tumor site
estômago distal
62 (35%)
4,79 ± 2,87
8,97 ± 6,52
16,12 ± 10,36
7,05 ± 7,75
8,09 ± 5,93
estômago proximal
70 (40%)
4,16 ± 3,10
8,33 ± 5,72
13,97 ± 9,09
3,61 ± 2,64
7,40 ± 6,63
estômago inteiro de 43 (25%)
4,60 ± 4,44
7,12 ± 4,74
15,31 ± 9,70
4,61 ± 3,43
7,06 ± 7,94
Stage
I
20 (11%)
4,25 ± 4,47
5,91 ± 3,40
13,40 ± 7,07
1,89 ± 0,83
5,89 ± 4,03
II
41 (23%)
4,19 ± 3,01
8,58 ± 5,09
14,70 ± 9,56
6,76 ± 7,96
8,91 ± 6,35
III
110 (63%)
4,66 ± 3,38
8,19 ± 5,75
15,56 ± 10,16
4,67 ± 4,01
7,70 ± 7,07
IV página 4 (3%)
4,20 ± 4,61
15,88 ± 17,90
11,01 ± 5,00
7,25 ± 6,33
4,03 ± 1,63
grau histológico Página 2
36 (21% )
5,05 ± 3,54 *
10,97 ± 7,33
15,78 ± 9,52
4,86 ± 4,75
8,08 ± 6,61 Sims 3
81 (46%)
3,92 ± 3,55
7,81 ± 5,16
14,30 ± 9,64
3,68 ± 2,75
7,18 ± 6,08
Mixed 1-2
6 (3%)
3,63 ± 4,51
7,17 ± 2.13
15,17 ± 12,40
8,00 ± 8,94
8,42 ± 6,02
Mixed 2-3
52 (30%)
4,55 ± 2,53
7,06 ± 5,27
15.65 ± 9,96
7,16 ± 7,74
8,44 ± 7,18
metástases linfonodais
Sem
40 (23%)
4,58 ± 3,39
8,70 ± 5,08
14,68 ± 7,31
5,97 ± 8,17
7,48 ± 4,47
Sim
135 (77%)
4,46 ± 3,35
8,16 ± 6,05
15,16 ± 10,33
4,78 ± 4,12
7,87 ± 7,23
* P Art < . 0,05
A relação entre a expressão do gene e quimio-sensibilidade para irinotecan
No conjunto de treinamento, a sensibilidade irinotecan foi testado com sucesso em todos os tumores, com taxa de inibição média de 43,3% (intervalo de 2% -89%, CI: 39 % -47%). Não houve associação significativa entre a sensibilidade irinotecano e as características clínicas (Tabela 3), incluindo a idade (P =
0,51), sexo (P =
0,77), local do tumor (P =
0,64), fase ( P =
0,41), grau histológico (P =
0,48) e metástases linfonodais (P =
0,47). No entanto, os níveis de mRNA de APTX (rho = -0,48, P Art < 0,001), BRCA1 (rho = -0,49, P Art < 0,001), ERCC1 (rho = -0,42, P Art < 0,001), ISG15 (rho = 0,34, P = 0,001
), e Topo1 (rho = 0,43, P
< 0,001) mostraram uma correlação com a sensibilidade irinotecano. Os doentes foram classificados de acordo com as suas taxas de inibição de irinotecano e divididos em grupos de irinotecano sensíveis e resistentes-irinotecano, utilizando a taxa de inibição mediana como o ponto de corte [19]. Os níveis de expressão do gene de APTX (P Art < 0,001), BRCA1 (P Art < 0,001) e ERCC1 (P Art < 0,001) foram significativamente menores nos pacientes irinotecan-sensíveis do que em pacientes resistentes ao irinotecan , enquanto ISG15 (P = 0,047
) e Topo1 (P = 0,002
) foram significativamente maiores (Figura 2A-e). As curvas ROC foram gerados para calcular a sensibilidade e especificidade da cada gene na predição sensibilidade irinotecano (Figura 2G-J). As áreas sob a curva ROC (AUC), sensibilidade e especificidade para a predição de sensibilidade irinotecan baseado em APTX, BRCA1, níveis ERCC1, ISG15 e mRNA Topo1 foram listadas na Tabela 4.Table Association 3 entre a sensibilidade irinotecano e as características clínicas
característica
taxa de inibição irinotecano
taxa de inibição irinotecano
média (IC 95%)
média (IC 95%)
conjunto de treinamento (N = 100)
conjunto testes independentes (N = 75)
Idade, y mediana (intervalo)
≥ 63
42% ( 36-47%)
44% (31-57%) Art < 63
45% (39-51%)
44% (34-54%) Sexo seguro
Masculino
43% (38-47%)
42% (33- 51%)
Feminino
45% (36-55%)
50% (31-68%)
Tumor site
estômago distal
42% (35-49%)
44% (28-60%)
estômago proximal
44% (38-51%)
47% (35-58%)
estômago inteiro de 43% (35 -51%)
37% (16-59%)
Stage
I
34% (21-47%)
36% (3-70%)
II
49% (40-57%)
50% (31-68%)
III
43% (38-48%)
44% (34-54%)
IV
33%
34%
grau histológico Página 2
41% (33-49%)
44% (21-68%) Sims 3
42 % (36-48%)
39% (27-51%)
Mixed 1-2
54%
58%
Mixed 2-3
46% (38- 54%)
49% (35-62%)
metástases linfonodais
Sem
42% (33-51%)
46% (27-65%)
Sim
44% (39-48%)
44% (34-53%)
índice Signature Art > 0,43
57% (52-63%) **
65% (61-70%) **
≤ 0,43
31% (27-36%)
22% (17 -28%)
** P Art < . 0,001
Figura 2 níveis de APTX (P < 0,001) expressão dos genes, BRCA1 (P < 0,001) e ERCC1 (P < 0,001) foram significativamente menores em pacientes irinotecano-sensíveis do que em pacientes resistentes a irinotecano, enquanto ISG15 (P = 0,047) e Topo1 (P = 0,002) foram significativamente mais elevados. Os diagramas de caixa mostraram os níveis de APTX (A), BRCA1 (B), ERCC1 (C) de expressão de ARNm, ISG15 (D) e Topo1 (E) em grupos de irinotecano sensíveis e resistentes-irinotecano, respectivamente (n = 100). As linhas dentro das caixas denotado as medianas. Os bigodes de diagramas de caixa: Min Max. Gráficos de curva ROC mostrou as AUC de APTX (F), BRCA1 (G), ERCC1 (H), ISG15 (I) e Topo1 (J) para a previsão de sensibilidade irinotecan. Sensibilidade (eixo Y) foi representada graficamente contra a fração de falso-positivos. (1 - especificidade)
Tabela 4 A sensibilidade e especificidade dos níveis de expressão de cinco genes para a predição de sensibilidade irinotecan
Genes
chemotheraputic agentes
Sensibilidade
Especificidade
AUC (95% CI)
P
APTX
irinotecano
73%
74%
0,758 (,669-,847) Art < 0,001
BRCA1
irinotecano
91%
58%
0.760 (,673-,846)
< 0,001
ERCC1
irinotecano
64%
79%
0,726 (,632-,821) Art < 0,001
ISG15
irinotecano
59%
73%
0,617 (0,494-0,740)
0,047
Topo1
irinotecano
48%
94%
0,664 (0,563-0,765)
0,002
A relação entre metilação SULF2 e sensibilidade para
irinotecan no conjunto de treinamento, o estado de metilação de SULF2 foi detectado com sucesso em todos os pacientes, com trinta e três (28%) transportando SULF2M e oitenta e quatro (72%) transportando SULF2U. Não houve associação significativa entre o estado SULF2 metilação e características clínicas. As taxas de inibição de irinotecano eram de 49,8% (intervalo de 2% -89%, 95% CI: 41% -59%) para o grupo SULF2M, e 40,2% para o grupo SULF2U (gama de 2% -84%, 95% CI: 34% - 46%, P = 0,08
).
o estabelecimento do modelo de expressão genética e a sua associação com a sensibilidade
irinotecano com base no nível de cinco genes e o estado de metilação SULF2 expressão, construiu-se uma assinatura por análise de regressão linear múltipla, como indicado nos métodos. O índice da assinatura de três genes variou 0,08-0,99 com valor médio de 0,43 ± 0,16. Houve uma correlação significativa entre o índice e sensibilidade irinotecan (rho = 0,71, P Art < 0,001) (Figura 3A). curva ROC foi gerado para calcular a sensibilidade e especificidade da assinatura de três genes na predição sensibilidade irinotecano (Figura 3B). A AUC foi (IC 95%: 0,755-0,901, P Art < 0,001) 0,828. Com o valor de limiar de 0,43, a sensibilidade e especificidade para a predição de sensibilidade irinotecano com base na assinatura de três genes atingiu 73% e 86%, respectivamente. Todos os autores leram e aprovaram o manuscrito final.
 Dicas sobre como adotar uma abordagem saudável para o Ano Novo
Dicas sobre como adotar uma abordagem saudável para o Ano Novo
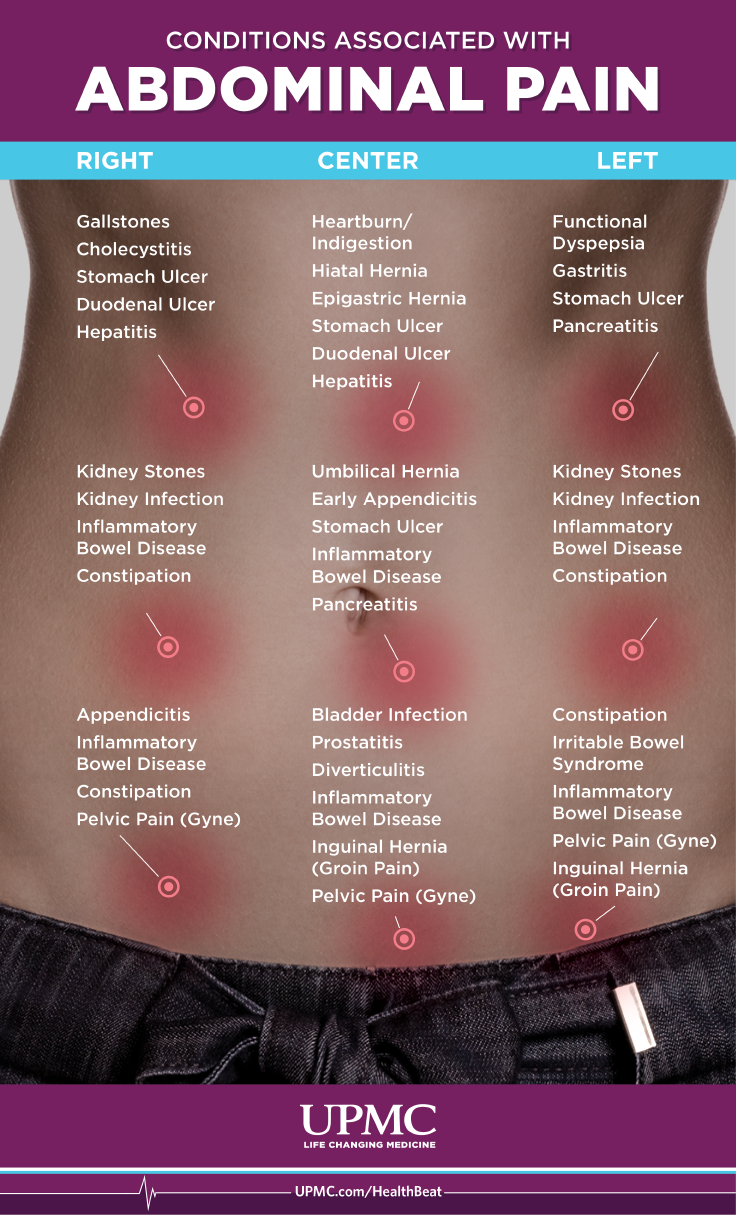 Dor de estômago:quando se preocupar com dor de estômago
Dor de estômago:quando se preocupar com dor de estômago
 Como embalar suplementos para uma viagem
Como embalar suplementos para uma viagem
 Receita de trufas de chocolate com morango
Receita de trufas de chocolate com morango
 Como cuidar da SII com noções básicas de nutrição
Como cuidar da SII com noções básicas de nutrição
 Por que você é um herói da saúde e o que fazer com essa energia
Por que você é um herói da saúde e o que fazer com essa energia
 Maneiras de ajudar seu filho a desenvolver bons hábitos alimentares
Resumo:Nossos médicos de saúde digestiva de Hinsdale, IL conversam com os pais sobre como ensinar as crianças a fazer escolhas alimentares saudáveis que os beneficiem a longo prazo. Uma apreciação
Maneiras de ajudar seu filho a desenvolver bons hábitos alimentares
Resumo:Nossos médicos de saúde digestiva de Hinsdale, IL conversam com os pais sobre como ensinar as crianças a fazer escolhas alimentares saudáveis que os beneficiem a longo prazo. Uma apreciação
 As mulheres correm maior risco de cálculos biliares e precisam de atenção médica
Você sofre de dor no ombro direito ou entre as omoplatas, acompanhada de vômitos e dor intensa e crescente no lado superior direito ou no centro do abdome? Todos estes podem ser sintomas de problemas
As mulheres correm maior risco de cálculos biliares e precisam de atenção médica
Você sofre de dor no ombro direito ou entre as omoplatas, acompanhada de vômitos e dor intensa e crescente no lado superior direito ou no centro do abdome? Todos estes podem ser sintomas de problemas
 A resistência aos antibióticos dobra em apenas duas décadas
A resistência aos antibióticos representa um grande desafio para muitas doenças infecciosas previamente curáveis. Atualmente, a resistência aos antibióticos está provando aumentar em um ritmo muito ma
A resistência aos antibióticos dobra em apenas duas décadas
A resistência aos antibióticos representa um grande desafio para muitas doenças infecciosas previamente curáveis. Atualmente, a resistência aos antibióticos está provando aumentar em um ritmo muito ma