Противоязвенной активностью флувоксамина у крыс и его влияние на окислителем и антиоксидантных параметров в ткани желудка
Аннотация
Справочная информация
Хотя многие препараты доступны для лечения язвы желудка, часто эти препараты неэффективны. Многие антидепрессанты, как было показано, чтобы иметь противоязвенной активностью в различных моделях экспериментальной язвы. Одним из таких лекарств, антидепрессант миртазапин, как сообщается, имеют противоязвенной эффект, который включает увеличение антиоксиданта и уменьшение окислителя, параметров. На сегодняшний день, однако, нет никакой информации относительно противоязвенной активности для аналогичного антидепрессант, флувоксамин. Целью данного исследования являлось изучение противоязвенного эффектов флувоксамина и определить свои отношения с антиоксидантами.
Методы
группах крыс кормили в течение 24 ч получали флувоксамин (25, 50, 100 и 200 мг /кг), ранитидин (50 мг /кг) или дистиллированную воду перорально через зонд. Индометацин (25 мг /кг) перорально вводили крысам в качестве неспецифического язвенного агента. Через шесть часов после индукции язв, желудки крыс были вырезаны и индекс язвы определяется. Отдельные группы крыс обрабатывали теми же дозами флувоксамин и ранитидина, но не с индометацином, чтобы проверить действие этих препаратов только на биохимические показатели. Желудки оценивали биохимически определить окислитель и антиоксидантные параметры. Мы использовали одностороннюю ANOVA и наименее вариантов существенной разницы (LSD) для анализа данных.
Результаты
25, 50, 100 и 200 мг /кг дозы флувоксамина, оказываемое противоязвенные эффекты 48.5, 67.5, 82.1 и 96.1 %, соответственно, по сравнению с контрольной группой крыс. Ранитидин показал эффект противоязвенной 86,5%. Никаких различий не наблюдалось при отсутствии индометацин лечения любой дозы флувоксамина или для ранитидина. Уровни антиоксидантных параметров, общего глутатиона и оксида азота, были увеличены во всех группах флувоксамин и в группе ранитидина по сравнению с индометацином только группой. Кроме того, флувоксамин и ранитидин снизились уровни параметров окислителя, миелопероксидазы и malondialdeyhyde, в тканях желудка крыс по сравнению с индометацином группой.
Заключение
Мы пришли к выводу, что флувоксамин имеет противоязвенные эффекты, и что они имеют место с помощью механизма, который включает в себя активацию антиоксидантных параметров и ингибирования некоторых токсичных параметров окислителя.
Справочная информация
стероидных и нестероидных препаратов, сигареты, потребления алкоголя, травма, сепсис, шок, хеликобактер пилори
, и стресс было показано, что способствует образованию язвы желудка [1-4]. Стресс является одним из наиболее агрессивных факторов и лежит в основе многих других заболеваний, помимо язв, например, депрессии. Стресс является одним из наиболее часто используемых методов для получения моделей язвы [5, 6]. Депрессия, сопровождается психотическими и соматическими симптомами, присутствует у большинства больных с желудочно кишечной системы (ГИС) язв [7]. Представляет интерес для данного исследования являются отчеты, которые показывают, что некоторые антидепрессанты могут также иметь анти-язвенные эффекты [8].
Самые ранние сообщили об использовании антидепрессантов для желудочно кишечного (GI) заболевание было использование трициклических антидепрессантов (ТЦА) для лечение язвенной болезни [8]. Противоязвенные эффекты некоторых других антидепрессантов, таких как флуоксетин, бупропион, dothiepin, мапротилин, миансерином, тримипрамин, idazoksan, моноаминооксидазы -B (МАО-В) ингибиторы, имипрамин, amiltriptiline, миртазапин, среди других, так как сообщалось [9-16 ]. Повышенная уязвимость к депрессии [17] и тревоги [18] у экспериментальных животных идет параллельно с развитием язв и то же самое справедливо и для человека [19, 20]. Кроме того, классические антидепрессанты [21, 22] и анксиолитиков [23, 24] может значительно уменьшить образование стрессовых язв, возможно, в большей степени, чем с традиционными видами терапии, такими как циметидин и антацидов [25].
Флувоксамин, селективный ингибитор обратного захвата серотонина (SSRI) препарат, ингибирует фермент CYP 1A2 [26], который, как известно, для получения активных форм кислорода [27]. Тем не менее, этиологические факторы неоднозначны примерно 60% -80% от язвенных заболеваний, а также physiopathologic условия в процессе болезни подобны [1]. Например, повышенные уровни активных форм кислорода (ROS), указаны в механизме как стресс и индометацин-индуцированное повреждение желудка [28]. Важные роли кислородных производных ROS и липопероксидов (ПОЛ) при острых желудочных поражений, индуцированные нестероидными противовоспалительными препаратами (НПВП), такие как индометацин, были поддержаны экспериментальными данными [29, 30]. <бр> в то время как некоторые SSRI препараты были зарегистрированы для повышения верхней ГИС кровотечение при сочетании с НПВС [31-33], флувоксамин могут быть полезны для желудочно-кишечного тракта, как следствие его тормозящее действие на фермент CYP 1A2 и результирующее снижение окислительного наносить ущерб. Важность увеличения антиоксидантными параметров и снижения параметров окислителя в противоязвенная эффект механизма миртазапина, антидепрессантами, также сообщалось [16]. На сегодняшний день, однако, нет никакой информации относительно противоязвенной активности флувоксамина. Целью настоящего исследования было поэтому исследовать эффекты флувоксамина в качестве индометацин-индуцированной модели язвы на крысах, и оценить его влияние на окислительных и антиокислительных параметров в ткани желудка крысы.
Методы
Животные
животные были получены из научно-исследовательского центра медицинского экспериментальной, Ататюрк университета. В общей сложности из 78 самцов белых крыс линии Вистар, весом от 190 до 210 г, были использованы для этого исследования. Животных кормили в нормальных условиях (22 ° C) в отдельных группах. Эксперименты на животных были проведены в соответствии с национальными рекомендациями по использованию и уходу за лабораторными животными и были одобрены местным комитетом по уходу за животными Ататюрка университета.
Химические
Все химикаты для лабораторных экспериментов были приобретены у компании Sigma Chemical (Германия) , Индометацин, флувоксамин, ранитидин и тиопентал натрия были получены из Дэва Холдинг-Турция, Solvay-Турция, FAKO-Турция и IE Uluagay-Турции соответственно.
Индометацин-индуцированный тест язвы
противоязвенного деятельности флувоксамине были исследованы в одном из индометацин-индуцированной модели язвенной болезни у крыс [34]. Флувоксамин в дозах 25, 50, 100 или 200 мг /кг [35, 36] и ранитидин в 50 мг /кг дозе, вводили 24-часовому голоданию групп крыс перорально через зонд. Равный объем дистиллированной воды, вводили в контрольной группе в качестве транспортного средства. Через пять минут после введения препарата, все группы получали 25 мг /кг индометацина перорально. Через шесть часов после того, как индометацин администрирования, все группы крыс были убиты с высокой дозой тиопентала натрия (50 мг /кг, внутрибрюшинно). вырезают Желудки всех крыс. Язва участки на поверхности желудки были исследованы макроскопически и измерены на квадратный миллиметр бумаги. Результаты, полученные из флувоксамин групп оценивали путем сравнения их с результатами контрольной и ранитидина групп. Затем, все желудках (флувоксамин групп, группа отрицательного контроля, группа положительного контроля, и интактные группы) содержались в температуре -80 ° С для биохимического исследовании глутатион (GSH), оксида азота (NO), миелопероксидазы (МРО) и малонового диальдегида . (MDA) уровни
группы, используемые для этого гнойника эксперимента можно суммировать следующим образом:
Группа 1: Флувоксамин 25 мг /кг + индометацин 25 мг /кг
Группа 2: Флувоксамин 50 мг /кг + индометацин 25 мг /кг
Группа 3: Флувоксамин 100 мг /кг + индометацин 25 мг /кг
Группа 4: Флувоксамин 200 мг /кг + индометацин 25 мг /кг
Группа 5: Ранитидин 50 мг /кг + индометацин 25 мг /кг
Группа 6: дистиллированная вода + индометацин 25 мг /кг
Группа 7:. интактной группы, которые получали только дистиллированную воду
В дополнение к этому язвенного эксперимента, мы оценили ли введение fluxoxamine ( 25, 50 100 и 200 мг /кг дозы) и ранитидин (50 мг /кг) до 24 часовому голоданию крыс, в отсутствие лечения индометацином, будет также изменить биохимических параметров. Для этой цели в общей сложности 36 крыс кормили в течение 24 ч при свободном доступе к воде. Затем крысы были разделены на 6 (N = 6) групп и обрабатывают флувоксамина при дозах 25, 50, 100 или 200 мг /кг и ранитидина при 50 мг /кг в. Последняя группа получала только дистиллированную воду в качестве транспортного средства с помощью перорального зонда. Через шесть часов после введения препарата, у всех крыс во всех группах были убиты с высокой дозой тиопентала натрия (50 мг /кг, внутрибрюшинно). В желудках всех крыс были вырезаны и оценивали как макроскопически и биохимически, как описано выше
Группы для этого контрольного эксперимента можно суммировать следующим образом:.
Группа 1: Флувоксамин 25 мг /кг
Group 2: Флувоксамин 50 мг /кг
Группа 3: Флувоксамин 100 мг /кг
Группа 4: Флувоксамин 200 мг /кг
Группа 5: Ранитидин 50 мг /кг
Группа 6: интактной группы, которые получили только дистиллированную воду.
биохимический анализ
биохимического исследования тканей желудка
После макроскопических анализов, глутатион (GSH), каталаза (CAT), супероксиддисмутазы (СОД), миелопероксидазы (МРО) и малонового ( были определены MDA) активность ферментов и уровни в тканях желудка у крыс. Для этой цели в желудках крыс замораживали при -80 ° С до того, пока биохимических исследований. Для приготовления гомогенатах ткани, ткани желудка измельчали с жидким азотом в ступке. Наземные ткани (0,5 г каждого) затем обрабатывают 4,5 мл соответствующего буфера. Смеси гомогенизировали на льду с использованием гомогенизатора Ultra-Turrax в течение 15 мин. Гомогенаты фильтровали и центрифугировали при помощи охлаждаемой центрифуге при 4 ° С. Супернатанты использовали для определения ферментативной активности. Все анализы проводили при комнатной температуре в трех повторностях.
Определения Всего GSH
Сумма в GSH в слизистой оболочке желудка измеряли в соответствии с методом Sedlak и Линдсей [37]. Поверхность слизистой оболочки желудка, собирали путем соскабливания, взвешивают, а затем гомогенизируют в 2 мл 50 мМ буфера Трис-HCl буфере, содержащем 20 мМ ЭДТА и 0,2 мМ сахарозы, рН 7,5. Гомогенат немедленно осаждали 0,1 мл 25% -ной трихлоруксусной кислоты, и осадок удаляли центрифугированием при 4200 оборотах в минуту в течение 40 мин при температуре 4 ° С. Супернатант использовали для определения GSH с использованием 5,5'-дитиобис (2-нитробензойной кислоты. Оптическую плотность измеряли при 412 нм с использованием спектрофотометра. Выражались Результаты уровня GSH в слизистой оболочке желудка в нмоль на миллиграмм ткани (нмоль /мг ткани). не
NO уровни
Тканевая NO уровни были измерены, как уровни общего нитрита + нитрата с использованием реагента Грисса, как описано ранее [38]. реагент фенилантраниловая состоит из сульфаниламиды и N- (1-нафтил ) -.. этилендиамин метод основан на-двухступенчатого процесса Первым шагом является превращение нитратов в нитриты с использованием нитратредуктазы Вторым шагом является добавление реагента Грисса, который преобразует нитрит в глубокий фиолетовый азо. соединение; фотометрическое измерение absobance при 540 нм обусловлена тем, что этот азо хромофора точно определяет концентрацию нитрита NO уровни не были выражены в мкмоль /г
МРО активность
МРО активность измеряли в соответствии с модифицированным методом.. Брэдли и др. [39]. Гомогенизированные образцы замораживают и оттаивают три раза, и центрифугировали при 1500 г в течение 10 мин при температуре 4 ° С. Активность МРО в надосадочной жидкости определ ли путем добавлени 100 мл супернатанта в 1,9 мл 10 мМ буфера /л фосфата (рН 6,0) и 1 мл 1,5 ммоль /л-дианизидина гидрохлорида, содержащего 0,0005% (вес /объем) перекись водорода , Изменения оптической плотности при длине волны 450 нм каждого образца регистрировали на приборе UV-VIS спектрофотометр. Была выражена активность МРО в желудочных тканях minimoles в минуту на миллиграмм ткани (ммоль /мин /мг ткани).
Определение перекисного окисления липидов или образование MDA
концентрации желудочного перекисного окисления липидов слизистых оболочек определяли путем оценки MDA с использованием тест тиобарбитуровой кислоты [40]. Если коротко, то желудки крысы быстро вырезают и промывали холодным солевым раствором. Чтобы свести к минимуму вероятность возникновения помех гемоглобина со свободными радикалами, любая кровь присоединившись к слизистой оболочке осторожно удаляли. Корпус слизистую оболочку соскабливают, взвешивают и гомогенизируют в 10 мл 100 г /л KCl. Гомогенат (0,5 мл) добавляли к раствору, содержащему 0,2 мл 80 г /л лаурилсульфата натрия, 1,5 мл 200 г /л уксусной кислоты, 1,5 мл 8 г /л 2-тиобарбитурат и 0,3 мл дистиллированной воды. Смесь инкубировали при 98 ° С в течение 1 ч. При охлаждении 5 мл н-бутанол: добавили: (L 15) пиридина. Смесь перемешивали в течение 1 мин и центрифугировали в течение 30 мин при скорости 4000 оборотов в минуту. Оптическую плотность надосадочной жидкости измеряли при 532 млн. Стандартная кривая была сгенерирована с использованием 1,1,3,3-тетраметоксипропана. Восстановление было более 90%. Результаты выражали в нмоль МДА на грамм влажной ткани (нмоль /мг ткани).
Статистический анализ
Данные представлены в виде средних значений ± стандартной ошибки (SE). Ферментативная активность и язву оценка результатов были подвергнуты однофакторного дисперсионного анализа, с наличием отрицательного и положительного контроля, с использованием программы SPSS 11.0 программного обеспечения. Различия между группами были достигнуты с использованием не менее значительную разницу вариант (LSD), и значение было заявлено на P &
ЛТ; 0.05.
Результаты
индометацин-индуцированный тест-язвой
макроскопических поражений с очевидными рубежах в различных формах и размерах были рассеяны неравномерно по всей поверхности желудка в желудке ткани у контрольных крыс, получавших индометацин. Гиперемию была более очевидной в контрольной группе, получившей индометацин по сравнению с группами, которые получали флувоксамин и ранитидин. Тяжесть гиперемию была параллельно с увеличением язвы. Как видно из таблицы 1, снижение встречаемости язвы 48%, 67,5%, 82,1% и 96,1% произошло в желудках группах крыс, получавших 25, 50, 100, и 200 мг /кг флувоксамин. Противоязвенного эффект 50 мг /кг ранитидина было 86,5%. Никаких различий не наблюдалось при отсутствии лечения индометацин следующей любой дозы флувоксамина или ranitidine.Table 1 Эффекты flovoksamine (FLU) и ранитидин (RAN) на индометацин (IND) индуцированных язв у крыс.
Препараты
доза
(мг /кг)
Количество животных
области (язвы мм2) <бр>
противоязвенные эффект (%)
P
FLU
25
&ЛТ; 0.05
+
6
15,3 ± 1,5
48,5
IND
25
Flu
50
&лт; 0.02
+
6
9,7 ± 0,9
67,5
IND
25
FLU
100
&л; 0.01
+
6
5,3 ± 0,4
82,1
IND
25
FLU
200
&л; 0,001
+ 6
1,2 ± 0,02
96,1
IND
25
RAN
50
&лт; 0,001
+
6
4,0 ± 0,6
86,5
IND
25
индометацин (Control)
25
6
29,7 ± 2,6 <бр> -
-
Результаты биохимических анализов
Все дозы флувоксамина и ранитидина значительно сократилось количество глутатиона в тканях желудка, когда по сравнению со здоровыми интактных крыс при введении в одиночку Тем не менее, 25 мг /кг дозы флувоксамин не влияет на уровни других параметров, которые мы измерили (MDA, NO и MPO) по сравнению со здоровыми интактных крыс (таблица 2). При дозах 50, 100 и 200 мг /кг флувоксамина значительно снизились уровни МДА и MPO и повышение уровня NO в ткани желудка по сравнению с интактной группой здоровых крыс. Подобные изменения наблюдались в тканях от ранитидина обработанных крыс. Индометацин применение значительно снижает уровень антиоксидантных параметров, GSH и NO, а также значительно увеличили уровни параметров окислителя, MPO и MDA. Все дозы флувоксамина и ранитидин, которые совместно с индометацином администрируемые вспять негативные последствия индометацина на ткани желудка (рисунки 1, 2, 3, 4). Рисунок 1 Эффекты флувоксамина (Flu) + индометацин (IND), ранитидин (RAN) + индометацин (IND) и только индометацин (IND) на уровнях tGSH в тканях желудка крыс. * Значимыми при р
&ЛТ; 0,05 по сравнению с контрольной группой. Рисунок 2
эффекты флувоксамина (FLU) + индометацин (IND), ранитидин (СРД) + индометацин (IND) и одна индометацин (СИН) на NO уровней в тканях желудка крыс. * Значимыми при р
&ЛТ; 0,05 по сравнению с контрольной группой. Рисунок 3
эффекты флувоксамина (FLU) + индометацин (IND), ранитидин (СРД) + индометацин (IND) и одна индометацин (СИН) на уровни МРО в тканях желудка крыс. * Значимыми при р
&ЛТ; 0,05 по сравнению с контрольной группой. Рисунок 4
эффекты флувоксамина (FLU) + индометацин (IND), ранитидин (СРД) + индометацин (IND) и одна индометацин (СИН) на уровни МДА в тканях желудка крыс. * Значимыми при р
&ЛТ; 0,05 по сравнению с контрольной группой.
Таблица 2 эффекты флувоксамина (Flu) в покое и ранитидин (RAN) только на tGSH, NO, MPO и уровни МДА в тканях желудка крыс.
Drugs
Dose
(mg/kg)
tGSH
MDA
NO
MPO
FLU
25
14.9 ± 0,6
2,1 ± 0,3
80,4 ± 6,3 1,0 ±
0,02
FLU
50
15,1 ± 0,3 * 1,8 ±
0,2 *
95,2 ± 4,5 *
0,8 ± 0,04 *
FLU
100
17,1 ± 0,8 * 1,7 ±
0,3 *
99,7 ± 5,7 * 0,5 ±
0,03 *
FLU
200
18,3 ± 0,6 * 1,6 ±
0,2 *
105,1 ± 5,2 * 0,4 ±
0,01 *
RAN
50
15.8 ± 0,4 * 2,1 ±
0,5 *
96,8 ± 4,7 * 0,6 ±
0,03 *
неповрежденными (Control)
-
12,7 ± 0,2
2,3 ± 0,4
83,4 ± 3,6
1,1 ± 0,05
* Значителен на р
&ЛТ; 0,05 по сравнению с интактным контролем.
Обсуждение
В этом исследовании, противоязвенное эффект флувоксамина был исследован у крыс с использованием индометацин-индуцированной модели язвы. Кроме того, оценивали влияние флувоксамина на окислителем и антиоксидантных параметров в ткани желудка крысы. Флувоксамин было установлено, значительно ингибирует индометацином индуцированных язв при всех испытанных дозах. Противоязвенного мощность флувоксамина была определена в зависимости от дозы; 200 мг /кг доза флувоксамина ингибируется индометацином индуцированных язв значительно более, чем делали ранитидин.
Индометацином было показано, дает более высокую желудочную повреждений у крыс по сравнению с другими НПВС [41]. По этой причине он стал предпочтительным препаратом для индукции модели язвы. Во многих экспериментальных исследованиях, антидепрессанты, как было показано, чтобы произвести противоязвенные эффекты за счет снижения секреции гистамина из тучных клеток, подавляя секрецию желудочного сока, и блокировал лейкотриенов (LTC <суб> 4, D <суб> 4, E <суб> 4) рецепторов [42, 43]. Помимо этих факторов, важным основным фактором индометацин-индуцированного повреждения желудка является ROS опосредованной перекисное окисление липидов [44] флувоксамина, препарат SSRI, ингибирует фермент CYP 1A2 [26], который, как известно, производят ROS [27]. По этой причине мы исследовали флувоксамине эффекты на GSH, НЕТ, деятельность МРО и МДА в индометацин-индуцированной язвенный желудка ткани крыс, в качестве первого подхода при исследовании механизма позади противоязвенного эффектов флувоксамина.
Роли токсичные радикалы кислорода были определены в этиопатогенезе indomethacin- индуцированного повреждения желудка [44]. Антиоксидантные параметры, как было показано уменьшить в ткани желудка, поврежденной индометацина [45]. Наши экспериментальные результаты согласуются с данными предыдущих данных. Флувоксамин в значительной степени предотвращал негативное влияние индометацина на желудочную уровнях GSH на всех использованных дозах. Желудочный уровень GSH был самым высоким в наиболее эффективной дозой флувоксамина. Кроме того, уровень GSH был ниже на 25 мг /кг, которая имела самый низкий противоязвенной эффект. Все дозы флувоксамина и ранитидин также увеличилось содержание GSH значительно при введении в отсутствие индометацин лечения. Наши экспериментальные результаты и ранее опубликованные литературные данные показывают, что существует важная взаимосвязь между уровнями GSH желудка и тяжесть язвы. В ткани, GSH и ГШ-связанные ферменты принимаются в качестве важных защитных средств в связи с их антиоксидантными свойствами [46]. Лечение
НПВС приводит к уменьшению этих антиоксидантов и инициирует процессы перекисного окисления липидов в ткани желудка, что приводит к повреждению желудка [47]. Все дозы флувоксамина использовали в нашем эксперименте (25, 50, 100 и 200 мг /кг) восстановил уровни GSH в желудочной ткани, которые уменьшились на индометацин; это повлияло на антиоксидантную систему защиты положительно и снижение повреждения желудка. GSH обезвреживает перекись водорода и /или органические кислоты, химического состава; Пероксид водорода накапливается в отсутствие GSH [48]. В присутствии переходных металлов, таких как Fe и Cu, перекись водорода вступает в реакцию с супероксид что приводит к образованию гидроксильного радикала, наиболее реакционноспособные и цитотоксическую форму РОС [49].
В ткани желудка, поврежденной индометацин, никаких уровней нет было показано, что уменьшается [50]. ОТСУТСТВИЕ известно модулировать уровень кислотности, секрецию слизи в желудке и кровоток в тканях желудка [51]. ОТСУТСТВИЕ также сообщалось, чтобы предотвратить перекисное окисление мембранных липидов [52]. Никаких уровней не было показано, что уменьшить в поврежденной ткани желудка [53]. Хаттаб и др сообщили, что L-аргинин почти полностью защищает от индометацин-индуцированной язвой желудка. Механизм этого не зависит от какой-либо модуляции секреции кислоты, муцина содержание или активность пепсина, но, как представляется, происходит через содержание слизистых оболочек NO. Это исследование также показало, что ингибитор NO-синтазы, L-NAME, образование обостряется язва [54]. В настоящем исследовании, все дозы флувоксамина, которые оказали значительное влияние противоязвенной, также увеличивается в желудке уровни NO значительно по сравнению с контрольным образцом. Было также отмечено, параллель между снижением NO уровней и степени тяжести повреждения желудка. Таким образом, можно сделать вывод о том, что противоязвенные эффекты флувоксамина могут быть смягчены с помощью L-NAME приложения, аналогично эффекту потенциируется применения L-аргинина. В нашем эксперименте ранитидин также было показано, чтобы увеличить уровни NO значительно по сравнению с контролем. Наши результаты согласуются с данными ранее сообщалось в литературе [30].
Индометацином было показано производить повреждения за счет увеличения слизистых оболочек уровни MPO и MDA в желудочном ткани [55]. MPO существует в полиплоидных клеток ядерных лейкоцитов (НЛП) и катализирует образование токсичных хлорноватистой кислоты (HOCl) из перекиси водорода [56]. Кроме того, полиморфные ядерные лейкоциты (PNLs) чрезмерно производят супероксид-анион (O2-) и гидроксильный радикал (ОН-), которые являются свободные радикалы кислорода [57]. Чрезмерное производство МРО и других активных радикалов вызывают окислительное повреждение; окислительное повреждение представлено измерения уровней перекисного окисления липидов [58]. Перекисное окисление липидов является важной причиной повреждения клеточных мембран; MDA является конечным продуктом перекисного окисления липидов и используется для определения уровня перекисного окисления липидов [59]. Желудочный MPO и MDA увеличивается в результате применения индометацина были снижены на флувоксамина. Флувоксамин сниженные уровни параметров окислителя и увеличение тех антиоксидантных параметров не только у крыс, индометацин, но и у здоровых, неповрежденных крыс.
CYP1A2 ферменты также известны для производства ROS [27]. Флувоксамин ингибирует эти ферменты [26]. Таким образом, упомянутые выше, антиоксидантные эффекты флувоксамина могут быть также связаны с ингибированием ферментов CYP1A2.
Желудочные побочные эффекты SSRI препаратов описаны в [31]. Совместное использование SSRI препаратов и индометацин Сообщалось, чтобы вызвать желудочно-кишечные кровотечения [60]. Тем не менее, несколько новых рецепторов арилпиперазина серотонина 1А (5HT1-A) агонисты, разработанные в качестве транквилизаторов, как было показано, имеют антисекреторных и гастрозащитных эффекты у крыс [61]. Кроме того, антагонисты 5HT1-увеличение потенции серотонина, связанных с сокращениями в ткани желудка [62], в то время как 5HT1-Агонист buspiron уменьшается желудка и кишечника вздутие [63]. В свете этой литературы, то можно предположить, что противоязвенное действие флувоксамина может быть связано с раздражением рецепторов 5HT1-A, но дальнейшие детальные исследования, чтобы прояснить этот момент.
Заключение
В заключение, мы сообщаем, что флувоксамин имеет противоязвенные эффекты. Индометацин вызывает повреждение желудка, не только ингибирования CYTO-защитный синтез ПГ, но и путем воздействия оксидантов и антиоксидантные механизмы, такие как GSH, NO, MPO и MDA. Флувоксамин по-видимому, оказывает свое противоязвенное действие путем активации антиоксидантных механизмов и ингибирования токсичных механизмов окислителя в тканях желудка.
Declarations
Выражение признательности
Мы хотели бы выразить нашу благодарность доцент д-р Zekai Halici за его вклад в эту работу.
авторов оригинальные представленные файлы для изображений изображения Ниже приведены ссылки на авторов оригинальных представленных файлов для изображений. 'Исходный файл для фигурного 1 12876_2008_328_MOESM2_ESM.pdf Авторского 12876_2008_328_MOESM1_ESM.pdf авторов исходного файла для фигурного 2 12876_2008_328_MOESM3_ESM.pdf Авторского исходного файла для фигурного 3 12876_2008_328_MOESM4_ESM.pdf Авторский исходный файл для исходного файла Рисунок 4 12876_2008_328_MOESM5_ESM.jpeg Авторского на рисунке 5 "исходный файл для фигурного 6 12876_2008_328_MOESM7_ESM.jpeg Авторского 12876_2008_328_MOESM6_ESM.jpeg авторов исходного файла для рисунок 7 12876_2008_328_MOESM8_ESM.jpeg Авторского исходного файла для рисунок 8 12876_2008_328_MOESM9_ESM.jpeg Авторского исходного файла для исходного файла рисунок 9 12876_2008_328_MOESM10_ESM.jpeg Авторского на рисунке 10 Конкурирующие интересы
ни один из авторов не имеет коммерческий интерес, финансовый интерес, и /или другие отношения с производителями лекарственных средств, лабораторных расходных материалов и /или медицинских устройств или с коммерческими поставщиками услуг, связанных с медицинской точки зрения.
 Ангиопластика может быть рискованной для людей с плохим кровообращением в ногах
Ангиопластика может быть рискованной для людей с плохим кровообращением в ногах
 10 наших лучших статей о микробиоте кишечника за 2020 год
10 наших лучших статей о микробиоте кишечника за 2020 год
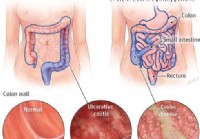 Воспалительное заболевание кишечника (ВЗК)
Воспалительное заболевание кишечника (ВЗК)
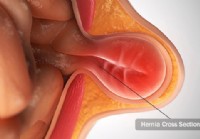 Грыжи:причины, типы и лечение
Грыжи:причины, типы и лечение
 Эндометриоз связан с повышенным риском развития болезни Крона, колита
Эндометриоз связан с повышенным риском развития болезни Крона, колита
 Является ли лапароскопическая холецистэктомия серьезной операцией?
Является ли лапароскопическая холецистэктомия серьезной операцией?
 Различные подтипы класса СРК
Обнаружили ли вы, что ваш СРК сильно отличается от СРК вашего друга? Или что истории, о которых вы читаете в Интернете, не всегда похожи на вашу жизнь? Это связано с тем, что СРК может проявляться по-
Различные подтипы класса СРК
Обнаружили ли вы, что ваш СРК сильно отличается от СРК вашего друга? Или что истории, о которых вы читаете в Интернете, не всегда похожи на вашу жизнь? Это связано с тем, что СРК может проявляться по-
 Признаком чего может быть запор?
Что такое запор? Запор возникает, когда стул редкий или затрудненный. Признаки того, что это может быть что-то более серьезное, включают обезвоживание, синдром раздраженного кишечника (СРК), которы
Признаком чего может быть запор?
Что такое запор? Запор возникает, когда стул редкий или затрудненный. Признаки того, что это может быть что-то более серьезное, включают обезвоживание, синдром раздраженного кишечника (СРК), которы
 Совет для здоровья:держите синдром раздраженного кишечника под контролем
Последние новости пищеварения Если пересадка почки не удалась, лучше повторить попытку Не позволяйте изжоге испортить вам праздник. Спрос на трансплантацию печени резко вырос Компьютерная томография
Совет для здоровья:держите синдром раздраженного кишечника под контролем
Последние новости пищеварения Если пересадка почки не удалась, лучше повторить попытку Не позволяйте изжоге испортить вам праздник. Спрос на трансплантацию печени резко вырос Компьютерная томография