Clinicopathologic Eigenschaften und die Behandlungsergebnisse von hepatoiden Adenokarzinom des Magens, eine seltene, aber einzigartige Unterart von Magenkrebs
Zusammenfassung
Hintergrund
Magen hepatoiden Adenokarzinom (HAC) ist eine spezielle Art von Magenkrebs, die morphologisch ahmt hepatozellulären Karzinoms. In dieser Studie führten wir eine Bewertung der klinisch-pathologische Merkmale, Behandlungsergebnisse und Prognose bei Patienten mit Magen-HAC.
Methoden kaufen Wir nacheinander aufgenommenen Patienten mit pathologisch bewährten Magen HAC an der Seoul National University Hospital zwischen Januar 1996 und Dezember 2008 und führten eine retrospektive Analyse. Unter 15.253 Patienten mit Magenkrebs, 26 Patienten (0,17%) wurden als Magen-HAC diagnostiziert.
Ergebnisse
Unter 26 Patienten, 22 waren männlich und das Durchschnittsalter war 63. Etappe bei der Diagnose war bei 3 Patienten IB Bühne, Stufe II bei 6 Patienten im Stadium III, bei 7 Patienten, und im Stadium IV bei 10 Patienten. Acht Patienten von 18 Patienten mit Stadium IB, II, III und IV nach kurativer Operation einen Rückfall. Rezidivfreie Überleben bei diesen Patienten war 16,67 Monate. Die häufigste metastatic Seite war intraabdominalen Lymphknoten (n = 9), gefolgt von der Leber (n = 8). Dreizehn Patienten erhielten eine palliative Chemotherapie. Das am häufigsten verwendete Therapie war eine Kombination von fluorpyrimidin und Platin. Partielles Ansprechen wurde bei einem Patienten und eine stabile Erkrankung bei 5 Patienten beobachtet. Das mediane Gesamtüberleben und progressionsfreie Überleben dieser Patienten waren 8,03 (95% CI: 6,59-9,47) und 3,47 Monate (95% CI: 0,65-6,29). Bzw.
Schlussfolgerungen
Gastric HAC ist eine sehr seltene, aber einzigartige Art von Magenkrebs. Früherkennung von dieser Art von Krebs ist von entscheidender Bedeutung für die Prognose eines Patienten. Weitere Studien der Biologie dieses Tumors zu offenbaren sind gerechtfertigt.
Schlüsselwörter Magen hepatoiden Adenokarzinom Behandlungsergebnis Prognose clinicopathologic Hintergrund
hepatoiden Adenokarzinom (HAC) zeigte eine histologische Aussehen typisch für ein hepatozelluläres Karzinom, darunter auch feste, trabekulären und pseudograndular Strukturen; Tumorzellen wurden rund oder polygonal in der Form [1]. HACs wurden in mehreren verschiedenen Organen beschrieben, einschließlich der Lunge, der Bauchspeicheldrüse, der Speiseröhre, Ampulla Vater, Dickdarm, Harnblase, Nierenbecken, Ovarien, Uterus und Zervix [2-12]. Der Magen ist das Organ, in dem HAC am häufigsten festgestellt wurde. Inzidenz von HAC ist bekannt, 0,38-0,73% zu sein, wie in einer früheren Studie berichtet [1, 13]
Alpha-Fetoprotein (AFP) ist ein fetales Serum-Protein von fötaler Leber produziert und Dottersackzellen und von einigen fötalen Magen-Darm-Zellen [14]. Bei Erwachsenen wird Serum AFP bei Patienten mit hepatozellulärem Karzinom, Dottersacktumoren erhöht und noncancerous Lebererkrankung. AFP-produzierenden Tumoren wurden in mehreren verschiedenen Organen berichtet [5-7]. Der Magen ist eine der häufigsten Lokalisationen von diesen Tumoren beeinflusst und der erste Fall beschrieben wurde [15]. Später Ishikura et al. vorgeschlagen gekennzeichnet, daß der Begriff "hepatoiden Adenokarzinom (HAC) des Magens" für die primäre Magenkarzinom histologisch durch hepatoiden Differenzierung und Produktion von großen Mengen an AFP [16]. Aber er berichtete Beobachtung der primären AFP-negativen Magenkarzinomen mit charakteristischen histologischen Merkmale nachahmt hepatozellulären Karzinoms [17]. Die klinisch-pathologische Entität wurde erweitert, um das Magenkarzinom zeigt Leber Differenzierung, ohne die Produktion von AFP umfassen. In Progression, Nagai et al. stellte fest, dass die Diagnose von HAC des Magens auf die Produktion von AFP nicht abhängig war, und schlug vor, dass die Diagnose über die Anerkennung der charakteristischen histologischen Merkmale [13]
HAC des Magens als seltene Unterart bekannt wurden, basieren sollte. daher bereits berichtet Fallberichte oder Fallserien auf Aggressivität oder Diagnose konzentrieren, anstatt das Behandlungsergebnis. Die Informationen wurden sehr begrenzt. In dieser Studie führten wir eine Bewertung der klinisch-pathologische Merkmale, Behandlungsergebnisse und Prognose bei Patienten mit Magen-HAC.
Methoden Eine Computersuche der Pathologie Berichte
zur Identifizierung von pathologisch bestätigt hepatoiden Adenokarzinom des Magens von Januar durchgeführt wurde, 1996 bis Dezember 2008 in Seoul National University Hospital. Unter 15.253 Patienten mit neu diagnostizierten Magenkrebs in dieser Zeit, 26 Patienten hatten hepatoiden Adenokarzinom in ihrer Pathologie Berichte.
Diagnose von HAC auf morphologischer Merkmale abhängig war. Pathologische Diagnose von 23 Patienten wurde in erster Linie durch Untersuchung von Proben Gastrektomie zeigt histologische Beobachtungen gemacht, die spezifische hepatoiden Strukturen, wie den trabekulären, pseudo-grandular Muster und hyaline Kügelchen enthalten sind; andere Patienten, die nicht Gastrektomie unterzogen wurden, waren aber stark suggestive HAC durch Biopsien wurden durch immunhistochemischen (IHC) Färbung (Anti-AFP, Anti-Hepatozyten, alpha-1-Antitrypsin) positiv und erhöhte Serum-AFP-Ebene bestätigt. Die Häufigkeit von Magen-HAC-Konten für 0,17% aller Magenkarzinome.
Pathologie Berichte, medizinische Aufzeichnungen und Belichtungen wurden überprüft. Clinicopathologic erhaltenen Daten enthalten Alter, Geschlecht, endoskopische Befund, histopathologischen Merkmale (Tumorlokalisation, IHC-Färbung, Serum-AFP-Ebenen, die Geschichte der chronischen Hepatitis, Stadium bei Diagnose, Behandlung Modalität und Gesamtüberleben. Nach dem 7
th Edition von der American Joint Committee on Cancer (AJCC), Stadium der Tumor reklassifiziert wurde.
Um die Prognose von Patienten mit HAC bestimmen, untersuchten wir freie Überleben (RFS) und Gesamtüberleben (OS). der Ausgangspunkt von RFS Rückfall in den frühen oder lokal fortgeschrittenen Krebserkrankung war der erste Tag der Operation und der Starttag OS war der Tag der Diagnose. bei Patienten mit fortgeschrittenem oder rezidivierendem Krebs für das Gesamtüberleben und Ansprechen des Tumors auf die palliative Chemotherapie beurteilt. zur Auswertung der Ergebnisse der palliativen Chemotherapie, die Ausgangspunkt für das Gesamtüberleben (OS) und das progressionsfreie Überleben (PFS) bei Patienten palliative Chemotherapie war der erste Tag der Chemotherapie. die Kaplan-Meier-Methode zur Schätzung von RFS, PFS und OS verwendet wurde. Statistische Vergleiche und 95% Konfidenzintervall wurden mit einem SPSS-Software-Paket Version 13.0 hergestellt. (SPSS Ins., Chicago, IL USA). Ansprechen des Tumors wurde nach den Antwortbewertungskriterien für soliden Tumoren (RECIST) bewertet.
Alle Patienten ihr Einverständnis gaben vor der Gastroskopie, Chirurgie oder Chemotherapie, und jedes Verfahren wurde nach den Regeln der guten klinischen Praxis durchgeführt. Diese Studie wurde von der Ethikkommission der Seoul National University Hospital (IRB No: 0911-064-301) genehmigt wurde.
Ergebnisse
1) klinisch-pathologische Merkmale von hepatoiden Adenokarzinom (HAC) des Magens
Eine Gesamt von 26 Patienten in die Studie eingeschlossen. Zweiundzwanzig Patienten waren männlich (Durchschnittsalter 63,4 Jahre, Bereich 36,4-74,1 Jahre). Nur ein Patient mit chronischer Hepatitis B. Stadium hatte zum Zeitpunkt der Diagnose war bei 3 Patienten IB Stufe, Stufe II bei 6 Patienten im Stadium III, bei 7 Patienten, und im Stadium IV bei 10 Patienten.
Endoskopischen Befund, 3 Bormann Typ war die gemeinsame (n = 11), gefolgt von Bormann Typ 2 (n = 5). Vier Patienten zeigten die frühe Art von Magenkrebs. Tumore traten vor allem im unteren Drittel, insbesondere des Antrums (n = 16, n = 13, jeweils). In IHC, waren 15 Patienten positiv für AFP (Dakopatts, Dänemark). Nur einer von vier Patienten mit negativen AFP wurde für alpha-1-Antitrypsin (Dakopatts, Dänemark) untersucht, und das Ergebnis war positiv. Serum AFP zugänglich war bei 11 Patienten, von denen 7 Patienten erhöhte Werte hatten, und die mittlere Serum-AFP betrug 208 ng /ml (Bereich 5- 4.750.000 ng /ml) (Tabelle 1) .Tabelle 1 Clinicopathologic Merkmale aller 26 Patienten
Eigenschaften
Kein Patienten
%
Alter, Median = 63,4 (36,4-74,1)
30- 60
10
38,5%
> 60
16
61,5%
Sex (n = 26)
männlich
22
84,6%
Female
4 12,5%
Bühne bei Diagnose (n = 26)
Stadium IB
3
11,5%
Stufe II
6 23,1%
Stufe III
7
26,9%
Stufe IV 10
38,5% Endoskopische (n = 23) zu finden
Borrmann Typ I
2
8,7%
Borrmann Typ II
5
21,7%
Borrmann Typ III
11
47,8%
Borrmann Typ IV
1 4,3%
EGC †
4 17,4%
Lage (n = 25)
Ober Drittel
2 8,0%
Mitte Drittel
5
20,0%
Lower Drittel
16
64,0%
ganzen Magen
2 8,0%
Immunohitstochemical Färbung (n = 26)
AFP (positiv /negativ /‡ NA)
15/4/7
Anti-Hepatozyten (positiv /negativ /‡ NA)
4/4/18
Anti-Chymotrypsin (positiv /negativ /‡ NA)
1/1/24
Serum AFP (n = 26)
Erhöhte (Median-Bereich)
7 (208 ng /ml,
5-4,750,000 ng /ml)
Normale
4 ‡ NA
15
† Magenfrüh Krebsart, ‡ Nicht beurteilt
von 23 Patienten, die Gastrektomie unterzogen, 21 Patienten für die Ergebnisse der endovaskulären ausgewertet oder endolymphatischer Tumor Embolien werden konnte. Von diesen hatten 71% endovaskulären Tumor Embolien und 71% endolymphatischen Tumor Emboli in chirurgischen Proben (Tabelle 2) hatte. Von 8 Patienten, die nicht Rezidiv zeigten, hatten zwei Patienten endovaskuläre Tumor Embolien und drei Patienten endolymphatischer Tumor Embolien hatte. Fast alle Patienten im Stadium IV, mit Ausnahme eines Patienten mit nur Gefäßtumor Embolien, die Gastrektomie unterzogen hatten beide endovaskulären und endolymphatischer Tumor Embolien bei chirurgischen specimens.Table 2 Pathologische Befunde und Laborbefunde
Finding
% (Anzahl der Patienten)
Gegenwart
Nicht vorhanden
Nicht bewertet
endolymphatischer Tumor Embolien (n = 23)
15
6 2
Endovascular Tumor Embolien (n = 23)
15
6 2 of 2) Behandlungsmuster und die klinischen Ergebnisse für alle Fälle von hepatoiden Adenokarzinom (HAC) des Magens
Abbildung 1 zeigt die Behandlungsmuster für alle Patienten. Sechzehn Patienten wurden früh oder als lokal fortgeschrittenem Stadium diagnostiziert und zehn Patienten zeigten Fernmetastasen bei der Diagnose. Von den 18 Patienten kurative Resektion unterzogen, unterzog 9 Patienten eine adjuvante Chemotherapie und die anderen 9 Patienten aufgrund Stadium nicht adjuvante Chemotherapie erhalten I (n = 3), Alter und schlechte Leistung (n = 2), Patienten Ablehnung (n = 2) , frühen Rezidiv (n = 1), und der Tod (n = 1). Zwei Patienten mit Stadium II, fünf Patienten mit Stadium III und einem Patienten mit Stadium IV nach kurativer Operation rezidivierendem. Median Follow-up-Dauer betrug 61,4 Monate (Bereich 4,8 bis 139,5 Monate). Neun Patienten, darunter drei Patienten mit Stadium Ib, drei Patienten mit Stadium II, einem Patienten mit Stadium III und 2 Patienten mit Stadium IV waren seuchenfrei. Zwei Patienten abgelaufen aufgrund postoperative Komplikationen (verzögerte Blutung und Sepsis). Von 10 Patienten, die zunächst im Stadium IV hatte, unterzog sich 7 Patienten Gastrektomie und 6 Patienten, darunter 3 nicht operable Patienten erhielten eine palliative Chemotherapie. Zwei von drei der Stufe IV Patienten, die Gastrektomie mit R0-Resektion und metastatectomy unterzogen wurden ohne Anzeichen einer Krankheit weiterverfolgt, und die andere mit palliativer Chemotherapie nach der Wiederholung bei postoperativen 9,2 Monate behandelt wurde. Sieben Patienten von 16 Patienten mit Anfangsstadium I-III rezidivierendem und sechs Patienten erhielten eine palliative Chemotherapie. Figur 1 Behandlungsmuster für alle Patienten. Stufe bei der Diagnose war im Stadium IB in 3 Patienten im Stadium II bei 6 Patienten im Stadium III, bei 7 Patienten, und im Stadium IV bei 10 Patienten. Neun Patienten, darunter drei Patienten mit Stadium Ib, drei Patienten mit Stadium II, einem Patienten mit Stadium III und 2 Patienten mit Stadium IV, wurden geheilt. Zwei Patienten abgelaufen aufgrund der postoperativen Komplikationen. Von 10 Patienten, die zunächst im Stadium IV hatte, 6 Patienten wurden Magen und 6 Patienten erhielten eine palliative Chemotherapie. Zwei von drei der Stufe IV Patienten, die Gastrektomie mit R0-Resektion unterzogen wurden ohne Anzeichen einer Krankheit weiterverfolgt. Sieben Patienten von 16 Patienten mit Anfangsstadium I-III rezidivierendem und sechs Patienten erhielten eine palliative Chemotherapie.
Rezidivfreie mediane Überlebenszeit von Patienten, die kurative Resektion 16,67 Monate (Bereich 1.63- 65,9) (Abbildung 2) wurden war. Die mittlere Gesamtüberlebenszeit der Stufe I-III und Stufe IV waren 28,0 und 8,2 Monate bzw. (Bereich 2,9-66,0 Monate 2,1 bis 60,87 Monate) (Abbildung 3). Die Überlebensunterschied zwischen den beiden Gruppen war marginal signifikant (p = 0,068). Abbildung 2 Kaplan-Meier-Kurve von RFS zu früh oder lokal Magen HAC fortgeschritten. Median RFS von Patienten, die kurative Resektion unterzogen war 16,67 Monate (Bereich 1.63- 65,9) (Vertical upticks repräsentieren Patienten am Leben).
3 Kaplan-Meier-Plot von OS Abbildung gemäß Stufe. Median OS der Stufe I-III und Stufe IV waren 28,0 und 8,2 Monate bzw. (Bereich 2,9-66,0 Monate 2,1 bis 60,87 Monate p = 0,068) (Vertical upticks repräsentieren Patienten am Leben)
Gesamt-Überleben von 18 Patienten mit. metastasiertem oder rezidivierendem Krebs war 9,63 Monate (95% CI: 4,34 bis 14,92, Bereich: 1.20- 60,87 Monate).
3) Ergebnisse der palliativen Chemotherapie bei metastasierendem /rezidivierende hepatoiden Adenokarzinom (HAC) der zehn Patienten
Magen hatte metastasiertem HAC und 8 rezidivierenden HAC hatte, von denen 13 Patienten mit palliativer Chemotherapie behandelt wurden. Die häufigste metastatic Seite war Lymphknoten (n = 9), gefolgt von der Leber (n = 8) und peritoneal seeding (n = 3). Portal Venenthrombose wurde in acht Patienten identifiziert.
Die am häufigsten verwendete Therapie war eine Kombination von fluorpyrimidin und Platin (n = 7), gefolgt von einer Kombination aus Paclitaxel und Cisplatin und TS-1 single (jeweils n = 2, n = 2) (Tabelle 3). Bewertung der Ansprechrate war möglich, in 12 von 13 Patienten mit palliativer Chemotherapie behandelt. Einer zeigte partielles Ansprechen und fünf Patienten zeigten eine stabile Erkrankung; die Rücklaufquote betrug 8,3% und die Krankheit Kontrollrate betrug 50% (95% CI: 25,4 -74,6) .Tabelle 3 Clinicopathologic Charakteristika der Patienten eine palliative Chemotherapie erhalten
Eigenschaften (n = 13 )
von Patienten No
%
Alter,
Median: 59 (36-74)
Sex
Male
12
92,3%
weiblich
1 7,7%
ECOG PS 0-1
11
84,6
2 2
15,4
Bühne
Stadium IV bei der Diagnose
6 46,2%
wiederkehrte Krebs
7
53,8%
Pfortaderthrombose
Ja
8 61,5%
No
5
38,5%
Metastasierung
LN
9
69,2%
Leber 8
61,5%
Peritoneal Seeding
3
23,1%
Pancreas
2
15,4%
Lunge
1 7,7%
Gastrectomy
Ja 10
76,9%
No
3
23,1%
Anzahl der metastatischen Orgel
1-2
8 61,5%
> 3
5
38,5%
Chemotherapie
bis 1. Zeile
bis 13
100%
Bis 2. Zeile
7
53,8%
Up bis 3. Zeile
1 7,7%
FP /XP /FOLFOX
chemotherapeutischer Wirkstoff †
7
53,8%
TP ‡ 2
15,4%
TS-1
2 15,4%
Andere (FL§, FM¶) 2
15,4%
† Cisplatin und 5-FU /Capecitabin und Cisplatin /Oxaliplatin, Leucovorin und 5-FU
‡ Paclitaxel und Cisplatin
§ 5-FU und Folinsäure
¶ 5-FU und MMC
OS und PFS von 13 Patienten, die palliative Chemotherapie waren 8,03 und 3,47 Monate, bzw. ( 95% CI: 6,59-9,47, Bereich: 0,63 bis 40,8 Monate, 95% CI: 0,65-6,29, 0,63-35,43 Monate, jeweils) (4 und 5). Abbildung 4 Kaplan-Meier-Plot von OS für Patienten, die palliative Chemotherapie. Median OS von 13 Patienten eine palliative Chemotherapie erhielten, betrug 8,03 Monate (95% CI: 6,59-9,47, Bereich: 0,63 bis 40,8 Monate)
Abbildung 5 Kaplan-Meier-Kurve von PFS für Patienten palliative Chemotherapie erhalten. Median PFS von 13 Patienten, die palliative Chemotherapie 3,47 Monate war, bzw. (95% CI: 0,65-6,29, Bereich: 0,63-35,43 Monaten beziehungsweise)
Diskussion
In dieser Studie wurde die Inzidenz von HAC betrug 0,17%, was relativ niedriger als 0,38 bis 0,73%, was in einer früheren Studie [1, 13] berichtet wurde. Niedrigere Inzidenz unserer Studie ist mit Schwierigkeiten bei der Diagnose dieser Neoplasma assoziiert. HAC ist eine seltene Art von Adenokarzinom des Magens und andere typische Diagnosen ausgeschlossen werden sollte. Diagnose von HAC oft mikroskopisch kleinen Beobachtung und IHC Studie, einschließlich anti-Hepatozyten, anti-AFP und Anti-Chymotrypsin erforderlich. Von den gesamten Themen in unserer Studie unterzog sich 88% Gastrektomie. Nur drei Patienten wurden mit HAC ohne Gastrektomie diagnostiziert. Es ist möglich, dass die meisten Patienten, die nur durch eine Biopsie diagnostiziert wurden und die nicht eine Operation erforderlich, nicht enthalten waren.
Primären Magenkrebs erhöhten Serum-AFP von Magen-Produktion von primitiven foregut Herkunft zeigen konnte, wie der Leber, und AFP produziert Leber metastatischen Läsionen; berichtete Inzidenz von AFP produzieren Magenkrebs hat von 1,3 bis 15% aller Fälle von Magenkrebs gewesen. In den frühen Tagen der HAC-Definition, wurde vorgeschlagen, dass HAC von AFP-produzierenden Magenkrebs entwickelt, in denen umfangreiche hepatoiden Differenzierung selten aufgetreten, weil nicht alle AFP-produzierenden Magen-Krebs ein hepatozelluläres Karzinom ähneln [18]. Später Ishikura et al. auf primären AFP-negativen Magenkarzinomen mit charakteristischen histologischen Merkmale nachahmt hepatozelluläres Karzinom berichtet [17]. Außerdem Nagai et al. berichtet, dass 46% der Magen HACs negativ gefärbten AFP zeigte und daß mikroskopisch hepatoiden Eigenschaften, unabhängig von AFP-Färbung wurden wichtiger für die Prognose [13]. In ihrer Studie wurden alle Patienten mit negativ AFP-gefärbten Magen HAC und zugänglich Serum hatte AFP normalen Serum-AFP-Ebenen. Daher zeigt Magenkrebs Leber Differenzierung, ohne die Produktion von AFP eine klinisch-pathologische Entität von HAC wurde.
In Magen HAC, Blutgefäße und lymphatischen Permeation und regionalen Lymphknotenmetastasen Werte häufiger vor als in schlecht differenzierten Adenokarzinom des Magens und primären HCC, und diese wurden mit einer schlechteren Prognose verbunden [1, 17]. In unserer Studie von 23 Patienten, die Gastrektomie unterzogen, hatten 71% endovaskuläre Tumor Embolien, die als die einer früheren Studie niedriger war [1]. Keiner der Patienten mit Stadium IB hatte mikroskopisch endovaskuläre oder endolymphatischer Invasion und sie nicht Rückfall (medianen Nachbeobachtungszeit = 61,37 Monate, Bereich 25,8-63,0 Monate). Sechs von acht Patienten, die nicht haben nicht endovaskuläre Invasion hat Rückfall, der ein guter Prädiktor für einen Rückfall sein kann, obwohl die Validierung erforderlich sein wird. Daher Diagnose von Magen-HAC zu einem früheren Zeitpunkt kann zu einer besseren Prognose führen. Das Überleben Unterschied zwischen Stadium I-III und Stufe IV marginal signifikant war, die von der kleinen Zahl von Patienten zur Folge haben könnte.
Nach einer randomisierten Studie zur First-Line-Therapie zur Behandlung von fortgeschrittenem Magenkrebs, Response-Rate von 1 Chemotherapie st Linie ist etwa 32-46% und OS von IV Magenkrebs Stadium ist 9,3-10,5 Monate [19]. In dieser Studie ist Median OS 8,03 Monate, die als die von früheren Berichten viel länger ist, die fünf Patienten eingeschlossen [20].
Relativ längeres Überleben mit guter Leistung und aktive Therapie, einschließlich Palliativ Gastrektomie und Chemotherapie assoziiert ist. In einem Xenotransplantat-Modell von AFP-produzierenden Magenkrebs, 5-FU, Doxorubicin und Epirubicin nicht Unterdrückung von Tumorwachstum induzieren; jedoch MMC und Cisplatin kann zu einem gewissen Grad [21] aktiv sein. Die meisten Patienten erhielten Platin basierten Chemotherapie. Die Krankheit Kontrollrate betrug 50%. Insbesondere wird ein Patient mit Anfangsstadium IV und zeigt ein partielles Ansprechen auf 1 st Linie palliative Chemotherapie (Cisplatin und 5-FU) zeigte Progression nach 26,2 Monate. Der Patient zeigte auch Teilantwort auf 2 nd Linie Cisplatin und Paclitaxel
HAC des Magens in all diesen Fällen wurde überarbeitet. aufgrund der seltene Auftreten dieser Neoplasmen werden die wichtigsten klinischen Eigenschaften dieser Typen von Tumoren in einem veröffentlichten Bericht [22] beschrieben. Die Mehrzahl der Patienten waren männlich und das Durchschnittsalter war etwa 64 Jahre alt. Die Antrum und Pylorus waren die häufigsten primären Standorte von Tumoren und deren AFP Ebenen als normal viel höher waren. Unsere Daten zeigen auch männliche Dominanz (11: 2) und das untere Drittel war die häufigste Stelle (65%); 63% der Patienten für Serum-AFP-Ebene geprüft hatte AFP erhöht, und 61% der Patienten wurden als Stufe I, II diagnostiziert oder III, und der andere wurde als Stadium IV diagnostiziert. Relapse Rate der Patienten mit frühen Stadium oder lokal fortgeschrittenem Stadium betrug 47%.
Diese Studie auch einige Einschränkungen. Der erste ist, dass dies eine retrospektive Studie von einem einzigen Zentrum ist; so können wir nicht die Möglichkeit eines Selektionsbias auszuschließen. Die zweite ist der Probengröße zu klein. Dennoch, wenn man bedenkt das seltene Auftreten von HAC und frühere Fallberichte oder Fallserie, präsentiert diese Studie die erste Bericht, der auf Rezidivrate konzentriert der frühen oder fortgeschrittenen Stadium HAC und Ansprechrate auf eine Chemotherapie und Behandlungsergebnisse von Endstadium HAC.
Fazit
Abschließend HAC des Magens ist eine seltene Art des Adenokarzinoms, mit einer Inzidenz von 0,17% der Magenkrebsfälle. Von den gesamten HAC Patienten wurden 60% der Patienten mit frühen Stadium oder lokal fortgeschrittenem Stadium diagnostiziert, und 47% von ihnen einen Rückfall. Alle Patienten mit Magenfrühkarzinomen Phase wurden geheilt. Daher ist die Früherkennung von dieser Art von Krebs von entscheidender Bedeutung für die Prognose eines Patienten. Weitere Studien, die Biologie und die Ergebnisse dieses Tumors zu offenbaren gerechtfertigt sind.
Erklärungen
Danksagungen und Finanzierung
Diese Studie wurde teilweise von der koreanischen Stiftung der Leberforschung (Grants 2011) unterstützt.
Wir würden wie unsere tiefste Dankbarkeit an Dr. Hye-Jung Chang von Universität Konyang Krankenhaus von Korea für ihre Kommentare zum Manuskript zum Ausdruck bringen.
Diese Studie teilweise auf der 2010 Gastrointestinal Cancer Symposium, Orlando, Florida vorgestellt wurde.
Autoren 'Original vorgelegt Dateien für Bilder
Nachfolgend finden Sie die Links zu den Autoren ursprünglich eingereichten Dateien für Bilder. 12876_2010_603_MOESM1_ESM.jpeg Autoren Originaldatei für Abbildung 1 12876_2010_603_MOESM2_ESM.png Autoren Originaldatei für Abbildung 2 12876_2010_603_MOESM3_ESM.png Autoren Originaldatei für Abbildung 3 12876_2010_603_MOESM4_ESM.png Autoren Originaldatei für Abbildung 4 Original-Datei '12876_2010_603_MOESM5_ESM.png Autoren für Abbildung 5 konkurrierende Interessen
Die Autoren erklären, dass sie keine Interessenkonflikte haben.
|  Die glutenfreie Lüge:Warum die meisten Zöliakie-Betroffenen langsam sterben
Konventionelle Medizin funktioniert normalerweise so… Ich habe ein Problem, der Arzt findet heraus, was das Problem ist, und gibt mir ein herkömmliches Rezept, das im Allgemeinen von Ärzten, Forscher
Die glutenfreie Lüge:Warum die meisten Zöliakie-Betroffenen langsam sterben
Konventionelle Medizin funktioniert normalerweise so… Ich habe ein Problem, der Arzt findet heraus, was das Problem ist, und gibt mir ein herkömmliches Rezept, das im Allgemeinen von Ärzten, Forscher
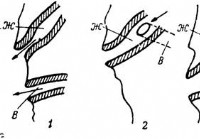 Akute Pankreatitis - Diagnose des akuten Abdomens
Es gibt die Meinung, dass die akute Pankreatitis eine sehr seltene Erkrankung ist. In zwei letzten Jahrzehnten wurde die bedeutende Erhöhung der Frequenz der scharfen Pankreatitis skizziert, und sie m
Akute Pankreatitis - Diagnose des akuten Abdomens
Es gibt die Meinung, dass die akute Pankreatitis eine sehr seltene Erkrankung ist. In zwei letzten Jahrzehnten wurde die bedeutende Erhöhung der Frequenz der scharfen Pankreatitis skizziert, und sie m
 Die Vorteile eines telemedizinischen Termins
Hätten Sie jemals gedacht, dass Telemedizin-Termine zur Regel werden würden? Die Wahrheit ist, dass die meisten medizinischen Einrichtungen seit Jahrzehnten Telemedizin in irgendeiner Form anbieten. V
Die Vorteile eines telemedizinischen Termins
Hätten Sie jemals gedacht, dass Telemedizin-Termine zur Regel werden würden? Die Wahrheit ist, dass die meisten medizinischen Einrichtungen seit Jahrzehnten Telemedizin in irgendeiner Form anbieten. V