Les résultats et les analyses post hoc des données de l'étude de phase 2 américaine sur 40 patients ont été présentés dans une affiche intitulée, " Opaganib, un inhibiteur oral de la sphingosine kinase-2 (SK2) dans la pneumonie COVID-19 :une étude randomisée, En double aveugle, Étude de phase 2A contrôlée par placebo, in Adult Subjects Hospitalized with SARS-CoV-2 Positive Pneumonia (NCT:04414618)". Les patients de l'étude ont été randomisés pour recevoir soit de l'opaganib soit un placebo en plus des soins standard (SoC), comprenant principalement de la dexaméthasone et/ou du remdesivir. Les résultats comprennent :
Le besoin d'une thérapie orale efficace pour traiter le COVID-19 est clair. Une telle thérapie améliorerait grandement notre capacité à gérer cette pandémie. Ces données, de cette étude clinique de preuve de concept de l'opaganib chez des patients atteints de COVID-19 sévère, suggèrent un rôle potentiel de l'inhibition de SK2 dans la lutte contre les effets de ce virus. Avec beaucoup plus de données sur l'opaganib attendues dans les semaines à venir, nous pourrions faire de réels progrès vers l'accès à une thérapie orale indispensable pour les patients qui ont actuellement peu d'options à leur disposition. »
Kevin Winthrop, MARYLAND, MPH, Professeur de maladies infectieuses, Université de la santé et des sciences de l'Oregon, qui a présenté les résultats au World Microbe Forum
« La présentation de ces données positives de notre étude exploratoire de phase 2 confirme notre confiance croissante dans le fait que l'opaganib pourrait être le premier roman, thérapie orale pour démontrer son efficacité dans le traitement du COVID-19 dans une vaste étude de stade avancé. Avec l'achèvement récent du recrutement de notre étude mondiale de phase 2/3 de 475 patients, nous en aurons une image plus claire dans un avenir très proche, " a déclaré Mark L. Levitt, MARYLAND, Doctorat., Directeur médical chez RedHill. « L'opaganib agit à la fois sur la cause et l'effet du COVID-19 via un double mode d'action antiviral et anti-inflammatoire unique. Étant ciblé sur l'hôte, l'opaganib devrait également maintenir son effet contre les variantes émergentes du SRAS-CoV-2, qui continuent de menacer les progrès réalisés contre la pandémie et soulignent le besoin urgent de traitements efficaces contre le COVID-19. »
L'étude mondiale de phase 2/3 de 475 patients sur l'opaganib dans le COVID-19 sévère a été approuvée dans 10 pays et le recrutement a été achevé, à travers 57 sites participants, le 6 juin. Le critère d'évaluation principal de l'étude est la proportion de patients respirant de l'air ambiant sans assistance en oxygène au jour 14.
Mesures de résultats supplémentaires importantes, comme le temps de sortie de l'hôpital, amélioration selon l'échelle ordinale de l'Organisation mondiale de la santé pour l'amélioration clinique et l'incidence de l'intubation et de la mortalité, seront également capturés dans la période de suivi pouvant aller jusqu'à 6 semaines. L'étude a reçu quatre recommandations indépendantes du DSMB pour continuer à suivre des examens de sécurité sans aveugle et un examen de futilité. En outre, une évaluation des taux d'intubation mixte en aveugle et de mortalité à ce jour était encourageante par rapport aux taux de mortalité signalés dans les grandes études de plateforme telles que RECOVERY, et d'autres études dans des populations de patients similaires.
 Gâteaux de poisson thaïlandais (avec haricots verts et mayonnaise épicée maison)
Gâteaux de poisson thaïlandais (avec haricots verts et mayonnaise épicée maison)
 Torsion d'un gros épiploon - Diagnostic de l'abdomen aigu
Torsion d'un gros épiploon - Diagnostic de l'abdomen aigu
 Produit chimique contre le cancer provenant d'un microbe intestinal commun
Produit chimique contre le cancer provenant d'un microbe intestinal commun
 Mars est le Mois national de la sensibilisation au cancer colorectal
Mars est le Mois national de la sensibilisation au cancer colorectal
 Briser le cercle vicieux SCD Brownies au beurre d'arachide
Briser le cercle vicieux SCD Brownies au beurre d'arachide
 Pain aux bananes sans céréales, sans produits laitiers, sans noix et à faible teneur en glucides
Pain aux bananes sans céréales, sans produits laitiers, sans noix et à faible teneur en glucides
 Qu'est-ce que l'infection à Helicobacter Pylori ?
Helicobacter pylori (H. pylori) est une bactérie en forme de tire-bouchon qui a été identifiée en 1982 comme une cause principale dulcères destomac et de gastrite chronique, affections autrefois consi
Qu'est-ce que l'infection à Helicobacter Pylori ?
Helicobacter pylori (H. pylori) est une bactérie en forme de tire-bouchon qui a été identifiée en 1982 comme une cause principale dulcères destomac et de gastrite chronique, affections autrefois consi
 Anorexie mentale
Centre de lanorexie mentale Diaporama de photos sur les troubles alimentaires Meilleures résolutions alimentaires Améliorer le diaporama dimmunité Commentaires des patients :Anorexie mentale - Traitem
Anorexie mentale
Centre de lanorexie mentale Diaporama de photos sur les troubles alimentaires Meilleures résolutions alimentaires Améliorer le diaporama dimmunité Commentaires des patients :Anorexie mentale - Traitem
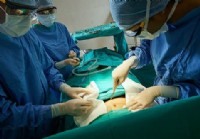 Qu'est-ce qu'une cholédochojéjunostomie ?
Quest-ce quune cholédochojéjunostomie ? Une cholédochojéjunostomie est une intervention chirurgicale visant à établir une connexion (anastomose) entre le canal cholédoque et le jéjunum. Cette techn
Qu'est-ce qu'une cholédochojéjunostomie ?
Quest-ce quune cholédochojéjunostomie ? Une cholédochojéjunostomie est une intervention chirurgicale visant à établir une connexion (anastomose) entre le canal cholédoque et le jéjunum. Cette techn