sottomucosa primaria plasmocitoma nodulare dello stomaco: una variante poco riconosciuta del linfoma gastrico
Abstract
Abstract
plasmocitoma gastrica (GP) è una rara variante di linfomi gastrici. Nel caso eccezionale che un paziente si presenta con GP, la lesione occupa lo strato mucoso nella stragrande maggioranza dei casi. Qui riportiamo un caso di plasmocitoma nodulare limitata alla sottomucosa senza evidenza di pylori
(Hp) infezione da Helicobacter. Il paziente era a 59 anni, presentando femminile senza sintomi particolari. Il tumore era ben delimitata e consisteva di una proliferazione monomorfe diffusa di plasmacellule con numerosi follicoli linfoidi sparsi in tutto il tumore. La superficie mucosa era intatto e non associata ad un qualsiasi noduli tumorali. Le cellule sono state diffusamente positivo per CD79a, bob1, EMA e IgA e costantemente negativo per CD3, CD19, CD20, PAX5, CD56, IgM e IgG. Inoltre, in
situ dimostrato clonalità in forma di λ restrizione luce-catena. Questo sottomucosa nodulare modello proliferazione di plasmocitoma è scarsamente riconosciuta e considerata come una nuova variante del linfoma
diapositive virtuali
La slitta virtuale (s) per questo articolo può essere trovato qui:. Http: //www. diagnosticpathol logia. diagnomx. eu /vs /3489998708673079
Parole
plasmocitoma solitario Stomaco Sottomucosa linfoma Sfondo
linfomi della zona marginale extranodale della mucosa tessuto linfoide associato (linfoma MALT) e diffuso a grandi cellule B linfomi sono ben documentato come i sottotipi più comuni di GI linfomi [1]. In questo contesto è anche importante notare che il linfoma MALT è spesso associata a pylori
(Hp) infezione da Helicobacter. Oltre a con una grande popolazione di linfociti che formano lesioni linfoepiteliali distinte, circa un terzo dei casi di linfoma MALT presenterà con vari gradi di differenziazione plasmocitaria [2]. piccola malattia intestinale immunoproliferativa (IPSID), in particolare, che è un sottotipo di linfoma MALT e osservata principalmente in Medio Oriente, in genere mostra colpendo differenziazione plasmocitaria [2].
Sul lato opposto dello spettro, plasmocitoma extraosseous (EP) , che è caratterizzata da un'espansione localizzata e monoclonale di plasmacellule in tessuti diversi osso, sorgono nel tratto respiratorio superiore che comprende dell'orofaringe, nasofaringe, seni e laringe [2]. Il prossimo luogo più frequente di insorgenza della lesione di massa è lo stomaco; tuttavia, questo è estremamente raro e rappresenta meno del 5% di tutte EP [3]. Inoltre, la stragrande maggioranza dei plasmocitomi gastrici convenzionali sono stati documentati in primo luogo nello strato mucoso [4-6].
Dettagli Questo rapporto di un caso eccezionalmente raro di un plasmocitoma nodulare che occupa la sottomucosa gastrica senza infezione da Hp sottostante. Per quanto a nostra conoscenza, solo due casi simili sono stati segnalati fino ad oggi e, quindi, questa condizione può essere efficacemente definito come entità poco riconosciuta di linfoma gastrico primaria.
Cofanetto
La storia clinica
A 59- femmina di anni con un passato storia clinica del carcinoma papillare della tiroide è stato presentato al nostro ospedale a causa di un tumore gastrico identificato nel corso di una esophagogastroduodenoscopic screening di massa (EGDS) l'esame, che ha rivelato una lesione senza intoppi elevata, a 2 cm di diametro, che occupa le pareti posteriori del corpus gastrica (Figura 1). Nessun cambiamento ulcerosa è stato osservato sulla superficie della mucosa, il paziente era priva di sintomi di accompagnamento e studio risultati di laboratorio erano tutti nella norma. Sulla base di una diagnosi di tumore sottomucosa non altrimenti specificato, un gastrectomia parziale è stata eseguita. Figura 1 Esofagogastroduodenoscopia. Ben delimitate, lesioni elevate sulla parete posteriore del corpus gastrica.
Caratteristiche di mieloma multiplo non erano evidenti e livelli di calcio nel siero, emoglobina e della creatinina del paziente erano entro i limiti normali. Non sono risultati significativi su un esame radiografico dello scheletro sono stati notati e ad emissione di positroni tomografia /tomografia computerizzata (PET /CT) non hanno mostrato altre lesioni. Infine, siero e proteine nelle urine elettroforesi ha dato risultati normali. Nessun ulteriore trattamento è stato eseguito. Il presente studio è stato approvato dal Comitato Etico di Kobe University Graduate School of Medicine.
Caratteristiche lordo
La mucosa della superficie del tumore era liscia e normale aspetto. Il tumore asportato misurato 2,0 × 1,5 × 1,5 cm di altezza, è stato ben delimitata, e consisteva in una massa morbida ed elastica biancastra situato nello strato sottomucosa. Il tumore aveva una superficie di taglio di colore beige omogeneo ed era focally emorragica
. Microscopica dispone
punto di vista istologico, il tumore era relativamente ben delimitata e tutto trova nello strato sottomucosa (Figura 2). La mucosa superficie che copre il tumore era intatto e non è stato associato con il nodulo tumore stesso, che consisteva di una proliferazione monomorfico diffusa di plasmacellule (Figura 3). I nuclei delle cellule tumorali sono state sfollate perifericamente e leggermente pleomorfo. Poche cellule tumorali contengono corpi Dutcher nei loro nuclei. Molti follicoli linfoidi sono stati sparsi in tutto il nodulo tumorale (figura 4) e sono zone mantello ben formati e normali che cercano centri follicolari, costituite in particolare da grandi centroblasti con sparsi macrofagi del corpo tingible. Giemsa mostrato alcuna Hp aderente alla superficie della mucosa gastrica. La biopsia del midollo osseo esemplare era normale e offerto alcuna prova suggestive di plasmacellule proliferazione. Rilievi immunoistochimici sono forniti in Figura 5. Le cellule tumorali sono stati diffusamente positive per CD79a, bob1, EMA, CD138, MUM-1, e IgA e negativo per CD5, IgM e IgG. Sebbene i follicoli linfoidi e un piccolo numero di dispersi reattivi cellule B nella zona interfollicolare erano positive per CD20, le cellule tumorali erano negative per CD20, CD19 e CD56. L'immunofenotipo dei centri germinali dei follicoli linfoidi sparsi era normale: CD10 positivo, Bcl-2 polarità negativa e conservati in Ki67 (dati non riportati). In situ ibridazione
per κ e catene leggere delle immunoglobuline lambda λ rivelato restrizione catene leggere nelle cellule tumorali. Inoltre, D2-40 colorazione non ha rivelato strutture seno-come nodulo tumorale, indicando che il nodulo differisce dal linfonodo. Figura 2 Il tumore forma un nodulo sottomucosa gastrica (HE macchia). Inserto mostra mucosa normale.
Figura 3 Il tumore si compone di proliferazione diffusa di plasmacellule leggermente pleomorphic. Inserto mostra corpi Dutcher (HE macchia).
Figura 4 Numerosi follicoli linfoidi giacevano tra le cellule tumorali (HE macchia).
Figura 5 studi di immunoistochimica. a) CD79a è diffusa positivo. Le cellule che dimostrano forte positività sono cellule B reattive. b) CD20 è positivo solo nel non-neoplastiche cellule B nei follicoli sparsi, e in piccole quantità nelle cellule reattive interfollicolari. c) Bob-1, d) EMA, e) ed f CD138) MUM-1 sono diffusamente positivo. Le cellule tumorali sono positive per g) IgA, e negativo per h) IgG e i) IgM. j) D2-40 colorazione non ha rivelato le strutture del seno, come nel nodulo tumorale. k) composito delle cellule tumorali rappresenta l'assenza di espressione catena leggera κ, e l) diffondere citoplasmatica λ espressione catena leggera.
Dati i risultati di laboratorio di cui sopra, le lesioni sono stati diagnosticati come sottomucosa primaria plasmocitoma nodulare dello stomaco.
Discussione
in questo rapporto descriviamo un caso estremamente raro di un plasmocitoma nodulare primaria in via di sviluppo nella sottomucosa gastrica, che molto probabilmente costituisce un'entità poco riconosciuta di linfoma gastrico primaria.
per quanto riguarda la proliferazione neoplastica delle cellule del plasma nello stomaco , plasmocitoma primario dovrebbe sempre essere distinto da altre malattie linfoproliferative con differenziazione plasmocitaria, come il mieloma delle plasmacellule, linfoma linfoplasmacitico (LPL), variante della malattia delle cellule del plasma di Castleman (PC-CD), e linfoma MALT.
La sistemica richiede un esame delle ossa l'aspirazione o biopsia midollare per distinguere questa condizione da un coinvolgimento gastrico osseo mieloma delle plasmacellule. Nel caso di specie, sintomi o reperti suggestivi di mieloma delle plasmacellule sono stati documentati. In termini di immunoistochimica, 67-79% dei casi di mieloma delle plasmacellule ossee dimostrare CD56 positività [7]. Anche se i risultati sono in ultima analisi inconcludenti a causa del numero di campione limitato, CD56 negatività potrebbe forse essere sfruttata come strumento per differenziare questa malattia da mieloma delle plasmacellule.
Lo stomaco è un sito relativamente comune per i linfomi extranodali. Mentre linfomi a cellule T e NK /T-cellulari sono anche noti per influenzare sporadicamente stomaco, la maggior parte dei linfomi gastrici primari sono di lignaggio B-cell [1, 8]. linfomi MALT più comunemente sorgono nel tratto GI e morfologicamente consistono di cellule eterogenee piccoli B, cellule monocitoidi, piccoli linfociti, così come immunoblasti sparse e cellule centroblast-simili [9]. Tipicamente, le cellule neoplastiche di linfoma MALT esprimono marcatori di lineage cellule B, e sono negativi per la ciclina D1, CD23, CD10 e CD5, con rare eccezioni [10]. differenziazione plasmocitaria è spesso presente nei linfomi MALT gastrici; tuttavia, si sviluppano nella mucosa e sono strettamente associati con il coinvolgimento del epitelio ghiandolare. Così essi sono spesso indicati come lesioni linfoepiteliali. Inoltre, la maggior parte dei casi (62-77%) sono associati con l'infezione Hp [9]. Il caso presentato qui, tuttavia, ha rivelato un modello completamente distinto di malattia:. Noduli "sottomucosa" ben delimitate-, una popolazione puramente plasmocitaria delle cellule tumorali, e nessun sottostante infezione da Hp
PC-CD è generalmente sintomatica, con febbre, sudorazione notturna, perdita di peso e lesioni multiple. PC-CD del tratto gastrointestinale è estremamente raro e c'è stato solo un caso clinico che documenta una lesione polipoide 4 cm di diametro che coinvolge retto [11]. Tipicamente, PC-CD mostra marcata proliferazione di vasi in aggiunta a prominente infiltrazione plasmocitaria nelle aree interfollicolari. I follicoli linfoidi mostrano un modello reattivo con caratteristiche ialino vascolari rare e vasi penetrato. Inoltre, PC-CD di solito si presenta con una vasta gamma di cellule B e plasmacellule sono di solito policlonale; tuttavia, ci sono state segnalazioni che dettagliano le prove immunofenotipica di Ig restrizione catena pesante e leggera, nonché [12]. Pertanto, un esame morfologico metodica dei follicoli e delle aree interfollicolari è indispensabile per distinguere PC-CD da plasmocitoma. Nel caso di specie, nessuna delle caratteristiche distintive associate con PC-CD sono stati identificati.
LPL di solito comporta il midollo osseo e la maggior parte dei pazienti in possesso di un siero paraproteina IgM. Istologicamente, c'è una proliferazione relativamente monotono di piccoli linfociti, plasmacellule e linfociti plasmacitoidi con relativamente poche cellule trasformate. corpi Dutcher, un aumento dei mastociti e emosiderina sono anche caratteristiche tipiche, e la catena leggera κ è espresso più frequentemente di quanto la catena leggera λ. C'è un caso clinico su LPL che si verificano nello stomaco; tuttavia, questo è stato infine trascurato come lesione gastrica di coinvolgimento secondaria [13]. Nel caso di specie, il paziente ha presentato senza sintomi, e visualizzato nessun linfoadenopatia o siero paraproteine. Inoltre, i nuclei delle cellule tumorali erano più pleomorfo e le cellule linfoidi non plasmocitaria mancava un componente neoplastica.
Solito linfomi MALT o LPLS espressi IgM, mentre plasmocitomi esprimono IgG. Nel caso qui riportato, le cellule tumorali sono stati diffusamente positive per IgA. Anche se plasmocitoma esprimendo IgA è un fenomeno raro, Shao et al ha recentemente riportato il verificarsi di un plasmocitoma esprimere IgA, che ha caratterizzato giovane età al momento della presentazione, a basso rischio di progressione a mieloma delle plasmacellule, e l'associazione con la malattia autoimmune o disfunzione immunitaria [14]. Al contrario, nel nostro caso, il paziente non ha presentato con una qualsiasi delle caratteristiche cliniche descritte da Shao et al.
Molti precedentemente riportati casi di plasmocitoma gastrica erano malattie essenzialmente mucosa [4-6], mentre il nostro caso ha mostrato una completamente diversa modello di proliferazione. Riteniamo pertanto che sia una variante poco riconosciuto e rara di plasmocitoma gastrica. Fino ad oggi, solo due casi hanno riportato plasmocitomi gastrici trova interamente nella sottomucosa, come descriviamo nel caso di specie [15, 16]. Un confronto di questi casi e la nostra è illustrato nella Tabella 1. L'età media dei tre casi, composto da due maschi e una femmina, era di 61 anni (range: 57-67 anni). La dimensione media del tumore è stata di 2,1 cm (range: 0,7-4,1 cm). Resezioni sono state eseguite e nessuno dei casi hanno mostrato alcuna evidenza di recidiva tumorale o lo sviluppo di mieloma sistemica dopo la prima treatment.Although è necessaria una maggiore corpo di casi per raggiungere conclusioni definitive, l'esperienza con questi tre casi suggerisce che la terapia aggressiva non è richiesto per i pazienti che hanno subito l'asportazione chirurgica completa. linfomi MALT, insieme con alcuni casi di plasmocitomi gastriche associate con infezione da Hp sono stati curati con riferito eradicazione Hp [17, 18]. Tuttavia, nessuna infezione Hp è stata rilevata nel nostro caso o qualsiasi degli altri casi precedentemente riportato. Pertanto, Hp eradicazione non è presumibilmente un mezzo efficace per il trattamento di questo subtype.Table 1 Sintesi di sottomucosa gastrica plasmocitoma
Età
sesso
Regione nello stomaco
Dimensioni (cm)
Terapia
sopravvivenza libera da malattia (anno)
Roost. et al (2007)
67
maschio
Angolo
0,7
EMR *
2,5
Navin. et al (2010)
57
maschio
grande curvatura
4.1
gastrectomia
alcuna informazione
nostro caso
59
femminile
Corpus
1.5
resezione parziale
1.5
* EMR, endoscopica resezione mucosa.
sparse follicoli linfoidi 'reattivi' nel nodulo tumorale sono la definizione reperti caratteristici nel caso di specie. Sebbene i due casi sottomucosa plasmocitoma precedentemente indicati sono stati anche ben circoscritta, il tumore descritto in questo studio presentato con una consistenza pura di plasmacellule senza la formazione di follicoli linfoidi. Anche se il motivo esatto per spiegare perché questo tumore presentato con follicoli linfoidi scattererd è chiaro, un'infezione sottostante o coinvolgimento linfonodale sono alcune spiegazioni plausibili. E 'noto che alcuni agenti infettivi, tra cui HP o il virus di Epstein-Barr inducono alterazioni infiammatorie con follicoli linfoidi nello stomaco [19, 20]; Tuttavia, HP e ibridazione in situ per Epstein-Bar RNA virus-codificato (EBER) erano entrambi negativi, in questo caso. Inoltre, D2-40 immunostaining non è riuscito a rivelare eventuali strutture del seno come ben sviluppate all'interno del nodulo tumorale. Va inoltre notato che i linfonodi non dovrebbero essere presenti in sottomucosa normale. Da questi risultati, si può dedurre che la possibilità di coinvolgimento linfonodale è improbabile. Tuttavia, la possibilità di coinvolgimento linfonodale, non si può escludere a causa della presenza di strutture sottili periferiche capsula-come, la morfologia ben demarcata, e alcuni vasi D2-40-positivo all'interno del nodulo. Ulteriore accumulo di casi simili e le loro successive analisi sono necessari per chiarire la reale portata di queste morfologie uniche.
Conclusioni
Per riassumere, la presente relazione descrive un caso estremamente raro di un plasmocitoma solitario primaria situata esclusivamente nella sottomucosa gastrica. Questo modello proliferazione è scarsamente riconosciuto e molto probabilmente costituisce una nuova variante del linfoma gastrico. Anche se la prognosi sembra essere eccellente, un maggior numero di casi simili è necessario al fine di chiarire le caratteristiche clinico-patologici di questa variante.
Consenso
consenso informato scritto è stato ottenuto da paziente per la pubblicazione di questo caso clinico e immagini di accompagnamento . Una copia del consenso scritto è disponibile per la revisione da parte Editor-in-Chief di patologia diagnostica
. Dichiarazioni
Ringraziamenti
Gli autori desiderano ringraziare il Dr. Richard H. Kaszynski presso il Dipartimento di Medicina Legale, Kobe University Graduate School of Medicine, per la sua modifica e contributo costruttivo nella formulazione di questo manoscritto.
autori fascicoli presentati originali per
di seguito sono riportati i link ai degli autori fascicoli presentati originali per immagini. 'file originale per la figura 1 13000_2012_709_MOESM2_ESM.tiff Autori 13000_2012_709_MOESM1_ESM.tiff autori file originale di' file originale per la figura 3 13000_2012_709_MOESM4_ESM.tiff Autori figura 2 13000_2012_709_MOESM3_ESM.tiff Autori file originale per la figura 4 file originale 13000_2012_709_MOESM5_ESM.tiff degli autori per la figura 5 'file originale per la figura 6 13000_2012_709_MOESM7_ESM.jpeg Autori 13000_2012_709_MOESM6_ESM.jpeg autori file originale per la figura 7 interessi concorrenti
non abbiamo alcun interesse in competizione per il nostro manoscritto. apporto
Autori
MK è stato responsabile per i dati raccolta e ha redatto il manoscritto. TI ha contribuito a rivedere questo manoscritto. CH, YK, FK, SH hanno contribuito alla diagnosi. HM era medico curante del paziente e ha reso contributo alla acquision dei dati clinici. Tutti gli autori hanno letto e approvato il manoscritto finale.
 Ricetta zuppa inglese al pompelmo rubino e crema pasticcera
Ricetta zuppa inglese al pompelmo rubino e crema pasticcera
 Cancro al pancreas:conosci i tuoi rischi
Cancro al pancreas:conosci i tuoi rischi
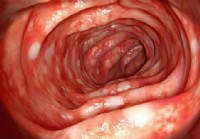 La colite ulcerosa è una malattia autoimmune?
La colite ulcerosa è una malattia autoimmune?
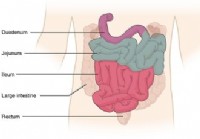 I 15 principali segnali di pericolo di cui hai bisogno per consultare un gastroenterologo
I 15 principali segnali di pericolo di cui hai bisogno per consultare un gastroenterologo
 Ocaliva approvato per malattie rare del fegato
Ocaliva approvato per malattie rare del fegato
 La tua tiroide sta distruggendo la tua funzione intestinale?
La tua tiroide sta distruggendo la tua funzione intestinale?
 Inibitori dell'aromatasi per prevenire la recidiva del cancro al seno
Gli inibitori dellaromatasi sono una classe di farmaci usati per prevenire la recidiva del cancro nelle donne in postmenopausa con carcinoma mammario positivo al recettore degli estrogeni. Questi farm
Inibitori dell'aromatasi per prevenire la recidiva del cancro al seno
Gli inibitori dellaromatasi sono una classe di farmaci usati per prevenire la recidiva del cancro nelle donne in postmenopausa con carcinoma mammario positivo al recettore degli estrogeni. Questi farm
 come evitare l'intossicazione alimentare durante le festività natalizie
La stagione delle vacanze significa che siamo spesso fuori casa più del normale. Mangiare fuori da un familiare o viaggiare per una vacanza può metterci a rischio di intossicazione alimentare, influen
come evitare l'intossicazione alimentare durante le festività natalizie
La stagione delle vacanze significa che siamo spesso fuori casa più del normale. Mangiare fuori da un familiare o viaggiare per una vacanza può metterci a rischio di intossicazione alimentare, influen
 20 ricette SIBO Super Bowl
20 ricette per feste del Super Bowl amichevoli SIBO Se sei un fan del Super Bowl, ma non sai come preparare cibo per feste SIBO friendly, ti ho coperto. Oggi condivido le mie ricette preferite per le
20 ricette SIBO Super Bowl
20 ricette per feste del Super Bowl amichevoli SIBO Se sei un fan del Super Bowl, ma non sai come preparare cibo per feste SIBO friendly, ti ho coperto. Oggi condivido le mie ricette preferite per le