Veiksmingas vaistų kūrimas turi supaprastinti į ciklą patekusių kandidatų skaičių, sumažinti proceso kainą ir laiką. Naujausi tyrimai rekomenduoja integruoti įvairius metodus kuriant mokslinių tyrimų ir plėtros (MTTP) vamzdynus, taip pat naudoti genetinius duomenis, kad būtų galima nustatyti labiausiai tikėtinus naujus vaistus. Šiuo tikslu proteomika ir transkriptomika yra viena vertingiausių sričių.
Dabar, Yra daugiau nei 150 klinikinių tyrimų, kuriuose tiriami vaistai, kurie, kaip manoma, gali būti veiksmingi didinant COVID-19 sergančių pacientų išgyvenamumą ir atsigaunant. Tai apima hidroksichlorokviną, chlorokvinas, ir baricitinibas.
Kitas būdas surinkti įrodymų apie potencialiai naudingus vaistus nuo COVID-19 yra rasti šeimininkus, kurie palengvina viruso patekimą ir infekciją, ir išnagrinėjus galimybę pakartotinai panaudoti ankstesnius narkotikų taikinius SARS-CoV, siekiant kovoti su dabartiniu virusu, sunkus ūminis kvėpavimo sindromas koronavirusas 2 (SARS-CoV-2).
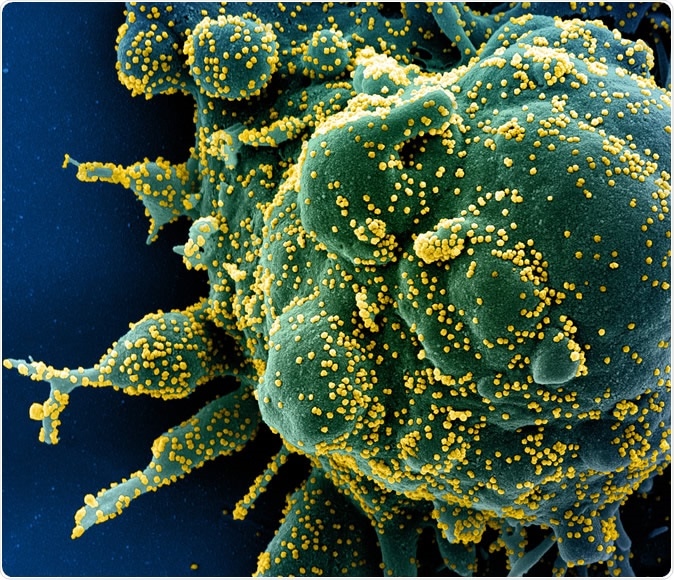 Naujas koronavirusas SARS-CoV-2 Spalvotas nuskaitymo elektroninis mikrografas apoptozinės ląstelės (žalia), labai užkrėstos SARS-COV-2 viruso dalelėmis (geltona), išskirtas iš paciento mėginio. Vaizdas užfiksuotas NIAID integruotame tyrimų centre (IRF) Fort Detricke, Merilandas. Kreditas:NIAID
Naujas koronavirusas SARS-CoV-2 Spalvotas nuskaitymo elektroninis mikrografas apoptozinės ląstelės (žalia), labai užkrėstos SARS-COV-2 viruso dalelėmis (geltona), išskirtas iš paciento mėginio. Vaizdas užfiksuotas NIAID integruotame tyrimų centre (IRF) Fort Detricke, Merilandas. Kreditas:NIAID Neseniai atliktas tyrimas nustatė daugiau nei 330 žmogaus šeimininko baltymų, būtinų virusui užkrėsti žmones. Jie sąveikauja su 26 virusiniais baltymais. Tai galėtų padėti tobulinti MTEP pirmuoju maršrutu.
Antrasis metodas buvo naudojamas keliuose tyrimuose, kurie davė 59 pelių genus, susijusius su ankstesne SARS-CoV infekcija. Tarp jų, yra 44, kurie turi atitikmenis žmogaus genome. Blokuodamas viruso ir žmogaus baltymų sąveiką, gali būti įmanoma veiksmingiau nukreipti virusinių infekcijų mechanizmus ir mažesnė atsparumo vaistams tikimybė, palyginti su tiesioginiu taikymu į virusą.
Pagrindinė šio požiūrio problema yra pavojus netyčia sukelti kitus padarinius, kurie gali pabloginti sudėtingas ligos sąlygas arba netgi jiems duoti naudos. Šiuo tyrimu siekiama įvertinti, kaip šie narkotikų taikiniai gali paveikti žmogaus kūno funkcionavimą, pagrįstas pagrindinės genetikos supratimu.
Tyrėjai naudojo protokolą vaistų prioritetų nustatymui, kuriuos jie sėkmingai sukūrė anksčiau, išbandyti 353 vaistų taikinius, kurie galbūt sąveikauja su virusu. Jie norėjo stebėti, kaip šie vaistai sukelia kitus išoriškai pastebimus infekcijos padarinius, taip pat kaip jie pasiekė numatytą ir nenumatytą poveikį sudėtingoms ligoms.
Pirmiausia jie sukūrė ligų atlasą, kuriame buvo rodomi žmogaus baltymai ir genai, dalyvaujantys viruso patekime. Tai buvo padaryta Mendelio atsitiktinės atrankos tyrimais, teikia daugiau nei 372, 000 unikalių prognozių, kaip vaistas veikia ligą. Tai buvo pagrįsta plazmos proteomika ir audiniams būdinga transkriptomika.
Kaip rezultatas, jie galėjo įvertinti, kaip šie 353 potencialūs vaistai gali veikti 49 virusinės infekcijos fenotipuose, kaip jie gali paveikti daugiau nei 500 sudėtingų ligų, ir pakeisti 72 ligos fenotipus. Šie rezultatai buvo įvertinti atsižvelgiant į vaistų tyrimų duomenis, taip pat narkotikų genomas, nustatyti geriausius vaistus, turinčius didžiausią pakartotinio naudojimo galimybę, ir mažiausiai šalutinių poveikių.
Jie sukūrė internetinę atviros prieigos platformą, kurioje yra visų bandymų rezultatai, kad kiekvienas galėtų greitai ištirti bet kurio vaisto rezultatus.
Tikslinių vaistų sąveikos atlasas apima daugiau nei 370, 000 tikslinių ligų asociacijų 11 audinių, kurie yra svarbūs COVID-19 scenarijui. Jų, 833 turėjo svarių įrodymų iš 11 audinių MR vaizdavimo. 726 iš jų taip pat parodė tvirtą kolokalizaciją, kolokalizacijos tikimybė viršija 70%. Tai buvo patikimiausi tyrimo rezultatai.
Tokių asociacijų aptikimo svarba yra galimybė atlikti analizę, kaip tam tikrų taikinių išraiška veikia konkrečias ligas, priklausomai nuo audinio. Pavyzdžiui, narkotikų taikinių poveikis Krono ligai, hipertenzija, atopiniai sutrikimai, ir būtų galima įvertinti diabetą. Bet kur nuo 11 iki 17 tikslinių genų buvo susiję su šiomis keturiomis ligomis, pagal kurį buvo tiriamas audinys.
Antra, narkotikų taikiniai buvo išanalizuoti, ar jie susiję su 49 virusinės infekcijos fenotipais. Buvo dvi stiprios asociacijos, būtent, genas NEU1 su lėtiniu hepatitu ir DPY19L1 genas su virusiniu enteritu. Taip pat buvo trys mažiau stiprios, bet įtaigios asociacijos, kaip JAK2 genas su lėtiniu hepatitu.
Trečia, tyrimas parodė 45 galimus būdus, kuriais baltymai gali paveikti ligos požymius, ir 430 panašių sąsajų su mRNR raiška. Tarp jų, buvo 95 taikiniai, susiję su 105 ligomis ar ligos išraiškomis. JAK2 genas, pavyzdžiui, yra susijęs su devyniais ligos fenotipais, nuo atopijos iki nutukimo, kuris rodo potencialiai pleiotropinius šio geno veiksmus.
Pagaliau, jie nustatė 249 asociacijas, kuriose narkotikų taikinys paveikė ligos fenotipą skirtingai, priklausomai nuo analizuojamo audinio. Tarp jų buvo 52 unikalūs genai, išreikšti 7 audiniuose, kad paveiktų 47 unikalias ligas.
Buvo 29 stipriai susiję su audiniais priklausomi vaisto taikinio poveikiai ligai daugiau nei viename audinyje, tarp kurių tik du neparodė tos pačios poveikio krypties, kai jie buvo išreikšti kraujyje, taip pat daugelyje kitų audinių.
Pavyzdžiui, DHODH genas veikia mažo tankio lipoproteinų cholesterolį (MTL). Vaistas, parduodamas nuo didelio MTL kiekio, vadinamas leflunomidu, veikia slopindamas šį geną. Leflunomidas taip pat laikomas COVID-19 gydymu.
Analizė parodė, kad šis vaistas yra išreikštas tik MTL atžvilgiu be daugelio kitų įvairių veiksmų, platų audinių spektrą nuo plaučių iki storosios žarnos.
Tyrėjai surinko 726 MR nustatytas asociacijas tarp tikslo ir ligos, naudojant klinikinių tyrimų duomenis ir tariamus įrodymus, kad jie sukėlė skirtingą fenotipinį poveikį įvairiems audiniams, sugalvoti daugiausiai narkotikų sukeliančių asociacijų. 499 iš jų buvo unikalios tikslo ir ligos poros, kiti stebimi daugiau nei viename audinyje.
Jie sukūrė keturias taškų klases, pvz., „omics“ balas, bandymo rezultatas, narkotikų vartojimo balas, ir infekcijos balas. Kiekvienas balas buvo įvertintas nuo 1 iki 100. 3 iš 4 klasių buvo du aukšti balai 2 iš 499 asociacijų, todėl jie tapo svarbiausiais vystymosi prioritetais. 77 pelnė aukštą rezultatą dviejose klasėse ir 97 vienoje. Likę 323 balai buvo visuotinai žemi, todėl laikomi mažiausio prioriteto narkotikų tikslais.
Kai kurie taikiniai apima ITGB5 geną, į kurį nukreiptas vaistas Cilengitide, kuris buvo skirtas glioblastomoms ir panašiems navikams gydyti. Jo aukšti balai ir genetinis profilis rodo, kad jis gali sumažinti aukštą kraujospūdį. Tarp 5 geriausių, visiems trūko tvirtų ryšių su tokiomis sąlygomis kaip širdies aritmija, kurie gali turėti įtakos jų naudojimui COVID-19.
Iš kitos pusės, TLR9 genas, kuris yra nukreiptas į vaistą hidroksichlorokviną, turi aukštus balus dviejose kategorijose, tačiau žemas - kitose dviejose. Kol kas nėra surinkta jokių klinikinių įrodymų, kad šio vaisto derinys su azitromicinu būtų antivirusinis ar klinikinis. Be to, šis genas gali padidinti embolinio insulto tikimybę, astma, ir tam tikros imuninės būklės.
Tyrimo metu buvo galima skatinti narkotikų tikslų nustatymą trimis būdais:išnagrinėti saugos problemas, kurios gali kilti dėl pakartotinio vaistų, skirtų gydyti COVID-19, gydymo; perspektyvių narkotikų taikinių nustatymas; ir išsiaiškinti, kaip vaisto taikinys veikia žmogaus fenomą skirtinguose audiniuose.
Naudojant šį metodą, potencialus vaistas, Baricitinibas, yra bandomas dėl veiksmingumo kovojant su COVID-19. Manoma, kad jis slopina JAK2 baltymą, ir taip sumažinti sisteminį uždegimą. Tačiau, dabartinis tyrimas parodė, kad jis taip pat gali sukelti lėtinį hepatitą. Iš tiesų, literatūroje teigiama, kad po gydymo JAK 2 inhibitoriumi ruxolitinibu hepatitas B vėl suaktyvėja.
Trys didelio potencialo vaistai iš šio tyrimo apima imunosupresinį vaistą Leflunomide, vartojamas reumatoidiniam artritui gydyti, be kitų sąlygų, ir Cilengitidas. Pirmasis turi antivirusinį aktyvumą prieš kelis virusus, ir dabartinis tyrimas taip pat rodo, kad jis turi lipidus mažinančių savybių, nors pastarasis turi antihipertenzinį poveikį, galbūt.
Pagaliau, kai kurie iš šių tikslų yra išreikšti keliuose audiniuose, kad būtų sukurtas tas pats fenotipas, tačiau kiti rodo besikeičiančią audinio išraišką.
Nors yra tam tikrų apribojimų, tyrimas suteikia statistinių genetikos tyrimų planą ir atviros prieigos platformą, pagal kurią prioritetų tvarka galima susitarti dėl vaistų tikslų prieš COVID-19. Genomo masto asociacijos tyrimai (GWAS) galėtų dar labiau pagerinti duomenų kokybę, todėl jis vis dar naudingesnis ieškant perspektyvių vaistų tikslų tarp potencialiai pakartotinai naudojamų vaistų.
medRxiv skelbia preliminarias mokslines ataskaitas, kurios nėra recenzuojamos ir todėl, neturėtų būti laikomas galutiniu, vadovauti klinikinei praktikai/su sveikata susijusiam elgesiui, arba traktuojama kaip nustatyta informacija.
 Gastroparezė
Gastroparezė yra sutrikimas, kuriam būdingi simptomai ir kai skrandis per ilgai ištuština savo turinį. Nėra jokių kliūčių ar užsikimšimų. Daugeliui žmonių, kuriems diagnozuota gastroparezė, priežas
Gastroparezė
Gastroparezė yra sutrikimas, kuriam būdingi simptomai ir kai skrandis per ilgai ištuština savo turinį. Nėra jokių kliūčių ar užsikimšimų. Daugeliui žmonių, kuriems diagnozuota gastroparezė, priežas
 Pilvo sąaugos
Kas yra pilvo sąaugos? Pilvo organų ir liaukų nuotrauka Pilvo sąaugos yra svarbios, nes jos yra dažna pilvo simptomų, ypač pilvo skausmo, priežastis ir gali sukelti žarnyno užsikimšimą ar obstrukcij
Pilvo sąaugos
Kas yra pilvo sąaugos? Pilvo organų ir liaukų nuotrauka Pilvo sąaugos yra svarbios, nes jos yra dažna pilvo simptomų, ypač pilvo skausmo, priežastis ir gali sukelti žarnyno užsikimšimą ar obstrukcij
 Saldus ir pikantiškas:aštrus brokolių padažas su paprastais krekeriais
Prieš porą savaičių Cheryl Cravino pasidalino su mumis savo SCD sėkmės istorija. Ji paminėjo, kad kuria visiškai naują SCD kulinarijos knygą. BOOM! – štai… Cheryl atsiuntė mums vieną iš anksto perž
Saldus ir pikantiškas:aštrus brokolių padažas su paprastais krekeriais
Prieš porą savaičių Cheryl Cravino pasidalino su mumis savo SCD sėkmės istorija. Ji paminėjo, kad kuria visiškai naują SCD kulinarijos knygą. BOOM! – štai… Cheryl atsiuntė mums vieną iš anksto perž