En bevis resonnement basert modell for diagnostisering av lymfeknutemetastaser i magekreft
Abstract
Bakgrunn
lymfeknutemetastase (LNM) i magekreft er en svært viktig prognostisk faktor som påvirker langsiktige overlevelse. For tiden er flere vanlige avbildningsteknikker benyttes for å evaluere lymfeknute status. Imidlertid er de ute av stand til å oppnå både høy sensitivitet og spesifisitet samtidig. For å håndtere denne komplekse saken, er en ny bevis resonnement (ER) basert modell foreslått å støtte diagnosen LNM i magekreft.
Metoder
Det er 175 påfølgende pasienter som gikk gjennom multidetector computertomografi (MDCT) fortløpende før operasjonen. Åtte indikatorer, som er serøse invasjon, tumor klassifisering, tumor forbedring mønster, tumor tykkelse, antall lymfeknuter, maksimal lymfeknute størrelse, lymfeknute stasjon og lymfeknute forsterkning benyttes for å evaluere tumoren og lymfeknute gjennom CT-bilder. Alle de ovennevnte indikatorene gjenspeiler den biologiske oppførsel av magekreft. En ER basert modell er konstruert ved å ta de ovennevnte indikatorene som input indeksen. Utgangen indeksen avgjør om LNM oppstår for pasientene, som er vedtatt av kirurgi og histopatologi. En teknikk som kalles k-fold kryssvalidering brukes til trening og testing av ny modell. Den diagnostiske evnen til LNM vurderes av mottakerdrifts karakteristiske (ROC) kurver. En radiolog klassifiserer LNM ved å vedta lymfeknute størrelse for sammenligning.
Resultater
134 av 175 tilfeller er tilfeller av LNM, og restene er ikke. Åtte indikatorene har statistisk signifikant forskjell mellom de positive og negative grupper. Følsomhet, spesifisitet og AUC for den ER basert modell er 88,41%, 77,57% og 0,813, henholdsvis. Men for radiologen evaluere LNM av maksimal lymfeknute størrelse, de tilsvarende verdiene er bare 63,4%, 75,6% og 0,757. Derfor kan den foreslåtte modellen oppnå bedre ytelse enn radiolog. Dessuten, den foreslåtte modellen utkonkurrerer også andre maskinlæringsmetoder.
Konklusjoner
Ifølge den biologiske oppførsel informasjon om magekreft, kan det ER basert modell diagnostisere LNM effektivt og preoperativt.
Nøkkelord
Magekreft Lymfe metastaser bevis resonnement Bakgrunn
Magekreft kreft~~POS=HEADCOMP har blitt en av de viktigste årsakene til kreft-relaterte dødsfall i verden [1]. Lymfeknutemetastase (LNM) er en svært viktig prognostisk faktor om langsiktig overlevelse [2]. TNM
en iscenesettelse system basert på amerikanske Joint Committee on Cancer er tatt som evalueres standard og har blitt allment akseptert [3]. Basert på denne standarden, 5-års overlevelse for pasienter i N0 scenen etter operasjonen er 86,1%, mens N1, N2 og N3 stadium pasientene kan få 58,1%, 23,3% og 5,9%, henholdsvis [4].
Tiden leger diagnostisere LNM empirisk basert på størrelsen av lymfeknuter som er avhengig av ulike avbildningsmetoder, for eksempel endoskopisk ultralyd (EUS), abdominal ultralyd, multi-slice spiral computertomografi (CT), magnetisk resonanstomografi (MRI) og positron Emission beregnet tomografi (PET). Imidlertid kan ingen av de ovennevnte tenkelig verktøy erverve lymfeknute status på en tilfredsstillende måte. Samtidig viser en systemisk vurdering som EUS, MDCT, konvensjonell MRI, og FDG-PET ikke kan brukes til å bekrefte eller utelukke tilstedeværelse av LNM pålitelig [2]. Årsaken er at store lymfeknuter kan være forårsaket av betennelse, mens små kan være forårsaket av metastasering. Derfor er enkelt lymfeknute størrelse ikke er en sterk prediktor. Faktisk har mange studier vist at LNM er relatert til tumor størrelse, patologisk lymfatisk engasjement, histologisk type og andre faktorer [5-8]. Derfor bør en fremgangsmåte som kombinerer lymfeknutestørrelse med disse faktorer tas i betraktning. Videre har noen forskere [9-11] diskutert mulighetene for diagnose av morfologiske egenskaper i rektum cancer. Ifølge disse undersøkelser, kan de morfologiske egenskaper, inkludert grensen kontur og signalintensitet av lymfeknuter delvis forbedre den diagnostiske evne til metastasering. Men disse studiene i hovedsak fokusere på MR avbildning i rektum cancer. For pasienter med magekreft i klinisk praksis, er magen CT en mer vanlig brukte avbildningsfunksjonalitet enn MR-undersøkelse. Derfor vurderer vi å bygge en modell for å diagnostisere LNM med flere indikatorer.
Ettersom det er kvalitative og kvantitative data i åtte indikatorer, en metode som kan integrere disse to typer data bør vedtas. ER tilnærmingen ble opprinnelig foreslått å håndtere flere attributt beslutningsanalyse problemer som involverer både kvalitative og kvantitative egenskaper under usikkerhet [12]. Kjernen er det ER algoritme som er utviklet på basis av beslutningen teori og Dempster-Shafer (D-S) teori bevis [13, 14]. Som ER kan integrere kvalitativ informasjon og kvantitative data rimelig, er det brukt. Et av målene i denne artikkelen er å analysere hvilke indikatorer er knyttet til den biologiske oppførsel av magekreft og konstruere en matematisk modell for å vurdere LNM preoperativt.
Metoder
Pasienter
I dette eksperimentet, 175 CT tilfeller innhentet fra Peking University Cancer Hospital & Institute (Beijing, Kina P. R.) utgjør prøvesettet. Ifølge den internasjonale behandling retningslinje av magekreft, er CT en av de mest brukte inspeksjoner [15]. Imidlertid er andre fremgangsmåter så som PET og EUS anvendt som er valgt sjekk. Disse pasientene ble gitt preoperativ kontrastoppladning abdominal i CT-undersøkelser og fikk gastrektomi mellom april 2006 og september 2008. Denne retrospektive studien ble godkjent av Institutional Review Board (IRB). De ble preoperativt undersøkt med MDCT. Merk at vi har fått informert samtykke fra alle valgte pasienter før rutinen kliniske forløpet av CT-undersøkelser. Det er 125 menn og 50 kvinner blant disse pasientene, og gjennomsnittsalderen er 59,8 år. Detaljene er vist i tabell 1.Table 1 pasientkarakteristika
Clinic patologiske funksjoner Book Verdi
Antall pasienter
175
Gjennomsnittsalder (y)
59.8 (30-85)
forholdet menn til kvinner
125: 50
Histopatologi
Adenocarcinoma
173 (98,9%)
Vel differensiert
6 (3,4%)
Moderat differensiert
91 (52%)
Dårlig differensiert
76 (43,5%)
Småcellet karsinom
2 (1,1%)
lymfeknutemetastase
Positiv
134 (76,6%)
Negativ
41 (23,4%)
indikatorer
Det er åtte indikatorer som ble hentet av to radiologer, en med tre år og en annen med åtte års erfaring i abdominal CT. De åtte indikatorene ble målt og tellet manuelt på MDCT bilder som følger: (1) serøse invasjon: aksiell og MPR-bilder blir vurdert for å fastslå den serosale invasjon samtidig. Hele jevning magesekken unormalt forbedrer lineære eller retikulære strukturer i fettlaget rundt magen indikert serøse invasjonen [16] product: (2) Tumor klassifisering. Tidlig magekreft eller Bormann klassifisering av avansert kreft i MPR-bilder er . bekreftet product: (3) Tumor ekstrautstyr mønster. Tumor ekstrautstyr er delt inn i tre mønstre på portalen fase av CT-bilder, som er slimhinneoverflaten ekstrautstyr, homogen ekstrautstyr og heterogen enhancement product: (4) tumortykkelse: Den maksimale tykkelsen på svulsten er målt ved de aksiale CT-bilder product: (5) antall lymfeknuter. antallet mage regionale lymfeknuter med størrelse større enn 3 mm i MDCT bilder i grupper telles [17]. Som lymfeknuter, som er mindre enn 3 mm, er for liten til å gjøre dem synlige, og er derfor utelatt product: (6) Maksimal lymfeknutestørrelse:. Den korte akse av de største lymfeknute detektert i CT-bilder måles product: (7) lymfeknutestasjon. den lymfeknute stasjonen med MDCT bilder basert på den japanske klassifisering av magekreft bestemmes [17] product: (8) lymfeknute ekstrautstyr.: det betyr CT demping verdien av lymfeknute, som måles ved portvene fase av CT-bildet.
i denne utredningen, er alle indikatorer målt manuelt. Antallet lymfeknuter er mengden av lymfeknuter rundt magen. Maksimal lymfeknute størrelse og lymfeknute forbedring ekstraheres fra den maksimale lymfeknute. Målet er å forutse om LNM skjer annet enn maksimal lymfeknute har LNM. Med andre ord er formålet å forutsi hvorvidt LNM forekommer for hver enkelt pasient. Det endelige resultatet for LNM diagnose fastsettes av kirurgi og histopatologi. Den patologisk resultat kan definitivt bekrefte om LNM skjer eller ikke. Vi ønsker ikke å forutse metastase for hver lymfeknute. Årsaken er at en-til-en lymfeknute korrespondanse med CT og patologi avhenger svært presis og god erfaring med radiolog. Det er vanligvis ikke konsekvent tilstrekkelig for forskjellige radiologer, som kan påvirke prediksjonsnøyaktigheten av den matematiske modellen. Derfor kan vi ikke gjøre en-til-en korrespondanse for hver lymfeknute. Detaljene er beskrevet i Tabell 2.Table 2 Beskrivelse av åtte indikatorer
Pasientdata
LNM (-)
LNM (+)
Pasient nummer
41/175
134/175
Måledata
tumortykkelse (mm)
13,3 ± 14,0
16,6 ± 28,4
Maksimal lymfeknute størrelse (mm)
6,5 ± 2,8
10,0 ± 5,5
antall lymfeknuter
7 ± 4
12 ± 8
lymfeknute ekstrautstyr
39,5 ± 58,5
62,5 ± 66,5
Count data
Tumor forbedring mønster
Pattern en
13/175
6/175
Pattern 2
26/175
118/175
Pattern 3
2/175
10/175
serøse invasjon
Ja
15/175
120/175
Ingen
26/175
14/175
Tumor klassifisering
Tidlig magekreft
9/175
1/175
Borrmann jeg
2/175
0/175
Borrmann II
3/175
9/175
Borrmann III
27/175
121/175
Borrmann IV
0/175
3/175
lymfeknuter stasjonen
Station 1
29 /175
44/175
Station 2
12/175
54/175
Station 3
0/175
36/175
verdien av måledata ble målt manuelt, og tellingen data var antall data.
eR basert modell
i denne modellen, representerer vi hvert tilfelle av en over-komplett ordliste der elementene er trenings prøvene. Dersom tilstrekkelige opplæring prøver er tilgjengelige fra hver enkelt klasse, vil det være mulig å representere prøven.
Anta at opplærings prøvene er betegnet med X = {X
1
, X
2
, ..., X
p
}
∈ R
MXN
, der n
er antall opplæring prøver, og m
er antall indikatorer. y
∈ {1,2, ..., p} er
er etiketten og p
klassen indeksen. T = [T
1
, T
2
..., T
m
]
T
betegner en testprøve. Den over komplett ordliste A
betegnes som følger: A
=
A
1
, etter 1
, etter A
1
, etter 2
, etter ...
, etter A
1
, etter n
A
2
, etter 1
, etter A
2
, etter 2
, etter ...
, etter A
2
, etter n
...
, etter ...
, etter ...
, etter ...
A
m
, etter 1
, etter A
m
, etter 2
, etter ...
, etter A
m
, etter n product: (1) Her A
består av opplæring prøver og En
m, n
representerer hver indikator i trening prøver. Ifølge grensene for ER, bør kolonnene i A Hotell og T
normaliseres først. Så hver indikator T i
i prøven er representert ved A Hotell og tilsvarende koeffisientene w
i
, jeg
= 1,2, ..., m
. Deretter bruker vi ER analytiske algoritme [13] som følger: T
j
=
μ
×
Π
k
=
1
n
ω
k
A
j
, etter k
+
1
-
ω
k
Σ
i
=
1
m
A
i
, etter k
-
Π
k
=
1
n
1
-
ω
k
Σ
i
=
1
m
A
i
, etter k
1
-
μ
×
Π
k
=
1
n
1
-
ω
k plakater (2) μ
= product: [
Σ
j
=
1
m
Π
k
=
1
n
ω
k
A
j
, etter k
+
1
-
ω
k
Σ
i
=
1
m
A
i
,
k
-
m
-
1
Π
k
=
1
n
1
-
ω
k
Σ
i
=
1
m
A
i
, etter k
]
-
1 product: (3) Alle indikatorene i T
kan representeres ved A
og w
i
, jeg
= 1,2, ..., m
bruker ER tilnærming. Anta at ER
representerer ER tilnærming. Derfor er T
representert som følger: T
=
ER
A
, etter ω
(4) hvor ω∈R
n
er koeffisientvektor. Det er imidlertid ikke mulig å garantere en optimal løsning, og i stedet vi erstatte den med tilnærmet løsning gitt i ligning (5): T
≈
ER
A
, etter ω product: (5) Som den nye saken kan være tilstrekkelig representert ved opplærings prøver fra samme klasse, får vi prediksjon av ω. model
0.948
0.020
0.000
0.908
0.988
ANN
0.798
0.043
0.000
0.713
0.882
SVM Alle forfattere lese og godkjent den endelige manuskriptet.
 Hva stopper diaré raskt?
Diaré eller løs avføring kan være forårsaket av en infeksjon, parasitter, visse medisiner, tarmsykdom, matintoleranse, hormon lidelser, tarmkreft eller laktoseintoleranse. Du kan stoppe diaré raskt me
Hva stopper diaré raskt?
Diaré eller løs avføring kan være forårsaket av en infeksjon, parasitter, visse medisiner, tarmsykdom, matintoleranse, hormon lidelser, tarmkreft eller laktoseintoleranse. Du kan stoppe diaré raskt me
 Gjør dagligvarebutikkfeil deg syk?
Å spille poker virker enkelt ... til du faktisk begynner å spille. Bare å forstå reglene er vanskelig nok. Da jeg først begynte å spille, pleide jeg å gi pengene mine til alle som en slags veldedighe
Gjør dagligvarebutikkfeil deg syk?
Å spille poker virker enkelt ... til du faktisk begynner å spille. Bare å forstå reglene er vanskelig nok. Da jeg først begynte å spille, pleide jeg å gi pengene mine til alle som en slags veldedighe
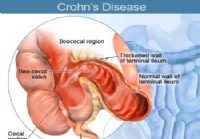 Crohns sykdom hos barn og tenåringer
Hva er Crohns sykdom? Bilder av detaljene i områdene som er berørt av Crohns sykdom. Crohns sykdom er en alvorlig, kronisk sykdom som påvirker fordøyelsessystemet. Kronisk betyr at sykdommen er lang
Crohns sykdom hos barn og tenåringer
Hva er Crohns sykdom? Bilder av detaljene i områdene som er berørt av Crohns sykdom. Crohns sykdom er en alvorlig, kronisk sykdom som påvirker fordøyelsessystemet. Kronisk betyr at sykdommen er lang