Гистологическое полный ответ на комбинированном доцетаксел /цисплатин /фторурацил неоадъювантной химиотерапии стадии Т4 аденокарциномы желудка
Аннотация
местного поздних стадий рака желудка имеет очень плохой прогноз. Когда рак желудка T4 вторглось в окружающие ткани и органы, целебный резекция маловероятно. Мы представляем здесь случай 63-летней женщины с Т4 неоперабельной аденокарциномы желудка. Она перенесла две 3-недельные циклы доцетаксел /цисплатин /фторурацил химиотерапии, после радикальной резекции желудка. Каждый цикл состоял из 75 мг /м
2 доцетаксел и 75 мг /м 2 цисплатин в 1 день и 200 мг /м 2 лейковорин и 500 мг /м 2 фторурацил в дни 1 через 5. пациент был показан полный гистологический ответ. Наши результаты указывают на то, что доцетаксел /цисплатин /фторурацил неоадъювантной химиотерапии является перспективным методом лечения поздних стадий рака желудка.
Ключевые слова
рак желудка неоадъювантной химиотерапии доцетакселом цисплатин фторурацил фон
рак желудка является одним из наиболее распространенных злокачественных опухолей и ведущей причиной смертности от рака во всем мире, по оценкам 900000 новых случаев заболевания и более 700000 смертей только в 2006 году [1, 2]. Радикальная резекция с расширенной лимфаденэктомии в настоящее время признается в качестве единственного потенциально лечебной терапии. Пациенты, которые представляют со стадией III или IV болезни, однако, не имеют право на получение лечебной резекции и, таким образом, имеют особенно плохой прогноз. Кроме того, местный рецидив или отдаленные метастазы могут развиваться в короткий промежуток времени, даже после того, как лечебной резекции [3]. За последнее десятилетие все большее число докладов показали, что неоадъювантная химиотерапия может быть полезным для пациентов с поздними стадиями T- и N-категории повреждений, возможно, в результате понижения стадии опухолей, улучшение скорости первичной резекции опухоли с отрицательным хирургическим краем, а в начале лечение микрометастатической болезни. Мы сообщаем здесь случай пациента с Т4 неоперабельной аденокарциномы желудка который показал полный гистологический ответ после доцетаксела на основе неоадъювантной химиотерапии.
Клинический случай
63-летняя женщина обратилась в нашу местную больницу из-за эпигастрии боль. Эндоскопическая экспертиза показала 45 × 52 мм нерегулярную повреждение в малой кривизне полости желудка. Биопсия показано недифференцированные аденокарциномы (рис 1А). Абдоминальная компьютерная томография (КТ) показала утолщение стенки желудка. Увеличенные метастатические лимфатические узлы не могут быть найдены. Облитерация жировых плоскостей между желудочной опухоли и соседних органов указывают на опухоль Т4 [4, 5] (рис 2А). Диагноз поздних стадиях рака желудка, T4n <суб> XM <суб> 0, Stage IIIA или Iς, была изготовлена в соответствии с нынешней системой ступенчатого Международный союз против рака TNM. Из-за трудности выполнения радикальной операции, рекомендуется, чтобы пациент пройти химиотерапию. Рисунок 1 Опухоль и гистологические особенности. (A) Биопсия указано недифференцированные аденокарциномы. (Б) Микроскопическое исследование вырезанных образца, не обнаруживала аденокарциномы желудка клеток и освещение поражения с регенеративным слизистой оболочки. Сальник дегенерация была замечена в слизистой оболочке. формирование фиброза и лимфатических фолликул наблюдались у стенки желудка. (C) Нет желудка остатки аденокарциномы не были обнаружены даже при иммуногистохимического окрашивания для CK20.
Рисунок 2 Компьютерная томография стенки желудка. (A) Брюшной компьютерная томография (КТ) показало утолщение стенки желудка. Облитерация жировых плоскостей между желудочной опухоли и соседних органов указывают на опухоль T4. (B) КТ после двух курсов химиотерапии показали значительное снижение первичного поражения и осветления жира плоскостей.
Неоадъювантной химиотерапии вводили с помощью доцетаксел, цисплатин, фторурацил и лейковорин. На 1-й день, 75 мг /м 2 доцетаксел и 75 мг /м 2 цисплатин вводили внутривенно. В дни с 1 по последний день цикла 500 мг /м 2 фторурацил и 200 мг /м 2 лейковорина назначали. Один цикл длился 3 недели, и были проведены два цикла. Другой КТ была проведена через 2 недели. Результаты показали резкое снижение первичного очага и уточнения жировых плоскостей между желудочной опухоли и соседних органов (рис 2В). Увеличенные метастатических лимфатических узлов и асцит не были найдены.
Хирургии была проведена через 4 недели после неоадъювантной химиотерапии. Нет явных перитонеальные метастазы не были найдены, и опухоль желудка не было очевидным. Хирургическая процедура была дистальной частичная резекция с запасом 5 см безопасности. Лимфатический узел рассечение D2 в соответствии с японским научно-исследовательского общества рака желудка (JRSGC) руководящих принципов [6] была выполнена, и 21 лимфатические узлы были расчленены. Метод Бильрот II был использован для реконструкции пищеварительного тракта.
Макроскопическое исследование показало, нерегулярный поражения, простирающееся на собственной мышцы, размером 10 × 12 мм, в меньшей кривизны желудка вырезанных образца. Микроскопическое исследование показало, что нет аденокарциномы желудка клетки не осталось, и поражение было покрыто регенеративной слизистой оболочки. Сальник дегенерация была замечена в слизистой оболочке. формирование фиброза и лимфатических фолликул наблюдались с подслизистой к subserosa (рис 1B). Нет желудка остатки аденокарциномы не были обнаружены даже при иммуногистохимического окрашивания для CK20 (рис 1C). Нет метастазов в лимфатических узлах был обнаружен на патологической экспертизы. Никакой дополнительной химиотерапии не проводилась после операции. Последующая деятельность по итогам экспертиза проводилась каждые 6 месяцев в общей сложности на 8 лет. Пациент оставался здоровым, без рецидива опухоли или метастазов. Она считалась имели полный гистологический ответ на лечение с неоадъювантной химиотерапии.
Обсуждение
5-летней выживаемости для всех желудочных больных раком, оперированных составляет всего 20% до 30%. Местные рецидивы Сообщалось, что основной причиной неэффективности лечения [7]. Когда рак Т4 желудка вторглось в окружающие ткани и органы, лечебные резекция достигается только 33,3% случаев, хотя пациенты, которые проходят резекция опухоли (либо лечебное или noncurative) имеют значительно лучшую выживаемость, чем те, кто не претерпевают резекцию [8 ].
в течение последних 20 лет, предоперационной химиотерапии был использован в попытке уменьшить желудочную частоту рецидивов опухоли и увеличить выживаемость. Две основные цели неоадъювантной химиотерапии понижение стадии первичной опухоли, чтобы увеличить шансы успешного полной резекции и уничтожение оккультные лимфатических узлов и отдаленных метастазов. У пациентов с клиническим ответом на химиотерапию имеют значительно лучшие прогнозы, чем те, без клинического ответа, особенно при полной (R 0) резекция выполняется [9-11].
Несколько режимов химиотерапии были разработаны для лечения поздних стадий рака желудка. Превосходные результаты были достигнуты при использовании эпирубицин и цисплатин непрерывной инфузии фторурацила (ECF). Фаза III рандомизированное исследование показало, что, по сравнению с фторурацилом /доксорубицин /метотрексат, ECF показал лучшую общую скорость отклика (Орр) (45% против 21%), а больше медиана времени до прогрессирования (TTP) (7,4 против 3,4 месяцев), и более общей выживаемости (ОВ) (8,9 против 5,7 месяцев) [12]. Таким образом, исследователи предложил ECF в качестве стандартной терапии [12, 13]. Совсем недавно, несколько новых агентов появились, в том числе таксанов, иринотекана и оксалиплатина. Доцетаксел был первым агентом пытался при поздних стадиях рака желудка и показали более высокую активность, чем альтернативные варианты. Используется в качестве единственного агента, сообщается доцетаксел иметь уровень ответа от 17% до 29% [14-16]. В сочетании с другими агентами, паклитаксел также показал обещание [17, 18]. Комбинированные схемы лечения, в том числе паклитаксел /5-фторурацил (5-ФУ) /цисплатин, привело к частоте ответа достигает 53%, медиана выживаемости от 7 до 14 месяцев [19-23]. Режим доцетаксел /цисплатин /фторурацил (ДДП) показал эффективность, сравнимую с другими режимами цисплатина или антрациклиновый комбинаций. В Исследовательской группе V325, Ван Cutsem и др
. сообщил, что добавление доцетаксела к цисплатином и фторурацилом (CF) значительно улучшило ТТП, выживание и скорость реакции в больных раком желудка [22]. В рандомизированном испытании II фазы швейцарской группы по клиническим исследованиям рака, Рот и др
. сравнили результат терапии DCF с теми доцетаксела и цисплатина (DC) и ECF. Они сообщается об ЧОО 25,0% (от 13 до 41%) для ECF, 18,5% (от 9 до 34%) при постоянном токе, и 36,6% (от 23 до 53%) для DCF (п = 119). Медиана общей выживаемости составили 8,3, 11,0 и 10,4 мес для ECF, округ Колумбия, и DCF, соответственно [23].
Hematotoxicity был главным побочным эффектом в доцетаксела испытаний распространенного рака желудка. Рот и др
. сообщили о высокой частоте фебрильной нейтропении, связанной с режимом DCF, которое произошло у 41% больных, по сравнению с 18% и 21% пациентов в ECF и оружия постоянного тока, соответственно [23]. После того, как доза доцетаксела была снижена, частота фебрильной нейтропенией снизилась. По данным литературы, 75 мг /м 2 доцетаксел в сочетании с КФ хорошо переносимым, и эта доза доцетаксела чаще предлагается для лечения рака желудка [24-26]. Кроме того, более высокая частота фебрильной нейтропении не переводили на более высокий уровень смертности. Эта токсичность была приемлемой, и нейтропения легко управляться с гранулоцитарный колониестимулирующий фактор (G-CSF). Интересно отметить, что более высокая частота токсичности как представляется, не влияют на качество жизни и клинические преимущества, которые были значительно выше, с режимом DCF, возможно, из-за более высокой противоопухолевой активности DCF [22].
Гистологическое регрессии опухоли сорт объективная мера воздействия неоадъювантной химиотерапии. Общий показатель полного клинического ответа на DCF для продвинутой опухоли желудка составляет от 2 до 4,9% [22, 23]. Скорость полного патологического ответа, однако, было неизвестно.
Снижение Быстрое опухоли перед тем хирургическое лечение является важным показателем успеха неоадъювантной химиотерапии. Рот и др
. Сообщается, что режим DCF приводит к более коротким медиана времени до ответа на лечение (TTR), чем в режиме ECF (медиана TTR 1,6 против 3,0 месяцев) [23]. Пациент с желудочным опухолью Т4, описанной здесь был показан полный патологический ответ на DCF химиотерапии в 10 недель. Эти результаты указывают на то, что DCF неоадъювантной химиотерапии является перспективным методом лечения поздних стадий рака желудка
Выводы
В заключение мы наблюдали случай местно-распространенным раком желудка карциномы, которые демонстрировали полный гистологический ответ после неоадъювантной химиотерапии. пациент выжил в течение более 5 лет. По нашему опыту, DCF неоадъювантной химиотерапии является перспективным методом лечения поздних стадий рака желудка.
Согласие
Письменное информированное согласие было получено от пациента к публикации этого доклада и любых сопроводительных изображений.
Сокращения
CF:
цисплатин /фторурацил
КТ:
компьютерной томографии
DC:
доцетаксел /цисплатин
DCF:
доцетаксел /цисплатин /фторурацил
ECF: эпирубицин
/цисплатин /фторурацил
ЧОО:
общую скорость отклика
G-CSF:
гранулоцитарный колониестимулирующий фактор
TTP:
время до прогрессирования
TTR:.
медиана времени до ответа на лечение
декларациях
Авторы "оригинал, представленный файлы для изображений изображения Ниже приведены ссылки на оригинальные файлы представленных авторов для изображений. 'Исходный файл для Рисунок 1 12957_2013_1639_MOESM2_ESM.tif Авторского 12957_2013_1639_MOESM1_ESM.tif авторов исходного файла для "исходного файла для фигурного 3 12957_2013_1639_MOESM4_ESM.tiff Авторского Рисунок 2 12957_2013_1639_MOESM3_ESM.tiff Авторского исходного файла для фигурного 4 исходного файла 12957_2013_1639_MOESM5_ESM.tiff Авторского на рисунке 5 Конкурирующие интересы
Ming Gao Го и другие соавторы не имеют конкурирующий интерес. вклады
Авторского
МГГ, QZ, JZD, З.Ы. участие в лечении пациента. Все авторы читали и одобрили окончательный вариант рукописи.
 Какие фрукты вредны для почек?
Людям, страдающим заболеваниями почек, следует избегать продуктов, богатых калием, таких как бананы, авокадо, абрикосы и т. д. Большинство фруктов не вредны для людей со здоровыми почками. Когда по
Какие фрукты вредны для почек?
Людям, страдающим заболеваниями почек, следует избегать продуктов, богатых калием, таких как бананы, авокадо, абрикосы и т. д. Большинство фруктов не вредны для людей со здоровыми почками. Когда по
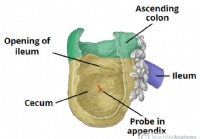 Приложение
1 Анатомическое строение и взаимоотношения 2 Сосудисто-нервное кровоснабжение 3 Лимфодренаж 4 Клиническая значимость:воспаление аппендикса приложение представляет собой узкую трубку со слепым концом
Приложение
1 Анатомическое строение и взаимоотношения 2 Сосудисто-нервное кровоснабжение 3 Лимфодренаж 4 Клиническая значимость:воспаление аппендикса приложение представляет собой узкую трубку со слепым концом
 Поиск диеты, благоприятной для целиакии
Несмотря на то, что безглютеновая диета — это отличная тенденция в питании, которой сейчас следуют некоторые, для других соблюдение безглютеновой диеты необходимо для их здоровья. Это связано с тем, ч
Поиск диеты, благоприятной для целиакии
Несмотря на то, что безглютеновая диета — это отличная тенденция в питании, которой сейчас следуют некоторые, для других соблюдение безглютеновой диеты необходимо для их здоровья. Это связано с тем, ч