Most, a Cincinnati Children májszakértői által vezetett tanulmány új részleteket tár fel a betegségről, amelyek a kezelés teljesen új megközelítésére utalnak. A felfedezések, augusztus 15 -én publikálták online 2021, a folyóiratban Hepatológia , lehetővé tették, mert a csapatnak sikerült funkcionális epe organoidokat növeszteni a beteg szövetekből.
"Ezeket az organoidokat a sejtek genetikai manipulációja nélkül fejlesztettük ki, májbiopsziából származó sejtekkel, - mondja Pranav Shivakumar, PhD, és Jorge Bezerra, Orvos, a gasztroenterológiai osztályról, Hepatology and Nutrition at Cincinnati Gyermekek és a tanulmány vezető szerzői. "Ez azért fontos, mert kisgyermekektől tanulmányozhattuk a működő emberi szöveteket, ahelyett, hogy támaszkodnánk rögzített sejtmintákra vagy egérmodellekre, amelyek nem teljesen utánozzák az emberi betegséget. "
Összehasonlítva a beteg organoidokat másokkal, amelyek egészséges májmintákból nőttek ki, a kutatók számos szerkezeti hibát észleltek a sejtekben, amelyek apró csöveket képeznek, amelyek epesavakat szállítanak el a májból; ez az emésztési folyamat kritikus aspektusa.
Az egészséges epeorganoidok szorosan kötött sejtekből álló gömböket képeznek, amelyek olyan formát öltenek, mint a cukorka kukorica. Ez az alak segíti a sejteket abban, hogy eligazodjanak a belső és külső felületek kifejlesztésében, amelyek különböző funkciókkal rendelkeznek. A sejtek felső vége befelé mutat, mindegyik sejt hajszálú csillót húzva a gömb közepébe. A sejtek szélesebb alsó végei védő külső réteget képeznek.
Azonban, a beteg organoidok sejtjei rendezetlen béléseket képeztek. Néhány sejtet úgy fordítottak, hogy csillóik kifelé mutassanak. Közben, a cellák közötti szoros szivárgásmentes kötések helyett, a bélés szabálytalan réseket mutatott a sejtek között, amelyek lehetővé tették a külső anyagok bejutását.
Ezeknek a hámsejteknek a bélése képezi az epevezetéket, amely lehetővé teszi az epe normális áramlását a májból a bélbe, és megakadályozza, hogy az epevezeték falait károsítsák az általuk szállított epesavak. Ha a bélés nem feszes, lehetővé teszi az epesavak és más szubsztrátok szivárgását a csatorna falába, ami irritálja a sejteket, és gyulladáshoz vezet, amely elpusztítja az eperendszert. Amikor ez történik, a májban fibrózis alakul ki, és gyermekeknél májelégtelenségig terjedhet. "
Jorge Bezerra, Orvos, Gasztroenterológiai osztály, Hepatológia és táplálkozás a Cincinnati Gyermekeknél
A permeabilitási probléma kimutatása önmagában is áttörés volt, csak a működő organoidok tanulmányozása tette lehetővé. Emberben, ez a meghibásodás a magzati fejlődés korai szakaszában kezdődik, jóval azelőtt, hogy szövetmintákat lehetett volna gyűjteni a rossz csatornaképződés kimutatására.
Az organoidok tanulmányozása, a kutatók sejtjelek közötti különbségeket észleltek a beteg és egészséges organoidok között, amelyek az epés organoidképződés rendellenességének okozói lehetnek. Ezek a jelek a fibroblaszt növekedési faktor-2-hez (FGF2) és az epidermális növekedési faktorhoz (EGF) kapcsolódtak.
"Amikor újra aktiváltuk ezeket az utakat, láttuk, hogy a beteg organoidokból sokkal több sejt fejlődött helyesen. A kezelt organoidok nem voltak tökéletesek, de sokkal közelebb voltak a normálhoz, ami arra utal, hogy képesek lehetnek a megfelelő májműködés támogatására, - mondja Shivakumar.
EGF és FGF2 kezelés esetén az epeúti atresia organoidok jobb polaritást mutattak, csökkent permeabilitás és kifejezett biomarkerek, amelyek a normál közel működését jelzik, - számol be a tanulmány.
A kutatócsoport, amely elérte ezt a sikert, az első szerző, Surya Amarachintha, PhD, és társszerzője, Pranavkumar Shivakumar, MPharm, PhD, mind a Cincinnati Children -től. A csapat együttműködött a Sun Yat-Sen Egyetem első kapcsolt kórházának és harmadik kapcsolt kórházának kollégáival is, Kanton, Kína.
További lépésekre van szükség ahhoz, hogy ezt a laboratóriumi edényfelfedezést kezelésre vigyük, - mondja Bezerra.
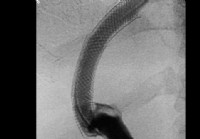 Hogyan működik a transzjuguláris intrahepatikus portoszisztémás shunt (TIPS)?
Hogyan működik a transzjuguláris intrahepatikus portoszisztémás shunt (TIPS)?
 A PENTAX Medical 125 dollárt emel,
A PENTAX Medical 125 dollárt emel,
 Valóban kockázatosak a gabonamentes diéták?
Valóban kockázatosak a gabonamentes diéták?
 Epesav felszívódási zavar tünetei, diagnózisa és kezelési útmutatója
Epesav felszívódási zavar tünetei, diagnózisa és kezelési útmutatója
 Személyre szabott táplálkozás és a bélmikrobióta
Személyre szabott táplálkozás és a bélmikrobióta
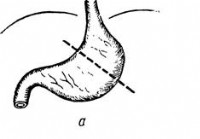 A hasi szervek csavarodása – Akut has diagnosztizálása
A hasi szervek csavarodása – Akut has diagnosztizálása
 Az idősebb népességű országokban magasabb a SARS-CoV-2 fertőzés és a halálozások száma,
mondja tanulmány Több mint egy éve a 2019-es koronavírus-járvány (COVID-19) világjárványa, a súlyos akut légzőszervi szindróma 2-es koronavírus (SARS-CoV-2) okozta, világossá vált a klinikai szindróma
Az idősebb népességű országokban magasabb a SARS-CoV-2 fertőzés és a halálozások száma,
mondja tanulmány Több mint egy éve a 2019-es koronavírus-járvány (COVID-19) világjárványa, a súlyos akut légzőszervi szindróma 2-es koronavírus (SARS-CoV-2) okozta, világossá vált a klinikai szindróma
 Colitis:tünetek, típusok, étrend és kezelés
Egy nő vastagbélgyulladással járó hasi fájdalomtól szenved. A vastagbélgyulladásnak számos oka van, beleértve a fertőzést, a gyulladásos bélbetegséget (a Crohn-betegség és a fekélyes vastagbélgyulladá
Colitis:tünetek, típusok, étrend és kezelés
Egy nő vastagbélgyulladással járó hasi fájdalomtól szenved. A vastagbélgyulladásnak számos oka van, beleértve a fertőzést, a gyulladásos bélbetegséget (a Crohn-betegség és a fekélyes vastagbélgyulladá
 A DNS -metakódolás javíthatja az emberi táplálkozás elemzését
Egy új tanulmány kimutatta, hogy a DNS metabarkódolása hatékony új eszközként szolgál az emberek növényi bevitelének nyomon követésére, amely segíthet a kutatóknak abban, hogy jobban megértsék, mit es
A DNS -metakódolás javíthatja az emberi táplálkozás elemzését
Egy új tanulmány kimutatta, hogy a DNS metabarkódolása hatékony új eszközként szolgál az emberek növényi bevitelének nyomon követésére, amely segíthet a kutatóknak abban, hogy jobban megértsék, mit es