Tento výskum, vedený University of Alabama v Birminghame, výskumník Charles O. Elson, M.D., profesor medicíny, zameraný na podskupinu T buniek známych ako T pamäť, alebo Tm bunky. Vedci z UAB použili ošetrenie trojitým úderom na odstránenie Tm buniek a zvýšenie počtu T regulačných, alebo Treg, bunky. Oba tieto výsledky boli schopné zabrániť kolitíde v myšacom modeli prenosu T buniek, a mali podobné inhibičné účinky na imunitne reaktívne CD4-pozitívne T bunky izolované zo vzoriek krvi pacienta s Crohnovou chorobou.
Tieto výsledky, Elson hovorí, podporovať potenciálnu imunoterapiu na prevenciu alebo zmiernenie zápalového ochorenia čriev.
Na pochopenie toho, ako a prečo liečba trojitým úderom, je potrebné určité znalosti, o ktorom bol denník informovaný Vedecká imunológia , Tvorba.
Zápalové ochorenia čriev sú dôsledkom nadmernej aktivácie imunitnej reakcie proti črevným mikróbom u geneticky citlivých hostiteľov. Jedným špecifickým mikrobiálnym antigénom, ktorý spôsobuje túto nadmernú reakciu krátkodobých T efektorových buniek, je bičík, proteínová podjednotka bakteriálnych bičíkov, dlhé chvostovité štruktúry, ktoré sa krútia ako vrtuľa, aby boli bakteriálne pohyblivé.
Jedna skupina imuno-dominantných bičíkov je z čeľade Lachnospiraceae, vrátane CBir1; viac ako polovica pacientov s Crohnovou chorobou má zvýšenú sérologickú reaktivitu na CBir1 a súvisiace bičíky.
Na rozdiel od krátkodobých T efektorových buniek, ktoré v boji proti infekciám pôsobia ako vojaci, Bunky pamäte T slúžia ako strážcovia, ktorí si pamätajú predchádzajúce stretnutie s bičíkmi. Majú dlhú životnosť a sú v kľude, s nízkou úrovňou metabolizmu. Ak sa reaktivujú novým stretnutím s bičíkovými antigénmi, prechádzajú hlbokým metabolickým prechodom a rýchlo expandujú do veľkého počtu patogénnych T efektorových buniek.
Tento metabolický spínač je riadený signálnym proteínom, mTOR, umiestnené v bunke Tm.
Preto aktivácia mTOR je potrebná na expanziu T buniek, čo z neho robí nevyhnutný metabolický kontrolný bod na vytváranie aktivovaných Tm buniek. Je to tiež kontrolný bod pre T naivné bunky, ktoré sa prvýkrát stretávajú s bičíkom.
Takže, Elson a kolegovia predpokladali, že aktivácia CD4-pozitívnych Tm alebo T naivných buniek antigénmi bičíkov, pričom sa súčasne vypne metabolický kontrolný bod pomocou inhibície mTOR, by malo za následok smrť alebo absenciu normálnej imunitnej reakcie na antigén, čo sa nazýva anergia. Tieto efekty pozostávajú z dvoch častí trojitého úderu, pričom tretia je indukcia Treg buniek.
Aktivácia bola vyvolaná syntetickým peptidom, ktorý mal viacnásobné opakovanie jedného epitopu CBir1. Takýto peptid môže selektívne stimulovať pamäťové bunky bez aktivácie vrodenej imunitnej reakcie.
Ak chcete vypnúť metabolický kontrolný bod, vedci UAB použili dve existujúce drogy, rapamycín a metformín. Rapamycín priamo inhibuje mTOR, a metformín zvyšuje inhibíciu aktiváciou kinázy nazývanej AMPK, ktorá negatívne reguluje aktivitu mTOR.
Elson nazýva túto liečebnú bunkovú aktiváciu so súčasnou inhibíciou metabolického kontrolného bodu, alebo CAMCI.
Parenterálna aplikácia CAMCI u myší úspešne zacielila na bunky CD4 pozitívne na mikrobiotické bičíkovce, čo vedie k významnej antigénne špecifickej smrti CD4-pozitívnych T buniek zhoršený vývoj a zhoršená reaktivácia reakcií pamäte pozitívnych na CD4, a podstatná indukcia CD4-pozitívnej reakcie Treg buniek. V myšom modeli predchádzala kolitíde a mala podobné inhibičné účinky na T-bunky špecifické pre mikrobiota-bičíkové CD4 pozitívne izolované od pacientov s Crohnovou chorobou.
Na potenciálnu budúcu liečbu pacientov s Crohnovou chorobou, iba zacielenie na jeden bičík pravdepodobne nebude mať veľký účinok, Hovorí Elson. „Namiesto toho, očakávame budúce použitie syntetického multi-epitopového peptidu obsahujúceho viacero CD4-pozitívnych T-bunkových bičíkových epitopov na zacielenie mnohých CD4-pozitívnych Tm buniek reagujúcich na mikrobiota-bičíkoviny, „Povedal Elson.“ V závislosti od sérologickej alebo CD4-pozitívnej reakcie T buniek na určité antigény mikrobioty, tento prístup CAMCI by mohol byť prispôsobený jednotlivcom s rôznymi kombináciami epitopov ako personalizovaná imunoterapia. “
Elson hovorí, že tento prístup CAMCI predstavuje ako prerušovanú pulznú terapiu na udržanie remisie u pacientov s Crohnovou chorobou.
A keďže epitopy autoantigénu sú lepšie študované v budúcnosti, tento prístup by sa mohol rozšíriť na liečbu iných zápalových alebo autoimunitných chorôb, ako je diabetes typu 1 alebo roztrúsená skleróza. “
Charles O. Elson, M.D., Výskumník UAB
Vo vyspelých krajinách, traja z každého 1, 000 ľudí má zápalové ochorenie čriev. Jeho hlavné formy, Crohnova choroba a ulcerózna kolitída majú značnú chorobnosť a vysoké náklady na zdravotnú starostlivosť, a žiadna súčasná terapia nemení prirodzenú históriu týchto chorôb.
 Ako hovoríte lekárovi, ktorý lieči tráviace problémy?
Ako hovoríte lekárovi, ktorý lieči tráviace problémy?
 Obmedzenie týchto druhov potravín vám môže pomôcť výrazne znížiť výskyt refluxu kyselín
Obmedzenie týchto druhov potravín vám môže pomôcť výrazne znížiť výskyt refluxu kyselín
 Kakanie 101:4 znaky, že vaše hovienka sú zdravé
Kakanie 101:4 znaky, že vaše hovienka sú zdravé
 Čo by ste mali vedieť o Keytrude (Pembrolizumab)
Čo by ste mali vedieť o Keytrude (Pembrolizumab)
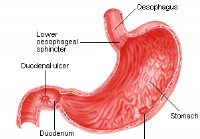 Peptické vredy
Peptické vredy
 U.S. Počet úmrtí na infekčné choroby sa nezmenil:Štúdia
U.S. Počet úmrtí na infekčné choroby sa nezmenil:Štúdia
 Aké sú najlepšie potraviny na jedenie, keď máte žalúdočný vred?
Čo je to žalúdočný vred? Žalúdočné vredy sú otvorené vredy, ktoré vznikajú na sliznici žalúdka, keď kyseliny zo strávenej potravy poškodia žalúdočnú stenu. Potraviny, ovocie a zelenina bohaté na vl
Aké sú najlepšie potraviny na jedenie, keď máte žalúdočný vred?
Čo je to žalúdočný vred? Žalúdočné vredy sú otvorené vredy, ktoré vznikajú na sliznici žalúdka, keď kyseliny zo strávenej potravy poškodia žalúdočnú stenu. Potraviny, ovocie a zelenina bohaté na vl
 Inhibítory Cox-2
Prezentácia obrázkov reumatoidnej artritídy Zúčastnite sa kvízu RA Prezentácia cvičení na zníženie bolesti pri RA Čo sú inhibítory Cox-2? Pre aké stavy sa predpisujú inhibítory Cox-2? Ktoré inhibíto
Inhibítory Cox-2
Prezentácia obrázkov reumatoidnej artritídy Zúčastnite sa kvízu RA Prezentácia cvičení na zníženie bolesti pri RA Čo sú inhibítory Cox-2? Pre aké stavy sa predpisujú inhibítory Cox-2? Ktoré inhibíto
 Chodím na pohotovosť pre IBS
Ľudia, ktorí majú IBS, sa, žiaľ, často ocitnú zle, keď idú na pohotovosť pre extrémne symptómy. Zdá sa, že celkové problémy vo vzťahu medzi lekárom a pacientom, pokiaľ ide o IBS, v dôsledku nedostatku
Chodím na pohotovosť pre IBS
Ľudia, ktorí majú IBS, sa, žiaľ, často ocitnú zle, keď idú na pohotovosť pre extrémne symptómy. Zdá sa, že celkové problémy vo vzťahu medzi lekárom a pacientom, pokiaľ ide o IBS, v dôsledku nedostatku