En plus des mutations du gène BRCA dont on parle souvent, il existe un nombre important d'autres mutations génétiques héréditaires qui augmentent le risque de développer un cancer du sein. En fait, on pense que les mutations dans plus de 100 gènes contribuent au risque, et le nombre de mutations génétiques non BRCA qui augmentent le risque de cancer du sein devrait augmenter à mesure que nos connaissances sur la génétique du cancer augmentent.
En plus des mutations des gènes BRCA1 et BRCA2, certaines d'entre elles incluent des mutations dans ATM, PALB2, PTEN, CDH1, CHEK2, TP53, STK11, PMS2, etc. Examinons l'importance de ces mutations non-BRCA1/BRCA2 dans le cancer du sein familial, et certaines des caractéristiques de celles que l'on trouve le plus souvent.
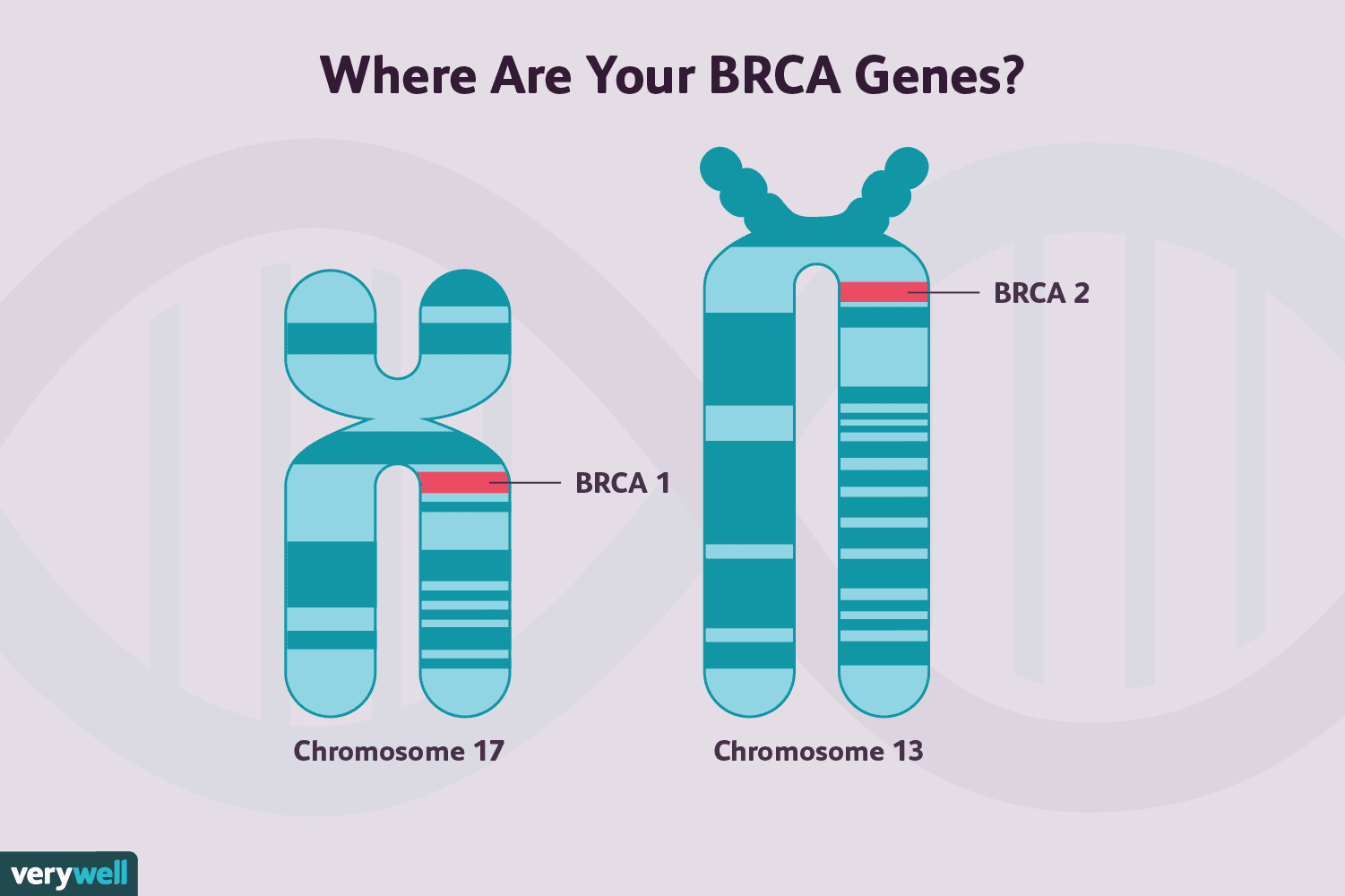
On pense actuellement que 5 % à 10 % des cancers du sein sont génétiques ou familiaux ( bien que ce nombre puisse changer au fur et à mesure que nous en apprenons plus), mais tous ces cancers ne sont pas dus à des mutations BRCA.
Au plus, 29 % (et probablement beaucoup moins) des cancers du sein héréditaires sont positifs pour les mutations des gènes BRCA1 ou BRCA2, et de nombreuses personnes poursuivent les tests pour les autres modifications génétiques connues.
Puisque la science derrière le cancer héréditaire est très anxiogène, pour ne pas dire déroutante et incomplètes, il est utile de commencer par parler de la biologie des mutations génétiques et de la manière dont ces modifications de l'ADN jouent un rôle dans le développement du cancer.
Lorsqu'on parle de mutations, il est important de faire la distinction entre les mutations génétiques héréditaires et acquises.
Les mutations génétiques acquises ou somatiques ont reçu beaucoup d'attention ces dernières années, car ces les mutations provoquent des changements qui favorisent la croissance du cancer. Les thérapies ciblées, des médicaments qui ciblent des voies spécifiques liées à ces changements, ont considérablement amélioré le traitement de certains cancers comme le cancer du poumon.
Les mutations acquises, cependant, ne sont pas présentes dès la naissance, mais se forment plutôt temps après la naissance dans le processus de transformation d'une cellule en cellule cancéreuse. Ces mutations n'affectent que certaines cellules du corps. Ils ne sont pas hérités d'un parent, mais plutôt "acquis" lorsque l'ADN des cellules est exposé aux dommages de l'environnement ou à la suite des processus métaboliques normaux du corps.
Les mutations héréditaires ou germinales, en revanche, sont des changements génétiques que les gens subissent nés avec, et qui sont transmis d'un ou des deux parents. Ces mutations affectent toutes les cellules du corps. Ce sont ces mutations héréditaires (et d'autres modifications génétiques) qui peuvent augmenter le risque qu'une personne développe un cancer et expliquent ce que l'on appelle le cancer du sein héréditaire ou familial.
Mutations génétiques héréditaires (germinales) vs acquises (somatiques)Beaucoup de gens se demandent exactement comment un gène anormal ou des combinaisons de gènes pourraient conduire au cancer du sein , et une brève discussion sur la biologie est utile pour comprendre de nombreuses questions, telles que pourquoi toutes les personnes atteintes de ces mutations ne développent pas un cancer.
Notre ADN est un plan ou un code utilisé pour fabriquer des protéines. Lorsque la carte ou le code est erroné (comme le "lettrage" dans un gène particulier), il donne les mauvaises directions pour synthétiser une protéine. La protéine anormale est alors incapable d'effectuer son travail habituel. Toutes les mutations génétiques n'augmentent pas le risque de cancer, et en fait, la plupart ne le font pas. Les mutations dans les gènes responsables de la croissance et de la division des cellules, ou « mutations motrices », sont à l'origine de la croissance des cancers. Il existe deux principaux types de gènes qui, lorsqu'ils sont mutés, peuvent entraîner une croissance incontrôlée connue sous le nom de cancer :les oncogènes et les gènes suppresseurs de tumeurs.
Plusieurs des gènes associés à un risque plus élevé de cancer du sein sont des gènes suppresseurs de tumeur. Ces gènes codent pour des protéines qui fonctionnent pour réparer les dommages causés à l'ADN dans les cellules (dommages causés par les toxines dans l'environnement ou les processus métaboliques normaux dans les cellules), servent à éliminer les cellules qui ne peuvent pas être réparées ou à réguler la croissance par d'autres moyens. Les gènes BRCA1 et BRCA2 sont des gènes suppresseurs de tumeurs.
Beaucoup de ces gènes sont autosomiques récessifs, ce qui signifie que chaque personne hérite d'une copie du gène de chaque parent, et les deux copies doivent être mutées pour augmenter le risque de cancer. De manière simpliste, cela signifie qu'une combinaison de facteurs génétiques et environnementaux (une mutation acquise dans l'autre gène) doit agir ensemble pour entraîner le développement d'un cancer. De plus, généralement, plusieurs mutations doivent se produire pour qu'une cellule devienne une cellule cancéreuse.
Ce que signifie avoir une prédisposition génétique au cancerToutes les mutations génétiques ou les changements génétiques n'augmentent pas le risque de cancer du sein au même degré , et c'est un concept important pour quiconque envisage des tests génétiques, d'autant plus que de nombreuses personnes ont entendu parler du risque très élevé conféré par les mutations BRCA. La pénétrance génétique est définie comme la proportion de personnes porteuses d'une mutation qui souffriront de la maladie (dans ce cas, développeront un cancer du sein).
Pour certaines mutations, le risque de cancer du sein est très élevé. Pour d'autres, le risque peut n'être augmenté que d'un facteur de 1,5. Il est important de comprendre cela lorsque l'on parle d'options préventives possibles.
Un autre concept important pour comprendre la génétique et le cancer, bien que trop complexe à explorer en détail ici, est celle de l'épigénétique. Nous avons appris que les changements dans l'ADN qui n'impliquent pas de changements dans les paires de bases (nucléotides) ou les "lettres" qui codent pour une protéine, peuvent être tout aussi importants dans le développement du cancer. En d'autres termes, au lieu de changements structurels dans l'épine dorsale de l'ADN, il peut y avoir des changements moléculaires qui modifient la façon dont le message est lu ou exprimé.
Les mutations du gène BRCA sont l'anomalie génétique la plus connue associée au cancer du sein, mais c'est été clair qu'il y a des femmes qui sont prédisposées au cancer du sein en raison de leurs antécédents familiaux, dont le test est négatif.
Une étude de 2017 a révélé que les mutations BRCA ne représentaient que 9 % à 29 % des maladies héréditaires cancers du sein. Même lorsque des tests ont été effectués pour 20 à 40 autres mutations connues, cependant, seulement 4% à 11% des femmes ont été testées positives. En d'autres termes, 64 % à 86 % des femmes suspectées d'avoir un cancer du sein héréditaire ont été testées négatives pour les deux mutations BRCA et 20 à 40 autres.
Nos connaissances sur les mutations génétiques qui augmentent le risque de cancer du sein sont encore incomplètes, mais nous sachez qu'il existe au moins 72 mutations génétiques liées au cancer du sein héréditaire. On pense que ces mutations (et d'autres encore non découvertes) sont responsables de 70 à 90 % des cancers du sein héréditaires dont le test de dépistage des mutations du gène BRCA est négatif. L'acronyme BRCAX a été inventé pour décrire ces autres mutations, signifiant cancer du sein familial non lié à BRCA1 ou BRCA2.
72 Mutations génétiques liées au cancer du sein héréditaireLes anomalies génétiques ci-dessous diffèrent par leur fréquence, le degré de risque associé, le type de cancer du sein auquel ils sont liés et les autres cancers associés aux mutations.
La plupart de ces cancers du sein présentent des caractéristiques similaires (telles que le type de cancer, statut des récepteurs et statut HER2) aux cancers du sein non héréditaires ou sporadiques, mais il existe des exceptions. Par exemple, certaines mutations sont plus fortement associées au cancer du sein triple négatif, notamment les mutations de BARD1 , BRCA1 , BRCA2 , PALB2 , et RAD51D .
Toutes les personnes qui ont les mutations génétiques suivantes ne sont pas identiques. En général, il peut y avoir des centaines de façons dont ces gènes sont mutés. Dans certains cas, le gène produira des protéines qui suppriment la croissance tumorale, mais les protéines ne fonctionneront pas aussi bien que la protéine normale. Avec d'autres mutations, la protéine peut ne pas être produite du tout.
Les mutations du gène BRCA 1 et les mutations du gène BRCA2 sont toutes deux associées à un risque accru de développer le cancer du sein, ainsi que certains autres cancers, bien que les deux diffèrent quelque peu en ce qui concerne ce risque.
En moyenne, 72 % des femmes qui ont des mutations BRCA1 et 69 % qui ont des gènes BRCA2 mutés développeront un cancer du sein avant l'âge de 80 ans.
De plus, les cancers du sein associés à ces mutations peuvent différer. Les cancers du sein chez les femmes qui ont des mutations BRCA1 sont plus susceptibles d'être triple négatif. Environ 75 % sont négatives pour les récepteurs aux œstrogènes, et elles sont également moins susceptibles d'être HER2 positives. Ils sont également plus susceptibles d'avoir un grade de tumeur plus élevé. Les cancers du sein chez les femmes porteuses de mutations BRCA2, en revanche, sont similaires aux cancers chez les femmes qui ne sont pas porteuses de la mutation du gène BRCA.
Le gène ATM code pour des protéines qui aident à contrôler le taux de croissance des cellules. Ils aident également à réparer les cellules endommagées (cellules dont l'ADN a été endommagé par des toxines) en activant des enzymes qui réparent ces dommages.
Ceux qui ont deux copies du gène muté ont un syndrome récessif autosomique rare connu sous le nom de ataxie télangiectasie. Avec l'ataxie-télangiectasie, les protéines défectueuses augmentent non seulement le risque de cancer, mais entraînent la mort prématurée de certaines cellules du cerveau, entraînant une maladie neurodégénérative progressive.
Les personnes qui ne possèdent qu'une seule copie mutée du gène (environ 1 % de la population) ont un risque à vie de 20 à 60 % de développer un cancer du sein.
On pense que les personnes qui ont cette mutation sont prédisposées au cancer du sein à un âge précoce , ainsi qu'au développement d'un cancer du sein bilatéral.
Le dépistage du cancer du sein par IRM du sein est recommandé à partir de 40 ans, et les femmes peuvent souhaiter envisager des mastectomies préventives. Les personnes ayant un gène ATM muté semblent également être prédisposées aux cancers de la thyroïde et du pancréas et sont plus sensibles aux radiations.
Les mutations du gène PALB2 sont également une cause importante de cancer du sein héréditaire. Le gène PALB2 code pour une protéine qui fonctionne en conjonction avec la protéine BRCA2 pour réparer l'ADN endommagé dans les cellules. Dans l'ensemble, le risque à vie de cancer du sein avec une mutation PALB2 est aussi élevé que 58% bien que cela puisse varier selon l'âge. Le risque est de 8 à 9 fois la moyenne pour les femmes de moins de 40 ans, mais d'environ 5 fois la moyenne pour les femmes de plus de 60 ans.
Parmi celles qui sont porteuses d'une copie du gène, 14 % développeront un cancer du sein à 50 ans et 35 % à 70 ans (moins qu'avec les mutations BRCA).
Les personnes qui ont une mutation PALB2 et qui développent un cancer du sein peuvent avoir un risque plus élevé de mourir de la maladie.
Les personnes qui héritent de 2 copies du gène PALB2 muté ont un type d'anémie de Fanconi caractérisée par un très faible nombre de globules rouges, de globules blancs et de plaquettes.
Le gène CHEK2 code pour une protéine qui est activée lorsque l'ADN est endommagé. Il active également d'autres gènes impliqués dans la réparation cellulaire.
Les risques à vie pour les porteurs de mutations tronquantes CHEK2 sont de 20 % pour une femme sans parent affecté, 28 % pour une femme avec un parent au deuxième degré affecté, 34 % pour une femme avec un parent au premier degré affecté et 44 % pour une femme avec un parent au premier et au deuxième degré affecté.
Pour les hommes et les femmes, le gène augmente également le risque de cancer du côlon et non -Lymphome de Hodgkin.
Les mutations de CDH1 provoquent une affection connue sous le nom de syndrome de cancer gastrique héréditaire.
Les personnes qui héritent de ce gène ont un risque à vie allant jusqu'à 80 % de développer un cancer de l'estomac et jusqu'à 52 % de développer un cancer du sein lobulaire.
Le gène code pour une protéine (la cadhérine épithéliale) qui aide les cellules à se coller les unes aux autres (l'une des différences entre les cellules cancéreuses et les cellules normales est que les cellules cancéreuses manquent de ces produits chimiques d'adhésion qui les font coller). Les cancers chez les personnes qui héritent de cette mutation sont plus susceptibles de métastaser.
Les mutations du gène PTEN sont l'une des mutations les plus courantes du gène suppresseur de tumeur. Le gène code pour les protéines qui régulent la croissance des cellules et aide également les cellules à se serrer les coudes.
Les mutations du gène semblent augmenter le risque que des cellules cancéreuses se détachent d'une tumeur et métastasant. Le PTEN est associé à un syndrome appelé syndrome tumoral d'hamartome PTEN ainsi qu'au syndrome de Cowden.
Les femmes porteuses d'une mutation PTEN ont un risque à vie de développer un cancer du sein allant jusqu'à 85 %, et ont également un risque accru de modifications mammaires bénignes telles que la maladie fibrokystique, l'adénose et la papillomatose intracanalaire.
Les mutations sont également liées à un risque accru de cancer de l'utérus (et de fibromes utérins bénins ), cancer de la thyroïde, cancer du côlon, mélanome et cancer de la prostate.
Les symptômes non liés au cancer comprennent une grosse tête (macrocéphalie) et la tendance à former tumeurs bénignes appelées hamartomes.
Les mutations de STK11 sont associées à une maladie génétique connue sous le nom de syndrome de Peutz-Jegher. STK11 est un gène suppresseur de tumeur impliqué dans la croissance cellulaire.
En plus d'un risque accru de cancer du sein (avec un risque à vie allant jusqu'à 50 %), le syndrome comporte un risque accru de nombreux cancers, dont certains comprennent le cancer du côlon, le cancer du pancréas, le cancer de l'estomac, le cancer de l'ovaire, le cancer du poumon, cancer de l'utérus, et plus encore.
Les conditions non liées au cancer associées à la mutation comprennent les polypes non cancéreux dans le tube digestif et système urinaire, taches de rousseur sur le visage et l'intérieur de la bouche, etc. Le dépistage du cancer du sein est souvent recommandé pour les femmes à partir de la vingtaine, et souvent avec une IRM avec ou sans mammographie.
Le gène TP53 code pour des protéines qui arrêtent la croissance des cellules anormales.
Ces mutations sont extrêmement fréquentes dans le cancer, avec des mutations acquises des mutations du gène p53 sont retrouvées dans environ 50 % des cancers.
Les mutations héréditaires sont moins fréquentes et associées à des affections connues sous le nom de syndrome de Li-Fraumeni, ou Syndrome de type Li-Fraumeni (qui a un risque de cancer plus faible). La majorité des personnes qui héritent de la mutation développent un cancer avant l'âge de 60 ans et, en plus du cancer du sein, sont susceptibles de développer un cancer des os, un cancer des surrénales, un cancer du pancréas, un cancer du côlon, un cancer du foie, des tumeurs cérébrales, une leucémie, etc. Il n'est pas rare que les personnes porteuses de la mutation développent plus d'un cancer primitif.
Les mutations héréditaires du gène p53 seraient responsables d'environ 1 % des cas de cancer du sein héréditaire. Les cancers du sein associés à la mutation sont souvent HER2 positifs et ont un grade tumoral élevé.
Le syndrome de Lynch ou cancer colorectal héréditaire sans polypose est associé à des mutations dans plusieurs gènes différents y compris PMS2, MLH1, MSH2, MSH6 et EPCAM.
Le SPM2, en particulier, a été associé à un double risque de cancer du sein. Le gène fonctionne comme un gène suppresseur de tumeur, codant pour une protéine qui répare l'ADN endommagé.
En plus du cancer du sein, ces mutations comportent un risque élevé de cancers du côlon , ovaire, utérus, estomac, foie, vésicule biliaire, intestin grêle, rein et cerveau.
Il existe plusieurs autres mutations génétiques associées à un risque accru de développer un cancer du sein, et on s'attend à ce que d'autres soient découverts dans un proche avenir. Certains d'entre eux incluent :
À l'heure actuelle, des tests sont disponibles pour les mutations du gène BRCA, ainsi que les mutations ATM, CDH1, CHEK2, MRE11A, MSH6, NBN, PALB2, PMS2, PTEN, RAD50, RAD51C, SEC23B et TP53, ce domaine devant se développer considérablement dans un proche avenir.
La disponibilité de ces tests soulève cependant de nombreuses questions. Par exemple, qui pourrait avoir un cancer du sein héréditaire et qui devrait être testé ? Que devez-vous faire si votre test est positif pour l'un de ces gènes ?
Idéalement, tout test ne devrait être effectué qu'avec les conseils et l'aide d'un conseiller en génétique . Il y a deux raisons à cela.
La première est qu'il peut être dévastateur d'apprendre que vous êtes porteur d'une mutation qui peut augmenter votre risque, et les conseils d'une personne qui connaît la gestion et le dépistage recommandés sont inestimables.
Comme indiqué précédemment, certaines mutations confèrent un risque élevé et d'autres un risque beaucoup plus faible. Certaines mutations pourraient être plus préoccupantes plus tôt dans la vie (par exemple, dans la vingtaine), tandis que d'autres pourraient ne pas nécessiter de dépistage précoce. Un conseiller en génétique peut vous aider à découvrir ce qui est actuellement recommandé en ce qui concerne le dépistage de votre mutation particulière tout en tenant compte de tout autre facteur de risque que vous pourriez avoir.
L'autre raison pour laquelle le conseil génétique est si important est que vous pouvez avoir un risque important de développer un cancer du sein même si vos tests sont négatifs. Il reste encore beaucoup à apprendre, et un conseiller en génétique peut vous aider à examiner vos antécédents familiaux pour voir si vous pouvez présenter un risque élevé malgré des tests négatifs, et planifier le dépistage en conséquence.
Test génétique pour le cancer du seinTout comme les personnes qui ont reçu un diagnostic de cancer du sein ont besoin de soutien, celles qui sont porteuses de gènes qui augmentent le risque ont besoin de soutien. Heureusement, il existe des organisations qui se concentrent spécifiquement sur le soutien aux personnes dans cette situation.
Une organisation, FORCE, qui est l'acronyme de Facing Our Risk of Cancer Empowered, offre une ligne d'assistance, un babillard électronique et des informations pour ceux qui sont confrontés à un cancer héréditaire.
D'autres organisations et communautés de soutien sont disponibles pour aider les gens à faire face aux décisions liées à un diagnostic de cancer du sein héréditaire.
Le terme "prévivant" a été inventé par FORCE pour décrire les personnes qui survivent à une prédisposition au cancer du sein. Si c'est la situation à laquelle vous faites face, vous n'êtes pas seul, et en utilisant le hashtag #previvor, vous pouvez en trouver beaucoup d'autres sur Twitter et d'autres médias sociaux.
Il peut être difficile d'en savoir plus sur les nombreuses mutations génétiques différentes qui augmentent le risque de cancer du sein au-delà des mutations BRCA, mais ces "autres" mutations sont d'une importance significative sachant que les mutations BRCA représentent une relative minorité des cancers du sein familiaux. En même temps, la science qui étudie le cancer du sein héréditaire en est encore à ses balbutiements et il reste encore beaucoup à apprendre. Si vous craignez d'avoir une mutation ou si vous avez appris que c'est le cas, il est utile d'en apprendre le plus possible. Les organisations de lutte contre le cancer héréditaire telles que FORCE peuvent non seulement vous fournir des informations supplémentaires, mais peuvent également vous aider à entrer en contact avec d'autres personnes confrontées à un voyage avec des questions et des préoccupations similaires.
 Comment préparer un bouillon d'os de bœuf nourrissant pour soigner votre intestin
Comment préparer un bouillon d'os de bœuf nourrissant pour soigner votre intestin
 Est-il normal de gonfler tous les jours ?
Est-il normal de gonfler tous les jours ?
 7 raisons pour lesquelles vous êtes ballonné
7 raisons pour lesquelles vous êtes ballonné
 Troubles digestifs :pourquoi ai-je du sang dans mes selles ?
Troubles digestifs :pourquoi ai-je du sang dans mes selles ?
 Pouvez-vous vivre avec une maladie rénale de stade I ?
Pouvez-vous vivre avec une maladie rénale de stade I ?
 Troubles d'élimination chez les enfants
Troubles d'élimination chez les enfants
 Faits saillants sur la santé :9 avril 2012
Dernières nouvelles de MedicineNet Les scientifiques identifient les gènes qui font vos empreintes digitales Médecins mal informés sur les droits des patients handicapés Les essais cliniques se diver
Faits saillants sur la santé :9 avril 2012
Dernières nouvelles de MedicineNet Les scientifiques identifient les gènes qui font vos empreintes digitales Médecins mal informés sur les droits des patients handicapés Les essais cliniques se diver
 Un vaccin naturel contre les maladies auto-immunes ? (Hmm)
Imaginez que cétait il y a 400 ans et que vous êtes malade... il savère que cest la même chose qui vient de tuer votre sœur et son plus jeune fils. Heureusement, le Docteur sait exactement quoi faire
Un vaccin naturel contre les maladies auto-immunes ? (Hmm)
Imaginez que cétait il y a 400 ans et que vous êtes malade... il savère que cest la même chose qui vient de tuer votre sœur et son plus jeune fils. Heureusement, le Docteur sait exactement quoi faire
 Mise à jour des dépistages du cancer du côlon
Le cancer du côlon (cancer colorectal) survient lorsque des cellules malignes se développent autour de votre rectum ou de la paroi interne de votre côlon. Il est essentiel dobtenir un diagnostic préci
Mise à jour des dépistages du cancer du côlon
Le cancer du côlon (cancer colorectal) survient lorsque des cellules malignes se développent autour de votre rectum ou de la paroi interne de votre côlon. Il est essentiel dobtenir un diagnostic préci